El herpes zóster (HZ) es una enfermedad producida por la reactivación del virus varicela zóster, caracterizada por una erupción cutánea vesiculosa generalmente localizada y dolorosa. Se ha observado un aumento de su incidencia en las últimas décadas. La neuralgia posherpética (NPH) es la complicación más frecuente, ocurre en alrededor del 18% de los afectos por HZ y puede ocasionar un dolor invalidante. Tanto la incidencia del HZ como de la NPH aumenta notoriamente con la edad. La NPH puede afectar a más del 30% de los mayores de 79 años con HZ. La vacuna del virus varicela zóster atenuado (VVZa) presenta una eficacia del 51% para la prevención del HZ, su eficacia disminuye con la edad, está contraindicada en inmunocomprometidos y está aprobada por la FDA para esta indicación en inmunocompetentes ≥50 años.
Recientemente, la FDA ha aprobado el uso de una nueva vacuna recombinante contra el HZ (VVZr) (Shingrix®, GlaxoSmithKline) para esta indicación. La VVZr contiene una glicoproteína E recombinante del virus varicela zóster junto al adyuvante ASO1B, se administra en 2 inyecciones subcutáneas separadas por 2 a 6 meses (tabla 1). La eficacia de la VVZr fue evaluada en 2 ensayos clínicos fase 3 aleatorizados versus placebo (ZOE-501 y ZOE-702). La mediana de seguimiento fue superior a 3 años en ambos estudios. En el estudio ZOE-50 que incluyó 15.411 pacientes ≥50 años, se describieron 6 casos de HZ en el grupo vacunado versus 210 en el grupo placebo. La eficacia global en la prevención del HZ fue del 97,2% (IC 95%: 93,7-99,0; p<0,001)1. En el estudio ZOE-70 que incluyó 13.900 pacientes ≥70 años, la eficacia en la prevención del HZ fue del 89,8% (IC 95%: 84,2-93,7; p<0,001) y del 88,8% (IC 95%; 68,7-97,1; p<0,001) en la prevención de la NPH2. En un análisis conjunto de ambos estudios la eficacia en la prevención de complicaciones post-HZ distintas a la NPH como el HZ diseminado, enfermedad oftálmica, neurológica o visceral, vasculitis secundaria o accidente vascular encefálico fue del 93,7% (IC 95%: 59,5-99,9%).3 En ambos estudios la tasa de efectos adversos graves fue similar en el grupo vacunado y en el grupo placebo. Los efectos adversos más frecuentes fueron dolor en el sitio de inyección, mialgias y fatiga.
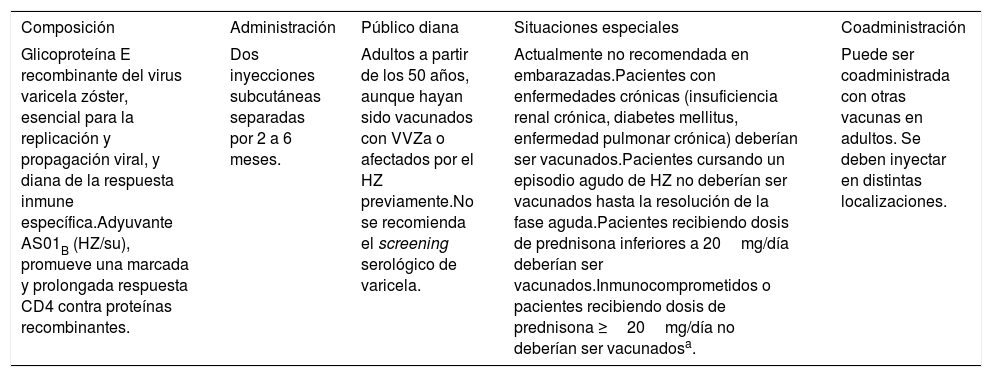
Características e indicaciones de la vacuna recombinante contra el herpes zóster (Shingrix®)
| Composición | Administración | Público diana | Situaciones especiales | Coadministración |
|---|---|---|---|---|
| Glicoproteína E recombinante del virus varicela zóster, esencial para la replicación y propagación viral, y diana de la respuesta inmune específica.Adyuvante AS01B (HZ/su), promueve una marcada y prolongada respuesta CD4 contra proteínas recombinantes. | Dos inyecciones subcutáneas separadas por 2 a 6 meses. | Adultos a partir de los 50 años, aunque hayan sido vacunados con VVZa o afectados por el HZ previamente.No se recomienda el screening serológico de varicela. | Actualmente no recomendada en embarazadas.Pacientes con enfermedades crónicas (insuficiencia renal crónica, diabetes mellitus, enfermedad pulmonar crónica) deberían ser vacunados.Pacientes cursando un episodio agudo de HZ no deberían ser vacunados hasta la resolución de la fase aguda.Pacientes recibiendo dosis de prednisona inferiores a 20mg/día deberían ser vacunados.Inmunocomprometidos o pacientes recibiendo dosis de prednisona ≥20mg/día no deberían ser vacunadosa. | Puede ser coadministrada con otras vacunas en adultos. Se deben inyectar en distintas localizaciones. |
En la actualidad no existe evidencia suficiente para recomendar la vacunación en inmunocomprometidos, aunque teóricamente sería posible.
HZ: herpes zóster; VVZa: vacuna con virus varicela zóster atenuado.
Fuente: Dooling et al.5.
La VVZr ha mostrado resultados superiores a VVZa en la prevención del HZ y de la NPH. Además, el análisis de coste-efectividad favoreció a la VVZr sobre la VVZa4. Esto ha llevado al comité consultor de vacunación (Advisory Committee on Immunization Practices [ACIP]) norteamericano a recomendar recientemente la vacunación con VVZr en inmunocompetentes ≥50 años, incluso en aquellos vacunados previamente con VVZa o que han padecido de HZ5. Aún no existe evidencia suficiente que permita recomendar la VVZr en inmunocomprometidos o en pacientes en tratamiento inmunosupresor con dosis de prednisona ≥20mg/día, aunque teóricamente sería posible.
La VVZr es una alternativa eficaz y segura en la prevención del HZ y de la NPH, y debería ser recomendada en adultos, lo que podría disminuir la morbilidad asociada a estas enfermedades.