En las úlceras crónicas de los pacientes con trasplante renal se plantea la etiología infecciosa, tumoral o secundaria al tratamiento. Hay otra causa, mucho menos frecuente, que hay que tener en cuenta para un correcto diagnóstico e intervención terapéutica. Una mujer de 62 años de edad con insuficiencia renal crónica, secundaria a nefropatía vascular en riñón único, realizó diálisis durante 12 años mediante una fístula arteriovenosa húmero cefálica derecha. En el año 2001 recibió un trasplante renal de cadáver y desde entonces mantenía una buena función renal y realizaba tratamiento con prednisona, ciclosporina y micofenolato, pasados 10 años se cambió la ciclosporina por rapamicina, al haber presentado un carcinoma espinocelular en la pierna izquierda. Consultó por una úlcera en el dorso de la mano derecha de 9 meses de evolución, se había iniciado al año de introducir la rapamicina con una erosión en ausencia de traumatismo y había evolucionado de forma tórpida y dolorosa. Había consultado en dermatología, donde se realizó un estudio histológico que fue inespecífico y cultivo de la biopsia, que fue positivo para Staphylococcus aureus, siendo tratada según el antibiograma específico, y en cirugía plástica, donde se practicaron 2 injertos de piel parcial sin éxito.
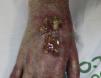
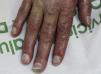
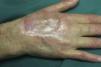
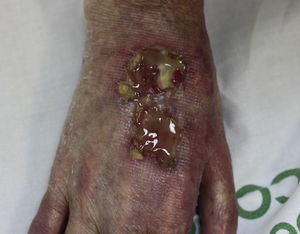
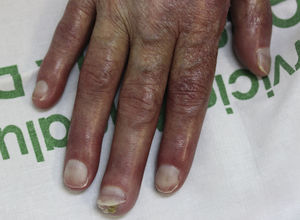
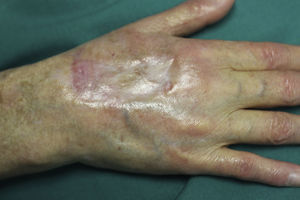
En la exploración, la úlcera ocupaba el dorso de la mano derecha con un tamaño de 6×3cm de diámetro, limpia y con la base sanguinolenta (fig. 1). La mano estaba fría e inmóvil, se disponía en forma de garra y tenía una coloración violácea, la piel era fina, seca, sin pelo, y en el pulpejo del dedo medio tenía una pápula queratósica dura y adherida (fig. 2). El pulso radial era nulo y en el brazo se mantenía una fístula arteriovenosa húmero cefálica, realizada 20 años antes, que al comprimirla permitía apreciar el pulso debilitado. Tras confirmar con ecografía doppler, el flujo muy disminuido a nivel de la arteria cubital y radial distal, fue intervenida de urgencia por el servicio de cirugía vascular, mediante ligadura de la fístula. Dos meses después la úlcera había curado con una cicatriz esclerosa y la mano tenía mejor color, aunque se mantenía inmóvil y atrófica (fig. 3). Se remitió al servicio de rehabilitación y su nefrólogo reintrodujo la rapamicina, 2 meses después presentó una úlcera sobre la cicatriz, como consecuencia de los masajes recibidos durante la rehabilitación, la rapamicina fue definitivamente suspendida y la lesión curó en el curso de pocas semanas. Se ha mantenido el seguimiento de la paciente durante los 3 últimos años sin recidiva de la misma, pero sin alcanzar la recuperación del aspecto y funcionalidad del miembro.
La causa de la úlcera fue el síndrome del robo vascular ocasionado por una fístula arteriovenosa, realizada más de 20 años antes que, como habitualmente sucede, se había mantenido después del trasplante. Es muy probable que la introducción de la rapamicina supusiera un elemento agravante para la mala evolución inicial, pero una vez suspendida los injertos realizados fueron infructuosos, debido al robo vascular que había producido una isquemia crónica. El diagnóstico se basó en la clínica: el aspecto del miembro, la textura y el color de la piel y la isquemia digital distal llevaron a la exploración del pulso y la temperatura, ambos claramente disminuidos. El tratamiento, mediante el cierre de la fístula permitió la revascularización y la curación en pocas semanas. La reintroducción de la rapamicina fue contraproducente y se manifestó con la formación de una nueva úlcera ante un traumatismo mínimo, que no curó hasta suspenderla. El síndrome del robo vascular, cuyo diagnóstico se demoró durante 9 meses, ha dejado una secuela permanente en la paciente.
Las fístulas arteriovenosas que se realizan para la hemodiálisis producen un robo vascular en el 70% de los pacientes, pero solo en el 10% llega a ser sintomático, ya que el robo se compensa con una revascularización colateral1. Los hemodializados de larga evolución, con más incidencia de calcifilaxis y factores de riesgo vascular, como la diabetes e hipertensión arterial, así como los diagnosticados de lupus eritematoso sistémico, tienen más probabilidades de padecer el síndrome del robo vascular2. Los síntomas relacionados con la isquemia comienzan durante el primer mes, siendo su presentación tardía más difícilmente reconocible. Las manifestaciones clínicas son insidiosas y se acompañan de dolor y parestesias, conducen a la necrosis isquémica con la consiguiente morbilidad3,4. En los pacientes trasplantados el síndrome del robo vascular está poco documentado y solo hay un caso publicado en el que un paciente trasplantado y portador de una fístula desde hacía 20 años presenta una úlcera en el dorso de la mano de causa traumática, cura de forma lenta y por segunda intención pero mantiene dolor, pérdida de movilidad y parestesias que no desaparecen hasta el cierre de la fístula5.
Por otro lado está la implicación de la rapamicina en el desarrollo y mantenimiento de la úlcera. Este fármaco que ejerce su acción mediante la unión a las proteínas citosólicas FKBP12, inhibiendo la vía mTOR, tiene un efecto antiproliferativo y antiangiogénico además de inmunosupresor. Su utilización en el trasplante de órgano sólido y hematológico ha aumentado, aunque los efectos secundarios como dislipemia, edema periférico, citopenia, acné, proteinuria y úlceras orales se describen en el 98% de los pacientes y dan lugar a la suspensión del mismo en el 46% de ellos6,7. La relación de la rapamicina con el curso tórpido de las úlceras está clara, por lo que no se aconseja su utilización en los 6 primeros meses después del trasplante debido a la mala evolución de la herida quirúrgica8. Introducida después es más eficaz, si bien ante una úlcera crónica hay que suspenderla lo que conduce a una evolución más favorable de la misma9,10.
En conclusión, dado que la fístula en los pacientes trasplantados, por regla general se mantiene es importante explorar la funcionalidad de la misma antes de iniciar el tratamiento con rapamicina.
Conflicto de interesesLa autora declara no tener ningún conflicto de intereses.