Las reacciones de hipersensibilidad (HS) a fármacos tienen un espectro clínico muy variado y pueden presentarse con diferentes tipos de lesiones cutáneas entre las que se encuentra el eritema nudoso.
Una mujer de 44 años, sin alergias medicamentosas conocidas, diagnosticada de enfermedad de Crohn 2 años antes, había comenzado tratamiento con azatioprina (AZT) hacía 3 semanas debido a una progresión analítica y radiológica de dicha enfermedad. Acudió a urgencias por lesiones eritematosas, dolorosas, de 7 días de evolución en ambos miembros inferiores asociadas a malestar general, pérdida de apetito y artralgias en rodillas y tobillos. No había presentado fiebre.
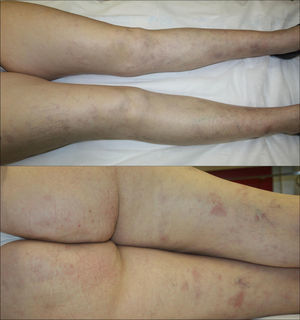
En la exploración se observaban, de forma dispersa en ambos miembros inferiores, múltiples nódulos subcutáneos de entre 10-20mm con eritema en superficie, dolorosos a la presión, así como algunas máculas de entre 15-20mm de coloración violácea y aspecto residual (fig. 1).
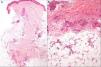
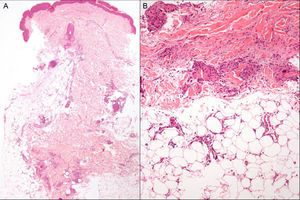
El estudio histopatológico de una de las lesiones mostró engrosamiento y fibrosis de los septos en el tejido celular subcutáneo, con un infiltrado inflamatorio crónico constituido por histiocitos, linfocitos y granulomas con células gigantes multinucleadas (fig. 2A yB). Con técnicas de PAS, Gram y Ziehl-Neelsen no se observaron microorganismos. En el estudio analítico destacaban los siguientes hallazgos: hemoglobina 10,4g/dl, volumen corpuscular medio 78,4fl, hemoglobina corpuscular media 25,3pg, aumento de transaminasas (GPT 82U/l, GGT 126U/l), proteína C reactiva 12,59mg/dl (rango normal: 0,1-0,5mg/dl), estudio de autoinmunidad sin alteraciones, Mantoux con una induración de 0mm y una radiografía de tórax sin alteraciones (tabla 1).
Revisión de casos publicados de EN como reacción de HS a azatioprina
| Edad/sexo | Enfermedad subyacente | Tiempo de latencia | Resolución (días) | Recurrencia tras re-exposición | |
|---|---|---|---|---|---|
| de Fonclare et al.1 | 17M | EII | 14 días | 16 días | 12h |
| 49M | EII | 8 días | 12 días | 4h | |
| 75V | EII | 14 días | 14 días | No realizada | |
| Vargas-Hitos et al.5 | 65M | Penfigoide ampolloso | 7 días | 14 días | No realizada |
EII: enfermedad inflamatoria intestinal; EN: eritema nudoso; HS: hipersensibilidad; M: mujer; V: varón.
Ante la posibilidad de que las lesiones fuesen atribuibles a la AZT se decidió suspender el fármaco, con resolución de la sintomatología sistémica en 24h y de las lesiones cutáneas en 3 días sin ningún otro tratamiento. Por todo ello se realizó el diagnosticó de reacción de hipersensibilidad a AZT con manifestación cutánea en forma de eritema nudoso.
La AZT es un precursor de la 6-mercaptopurina, utilizado como fármaco inmunosupresor en el tratamiento de enfermedades inflamatorias crónicas como la enfermedad inflamatoria intestinal (EII).
Los efectos adversos relacionados con el uso de este fármaco pueden clasificarse en reacciones tempranas o tardías.
Las reacciones tempranas son comunes1, entre ellas se encuentran las reacciones de HS. Estas, son reacciones idiosincrásicas que ocurren aproximadamente en un 2% de los pacientes, en las primeras 4 semanas de tratamiento, aunque es probable que estén infradiagnosticadas1,2. Se manifiestan con un cuadro clínico de fiebre, hipotensión, malestar general, artralgias, síntomas gastrointestinales, hepatitis, pancreatitis, nefritis, neumonía, pericarditis y/o lesiones cutáneas1,3. Las lesiones se resuelven de forma rápida en 2-3 días tras la suspensión del fármaco2. Muchos casos se diagnostican inicialmente como cuadros infecciosos o de exacerbación de la enfermedad de base y la reacción de HS no se detecta hasta el momento de la re-exposición al fármaco2,3. La recurrencia del cuadro clínico tras la re-exposición al fármaco es la forma de confirmar la relación causa-efecto, pero dado que aparece de forma más intensa y con un intervalo de tiempo menor, en ocasiones de pocas horas3, está contraindicada2. De los pacientes con reacciones de HS a AZT se ha sugerido un riesgo mayor en aquellos que padecen EII, que podría estar determinado por un polimorfismo en el gen que codifica la inosina trifosfato pirofostasa4.
En 2011, Bidinger et al. revisaron todos los casos publicados de HS a AZT, aproximadamente un 50% presentaban manifestaciones cutáneas2. De estas, la forma de presentación más frecuente fue el síndrome de Sweet seguida en orden de frecuencia por exantemas maculopapuloso, vesiculoso, pustuloso o urticariforme inespecíficos, vasculitis de pequeño vaso, eritema nudoso1,5 y pustulosis exantemática aguda generalizada. Desde entonces se han publicado una decena de casos más con afectación cutánea, la mayoría de ellos en forma de síndrome de Sweet y 2 casos de hidradenitis ecrina neutrofílica6,7, asociación que no había sido descrita previamente. En el estudio histopatológico lo más frecuente es encontrar hallazgos de dermatosis neutrofílica2.
El eritema nudoso asociado a EII se observa hasta en un 10% de pacientes con colitis ulcerosa y un 15% con enfermedad de Crohn; las lesiones suelen presentar un curso paralelo a la actividad de la enfermedad y resolverse con el adecuado tratamiento de la misma8.
Las reacciones tardías, como la mielosupresión, son dosis dependientes y pueden evitarse en gran parte mediante la determinación de la actividad de la enzima tiopurin-metiltransferasa1.
En nuestra paciente, las lesiones se resolvieron sin tratamiento en 3 días. Una vez resuelto el cuadro se inició tratamiento con infliximab que tuvo que ser suspendido por reacción infusional y posible toxicodermia. Un año después de la consulta, ha presentado algunos brotes de su enfermedad en forma de cuadros suboclusivos, sin nuevos episodios de eritema nudoso.
La presencia de lesiones de eritema nudoso en pacientes tratados con AZT, sin datos de brote de EII o infección intercurrente, deberán alertarnos de una posible reacción de HS al fármaco.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.