La talidomida es el fármaco de elección en el tratamiento del eritema nodoso leproso severo/recurrente. Su uso ha sido relacionado con trombosis venosas profundas (TVP) en pacientes con enfermedades hematológicas (especialmente cuando se le asocia con corticoides y quimioterapia).
Presentamos un caso de TVP en un hombre de 43 años, con lepra lepromatosa en tratamiento con talidomida y prednisona por una leprorreación tipo 2 (eritema nodoso leproso), con anticuerpos antifosfolípidos positivos transitorios.
Resaltamos la importancia de tener en cuenta esta posible complicación, potencialmente fatal, en pacientes tratados con talidomida por enfermedades dermatológicas.
Thalidomide is the treatment of choice for severe or recurrent erythema nodosum leprosum. Its use has been associated with deep vein thrombosis in patients with blood disorders, however, particularly when used in combination with corticosteroids or chemotherapy. We describe a case of deep vein thrombosis in a 43-year-old man with lepromatous leprosy who was being treated with thalidomide and prednisone for a type 2 leprosy reaction (erythema nodosum leprosum); the patient also had transiently positive antiphospholipid antibody results. We stress the importance of considering deep vein thrombosis, a potentially fatal complication, in dermatology patients treated with thalidomide.
La lepra o enfermedad de Hansen es una enfermedad infecciosa granulomatosa crónica, causada por Micobacterium leprae, que afecta principalmente a áreas frías del cuerpo como la piel, las vías aéreas respiratorias altas, el segmento anterior del ojo, los segmentos superficiales de nervios periféricos y los testículos. Recientemente se ha identificado un nuevo Micobacterium, el M. lepromatosis sp. nov1, causante de la lepra lepromatosa difusa (también conocida como lepra de Lucio y Lapati2), que es una forma particular de lepra endémica en Méjico y en el Caribe.
La infección se considera «paucibacilar» (cuando no se encuentran bacilos ácido alcohol resistentes en los tejidos o en los frotis) o «multibacilar» (cuando se encuentra uno o más bacilos ácido alcohol resistentes). El tratamiento de los pacientes con lepra paucibacilar, según la pauta de la Organización Mundial de la Salud (OMS), se realiza con la asociación de sulfona y rifampicina durante 6 meses, mientras que los casos de lepra multibacilar se tratan con sulfona, rifampicina y clofazimina durante un año. Otros antibióticos bactericidas para M. Leprae, como las fluoroquinolonas, la minociclina y la claritromicina, pueden ser una alternativa cuando existe resistencia, recaída, falta de respuesta o intolerancia a la sulfona.
Característicamente los pacientes con lepra pueden presentar reacciones agudas, mediadas inmunológicamente, denominadas leprorreacción tipo 1 (reacción de regresión) y tipo 2 (eritema nodoso leproso).
La talidomida es el fármaco de elección en el tratamiento del eritema nodoso leproso grave/recurrente. Su uso se ha relacionado con complicaciones graves como trombosis venosa profunda (TVP)3, teratogenicidad, neuropatía e hiperpotasemia.
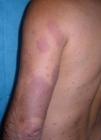
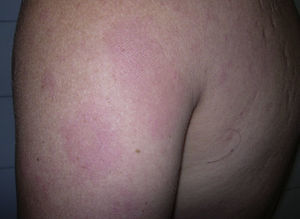
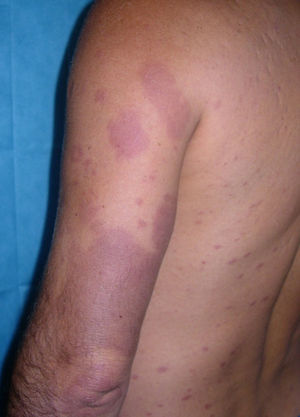
Caso clínicoSe trata de un varón de 43 años de edad, originario de Brasil, que consultó en 2008 por lesiones cutáneas de 3 años de evolución, que consistían en placas eritematosas ligeramente infiltradas, de bordes netos, con pérdida de sensibilidad táctil y dolorosa, localizadas en los miembros, los glúteos y el tronco (fig. 1). Se realizó una biopsia cutánea que mostró una dermatitis granulomatosa intersticial con un moderado infiltrado linfocitario perivascular superficial y cúmulos histiocitarios en la unión entre la dermis reticular y la dermis papilar. La técnica de Ziehl-Neelsen mostró escasos bacilos ácido alcohol resistentes sueltos y agrupados en globias. El estudio del moco y la linfa fue positivo (índice bacteriológico ++ y morfológico del 40%). Un electromiograma mostró una polineuropatía axonal leve-moderada de predominio sensitivo. Inicialmente se diagnosticó lepra borderline lepromatosa (aunque posteriormente reevaluando el caso se llegó a la conclusión de que se trataba de una lepra lepromatosa) y se pautó tratamiento con rifampicina 600mg/día, clofacimina 50mg/día (más 300mg el primer día del mes) y sulfona 100mg/día. A los 6 meses de iniciado el tratamiento el paciente acudió por aparición de nuevas lesiones y empeoramiento de las previas, junto a fiebre de 38°C. Se realizó una nueva biopsia de piel, que mostró una reacción granulomatosa de predominio perivascular y perianexial con presencia de histiocitos espumosos que respetaba la epidermis; con la técnica de Ziehl se encontraron abundantes bacilos. Ante este cuadro inicialmente tuvimos dificultades diagnósticas y se interpretó como leprorreacción tipo 1, por lo que se trató con prednisona 30mg/día. El paciente continuó con empeoramiento de las lesiones (fig. 2) y aparecieron lesiones sugestivas de eritema nodoso, por lo que se decidió iniciar tratamiento con talidomida (hasta 150mg/día) y disminuir gradualmente la dosis de corticoides. A los dos meses de iniciado el tratamiento con talidomida acudió por edema y dolor en el miembro inferior derecho, por lo que se realizó una ecodoppler que mostró una TVP infrapoplítea. En una analítica el hemograma, el perfil bioquímico y la coagulación fueron normales, mientras que los anticuerpos antifosfolípidos (aPL) mostraron resultados ligeramente aumentados, anticuerpos anti-β2 glucoproteína (anti-β 2GPI) IgA: 34,0 U (valor normal<20), anticuerpos antifosfatidil serina IgG: 33,6 U (valor normal<16,0), anticuerpos anticardiolipina (aCL) IgG: 27,70 UFL/ml (valor normal<25,00) y aCL IgM normales. Estas determinaciones se repitieron a las 8 semanas y mostraron resultados negativos o normales. Se suspendió la talidomida e inició anticoagulación con enoxaparina seguida de acenocumarol.
DiscusiónLa presencia de aPL se ha relacionado con numerosas enfermedades infecciosas, tanto víricas (virus de la inmunodeficiencia adquirida, virus hepatitis C, parvovirus B19) como bacterianas (sífilis, malaria y lepra); generalmente es transitoria y puede desaparecer con el tratamiento4. Se han encontrado aCL positivos en el 42,7% (rango: 21 al 67%) y anti-β 2GPI en el 44,8% (rango: 2,9 al 89%) de los pacientes con lepra lepromatosa o borderline lepromatosa5. En un estudio6 encontraron que los aCL son más frecuentes en pacientes con lepra multibacilar (80,7%) que en los pacientes que presentan lepra paucibacilar (8,3%) y que los títulos no se vieron afectados por el tratamiento.
El hallazgo de aCL, anticoagulante lúpico (AL) o anti-β 2GPI es considerado un factor independiente de riesgo de trombosis, y solo la presencia de uno de ellos de forma estable (en dos o más ocasiones separadas por 12 semanas) permite clasificar dentro del síndrome antifosfolípido (SAF) a un paciente con trombosis vasculares o complicaciones del embarazo7.
En nuestro paciente encontramos anticuerpos anti-β2GPI de tipo IgA, que no están incluidos en los criterios diagnósticos de SAF, criterios que de todos modos tampoco cumpliría estrictamente, ya que solo mostró resultados positivos en una determinación.
La mayoría de los estudios8 sostienen que los aPL relacionados con infecciones son predominantemente IgM, mientras que Loizou et al.4 encontraron que, en los pacientes con lepra, los aCL IgA fueron los más frecuentes.
Por otro lado, existe cierta controversia, puesto que muchos autores refieren que los aPL que acompañan a las infecciones no se asocian a estados procoagulantes9. En las enfermedades autoinmunes (lupus eritematoso sistémico, síndrome antifosfolípido primario) la unión de los aPL a los fosfolípidos es reforzada por el cofactor β2GPI, mientras que los aPL no trombogénicos no requieren este cofactor para reforzar dicha unión. Se distinguieron así dos tipos de aPL, los «autoinmunes o dependientes de la β2GPI» y los «infecciosos o independientes de la β2GPI»; sin embargo, esta distinción no es absoluta.
Akerkar SM et al.10 describen un caso de gangrena asociada a la presencia de aCL IgM elevados en una paciente con lepra borderline tuberculoide, y Wallin L et al.11 recogen el caso de una paciente con lepra lepromatosa que presentó una obstrucción de las arterias peroneas secundaria a la presencia de aCL y AL, afirmando que pueden ser responsables e inducir eventos trombóticos.
La talidomida, usada como único agente en pacientes con enfermedades hematológicas, no ha sido relacionada con un mayor número de eventos trombóticos (tasa de TVP del 1%). El riesgo aumenta cuando se combina con otros fármacos, como dexametasona o quimioterápicos (aumentando la incidencia a un 10%) y especialmente en pacientes con enfermedades neoplásicas (carcinoma de células renales metastásico, síndrome mielodisplásico y mieloma múltiple)3. En todos los estudios el riesgo es mayor en los 2 primeros meses de tratamiento, como sucedió en nuestro caso. En un estudio12 de 25 pacientes con enfermedades dermatológicas tratados con talidomida (100-300mg/día) como único agente 5 (el 20%) presentaron TVP como complicación; 4 de ellos tenían diagnóstico de eritema nodoso leproso.
Encontramos además otros 4 casos13–16 de pacientes con eritema nodoso leproso tratados con talidomida en combinación con corticoides que presentaron una TVP como complicación, uno de los cuales recibía además ciclofosfamida15, mientras que otro desarrolló un tromboembolismo pulmonar16.
En nuestro paciente, que presentó aPL transitorios en probable relación con la enfermedad de Hansen, el uso de talidomida junto a prednisona pudo actuar como desencadenante del evento trombótico.
Como conclusión resaltamos la importancia de tener en cuenta los eventos tromboembólicos como posibles complicaciones graves en pacientes tratados con talidomida por enfermedades dermatológicas, especialmente cuando se asocia a glucocorticoides, quimioterápicos y/o otros factores trombofílicos predisponentes. Es necesario realizar más estudios para establecer guías de profilaxis de eventos tromboembólicos en estos pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Al Dr. Carlos Zarco Olivo.