Secukinumab (SEC) y ustekinumab (UST) son anticuerpos monoclonales altamente efectivos en el tratamiento de la psoriasis1, aunque en los estudios pivotales SEC presenta mayores tasas de eficacia2. Su mecanismo de acción difiere en la diana inhibida de la cascada inflamatoria. SEC bloquea la interleucina (IL)-17, mientras que UST bloquea IL-12 e IL-23. Los ensayos clínicos han mostrado la efectividad de SEC en pacientes previamente tratados con otros fármacos sistémicos, incluidos los anticuerpos monoclonales anti-TNF3. Sin embargo, hasta la fecha no existen publicaciones de su efectividad tras el fracaso terapéutico con UST.
En este trabajo nos propusimos evaluar la eficacia de SEC en pacientes con fracaso terapéutico primario o secundario a UST, definido como no alcanzar una reducción del 75% del Psoriasis Area and Severity Index (PASI) basal en la semana 12 o la pérdida de esta respuesta en las semanas siguientes, respectivamente. El objetivo primario fue evaluar en los pacientes tratados con SEC la obtención de la respuesta terapéutica PASI90 (reducción del 90% del PASI basal), la obtención de un Physician Global Assessment (PGA) menor o igual a 1 (ausente o mínimo) y un Dermatology Life Quality Index (DLQI) menor o igual a 5 en la semana 12. El objetivo secundario fue evaluar si esta respuesta se mantenía en la semana 24.
Se evaluaron retrospectivamente seis pacientes con psoriasis en placas sin adecuada respuesta al tratamiento previo con UST y que fueron tratados con SEC según ficha técnica (inducción completa y mantenimiento con 300mg/4semanas). Se midieron el PASI, el PGA y el DLQI basal y en las semanas 12 y 24.
Las características clínico-epidemiológicas se describen en la tabla 1. Se trata de seis pacientes varones de entre 32 y 61años de edad (mediana 51años) con psoriasis de más de 10años de evolución (mediana 16años).
Características clínico-epidemiológicas de los pacientes
| Sexo | Edad (años) | Peso (kg) | IMC (kg/m2) | Tabaquismo | Años con psoriasis | Artritis psoriásica | Comorbilidades | Tratamientos sistémicos previos |
|---|---|---|---|---|---|---|---|---|
| H | 46 | 107 | 32,0 | Sí | 26 | No | Colitis microscópica, enfermedad pulmonar obstructiva crónica, hipertensión arterial, insuficiencia cardíaca | CIC, MTX |
| H | 61 | 90 | 29,7 | No | 17 | No | No | CIC, MTX, ACT, anti-TNF |
| H | 58 | 61 | 25,1 | No | 16 | Sí | Hipertensión arterial, osteoporosis | Leflunomida, anti-TNF |
| H | 56 | 85 | 28,1 | No | 16 | No | No | CIC, MTX, ACT |
| H | 32 | 93 | 30,7 | Sí | 10 | No | No | MTX |
| H | 35 | 75 | 25,9 | Sí | 11 | No | Asma bronquial, vértigo posicional paroxístico | CIC |
ACT: acitretino; anti-TNF: anticuerpo monoclonal contra el factor de necrosis tumoral alfa; CIC: ciclosporina; H: hombre; MTX: metotrexato.
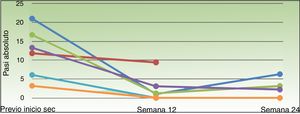
En la tabla 2 se recoge la respuesta a tratamiento con UST y SEC. Cuatro pacientes presentaron fallo primario a UST y dos, fallo secundario. Previo al inicio de SEC, el PASI variaba entre 3,2 y 21 (mediana 12,6), el PGA entre 3 y 4 (mediana 3) y el DLQI entre 2 y 25 (mediana 13,5). No se realizó tratamiento concomitante a la administración de SEC. Todos los pacientes presentaron una reducción de la actividad de la enfermedad a la semana 12 (fig. 1), con PASI90 en el 66,7% (4/6), PGA y DLQI ≤1 en el 83,3% (5/6). En un paciente se suspendió SEC por no alcanzar el PASI50. A la semana 24, el 33,3% (2/6) de los pacientes alcanzó el PASI90, el 66,6% (4/6) logró el PASI75, el 50% (3/6) tenía un PASI absoluto menor a 3 y el 66,6% (4/6), un PGA y DLQI ≤1. No se observaron efectos adversos significativos durante las 24 semanas de tratamiento con SEC.
Respuesta a secukinumab en pacientes con psoriasis en placas tras fracaso terapéutico con ustekinumab
| Tratamiento con UST | Previo inicio SEC | SEC semana 12 | SEC semana 24 | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| PASI previo | PASI semana 12 | Fallo a UST | PASI | DLQI | PGA | PASI | PASI90 | DLQI | PGA | PASI | PASI90 | DLQI | PGA |
| 39 | 11,9 | Primario* | 21 | 22 | 3 | 1 | Sí | 13 | 2 | 6.3 | No | 13 | 2 |
| 43,5 | 9,1 | Secundario** | 11,8 | 2 | 3 | 9,4 | No | 0 | 1 | NT | NT | NT | NT |
| 9,1 | 8,4 | Primario* | 16,7 | 8 | 4 | 1,2 | Sí | 0 | 1 | 3,2 | No | 1 | 1 |
| 22,1 | 0 | Secundario** | 13,3 | 25 | 3 | 3,1 | No | 1 | 1 | 2,2 | No | 1 | 0 |
| 18 | 4,8 | Primario* | 6,1 | 19 | 3 | 0 | Sí | 0 | 0 | 0 | Sí | 0 | 0 |
| 3,2 | 4 | Primario* | 3,2 | 4 | 3 | 0 | Sí | 0 | 0 | 0 | Sí | 0 | 0 |
DLQI: Dermatology Life Quality Index; NT: tratamiento suspendido por falta de respuesta (no alcanzó el PASI50 en la semana 12); PASI: Psoriasis Area and Severity Index; PGA: physician global assessment; SEC: secukinumab; UST: ustekinumab.
En esta serie de seis pacientes con fracaso terapéutico a UST se logró el objetivo primario con SEC en cuatro de ellos a la semana 12, y el objetivo secundario en solo dos pacientes a la semana 24, utilizando PASI90 como marcador de respuesta (siguiendo la tendencia actual hacia resultados más exigentes con los nuevos tratamientos biológicos). Sin embargo, la mayoría alcanzó el PASI75 y un PGA ≤1 a las semanas 12 y 24, siendo relevante la mejoría en la calidad de vida referida por los pacientes, con una reducción del DLQI en prácticamente la totalidad de ellos.
Los resultados obtenidos con SEC son inferiores a los publicados en estudios pivotales2,3, lo cual puede deberse a que en nuestro estudio se incluyeron pacientes con fracaso a múltiples tratamientos sistémicos previos, por lo que su enfermedad puede considerarse de difícil manejo. Otra explicación se basa en el mecanismo de acción, ya que UST, a través de la inhibición de la IL-23, inhibe indirectamente a la IL-174. Por lo tanto, los pacientes con fallo terapéutico a UST ya habían experimentado un cierto bloqueo de esta IL proinflamatoria (diana de SEC) sin obtener una respuesta clínica adecuada. Para avalar esta hipótesis, sería importante conocer la respuesta a SEC en pacientes con fracaso terapéutico a anti-TNF, fármacos que no inhiben la IL-17. Sin embargo, no hemos encontrado publicaciones que aborden esta situación clínica. En los ensayos clínicos pivotales de SEC, menos del 10% de los pacientes habían presentado previamente fracaso terapéutico a anti-TNF2,3, y lamentablemente no se realizó un análisis de este subgrupo.
Por último, no hemos identificado factores pronósticos de respuesta terapéutica a SEC tras el fracaso con UST.
Las principales fortalezas de este trabajo son la utilización de múltiples criterios de respuesta clínica (PASI, PGA y DLQI) previo y durante la terapia biológica, así como un seguimiento de la respuesta hasta las 24 semanas, y las principales limitaciones son su carácter retrospectivo y el pequeño número de pacientes incluidos.
En conclusión, SEC puede ser una alternativa terapéutica en pacientes con fallo al tratamiento a UST.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses relacionado con este trabajo.