La pustulosis exantemática aguda generalizada (PEAG) es una erupción cutánea poco frecuente (incidencia estimada entre 1-5 casos/millón/año1) generalmente inducida por medicamentos, recientemente revisada en esta Revista2. Consiste en la aparición rápida de numerosas pústulas no foliculares y estériles sobre un trasfondo de piel eritemato-edematosa, acompañado de fiebre y leucocitosis. La erupción es autolimitada una vez que se elimina el fármaco responsable. Son pocos los casos publicados de PEAG inducida por nistatina, un antifúngico de uso generalizado en todo el mundo y que suele ser bien tolerado debido a su mínima absorción sistémica. En todos los casos publicados las pruebas epicutáneas han demostrado ser eficaces para confirmar el diagnóstico de esta toxicodermia.
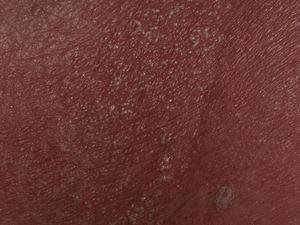
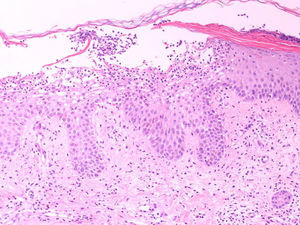
Una mujer de 83 años de edad, con antecedentes de HTA, diabetes mellitus y alergia a sulfamidas ingresó en nuestro hospital por presentar un cuadro de fiebre, malestar y rash cutáneo de una semana de evolución. Las lesiones cutáneas habían aparecido 48h después de haber iniciado tratamiento con enjuagues de nistatina por candidiasis oral como única modificación en sus tratamientos habituales. Al ingreso, la paciente se encontraba febril (38,3°C) y eritrodérmica, con la piel cubierta por numerosas pústulas de 1-3mm de diámetro no centradas por folículos, más evidentes en el tronco y la raíz de las extremidades (fig. 1). No había afectación de las mucosas y el signo de Nikolsky era negativo. En la analítica destacaba la presencia de leucocitosis (18.400/μl) con neutrofilia (88,9%) sin eosinofilia, además de la elevación de los reactantes de fase aguda (VSG: 63mm; PCR: 127mg/dl). Los hemocultivos, los cultivos de 2 de las pústulas y las serologías víricas efectuadas (rubeola, CMV, Epstein-Barr, parvovirus B19, enterovirus, varicela-zoster y VIH) fueron negativos. La biopsia de una de las pústulas mostró una dermatitis espongiforme con formación de pústulas subcórneas y un infiltrado dérmico rico en polimorfonucleares y eosinófilos (fig. 2), además de negatividad para tinción PAS. Se suspendieron los enjuagues con nistatina y, tras una corta tanda de corticoides por vía oral, la paciente fue dada de alta al cabo de 13 días con buen estado general, mostrando únicamente eritema y mínima descamación residuales.
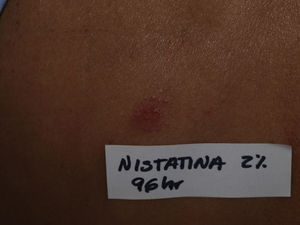
Seis meses después se realizaron pruebas epicutáneas en condiciones habituales con la serie estándar del Grupo Español de Dermatitis de Contacto y Alergia Cutánea (GEIDAC) y nistatina 2% vas (AllergEAZE Brial Allergen GmbH, Alemania). Los resultados mostraron únicamente un parche positivo a la nistatina a las 48 y 96h (fig. 3); el estudio posterior con nistatina 2% en vaselina en 11 controles fue negativo. La reacción producida por el parche en nuestra paciente reproducía tanto clínica como histológicamente la toxicodermia desarrollada inicialmente, confirmando el diagnóstico de PEAG inducida por nistatina.
La nistatina es un fármaco fungistático del grupo de los poliénicos, que se aísla a partir de Streptomyces noursei; se trata de una sustancia ampliamente utilizada en todo el mundo debido a su eficacia anti-Candida y a su buena tolerancia, siendo las candidiasis orofaríngeas su principal indicación en forma de enjuagues orales. Los episodios de toxicodermia debidos a este fármaco son poco frecuentes, ya que apenas sufre absorción intestinal tras su ingesta; por ello, las reacciones sistémicas que puede provocar son excepcionales. En nuestro caso el cuadro clínico (incluidas la imputabilidad cronológica y la evolución de las lesiones) y los hallazgos histopatológicos fueron característicos de PEAG según los criterios actualmente vigentes2.
En la revisión de la literatura hemos encontrado 5 casos previos de PEAG inducidos por nistatina, ninguno de ellos en nuestro país, todos clínicamente superponibles a nuestro caso, y también confirmados mediante diversos tipos de pruebas (epicutáneas, tests intradérmicos)3–6. Además de la PEAG, en todos aquellos casos publicados en que se describen de forma aislada otros tipos de toxicodermias inducidas por nistatina oral (dermatitis generalizada7, erupción maculopapular8, erupción generalizada con angioedema9, rash maculopapular generalizado10), las pruebas epicutáneas realizadas a diferentes concentraciones —siempre superiores al 10%— también mostraron invariablemente resultados positivos. En nuestro caso hemos demostrado que un parche con nistatina al 2% es suficiente para llegar al diagnóstico. En general, se sabe que la sensibilidad de las pruebas epicutáneas en el estudio de casos de PEAG es cercana al 50% (80% para algunos antibióticos), porcentaje superior al encontrado en otros tipos de toxicodermias incluido el síndrome de Stevens-Johnson2.
La suma de todas estas evidencias confirma la participación de linfocitos T fármaco-específicos en los mecanismos fisiopatológicos de la enfermedad, representando la PEAG una forma peculiar de reacción de hipersensibilidad tardía.
En conclusión, la PEAG debería estar incluida en el diagnóstico diferencial de las erupciones cutáneas pustulosas en aquellos pacientes en tratamiento con nistatina oral, a pesar de su mínima absorción digestiva. Tanto en el caso de PEAG como en otras toxicodermias inducidas por este fármaco, las pruebas epicutáneas tienen un valor diagnóstico definitivo. En nuestro caso obtuvimos resultados positivos con el fármaco diluido a concentraciones inferiores a las referenciadas previamente en la literatura.