A pesar de la eficacia de los inhibidores del factor de necrosis tumoral alfa (TNF-α) en el manejo de la psoriasis moderada-grave, se han descrito algunos efectos adversos, relacionados con la psoriasis, en pacientes en tratamiento con dichos agentes biológicos. Los más comúnmente descritos son la psoriasis de nueva aparición en pacientes sin psoriasis previa, y el agravamiento o modificación de la morfología de una psoriasis ya conocida. Un porcentaje importante de las psoriasis de nueva aparición es en forma de psoriasis pustulosa, principalmente con afectación palmoplantar1,2, mientras que la psoriasis guttata es la más frecuente en pacientes con psoriasis previa3,4. Describimos un paciente con psoriasis en placas en tratamiento con etanercept que presentó una exacerbación con cambio de morfología de su psoriasis a una forma pustulosa generalizada, inmediatamente después de realizar una prueba de la tuberculina (PPD), sugiriendo una asociación entre las dos circunstancias.
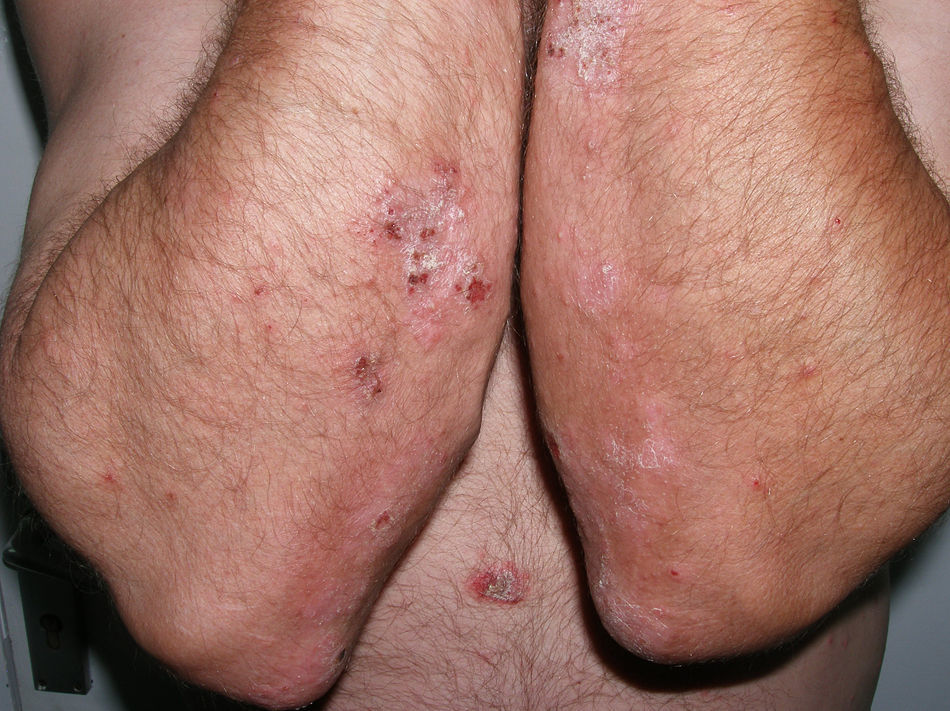
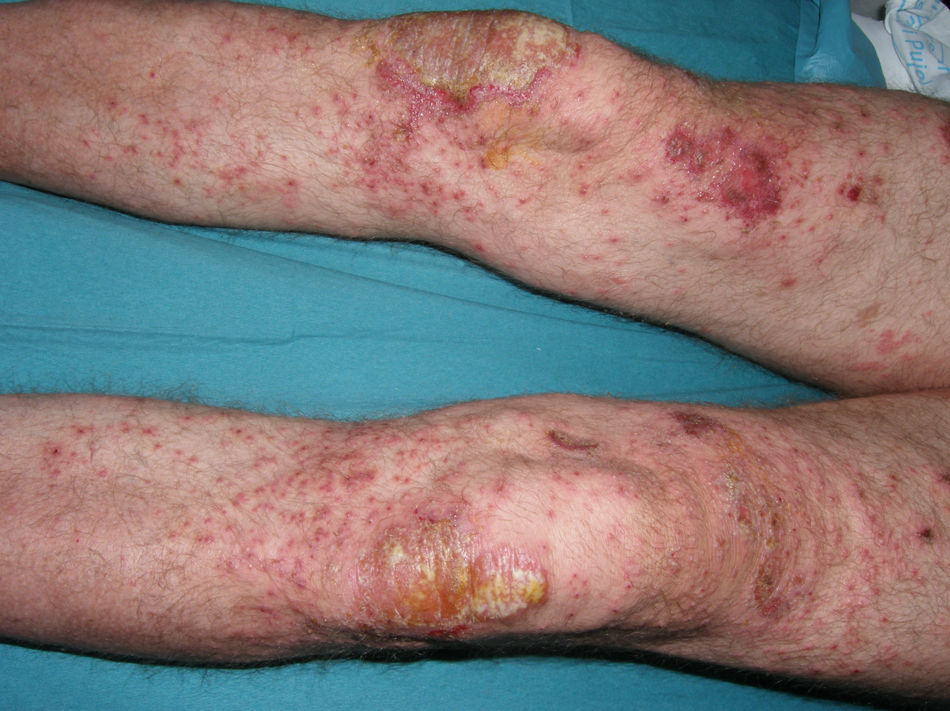
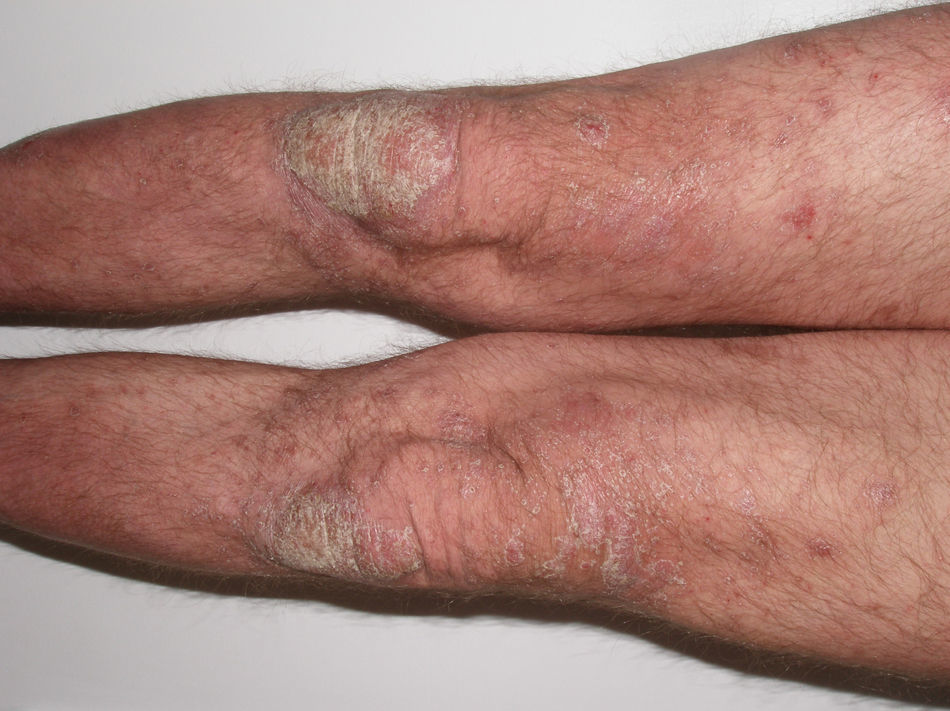
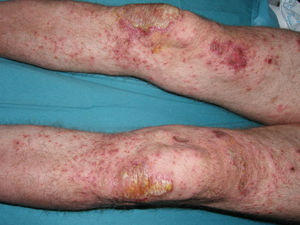
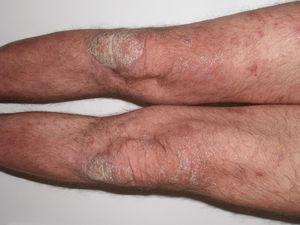
Varón de 49 años con una historia de psoriasis en placas de 29 años de evolución que había tratado previamente con corticoides tópicos y que realizó 2 años de tratamiento con acitretino que se retiró por dislipemia. En el año 2005, con un PASI de 19,8, empezó tratamiento con etanercept (25mg dos veces por semana), con una excelente respuesta durante 1 año. Cuatro meses después de la interrupción del tratamiento con etanercept presentó una recaída (PASI 22), por lo que se optó por reiniciar el tratamiento con etanercept 50mg dos veces por semana durante las primeras 12 semanas, con una dosis de mantenimiento posterior de 25mg dos veces por semana. Durante los 3 años de tratamiento con etanercept, el paciente permaneció bien controlado, con un PASI medio de 3. Sin embargo, 24 horas después de la realización del PPD anual de rutina, aparecieron algunas pústulas sobre las placas residuales de psoriasis (fig. 1); 48 horas más tarde, la erupción evolucionó hacia una psoriasis pustulosa generalizada que afectaba principalmente las extremidades (fig. 2). Los cultivos bacterianos fueron negativos y la histología compatible con el diagnóstico de psoriasis pustulosa. Ante la sospecha de una reacción paradójica relacionada con etanercept, se suspendió el fármaco y se inició ciclosporina (4mg/kg/d). El brote fue controlado después de dos semanas (fig. 3). Posteriormente, se inició tratamiento con ustekinumab, mientras se disminuía progresivamente la dosis de ciclosporina.
La psoriasis puede ser paradójicamente agravada o inducida por los 3 anti-TNF disponibles2,5. Sin embargo, mientras que los anticuerpos monoclonales (infliximab y adalimumab) principalmente inducen la aparición de un primer brote de psoriasis, etanercept se relaciona de forma más habitual con exacerbaciones de psoriasis previas6. Los mecanismos responsables de estos efectos paradójicos son desconocidos. En la psoriasis pustulosa palmoplantar, no se han identificado factores desencadenantes y se postula un posible papel causal de los inhibidores del TNF-α. La psoriasis pustulosa generalizada se ha relacionado con algunos factores como: el embarazo, infecciones, irritación cutánea importante como consecuencia de medicación tópica, o con algunos fármacos (litio, salicilatos, indometacina y algunos betabloqueantes). Por el contrario, las erupciones pustulosas generalizadas en pacientes con psoriasis en placas estables se han relacionado con la luz ultravioleta, infecciones y la dermatitis alérgica de contacto7,8, pero no se ha descrito en la literatura en pacientes con psoriasis en tratamiento con anti TNF-α. En nuestro caso el desarrollo súbito del brote sólo 24 horas después de la realización del PPD y tras un blanqueamiento continuado en los últimos 3 años de tratamiento con etanercept sugiere un efecto sinérgico entre el fármaco biológico y la prueba diagnóstica. El desarrollo de una psoriasis pustulosa generalizada como complicación del PPD no está recogida en la literatura, pero existe un caso con antecedentes de psoriasis en placas, que no estaba recibiendo ningún tratamiento sistémico en el momento de la prueba de la tuberculina, que presentó una exacerbación pustulosa después de la realización de dicha prueba9. Por otra parte, el brote pustuloso de nuestro paciente podría ser considerado como una presentación atípica de una pustulosis aguda exantemática generalizada secundaria a la prueba de la tuberculina. Sin embargo, tanto los hallazgos histológicos como la convivencia de algunas lesiones típicas de psoriasis en placas con la erupción pustulosa hacen poco probable esta opción. Así, aunque la evolución cronológica es compatible con una relación de causalidad directa entre el PPD y el brote, la explicación de este fenómeno sigue siendo especulativa. Posiblemente, la prueba de la tuberculina actuó como un desencadenante traumático o infeccioso, que fue capaz de activar la inmunidad innata, aumentando la producción de TNF-α por parte de las células dendríticas plasmocitoides y estimulando la activación local y la expansión de los linfocitos T patogénicos que condujeron al desarrollo del brote. Dado que el tratamiento con el mismo agente (o uno de la misma familia)5 podría causar la persistencia del brote, se decidió cambiar a otro tratamiento con un mecanismo de acción diferente que consiguió un control de las lesiones en pocos días. En conclusión, nuestro caso amplía las complicaciones que podemos ver en pacientes con psoriasis en tratamiento con etanercept en relación con la prueba de la tuberculina.
Conflicto de interesesEl Dr. Carlos Ferrándiz y el Dr. José Manuel Carrascosa han percibido honorarios como consultores y/o ponentes patrocinados por Wyeth, Abbott, Shering-Plough y Janssen-Cilag.
Los demás autores declaran no tener ningún conflicto de intereses.