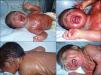
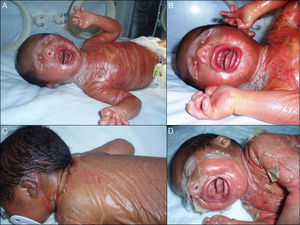
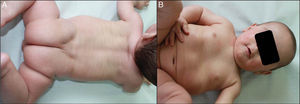
Presentamos el caso de un recién nacido pretérmino a las 36 semanas de gestación, sin antecedentes familiares de interés, diagnosticado intraútero de eclabium y ectropión, con sospecha diagnóstica de feto arlequín. Desde el nacimiento presenta una membrana que recubre a modo de coraza la práctica totalidad de la superficie corporal (fig. 1A) además de ectropión, eclabium, manos en garra (fig. 1B) y retracción de ambos pabellones auriculares (fig. 1C). Los primeros días de vida la membrana se fue fisurando y posteriormente presentó descamación en grandes láminas (fig. 1D), que dejaba una piel eritematosa y exudativa de base, retirándose dicha membrana hacia la segunda semana de vida. La evolución a lo largo de los meses fue muy buena, con piel de aspecto prácticamente normal al año de vida (fig. 2A), presentando únicamente leve eritema y descamación en ambas mejillas (fig. 2B) y mínima hiperqueratosis en los codos y las rodillas, diagnosticándose de bebé colodión autorresolutivo. Se realizó estudio genético que diagnosticó al niño como portador homocigoto de una mutación en el gen ALOX12B, que da lugar a la pérdida de un aminoácido, la glutamina, en la posición 136 del exón 3, y a los padres como portadores heterocigotos sanos de esta mutación. Actualmente el paciente tiene 2 años y no tiene lesiones, salvo las comentadas previamente.
A. Membrana brillante que cubre a modo de coraza la práctica totalidad de la superficie corporal. B. Ectropión, eclabium y manos en garra. C. Retracción del pabellón auricular izquierdo y membrana en la espalda con fisura en la zona central dorsal. D. Descamación en grandes láminas que afecta a toda la membrana.
El bebé colodión (BC) nace con una membrana brillante, transparente y tirante similar a una coraza que cubre toda la superficie corporal y recuerda a una envoltura de celofán1,2. Puede provocar ectropión, eclabium, pseudocontracturas, ausencia de cejas, pelo ralo e hipoplasia de cartílago nasal y auricular1,2. Es una membrana inelástica, por lo que desde el nacimiento con la respiración y los movimientos del niño se va fisurando, provocando una descamación en grandes láminas, retirándose totalmente a las 2-4 semanas de vida3. Es una entidad infrecuente, con una incidencia entre 1/50.000 o 100.000 nacimientos, y constituye la presentación clínica inicial de diversas enfermedades genéticas, aunque la mayoría pertenecen a las ictiosis congénitas autosómicas recesivas (ICAR)4. El BC puede desarrollar en el futuro fenotipos muy diversos, desde piel con apariencia normal hasta ictiosis muy grave, aunque la mayoría de ellos son diagnosticados de ictiosis lamelar o eritrodermia ictiosiforme congénita1,3. El BC autorresolutivo es una de las formas menores de las ICAR que podemos encontrar4. Entre el 10-24% de los BC son autorresolutivos, que son aquellos que muestran una resolución espontánea de su problema y presentan en la edad adulta una piel normal o signos leves de ictiosis1,5. Respecto a la epidemiología de las ICAR, en España, Hernández-Martín et al. publicaron un estudio donde se estimaba la prevalencia de ICAR en aproximadamente 16 casos por millón, con una prevalencia de BC autorresolutivo del 4,2% respecto al total de las ICAR6.
Se ha asociado el BC autorresolutivo con mutaciones en los genes TGM1, ALOXE3 o ALOX12B1,3–5,7. Nuestro paciente fue diagnosticado como portador homocigoto de una mutación en el gen ALOX12B que no había sido descrita previamente en la literatura. El gen ALOX12B se identificó por primera vez en el año 2002, está conformado por 15 exones y codifica las LOX epidérmicas eLOX-3 y 12R-LOX8. Su expresión predominante en las capas suprabasales de la epidermis apoya su papel en las fases avanzadas de la diferenciación epidérmica y participación en el procesamiento de los cuerpos lamelares. Además, actúa en la vía de las hepoxilinas, por lo que se cree que pueda participar en la formación de los lípidos intercelulares de la capa córnea o actuar como señales para promover la diferenciación de los queratinocitos8.
Desde la identificación del gen ALOX12B se han descrito más de 30 mutaciones, y se le considera junto con el gen ALOXE3 responsables del 14-17% de las ICAR y del 72,2% de los BC autorresolutivos8. El mecanismo concreto que conduce a la alteración de la permeabilidad de la piel en los pacientes con alteraciones en el gen ALOX12B y el motivo de la aparición de las lesiones del período neonatal en los BCAR no ha sido completamente aclarado7. Se ha especulado que estas mutaciones en ALOX12B reducen la actividad enzimática en el útero, pero no en vivo8. En el útero la presión hidrostática es elevada, y la quelación de moléculas de agua convierte la enzima mutada en una conformación inactiva. Después del nacimiento, tras bajar la presión, la enzima vuelve a su forma activa e incrementa su actividad hasta niveles suficientes para mantener el fenotipo normal o mínimamente alterado8,9.
Los BC son habitualmente prematuros, con morbimortalidad perinatal aumentada. Entre las complicaciones que se pueden producir destaca un aumento de la pérdida de agua transepidérmica hasta 7 veces más de lo que ocurre en la piel sana, inestabilidad en la temperatura, hipotermia, deshidratación hipernatrémica, dificultad en la alimentación, hipohidrosis, infecciones cutáneas o sistémicas, ectropión, queratitis y obstrucción del canal auditivo1,2,5,10. Además, la membrana puede provocar compresión mecánica que produzca isquemia en EE distales2.
El manejo del BC debe realizarse en una UCI neonatal, con un nivel de humedad en la incubadora de al menos el 60%, con monitorización de la temperatura y los electrolitos, soporte calórico, así como sonda nasogástrica si la alimentación está comprometida. Aunque los antibióticos profilácticos no están recomendados, sí debe realizarse una vigilancia muy estrecha para instaurar antibioterapia de forma temprana en caso de que existan signos de infección2. La aplicación de emolientes disminuye la pérdida de agua transepidérmica, y por tanto las complicaciones que se derivan de ella, aunque previo a su aplicación debe realizarse una adecuada higiene y lavado de manos del personal sanitario para disminuir el riesgo de infección que en algunos artículos se ha relacionado con la aplicación de emolientes2.
La mortalidad actual en el BC es de aproximadamente el 5%, mientras que hacia el año 1960 se estimaba en torno al 50%2,10. Se cree que la gran mejoría del pronóstico se debe a los avances en los cuidados neonatales actuales2.
Este nuevo caso de BC destaca por su evolución hacia BC autorresolutivo, entidad muy infrecuente, que supone un reto no desde el punto de vista diagnóstico, sino por la dificultad para establecer un pronóstico a largo plazo de manera inmediata, ya que no se puede prever si el BC acabará siendo un BCA o por el contrario desarrollará una enfermedad muy severa. Además, en nuestro paciente el estudio genético realizado detectó una mutación en el gen ALOX12B que no había sido descrita previamente en la literatura como mutación causal confirmada de BC autorresolutivo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.