El imiquimod es un excelente tratamiento para las queratosis actínicas, sin embargo, su pauta prolongada de 4 semanas y la reacción local que produce pueden limitar su utilización. Los objetivos del estudio son demostrar la eficacia del imiquimod al 5% para las queratosis actínicas aplicado en una pauta continuada de 12 días y correlacionar el grado de reacción local con la eficacia.
Pacientes y métodosSe incluyeron pacientes con al menos 8 queratosis actínicas que se trataron con imiquimod en crema al 5% durante 12 días seguidos. Se evaluó la reacción local como leve, moderada o intensa. El estudio estadístico de la correlación entre la reacción local y la respuesta clínica se realizó con la prueba χ2 de Pearson y el test de correlación rho de Spearman.
ResultadosUn total de 65 pacientes completaron el estudio. Se obtuvo un 52,3% de respuestas completas y un 75,4% de respuestas parciales. Encontramos una asociación estadísticamente significativa entre el grado de reacción local y la respuesta al tratamiento tanto en la prueba χ2 de Pearson como en el test de correlación rho de Spearman.
ConclusionesLa pauta continuada de imiquimod al 5% aplicado durante 12 días es eficaz para el tratamiento de las queratosis actínicas. El grado de reacción local durante el tratamiento se correlaciona con la respuesta clínica.
Imiquimod is an excellent option for patients with actinic keratosis, although its use may be limited by the long course of treatment required (4 weeks) and the likelihood of local skin reactions. The objectives of the present study were to demonstrate the effectiveness of a 12-day course of imiquimod 5% for the treatment of actinic keratosis and to examine the association between treatment effectiveness and severity of local reactions.
Patients and methodsWe included patients with at least 8 actinic keratoses treated with imiquimod 5% cream for 12 consecutive days. Local reactions were classified as mild, moderate, or severe. The statistical analysis of the association between local reactions and clinical response was based on the Pearson χ2 test and the Spearman rank correlation test.
ResultsSixty-five patients completed the study. Complete response was recorded in 52.3% and partial response in 75.4%. We found a statistically significant association between severity of the local reaction and response to treatment in both the Pearson χ2 test and the Spearman rank correlation test.
ConclusionsA 12-day course of imiquimod 5% proved effective for the treatment of actinic keratosis. Severity of local reactions during treatment was correlated with clinical response.
Las queratosis actínicas (QA) constituyen una patología de interés creciente en Dermatología. Se definen como una neoplasia intraepidérmica que aparece en la piel dañada por el sol y caracterizada histológicamente por una atipia de los queratinocitos1. Para su tratamiento, la crioterapia es el método más frecuentemente utilizado por la mayoría de dermatólogos cuando se tratan lesiones aisladas. Para los pacientes con múltiples QA, o en aquellos que presenten un campo de cancerización, se emplean los llamados tratamientos de campo. Estos son capaces de eliminar tanto las lesiones clínicamente visibles como aquellas subclínicas correspondientes a displasia de queratinocitos2,3. El imiquimod es uno de los tratamientos de campo de los que se tiene una mayor experiencia y conocimiento. La concentración más empleada es de 5% y el esquema de tratamiento más frecuentemente utilizado es de 3 veces a la semana durante 4 semanas. Su complejo mecanismo de acción antitumoral combina sinérgicamente la liberación de citoquinas proinflamatorias, la actividad antiangiogénica y la estimulación de la apoptosis4. El principal efecto secundario que habitualmente aparece durante el tratamiento con imiquimod es una reacción cutánea local en forma de eritema, edema, prurito, erosión, ulceración, costras y exudación en diferentes grados, que se inicia a los pocos días de comenzar el tratamiento, alcanza su máxima intensidad a las 4 semanas y se resuelve en 2 semanas aproximadamente tras finalizar el tratamiento. La gravedad de esta reacción local parece ser dosisdependiente5 y, teniendo en cuenta su mecanismo de acción, podría asociarse a una mejor respuesta. También se pueden referir durante el tratamiento con imiquimod la aparición de efectos secundarios sistémicos debido a la absorción del producto y a la consecuente liberación de interleucinas y sobre todo de interferón. Estos cuadros sistémicos consisten en síntomas pseudogripales, cefalea, náuseas, mialgias o artralgias5, y aunque están bien reconocidos y asociados al tratamiento, parecen ser poco frecuentes, del 0,46 al 6% de los pacientes según las series que lo refieren6-8. Todos estos efectos secundarios, locales y sistémicos, pueden condicionar la prescripción de este medicamento y también pueden influir en la correcta cumplimentación por parte del paciente.
Este trabajo se ha diseñado sobre la hipótesis de que concentrando la pauta de imiquimod debería mantenerse la misma eficacia si se desarrolla una reacción local adecuada.
El objetivo principal del estudio es demostrar que la aplicación diaria de imiquimod 5% en crema durante 12 días consecutivos es eficaz para el tratamiento de las QA. El objetivo secundario es estudiar los efectos secundarios locales y sistémicos y realizar una correlación entre el grado de reacción local y la respuesta al tratamiento.
Material y métodosSe diseñó un ensayo clínico no controlado en el que se incluyeron pacientes con QA para recibir tratamiento con imiquimod en crema al 5%. Los pacientes elegibles debían presentar un área de 25cm2 aproximadamente, en la cara o el cuero cabelludo, con al menos 8 QA no hipertróficas. Los pacientes fueron incluidos en el estudio desde julio de 2015 hasta octubre de 2016.
Se descartaron como zonas de tratamiento la zona perioral y la periocular. Se excluyeron a los pacientes que habían sido tratados en la zona elegida con crioterapia en los 3 meses anteriores a incluirse en el estudio o con un tratamiento de campo en la misma zona (imiquimod, terapia fotodinámica, ingenol mebutato, 5-fluoracilo o diclofenaco) en los 6 meses anteriores. También se excluyeron a los pacientes con tratamiento inmunosupresor y pacientes con enfermedades hereditarias que predisponen al cáncer cutáneo (síndrome de Gorlin, xeroderma pigmentoso).
El estudio recibió la aprobación del Comité Ético del Instituto Valenciano de Oncología y se obtuvo el consentimiento informado por escrito de todos los pacientes participantes.
En la visita de inicio a los pacientes se les realizaba una fotografía de la zona de piel seleccionada para el tratamiento, se contaban las QA y se identificaban en la fotografía. Se les pautaba imiquimod 5% en crema (Imunocare®, Laboratorios IFC, Santander, España) y se les indicaba que debían aplicar un sobre del producto en la zona de tratamiento, por la noche, durante 12 días consecutivos.
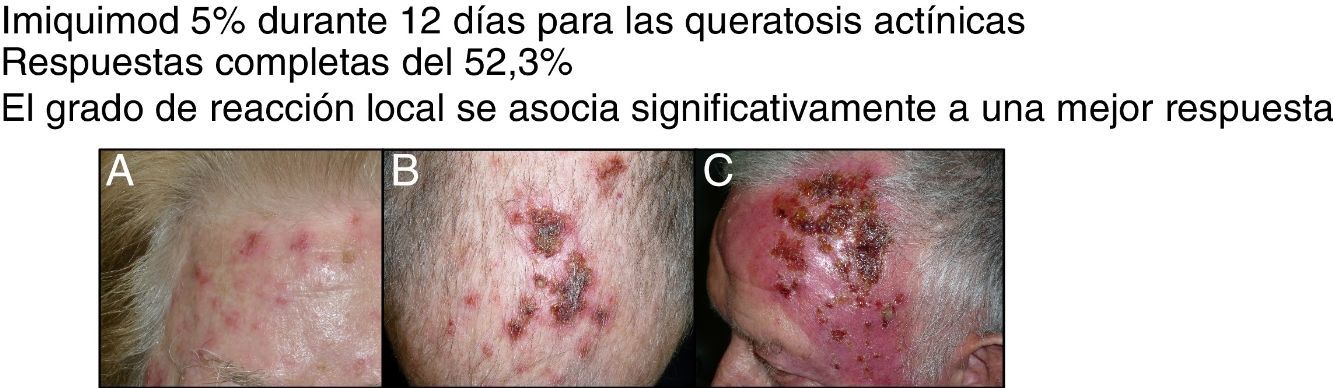
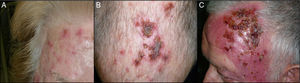
La visita de fin de tratamiento se realizaba de uno a 5 días después de completar los 12 días de tratamiento. Se preguntaba al paciente el número total de sobres que había aplicado. En esta visita se evaluaba la reacción local de la piel, que se clasificó como ausente (1), leve (2), moderada (3) o intensa (4) (fig. 1). La reacción local leve se definió como la aparición de un ligero eritema y costras limitado de forma puntual a las lesiones de QA. La reacción local moderada se definió como la presencia de eritema, edema, ulceración y costras en menos del 50% de la zona de tratamiento. La reacción local intensa se definió como la existencia de eritema, edema, ulceración, costras y exudación que ocupaban prácticamente toda la zona de tratamiento e incluso fuera de la zona de tratamiento. En esta visita, además, se le preguntaba al paciente si había desarrollado algún síntoma sistémico asociado al tratamiento como febrícula, astenia, cefalea, náuseas, mialgias o artralgias, en cuyo caso se clasificaba como reacción sistémica presente. La visita del fin de estudio se realizaba aproximadamente un mes después de la visita de fin de tratamiento. En esta visita se evaluaba la eficacia del tratamiento mediante la respuesta clínica completa (RCC) y la respuesta clínica parcial (RCP). Esta respuesta fue definida con el porcentaje de QA resueltas en esta visita y calculado como el cociente entre las QA cuantificadas tras el tratamiento y las QA cuantificadas antes del tratamiento. La RCC se definió como la ausencia total de QA o de lesiones sospechosas de QA desde el punto de vista clínico, confirmada mediante evaluación visual y al tacto, y la RCP se definió como la reducción de más del 75% de las QA iniciales evaluada mediante exploración visual y al tacto9.
La relación entre la reacción local y la respuesta completa al tratamiento se evaluó mediante tablas de contingencia y las diferencias de distribución se compararon mediante la prueba de χ2de Pearson. Además, el valor del porcentaje de QA resueltas se correlacionó con el grado de reacción local mediante la prueba rho de Spearman. El nivel de significación estadística se estableció para valores de p<0,05. Se empleó el paquete estadístico SPSS versión 15.0.
ResultadosSe incluyeron en el estudio 71 pacientes. Las características de los pacientes se detallan en la tabla 1. La edad media fue de 77,8 años, con un predomino claro del sexo masculino, 65 hombres (91,5%) frente a 6 mujeres (8,5%). La mediana de QA fue de 12 (8-30). La localización más frecuente fue el cuero cabelludo (29 casos, 40,8%).
Características de los pacientes (n=71)
| Edad | -Media: 77,8 (DE: 12,4) -Mediana: 78 (Intv. Interc.: 70-82) |
| Sexo | -Hombres: 65 (91,5%) -Mujeres: 6 (8,5%) |
| Localización | -Cuero cabelludo 29 (40,8%) -Frente/sien: 25 (35,2%) -Cara: 17 (23,9%) |
| N.o QA | -Media: 13,2 -Mediana: 12 |
DE: desviación estándar; Intv. Interc.: intervalo intercuartílico.
Las visitas de fin de tratamiento y fin de estudio las completaron correctamente 65 pacientes.
En la visita fin de tratamiento, de los 65 pacientes, 59 aplicaron los 12 sobres, los 6 pacientes restantes suspendieron el tratamiento a causa de los efectos secundarios. Un paciente aplicó 11 sobres, 2 pacientes usaron 10 sobres, un paciente 8 sobres y 2 pacientes aplicaron solo 7 sobres. La tabla 2 muestra los resultados de la reacción local. Todos los pacientes desarrollaron algún grado de reacción local. Un 58,5% tuvo una reacción local intensa. Los 6 pacientes que aplicaron menos de 12 sobres desarrollaron una reacción local intensa.
En cuanto a los síntomas sistémicos, estos lo refirieron 13 pacientes, lo que supone el 20% de la serie, la mayoría de ellos en forma de mal estar general, febrícula y síntomas pseudogripales. De estos 13, solo 3 interrumpieron el tratamiento antes de los 12 días. Dos pacientes aplicaron 7 sobres y uno aplicó el imiquimod durante 8 días seguidos. De estos casos que desarrollaron síntomas sistémicos, en 11 fue una reacción local intensa y en 2 fue moderada.
En cuanto a la eficacia del tratamiento con imiquimod al 5% con la pauta continuada de 12 días seguidos obtuvimos una RCC en 34 pacientes (52,3%) y RCP en 49 (75,4%).
Los resultados de la relación entre la reacción local y la respuesta completa al tratamiento se exponen en la tabla 3. De los 38 pacientes que desarrollaron una reacción local intensa, 27 (71,1%) obtuvieron una RCC; sin embargo, la mayoría de los pacientes con una reacción local leve o moderada no tuvieron RCC. Estas diferencias fueron estadísticamente significativas. En la prueba rho de Spearman obtuvimos un coeficiente de correlación de 0,557 (p>0,0001), por lo tanto existe una correlación positiva moderada entre la reacción local y la respuesta al tratamiento: a mayor reacción local, mayor respuesta al tratamiento. Entre los 38 pacientes que desarrollaron una reacción local intensa se encuentran los 6 que habían abandonado el tratamiento antes de los 12 días. De ellos, 5 (83%) obtuvieron RCC. De los otros 32 casos con reacción local intensa hubo 22 con RCC (69%).
DiscusiónEl imiquimod al 5% es un tratamiento utilizado desde hace casi 20 años para las QA. Es de todos conocida la reacción local que produce, pero cuenta con el aval de multitud de estudios y experiencia que confirman su seguridad y eficacia. Sin embargo, esta reacción local, junto con lo prolongado que puede suponer las 4 semanas que habitualmente dura el tratamiento, pueden condicionar su prescripción. Según nuestros resultados, la pauta de 12 días seguidos de imiquimod al 5% en crema es eficaz para las QA. Hemos obtenido un 52,3% de pacientes con todas sus QA resueltas con esta pauta continuada y en 49 pacientes (75,4%) se curaron más del 75% de sus QA. Estos resultados son similares a los obtenidos en el metaanálisis de Hadley et al. en el que se incluyeron 1.293 pacientes con QA10 y donde se obtuvieron un 50% de RCC y un 65% de RCP. Además, comparando estos resultados con los obtenidos por otros tratamientos tópicos para las QA en los que se obtienen RCC del 42,2% con ingenol mebutato11 y del 39,6% de RCC con diclofenaco12, la pauta continuada de imiquimod parece muy eficaz. Hay dos motivos por los que nuestros resultados parecen especialmente interesantes. En primer lugar, los trabajos de referencia de imiquimod para las QA que se incluyen en los dos metaanálisis publicados tienen unas pautas de administración de 12 a 16 semanas10,13, tiempo significativamente superior al empleado en este trabajo. En varios estudios en los que emplean el imiquimod 3 veces a la semana durante 4 semanas (pauta que figura actualmente en la ficha técnica del producto) se obtienen unas RCC del 26,8 al 40,5%8,9,14,15, porcentajes inferiores a los obtenidos en el actual trabajo. Por otro lado, los pacientes que incluimos en este estudio tenían un número de QA muy superior a la mayoría de trabajos de imiquimod6,14-17 y al de otros tratamientos tópicos para QA con criterios de inclusión poco ambiciosos, con pacientes de solamente 5 QA11,18. Por todo ello, esta pauta continuada de imiquimod sería recomendable en primer lugar por la eficacia que parece tener y además porque disminuye en gran medida el tiempo de aplicación y la resolución de la reacción local, que con la pauta tradicional se puede prolongar hasta 2 meses desde el inicio del tratamiento.
Hay muchos trabajos en la literatura que sugieren que el grado de reacción local producido por imiquimod es dosisdependiente y que parece asociarse a una mejor respuesta13,19-21. Sin embargo, se trata de observaciones y hallazgos comentados en la discusión y que no formaban parte de los objetivos de dichos estudios. En este contexto y basados en nuestra experiencia desarrollamos el segundo objetivo de este trabajo, en el que se ha podido demostrar de manera estadísticamente significativa, tanto por una tabla de contingencia de χ2 de Pearson como por el test de correlación rho de Spearman, que el grado de reacción local durante el tratamiento con imiquimod puede predecir la respuesta. Aquellos pacientes con un mayor grado de reacción, que habitualmente vienen a la consulta, serán precisamente los que mejor respondan y esto puede ayudar en la consulta para tratar de convencerles de que su tratamiento va a ser un éxito precisamente por esa reacción.
Por otra parte, hemos encontrado en nuestros resultados muchos pacientes (20%) que refirieron síntomas sistémicos. Según lo que hemos encontrado en la literatura, el porcentaje de pacientes con síntomas sistémicos sería inferior al 6%, sobre todo en forma de cefalea. Estos efectos secundarios probablemente son debidos a la absorción sistémica del fármaco y a la liberación de interferón y parece que, una vez más, son dosisdependientes. En aquellos pacientes con una mayor reacción local el hecho de continuar aplicando el tratamiento sobre la piel inflamada y erosionada produce una mayor absorción y una mayor probabilidad de presentar síntomas sistémicos7. En concreto, en nuestros 13 pacientes con síntomas sistémicos, 11 habían también desarrollado una reacción local intensa, lo que va a favor de esta hipótesis. Por todo ello, parece sensato proponer el empleo de imiquimod para las QA hasta alcanzar una reacción local que asegure la eficacia del tratamiento, pero sin necesidad de prolongar dicha reacción para evitar así los síntomas sistémicos. En este sentido, Dirschka et al. proponen personalizar el tratamiento con imiquimod al 3,75% según la reacción local del paciente22, y en un trabajo australiano obtienen muy buenos resultados con una pauta de imiquimod en oclusión durante solamente una semana en pacientes con cáncer de piel no melanoma23. Por otro lado, según nuestros resultados, en los que hemos encontrado un 9% de abandonos, un 58% de pacientes con una reacción local intensa y un 20% de pacientes con síntomas sistémicos, podríamos concluir que aunque la eficacia de esta nueva pauta parece superior a la convencional, puede ser a expensas de una menor tolerancia. Además, en esta línea, es interesante observar que entre los pacientes con reacción local intensa, se encuentran los 6 que abandonaron el tratamiento antes de los 12 días y de estos se obtuvo RCC en 5, lo que supone un 83% frente al 69% de RCC entre los otros pacientes con reacción local intensa. Por lo tanto, puede ser interesante el empleo de imiquimod hasta alcanzar un grado de reacción local que asegure la eficacia del tratamiento y que se alcanzará en cada paciente en un tiempo determinado. Por todo ello, insistimos en buscar un balance entre le reacción local del paciente, la tolerancia y, con ello, la eficacia, para personalizar la pauta a cada paciente.
Las limitaciones del estudio son principalmente dos. La primera es que no se ha hecho un cálculo del tamaño muestral para lograr el objetivo del estudio: conocer la eficacia de la nueva pauta de tratamiento. La segunda limitación es la ausencia de grupo control con la pauta convencional.
En conclusión, presentamos una pauta continuada de imiquimod al 5% para el tratamiento de las QA. Esta pauta produce una adecuada reacción local, igual a la obtenida con la pauta convencional, lo que asegura el mecanismo de acción del fármaco y por lo tanto la eficacia del mismo.
Conflicto de interesesC. Serra-Guillén imparte charlas remuneradas para laboratorios IFC. El resto de los autores declaran no tener ningún conflicto de intereses.