La dermatitis catamenial es una rara enfermedad cuya presentación clínica es en forma de brotes mensuales de lesiones variables en la piel desencadenados por la fluctuación hormonal propia del ciclo menstrual.
Una mujer de 46 años presentaba brotes mensuales de una lesión en su antebrazo derecho desde 2013. Unos meses antes se le había retirado un DIU Mirena® (Bayer Hispania SL [Bayer]) implantado en 2011. Era fumadora y tomaba, de vez en cuando, ibuprofeno, aunque nunca para la dismenorrea. La paciente asociaba la aparición de la lesión 3-4 días antes de la aparición de su menstruación, experimentando una resolución espontánea los días 4-5 del ciclo menstrual.
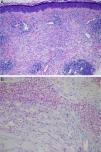
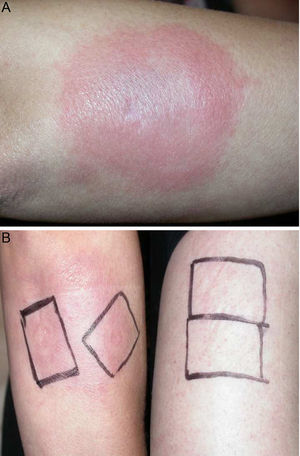
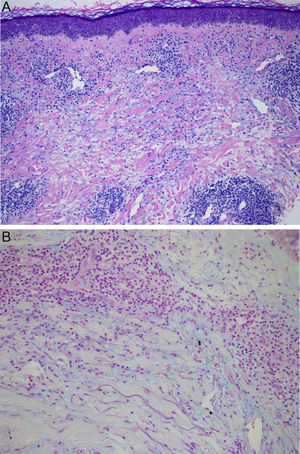
El examen físico reveló la presencia de una dolorosa placa eritematosa-edematosa en el antebrazo derecho de unos 10cm de diámetro (fig. 1 A). Las pruebas epicutáneas se realizaron con la serie estándar del Grupo Español en Investigación de Dermatitis de Contacto y Alergia Cutánea (GEIDAC) y con progesterona (PG); Norlevo® (Laboratoire HRA-Pharma) en vaselina y Progeffik® (Laboratorios Effik) en contacto directo con el área de la lesión y sobre piel sana (fig. 1 B). Todas las pruebas dieron negativo, tanto a las 48 como a las 96 h, al igual que la intradermorreacción, que se llevó a cabo con PG (Carborprot®, Pfizer) y que se leyó 15 min después de la infiltración y transcurridas 96 h. La biopsia confirmó la presencia de un denso infiltrado linfohistiocítico intersticial y mucina entre las bandas de colágeno de la dermis (fig. 2 A y B).
Se administraron, tanto preventivamente como durante el brote, fármacos antiinflamatorios no esteroideos, corticoides tópicos y orales, con resultado de resolución parcial de la sintomatología, pero sin lograr la prevención de los brotes en meses subsiguientes. Posteriormente, la paciente empezó un tratamiento con Progeffik® 300mg/día durante un mes de duración. La lesión se mantuvo durante ese período, lo cual llevó a diagnosticar dermatitis autoinmune por PG (DAP). Llegados a este punto, la paciente inició un tratamiento fuera de indicación con acetato de ulipristal (Esmya®, Gedeon Richter Iberica) 5mg/día en períodos de 3 meses con parones cada 1-2 meses, logrando la resolución completa de los síntomas cutáneos durante el tratamiento. A día de hoy, la paciente lleva 9 meses a tratamiento con acetato de ulipristal. Después del duodécimo mes de tratamiento, el fármaco será interrumpido y se adoptará una estrategia de «mantenernos a la espera» hasta que la paciente llegue a la menopausia.
La DAP es una dermatitis catamenial caracterizada por la aparición de lesiones de la piel premenstruales debido a un aumento de los niveles PG durante la fase luteal del ciclo menstrual1.
La etiopatogénesis de esta enfermedad no se ha establecido aún, pero probablemente se deba a los pocos casos descritos hasta la fecha (tabla 1). No obstante, se considera que los anticuerpos anti-PG se producen como resultado de una sensibilización a la PG. Los anticuerpos desencadenan las manifestaciones clínicas, ya que la ovulación induce la subida de PG durante la fase luteal1,2. Se han descrito antecedentes de exposición a anticonceptivos sistémicos hasta en el 66% de los casos1. Así pues, se cree que esta exposición podría llevar a una sensibilización a hormonas exógenas y a un desencadenamiento de la sintomatología como resultado de una reacción cruzada con la PG endógena1. En el 33% de casos restantes no se ha hallado exposición previa a hormonas exógenas y se cree que otros mecanismos patológicos autoinmunes contra la PG endógena (embarazo, menarquia…)1-4 son los responsables.
Resumen de los casos publicados
| Número de casos publicados | Fechas de publicación | Media de edad (rango) | Manifestaciones cutáneas Número de casos (%) | Ubicación Número de casos (%) | Biopsia cutánea Número de casos (%) | Diagnóstico Número de casos (%) | Tratamiento Número de casos (%) |
|---|---|---|---|---|---|---|---|
| 97 | 1964-2017 | 33,01 (15-55) | Placas eritematoso-edematosas: 32 (32,9%) Urticaria generalizada± angioedema: 31 (31,9) Erupción vesiculoampollosa: 13 (13,4) Eritema multiforme: 13 (13,4) Erosión de mucosa: 12 (12,3) Placas eccematosas: 10 (10,3) Anafilaxis: 8 (8,24) EFM: 3 (3,04) Púrpura: 2 (2,06) Placa única: 1 (1,03) | Extremidades superiores: 62 (63,9) Tronco: 56 (57,7) Extremidades inferiores: 51 (52,57) Rostro y cuello: 29 (29,8) Mucosa oral: 21 (21,6) Mucosa genital: 5 (5,15) | Sin biopsia: 44 (45,36) Con biopsia: 53 (54,63) Infiltrado linfohistiocítico perivascular superficial y profundo: 42 (79,24) Dermatitis de la interfase: – Liquenoide: 2 (3,7) – Vacuolización de la capa basal: 26 (48,38) Cambios epidérmicos (hiperqueratosis, acantosis, espongiosis): 16 (30,18) Edema dérmico: 7 (13,20) Melanófagos: 3 (5,6) Extravasación sanguínea: 2 (3,77) Vesículas subepidérmicas: 2 (3,77) | Intradermorreación a la PG: 73 (75,25) PG intramuscular: 8 (8,24) Clínico: 8 (8,24) PG intravaginal: 3 (3,09) Pruebas epicutáneas: 2 (2,06) Ac. circulantes: 2 (2,06) PG oral: 2 (2,06) Pruebas inmunológicas in vitro: 1 (1,03) | AO: 18 (18,55) E. conjugados: 18 (18,55) Análogos de la GnRH: 14 (14,43) Ooforectomía: 11 (11,34) Anti-HIS: 9 (20,61) Tamoxifeno: 8 (8,24) CT tópicos: 8 (8,24) Sin tratamiento: 7 (7,2) CT sistémicos: 6 (6,18) Desensitización: 6 (6,18) Danazol: 4 (4,12) Azatioprina: 2 (2,06) Embarazo: 1 (1,03) Dapsona: 1 (1,03) HCQ: 1 (1,03) CsA: 1 (1,03) Retirada de DIU: 1 (1,03) Interrupción THS: 1 (1,03) |
| Caso número 98 | Oscoz-Jaime (2017) | 46 | Dolorosa placa única eritematoso-edematosa de 10cm de tamaño, siempre en la misma ubicación | Antebrazo derecho | Infiltrado granulomatoso intersticial | PG oral | Acetato de ulipristal |
Edad en años.
HCQ: hidroxicloroquina.
Ac: anticuerpos; Anti-HIS: antihistamínicos; AO: anticonceptivos orales; CsA: ciclosporina; CT: corticoides; DIU: dispositivo intrauterino; EFM: erupción fija a medicamentos; E: estrógenos; PG: progesterona; THS: terapia hormonal sustitutiva.
Lo cierto es que la presentación clínica es muy diversa. Se han descrito casos compatibles con síndrome de Steven-Johnson, eritema multiforme, dermatitis herpetiforme, eccema, urticaria, estomatitis, petequias3 o, en raras ocasiones, casos de reacción fija a medicamentos3,5,6, como en nuestro caso. La sintomatología suele aparecer entre 3 y 10 días antes de la menstruación y resolverse entre 5 y 10 días después del inicio de la menstruación, coincidiendo con el descenso de los niveles de PG2,7.
Los criterios que han de darse para llegar un diagnóstico definitivo de DAP todavía no se han establecido1,8, si bien la mayoría de los autores proponen 3criterios diagnósticos:
- 1.
Clínica cíclica: empieza unos días antes de la menstruación (3-10 días) y se cura espontáneamente tras el fin de la menstruación.
- 2.
Interrupción de los brotes con tratamientos que inhiben la ovulación o las subidas de los niveles de PG.
- 3.
Desencadenamiento de sintomatología por pruebas de sensibilización a la PG (pruebas de alergia de contacto9, intradermorreacción1,3,9, provocación oral1,9, intramuscular1,3 o vaginal con PG3), o una demostración de anticuerpos circulantes anti-PG1.
El objetivo del tratamiento es inhibir la ovulación a fin de bloquear los mecanismos que causan los niveles altos de PG durante la segunda fase del ciclo. A día de hoy, los anticonceptivos orales son el tratamiento de primera línea. En cualquier caso, en función de la edad y las características clínicas del paciente, también pueden utilizarse otros fármacos (estrógenos conjugados, análogos de la GnRH, tamoxifeno, danazol, etc.). En casos graves y refractarios, puede realizarse una ooforectomía bilateral2. El acetato de ulipristal es un antagonista del receptor de PG que actúa sobre los niveles de PG. Se cree que inhibe la ovulación bloqueando tanto la expresión de los genes dependientes de la PG, como los picos de hormona luteinizante10. Debido a la edad de la paciente y al hecho de que era fumadora, se optó por instaurar un tratamiento con acetato de ulipristal como una alternativa válida.
La DAP es una dermatosis extremadamente rara si tenemos en cuenta el número de mujeres que son tratadas con anticonceptivos orales en todo el mundo. Esto es algo que hemos de tener en cuenta, ya que cabe esperar un aumento de su incidencia como consecuencia del mayor uso de anticonceptivos orales entre la población femenina. Hemos descrito el tercer caso publicado por autores españoles4,7 y el primer caso de DAP tratada, con efectividad, con acetato de ulipristal. Proponemos el acetato de ulipristal como una opción terapéutica efectiva en casos seleccionados.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
NotaCon fecha 9 de febrero 2018 (posterior al inicio del tratamiento de la paciente) la Agencia Española de Medicamentos y Productos Sanitarios publicó la siguiente alarma: «Tras la notificación de casos graves de daño hepático en mujeres tratadas con Esmya se han establecido medidas provisionales mientras se finaliza la evaluación detallada de toda la información disponible, por lo que se recomienda vigilar función hepática y no iniciar nuevos tratamientos como medidas cutelares».