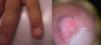
Paciente varón de 28 años, sin antecedentes patológicos de interés, que consultó por una lesión exofítica, de crecimiento lento y progresivo, localizada en la región periungueal del tercer dedo de la mano izquierda de 2 años de evolución. Reconocía haber tenido múltiples parejas sexuales hasta hace 6 años.
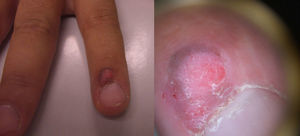
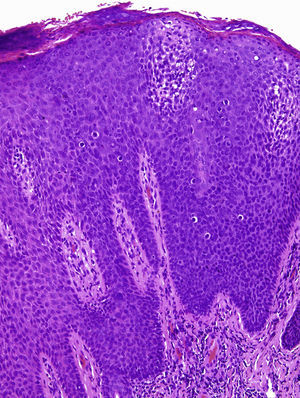
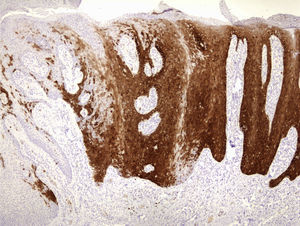
En la exploración se observaba una lesión periungueal exofítica, de 0,7cm de diámetro, de coloración rojo-grisácea y de superficie hiperqueratósica (fig. 1). El estudio anatomopatológico mostraba una epidermis hiperplásica, con pérdida de la arquitectura celular normal, atipia citológica moderada, disqueratosis y coilocitos en la epidermis (fig. 2); además de una sobreexpresión de la proteína de supresión tumoral P16 (fig. 3). Con el diagnóstico de una papulosis bowenoide (PB) extragenital se reinterrogó al paciente, quien negaba antecedentes de verrugas en la zona genital/anal, así como en su pareja actual. Se realizó un estudio analítico con recuento linfocitario incluyendo CD4 y CD8 y la serología para el VIH, que resultó normal. La captura de híbridos de la lesión fue positiva para el serotipo virus del papiloma humano (VPH) 42. Se decidió hacer una extirpación completa de la lesión y controles periódicos, que incluyeron a su pareja sexual, estando asintomático al año del diagnóstico.
El concepto PB fue introducido para describir múltiples pápulas verrugosas localizadas en la región genital y que histológicamente simulan una enfermedad de Bowen (EB) y clínicamente recuerdan a los condilomas o verrugas genitales. Es típica de gente joven y sexualmente activa con afectación predominante del área genital/crural y perianal. Se han descrito casos de BP extragenital en pacientes con lesiones genitales concomitantes o no y con inmunodeficiencia o no1.
Se asocia a la infección del VPH, y particularmente el VPH16 se ha vinculado estrechamente con la PB1,2. Otros tipos de VPH relacionados con la BP han sido 18, 31-35, 39, 42, 48 y 51 a 541–4. El HPV 16, 18 y el 33 son los considerados con mayor potencial oncogénico.
Se considera un carcinoma escamoso in situ, con un riesgo estimado de transformación a carcinoma invasivo del 2,6%2. El mecanismo oncogenético se iniciaría con la infección de las células por el VPH induciendo en ellas alteraciones genéticas. Los serotipos de alto riesgo producen 2 oncoproteínas (E6-E7) capaces de inactivar las proteínas de supresión tumoral RB y la P53, respectivamente, dando lugar a la proliferación celular descontrolada4. Se ha demostrado la presencia de VPH en las lesiones de PB y en la piel sana adyacente, lo que indica que la infección por el VPH es necesaria pero no suficiente para el desarrollo de una PB. Su desarrollo puede necesitar la presencia de otras alteraciones, como mutaciones genéticas adicionales de la célula huésped3,4.
La histopatología es similar a la de la EB, observandose en la PB la presencia de cambios más focales y menos intensos1,5,6. El diagnóstico diferencial entre estas 2 entidades requiere siempre un correlato clinicopatológico.
La verdadera frecuencia de esta entidad es desconocida, por ser fácilmente confundida con otros procesos víricos, realizándose destrucción de la lesión sin un estudio histopatológico previo7. Suelen ser lesiones recurrentes, y dada su posible capacidad de evolución a un carcinoma invasivo se recomienda la exploración periódica del paciente y de sus parejas sexuales y el estudio de su inmunidad en el caso de lesiones persistentes o recidivantes7. El curso de la BP varía entre un rango que va desde la progresión y la cronificación de las lesiones hasta la resolución espontánea. El tratamiento más eficaz es un tratamiento conservador que implique la destrucción de las lesiones, pudiendo realizarse cualquier tipo de técnica como la resección simple, la electrocoagulación y la criocirugía entre otros6,8.
Generalmente se presentan en asociación con lesiones genitales o en pacientes con antecedentes de haber presentado otras lesiones por VHP8–10 (tabla 1). El mecanismo de transmisión en este tipo de lesiones se considera que es por contacto directo, autoinoculación con la zona afectada o a través de fómites1,2,7,9. El mecanismo de transmisión justifica las diferentes localizaciones reportadas como son el cuello, el abdomen, el hombro, el mentón y la región periungueal, entre otras1–10.
Algunos casos publicados de papulosis bowenoide extragenital
| Casos | Inmunodeficiencia | Localización | HPV detectado | Transmisión | Lesiones genitales |
| Bart5 | Desconocida | Mentón | No realizado | Desconocido | |
| Grussendorg-Conen6 | Cuello | HPV 16 | No | ||
| Rüdlinger et al.3 | No | Periungueal | HPV35 | Contacto directo | Sí |
| Grob et al.7 | No | Cuello | HPV16 | Cuchillas | No |
| Johnson et al.1 | No | Cuello | 42 | Cuchillas | No |
| Fader et al.2 | VIH | Cuello | HPV 31, 33, 35 | Cuchillas | Sí (no actuales) |
| Baron et al.9 | Cuello | 18 | |||
| Purnell et al.10 | Linfopenia idiopática de CD4 | Digital | 18 | No | |
| Papadopoulos et al.4 | NoVIH | HombroAbdomen | 6, 1, 42, 43, 44no identificados | NoNo | |
| Oh et al.8 | No | Interdigital pie | 16 | Tiña pedis | No |
| Nuestro caso | No | Periungueal | 42 | No |
Describimos un nuevo caso de un paciente con una BPE con afectación de la región periungueal de un dedo de la mano, sin asociación con lesiones genitales en la actualidad ni en el pasado. Existen otros 2 casos similares reportados en la literatura. En uno de ellos se describieron lesiones de PB en la región perianal en el momento del diagnóstico de la lesión ungueal10, y en el otro caso estaba en asociación con una inmunodeficiencia4. Consideramos importante, según lo descrito en el presente caso, valorar el estudio anatomopatológico en todos los casos de lesiones verrugosas que aparezcan en pacientes jóvenes y sexualmente activos, aun cuando estén localizadas a distancia de la región genital, así como incorporar en la anamnesis preguntas acerca de la presencia de lesiones genitales en el paciente o su pareja o de posibles estados de inmunosupresión.