Omalizumab es un anticuerpo monoclonal anti-IgE únicamente aprobado para su uso en el asma grave refractario. En los últimos años han sido publicados un gran número de casos clínicos de urticaria crónica de difícil manejo terapéutico que han respondido de forma adecuada al tratamiento con omalizumab. Por ese motivo, se han puesto en marcha ensayos clínicos para ampliar la indicación a esta enfermedad, y recientemente el fármaco ha sido incluido en una guía de consenso para el tratamiento de la urticaria crónica como fármaco de tercera línea después de los antihistamínicos selectivos a dosis altas. El objetivo de este artículo es realizar una actualización integral de la aplicación de omalizumab en el tratamiento de la urticaria crónica: revisaremos su estructura, discutiremos los hipotéticos mecanismos de acción en esta enfermedad y expondremos su modo de empleo y las diferentes posologías empleadas en las series de casos publicados hasta el momento. Por otro lado, también enumeraremos sus efectos secundarios y daremos las pautas de prevención a seguir para minimizar su efecto secundario más temible, la anafilaxia. En definitiva, y según la experiencia de muchos investigadores, omalizumab se perfila como un fármaco novedoso que ha mostrado resultados prometedores en algunos tipos de urticaria crónica espontánea resistente con un buen perfil de seguridad, aunque con la principal limitación de su elevado coste económico.
Omalizumab is a monoclonal anti-immunoglobulin E antibody currently only approved for use in severe, refractory asthma. In recent years, many authors have reported satisfactory results with omalizumab in patients with difficult-to-treat chronic urticaria. As a result, clinical trials were undertaken to broaden the indication of omalizumab to include chronic urticaria, and the drug was recently cited as a third-line treatment after selective antihistamines at high doses in a consensus document on the treatment of chronic urticaria. In this article our aim is to provide a comprehensive update on the use of omalizumab in the treatment of chronic urticaria. The structure of this biologic agent and its possible mechanisms of actions in this setting will be presented. Treatment strategies and the different dosage regimens used in the series of cases published to date will also be reviewed. Finally, we will discuss the adverse effects that may arise with treatment and the recommended strategies for minimizing the most feared effect, anaphylaxis. Based on the experience of many researchers, omalizumab is emerging as a novel treatment for certain types of spontaneous refractory chronic urticaria and has shown promising results in this setting. The drug has a good safety profile and the main limitation is its high cost.
La urticaria crónica se caracteriza por la aparición de habones acompañados o no de angioedema durante un periodo superior a 6 semanas1. Es una entidad cutánea de diagnóstico clínico sencillo, pero de etiología multifactorial, curso impredecible y difícil manejo terapéutico. Puede afectar al 0,5-1% de la población en algún momento de su vida2 y produce un gran impacto negativo sobre la calidad de vida de los pacientes, que puede equipararse al producido por una enfermedad arterial coronaria grave3.
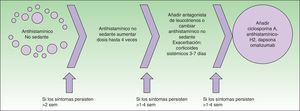
En 2008 se celebró en Berlín una reunión conjunta de la Sección de Dermatología de la European Academy of Allergology and Clinical Immunology, la Global Allergy and Asthma European Network, el European Dermatology Forum y la World Allergy Organization en la que se estableció una guía de consenso para el tratamiento de la urticaria crónica4 (fig. 1). Esta guía incluye como fármaco de tercera línea, entre otros, la utilización de omalizumab en aquellos casos refractarios a dosis elevadas de antihistamínicos selectivos.
Algoritmo terapéutico recomendado en la EAACI/GA2LEN/EDF/WAO4.
Omalizumab es un anticuerpo monoclonal recombinante que se une a la IgE libre circulante y bloquea su acción sobre las células diana. Su uso ha sido aprobado por la FDA (2003) y la EMEA (2005) únicamente para el tratamiento del asma bronquial moderada-grave en pacientes con una edad igual o superior a 6 años. Sin embargo, en los últimos años han aparecido numerosas publicaciones sobre la eficacia del omalizumab en urticaria crónica grave refractaria a otros tratamientos.
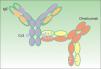
Omalizumab: estructura y funciónEstructura de omalizumabOmalizumab es un anticuerpo monoclonal humanizado de 149 KDa obtenido mediante la tecnología de ADN recombinante. Es un anticuerpo de tipo IgG1 compuesto por una fracción murina del 5% y una fracción humana del 95%5. La fracción murina es la activa y está minimizada para evitar respuestas de anafilaxia.
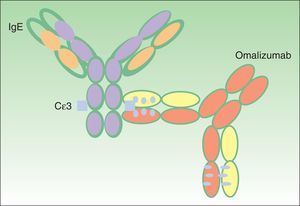
El anticuerpo se une al dominio C¿3 de la IgE humana (fig. 2), muy cercano al sitio de unión a los receptores de IgE de alta y baja afinidad (Fc¿RI y Fc¿RII, respectivamente). Puede unirse a la IgE que está libre en suero o en el intersticio, pero no a las moléculas de IgE unidas a la superficie de la célula, ya que en este caso el sitio de unión a omalizumab está ocupado por el receptor6.
Mecanismo de acción de omalizumabOmalizumab presenta 2 mecanismos de acción fundamentales:
- -
Reducción de la IgE libre en plasma: omalizumab se une a la molécula de IgE en la misma región que a su receptor en las células diana (basófilos y mastocitos), independientemente de su especificidad. Forma complejos pequeños (trímeros o hexámeros de menos de 1000 KDa), biológicamente inertes (no activan el complemento), que son lentamente eliminados por el sistema reticuloendotelial. De este modo, en el caso de los receptores de alta afinidad presentes en basófilos y mastocitos, bloquea la unión IgE- Fc¿RI e impide la activación celular y la liberación de sustancias vasoactivas como la histamina y otros mediadores inflamatorios como leucotrienos, triptasa, quimasa, prostaglandina D2 y citocinas7. Estas sustancias son las responsables de las manifestaciones clínicas características de las reacciones de hiperreactividad nasal, conjuntival, bronquial y cutánea.
- -
Disminución indirecta del número de receptores Fc¿RI en las células diana8: se considera que este efecto es secundario a la eliminación de la IgE sérica. En estudios previos se ha observado una fuerte correlación entre la concentración sérica total de IgE y la cantidad de Fc¿RI de basófilos de sangre periférica, puesto que la expresión del receptor se reduce considerablemente cuando estas células se cultivan en ausencia de IgE9,10. Lo mismo ocurre en las células maduras de la médula ósea que están expuestas a una cantidad muy baja de IgE, las cuales tendrán una expresión muy reducida del Fc¿RI. Un estudio farmacocinético demostró una media de disminución de la expresión de receptores del 73% con un máximo de inhibición a los 14 días de tratamiento con omalizumab11. La reducción en el número de receptores de alta afinidad podría explicar la eficacia del omalizumab en el tratamiento de la urticaria crónica autoinmune con anticuerpos contra dicho receptor, ya que disminuiría su diana.
Sin embargo, existen datos clínicos y de laboratorio que sugieren que el mecanismo del omalizumab es multifactorial y que además podría actuar sobre otras dianas celulares en el sistema inmunitario aún no bien estudiadas. Así, Sanchez-Machín et al. observaron un aumento de actividad de los linfocitos T CD4+en el suero de un paciente con urticaria crónica no autoinmune que respondió rápidamente a omalizumab 300mg cada 2 semanas12. Iemoli et al. encontraron una reducción de la activación de los linfocitos B, disminución de TNF-alfa y de IL4 y aumento de la síntesis de IFN-gamma en el suero de otro paciente con urticaria crónica idiopática tratado con omalizumab13.
PosologíaOmalizumab está disponible en jeringas precargadas de aplicación subcutánea. Existen 2 presentaciones: 75 y 150mg. La dosis apropiada y la frecuencia de administración de omalizumab se determina a partir de la concentración basal de IgE (UI/ml), medida antes de iniciar el tratamiento, y del peso corporal (kg) del paciente, siendo la dosis aprobada del fármaco para el tratamiento del asma de 0,016mg/kg por UI/ml de IgE, teniendo en cuenta que la cuantificación de IgE inicial no debe ser superior a 1.500 UI/ml. La utilización de omalizumab a esta pauta terapéutica se asocia con una reducción de la concentración basal de IgE cercana al 95% en los 3 primeros días de tratamiento14. Se suele repetir la administración a dosis de 2 o 4 semanas hasta las 16 semanas del inicio. Con la dosis recomendada la IgE sérica decrece rápidamente y alcanza un nadir de <50ng/ml (20,8UI/ml), niveles a los que se ha demostrado beneficios en el asma alérgica y en la rinitis, y los efectos pueden durar hasta meses si se consigue bloquear toda la IgE sérica15. Respecto a su eliminación, omalizumab tiene una vida media de 26 días con un aclaramiento promedio de 2,4±1,1ml/kg/día por parte del sistema reticuloendotelial. Se ha observado que el efecto del omalizumab se mantiene durante meses. No es necesario realizar un ajuste de dosis en función de la edad (12-76 años), raza, grupo étnico o sexo.
SeguridadOmalizumab parece ser un fármaco seguro y bien tolerado. Se han descrito escasos efectos secundarios, y la mayoría de ellos son de carácter leve. Las reacciones adversas más frecuentemente informadas durante los ensayos clínicos fueron reacciones cutáneas en el lugar de la inyección y la urticaria. Las primeras incluyen dolor, tumefacción, eritema y prurito, y ocurren aproximadamente en un 40% de los pacientes16; la urticaria aparece en un 4,9% de los pacientes17. En la siguiente tabla se enumeran las reacciones adversas registradas en la población tratada con omalizumab en los ensayos clínicos, por sistema de órganos y frecuencia (tabla 1).
Reacciones adversas descritas con omalizumab
| Trastornos de la piel y reacciones en el lugar de administración | |
| Frecuentes | Reacciones en el lugar de la inyección como tumefacción, dolor y prurito |
| Poco frecuentes | Fotosensibilidad, urticaria, rash y prurito |
| Raras | Angioedema |
| No conocida | Alopecia |
| Trastornos del sistema nervioso | |
| Frecuentes | Cefaleaa |
| Poco frecuentes | Síncope, parestesia, somnolencia y mareo |
| Trastornos gastrointestinales | |
| Muy frecuentes | Pirexiab |
| Frecuentes | Dolor abdominal superior |
| Poco frecuentes | Signos y síntomas dispépticos, náuseas y diarrea |
| Trastornos del sistema inmunológico | |
| Raras | Reacción anafiláctica y otros procesos alérgicos graves |
| No conocida | Enfermedad del suero |
| Infecciones e infestaciones | |
| Poco frecuentes | Faringitis |
| Raras | Infección parasitaria |
| Trastornos de la sangre | |
| No conocida | Trombocitopenia idiopática grave |
| Trastornos vasculares | |
| Poco frecuentes | Hipotensión postural, rubor |
| Trastornos del sistema respiratorio | |
| Poco frecuentes | Broncoespasmo alérgico, tos |
| Raras | Laringoedema |
| No conocida | Vasculitis granulomatosa alérgica (síndrome de Churg Strauss) |
| Trastornos musculoesqueléticos | |
| No conocidos | Artralgia, mialgia, tumefacción articular |
| Alteraciones del estado general | |
| Poco frecuentes | Síndrome pseudo-gripal, brazos hinchados, incremento de peso y fatiga |
Las reacciones adversas se enumeran en orden decreciente de gravedad dentro de cada intervalo de frecuencia. Las categorías de frecuencia se definen como: muy frecuentes (≥1/10), frecuentes (≥1/100 a <1/10), poco frecuentes (≥1/1.000 a <1/100), raras (≥1/10.000 a <1/1.000) y muy raras (<1/10.000). Las reacciones notificadas en la fase de poscomercialización se enumeran con frecuencia no conocida (no puede estimarse a partir de los datos disponibles).
Modificado de la ficha técnica de omalizumab.
La reacción adversa más temible es la anafilaxia. Esta es debida a la fracción murina de la estructura de omalizumab. En 2007 la Academia Americana de Asma, Alergia e Inmunología creó la Omalizumab Joint Task Force para registrar datos sobre la anafilaxia asociada a omalizumab: observaron una incidencia de anafilaxia del 0,2%. Comprobaron que el 61% de estas reacciones ocurrían dentro de las 2 primeras horas posteriores a las 3 primeras inyecciones y el 14% dentro de los primeros 30min después de la cuarta o posteriores inyecciones. De acuerdo con estas observaciones se establecieron las siguientes recomendaciones en todos los pacientes en los que se instaura el tratamiento con omalizumab18 (tabla 2).
Recomendaciones para evitar el riesgo de anafilaxia según la Omalizumab Joint Task Force
| 1. Obtención de consentimiento informado2. Educación del paciente frente a las reacciones anafilácticas3. Proporcionar al paciente adrenalina autoinyectable4. Periodo de observación de 2h después de las 3 primeras inyecciones5. Periodo de observación de 30min a partir de la cuarta inyección |
Siguiendo las anteriores recomendaciones se pueden detectar precozmente el 77% de las reacciones anafilácticas y ser adecuadamente tratadas19.
Omalizumab fue evaluado en un extenso programa que incluyó 12 ensayos clínicos en fase iiB/iii que seleccionó a más de 5.243 pacientes en tratamiento con omalizumab por asma y rinitis graves IgE mediadas, y se concluyó que omalizumab tenía un perfil de seguridad comparable al del grupo control o las terapias estándar con antihistamínicos antiH1, no aumentando tampoco el riesgo de cáncer en estos pacientes20. Busse et al., por su parte, han realizado una revisión reciente sobre la incidencia de tumores primarios en 32 estudios aleatorizados, doble ciego y controlados con placebo, y concluyeron que no había asociación estadísticamente significativa entre el tratamiento con omalizumab y el desarrollo de neoplasias21.
Actualmente la FDA está evaluando los resultados provisionales de seguridad de un estudio en curso con omalizumab. Se trata de un estudio observacional de alrededor de 5.000 pacientes tratados con omalizumab y unos 2.500 pacientes control, cuyo objetivo principal es evaluar el perfil a largo plazo de omalizumab en pacientes seguidos durante 5 años22.
Omalizumab en urticaria crónicaOmalizumab está siendo utilizado con éxito en el tratamiento de la urticaria crónica. Prueba de ello es la existencia de al menos 105 casos publicados de pacientes con urticaria crónica grave tratados con omalizumab. Además, un total de 139 pacientes han sido incluidos en estudios aleatorizados que comparaban omalizumab con placebo. Los datos más relevantes de estos estudios están reflejados en la tabla 3. Como se puede observar, el fármaco ha demostrado eficacia en casos de urticaria crónica autoinmune y no autoinmune, con resultados variables en los casos de urticaria física y colinérgica.
Ensayos clínicos y series de casos publicados de pacientes con urticaria crónica tratados con omalizumab
| Primer autor | Año | N.° casos | Tipo urticaria | Dosis | Comentarios |
| Casos clínicos/series de casos/ensayos clínicos no aleatorizados | |||||
| Boyce23 | 2006 | 1 | UCFr | 375mg/2sem | Respuesta completa en paciente de 12 años |
| Spector et al.24 | 2007 | 3 | 2 UCI1 UCA | Variable | Respuesta completa en los 3 pacientes |
| Güzelbey et al.25 | 2008 | 1 | UCS | 150mg/4sem | Respuesta completa en urticaria solar |
| Godse26 | 2008 | 1 | UCI | 300mg/4sem | Mejoría importante en todos los pacientes |
| Metz et al.27 | 2008 | 1 | UCCo | 150mg/4sem | Respuesta completa |
| Otto et al.28 | 2009 | 1 | UCCo | 300mg/4sem | Mejoría importante |
| Magerl et al.29 | 2010 | 8 | 7 UCI1UCP | Variable | Respuesta en todos los pacientes, en 6/8 respuesta clínica completa |
| Vestergaard et al.30 | 2010 | 2 | 2 UCI | Variable | Respuesta completa |
| Krause et al.31 | 2010 | 1 | UCFa | 300mg/2sem | Respuesta completa |
| Waibel et al.32 | 2010 | 1 | UCS | 400mg/2sem | Respuesta parcial |
| Romano et al.33 | 2010 | 2 | 2 UCI | 400mg/2sem | Respuesta completa |
| Bullerkotte et al.34 | 2010 | 1 | UCS | 450mg/2sem | Respuesta completa |
| Sabroe35 | 2010 | 1 | UCCo | 300mg/2sem | No respuesta |
| Bindslev-Jensen et al.36 | 2010 | 1 | UCP | 150mg/2sem | Respuesta completa asociada a disminución de degranulación del test de basófilo |
| Al-Ahmad37 | 2010 | 3 | 3 UCA | 300mg/4 sem | Respuesta en todos los pacientes |
| Iemoli et al.13 | 2010 | 1 | UCI | 300mg/2sem | Respuesta completa asociada a disminución del TNF alfa e IL-4 y aumento de IFN gamma |
| Saavedra et al.8 | 2011 | 1 | UCI | 300mg/2 sem | Respuesta satisfactoria asociada a regulación negativa del 80% de FceRI |
| Groffik et al.38 | 2011 | 9 | 9 UCI | Variable | Respuesta en todos los pacientes |
| Metz et al.39 | 2011 | 7 | 2 UCS1 UCCal1 UCFr1 UCP1 UCFa | Variable | Respuesta completa en urticaria solar, por frío, por presión retardada y facticiaNo respuesta en urticaria por calor |
| Godse26 | 2011 | 5 | 5 UCI | 300mg/2-4 sem | Mejoría importante en todos los pacientes |
| Sánchez-Machín et al.12 | 2011 | 1 | 1 UCI | 300mg/2sem | Respuesta completa asociada al aumento de la actividad de los linfocitos T CD4+ |
| Duchini et al.40 | 2011 | 1 | UCS | 150mg/4sem | No respuesta |
| Büyüköztürk et al.41 | 2012 | 14 | 2 AE12 UCI | Variable | Mejoría importante en la actividad de la urticaria y en la calidad de vida de los pacientes |
| Ivyanskiy et al.42 | 2012 | 19 | 12 UCI6 UCA1 UCP | 150mg/2 sem | 11/19 pacientes respuesta completa, 5/19 respuesta parcial y no respuesta en 3/19 pacientes |
| Estudios observacionales | |||||
| Kaplan et al.43 | 2008 | 12 | 12 UCA | Variable | Respuesta completa en 7/12 pacientes, 4/7 mejoría importante y no respuesta en un paciente |
| Ferrer et al.44 | 2011 | 9 | 9 UCI | 300mg | Respuesta en todos los pacientes, 7/9 pacientes respuesta clínica completa |
| Ensayos clínicos aleatorizados controlados con placebo | |||||
| Maurer et al.45 | 2011 | 27 casos22 control | 27 UCA | Variable | IgE+frente a tiroperoxidasaProtección frente al desarrollo de habones en el 70,4% de los pacientes tratados con omalizumab frente al 4,5% con placebo |
| Saini et al.46 | 2011 | 21 UCI25 UCI23 UCI21 placebo | 69 UCI | 600mg300mg75mgplacebo | Busqueda de dosis: mejoría importante con 300mg y 600mg y falta de respuesta con 75mg. No se incluye dosis de 150mg en el estudio |
AE: angioedema; UCA: urticaria crónica autoinmune; UCCal: urticaria por calor; UCCo: urticaria crónica colinérgica; UCF: urticaria por frío; UCFa: urticaria crónica facticia; UCI: urticaria crónica idiopática; UCP: urticaria crónica por presión; UCS: urticaria crónica solar.
En la mayoría de artículos publicados se ha utilizado omalizumab en urticaria crónica siguiendo las mismas pautas que para el tratamiento del asma alérgica grave: entre 75 y 375mg cada 2 o 4 semanas, dependiendo del peso y de la IgE iniciales del paciente. En la bibliografía disponible existe un único ensayo clínico que estudia la dosis de inicio de omalizumab en el tratamiento de la urticaria crónica no autoinmune realizado por Saini et al.46, en el que se dividieron un total de 90 pacientes en 4 grupos de tratamiento: se administró una única dosis de 600, 300 y 75mg y placebo respectivamente a cada grupo. A las 4 semanas de la inyección se evaluó la respuesta, obteniendo un descenso medio del UAS de 14,6 puntos en el grupo que recibió 600mg de omalizumab, 19,9 puntos en el grupo de 300mg de omalizumab, 9,8 puntos en el grupo de 75mg de omalizumab y 6,9 puntos en el grupo que recibió placebo. Se concluyó que la dosis más efectiva podría ser de 300mg y que la dosis de 75mg tiene eficacia similar a placebo en el tratamiento de la urticaria. Esta dosis concuerda con la utilizada en la mayoría de estudios experimentales disponibles en los que se ha conseguido una respuesta clínica satisfactoria. Sin embargo, hay que remarcar que en este estudio no se incluyó la dosis de 150mg de omalizumab, en contraposición con una serie más reciente de 19 casos de pacientes con urticaria crónica (63% idiopática, 32% autoinmune), en la que Ivyanski et al.42 utilizaron precisamente una dosis fija de 150mg cada 2 semanas en todos los pacientes, con una resolución completa en 11/19 pacientes (58%), una resolución parcial en 5/19 (26%) y falta de respuesta en solo 3/19 pacientes (16%), proponiendo por tanto la dosis de 150mg como dosis mínima efectiva en el tratamiento de la urticaria crónica.
Tampoco se dispone de datos concluyentes sobre dosis de mantenimiento ni intervalos de administración. Romano et al.33 intentaron aumentar el intervalo entre dosis a más de 4 semanas en 2 casos graves de urticaria crónica con recaída clínica y aparición de los habones tras el éxito terapéutico temprano. Sin embargo, Ferrer et al.44 utilizaron intervalos variables de omalizumab a 300mg en sus pacientes y administraron dosis mensuales a 5 pacientes, bimensuales a un paciente y hasta trimestrales en 3 pacientes, consiguiendo una respuesta clínica favorable en todos ellos.
ConclusionesOmalizumab es un anticuerpo monoclonal anti-IgE aprobado únicamente en la actualidad para el tratamiento del asma grave. Se ha estudiado su aplicación en el tratamiento de otras enfermedades en cuya base fisiopatogénica interviene también la elevación del nivel de IgE sérico como la dermatitis atópica47 y la alergia alimentaria, pero también ha sido empleado en casos graves de urticaria crónica espontánea refractaria a otros tratamientos, en la que ha mostrado resultados prometedores con gran mejoría clínica, según la experiencia de algunos investigadores. El principal mecanismo de acción de omalizumab en la urticaria crónica se basa en el bloqueo de la unión de la IgE con el receptor Fc¿RI en las células receptoras, que induce secundariamente una reducción de la IgE libre plasmática, así como del número de receptores Fc¿RI en la superficie de mastocitos y basófilos. No obstante, se ha demostrado experimentalmente que el fármaco también puede actuar sobre otras dianas como la inmunidad celular por mecanismos todavía no aclarados. Se trata de una molécula con un buen perfil de seguridad según los ensayos clínicos disponibles, siendo la anafilaxia (su efecto adverso más grave) poco frecuente y controlable si se adoptan unas medidas preventivas adecuadas. La posología adecuada en urticaria crónica está aún por determinar, y en la mayoría de casos publicados se han utilizado las dosis correspondientes al tratamiento del asma calculadas a partir del peso y de la IgE sérica del paciente, aunque la dosis óptima podría estar entre 150-300mg cada 2-4 semanas. Su principal limitación es su elevado coste, pero su uso compasivo puede estar justificado en casos refractarios de urticaria crónica grave con gran deterioro en la calidad de vida de los pacientes.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLa Dras. Laura Francés y María del Carmen Leiva declaran no tener ningún conflicto de intereses.
El Dr. Juan Francisco Silvestre es miembro de un Advisory Board de Novartis.