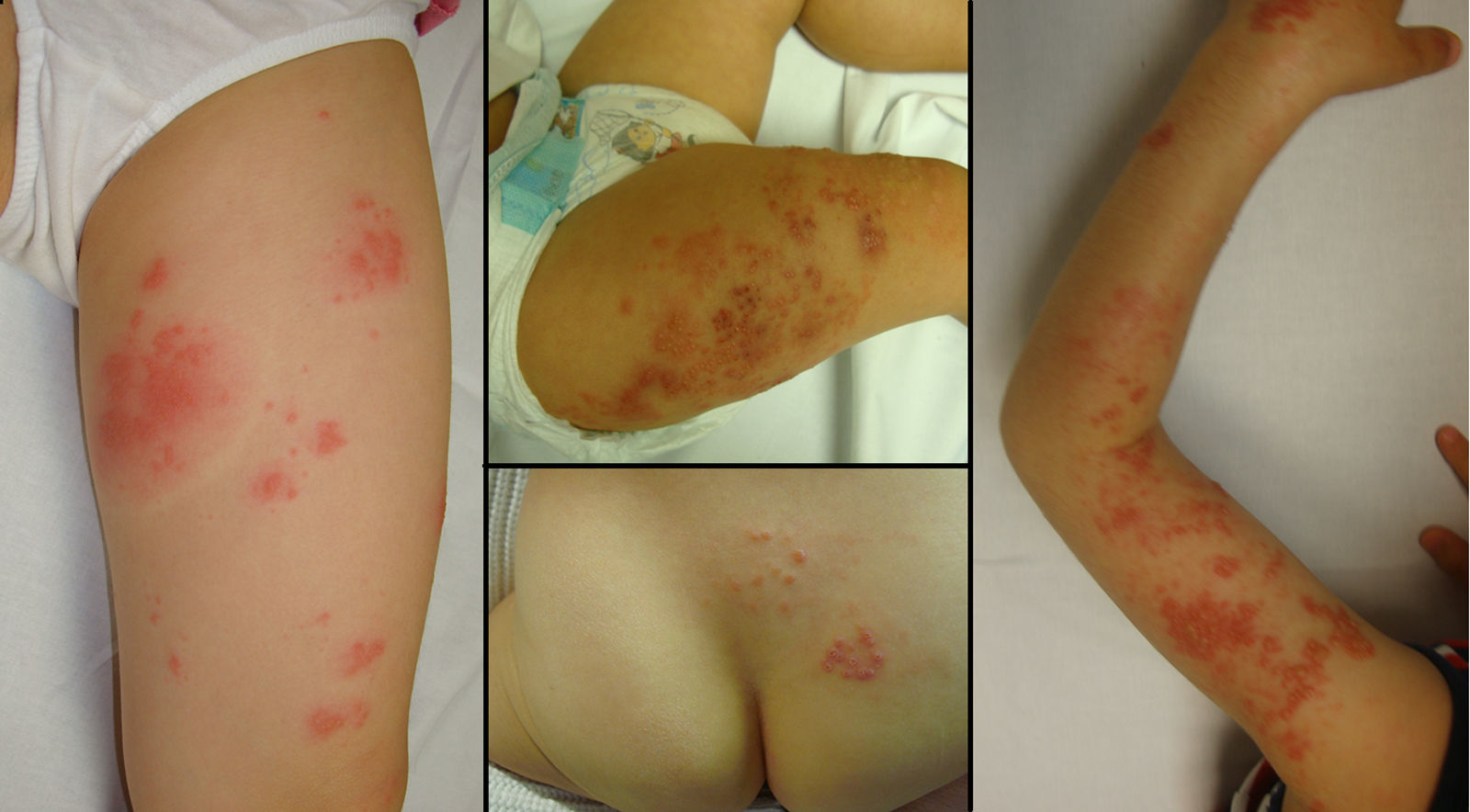
Con la instauración de la vacuna contra el virus de la varicela-zóster (VVZ) se esperaba la ausencia de herpes zóster (HZ) en niños vacunados, pero tras varios años de experiencia hemos continuando atendiendo casos de HZ en niños. Presentamos 8 casos recogidos entre 2010 y 2013 en las guardias de dermatología. En el periodo señalado el área poblacional del Hospital Universitario Fundación Alcorcón era de 247.000 habitantes. En la tabla 1 y la figura 1 aparecen reflejadas las características clínico-epidemiológicas de los pacientes. Se observó una ligera predominancia del sexo masculino, siendo la relación varón/mujer de 6/2. Las edades estaban comprendidas entre los 18 meses y los 5 años, siendo la media de 3,5 años. Todos los pacientes habían sido vacunados con una única dosis entre los 15 y los 17 meses de edad. Desarrollaron el HZ tras una media de 2,2 años tras la vacunación, el caso más precoz tan solo tras 3 meses. En 2 de los casos se realizó PCR para el VVZ, positivo en ambos, no estando disponible en nuestro hospital la diferenciación entre cepa vacunal y salvaje. Los dermatomas más frecuentemente afectados fueron los de los miembros inferiores. El tratamiento varió en función del tiempo de evolución de las lesiones, su extensión y las molestias subjetivas de los pacientes; así, en 5 de los 8 casos fue necesario el inicio de tratamiento con aciclovir por vía oral y en el resto se establecieron cuidados tópicos con fomentos astringentes y pomadas antibióticas. Ningún paciente tenía factores de riesgo de inmunosupresión ni comorbilidades asociadas. Únicamente destacaban 3 casos con dermatitis atópica, aunque ninguno había precisado tratamiento esteroideo oral en el último año. Seis de los 8 casos contaban con una analítica en el último mes que no mostraba alteraciones. Por último, la evolución de los pacientes fue favorable con el tratamiento pautado y en el seguimiento posterior no se registró ninguna complicación tipo neuralgia posherpética o cicatrices, ni ningún caso de recurrencia.
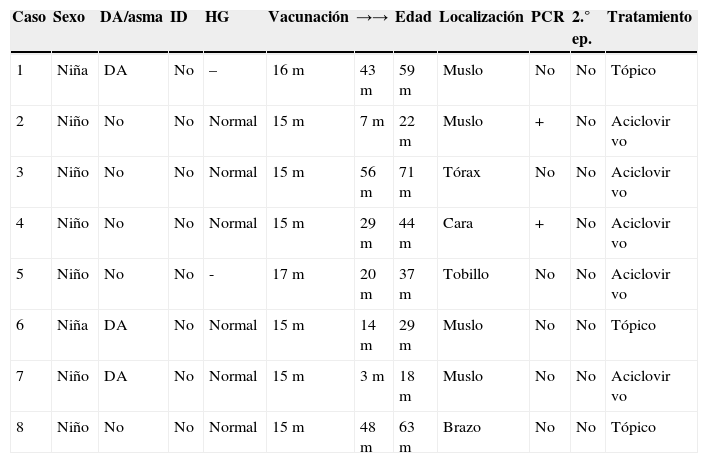
Características clínico-epidemiológicas de los pacientes
| Caso | Sexo | DA/asma | ID | HG | Vacunación | →→ | Edad | Localización | PCR | 2.° ep. | Tratamiento |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | Niña | DA | No | – | 16m | 43m | 59m | Muslo | No | No | Tópico |
| 2 | Niño | No | No | Normal | 15m | 7m | 22m | Muslo | + | No | Aciclovir vo |
| 3 | Niño | No | No | Normal | 15m | 56m | 71m | Tórax | No | No | Aciclovir vo |
| 4 | Niño | No | No | Normal | 15m | 29m | 44m | Cara | + | No | Aciclovir vo |
| 5 | Niño | No | No | - | 17m | 20m | 37m | Tobillo | No | No | Aciclovir vo |
| 6 | Niña | DA | No | Normal | 15m | 14m | 29m | Muslo | No | No | Tópico |
| 7 | Niño | DA | No | Normal | 15m | 3m | 18m | Muslo | No | No | Aciclovir vo |
| 8 | Niño | No | No | Normal | 15m | 48m | 63m | Brazo | No | No | Tópico |
DA: dermatitis atópica; ep.: episodio; HG: hemograma; ID: inmunodepresión; →→: tiempo transcurrido desde el momento de la vacunación hasta el desarrollo del herpes zóster.
La vacuna contra el VVZ es de virus vivos atenuados, derivados de la cepa Oka del VVZ. Su uso en niños menores de 12 años se aprobó en el año 2003 (Varivax®). A pesar de que la Asociación Española de Pediatría en sus últimas recomendaciones aconseja la administración de 2 dosis (una primera a los 12-15 meses y una segunda a los 2-3 años), únicamente 3 comunidades autónomas se ciñen a esta pauta (Ceuta, Melilla y Navarra), siendo la tónica general la administración de una única dosis a los 11-12 años. Durante 2010 y 2013 en la Comunidad de Madrid se administraba una sola dosis a los 15 meses y se recomendaba la vacunación de niños con 11 años que no hubiesen sido vacunados previamente y que fuesen seronegativos. Recientemente estas recomendaciones han cambiado, y desde el pasado 1 de enero de 2014 ha pasado a administrarse únicamente a los 12 años en aquellos niños sin previa vacunación y que no han pasado la enfermedad.
Con la instauración de la vacuna contra el VVZ se esperaba una ausencia total de HZ en niños vacunados, pero tras varios años de experiencia se han ido registrando casos de HZ en niños vacunados y sanos. En algunos de ellos se ha realizado PCR, que ha resultado positiva para la cepa Oka1–4. Esta cepa podría reactivarse en forma de zóster diseminado (si los títulos de anticuerpos son bajos, pudiéndose confundir con formas de infección por cepa salvaje) o en forma de zóster metamérico3. Esta última entidad podría estar probablemente infradiagnosticada debido a la creencia de que la cepa vacunal no tiene capacidad de reactivarse, a la rareza de los HZ en los niños y a que los casos de HZ posvacunales son más leves, por lo que podrían consultar con menor frecuencia3. Se ha observado también que las reactivaciones podrían ser más frecuentes si los títulos de Ac anti-VVZ son bajos3 y si tras la vacunación se dio algún tipo de exantema, ya que se postula que son las lesiones cutáneas las que posibilitarían el paso del VVZ a los nervios, estableciendo así la infección latente2,5. Las diferencias principales entre los HZ posvacunales frente a los HZ tras primoinfección son que las lesiones suelen ser menos dolorosas, más pequeñas, con menor frecuencia de vesículas y predominio de dermatomas lumbosacros frente a los torácicos, ya que esta es la localización más frecuente de administración de la vacuna6.
Como conclusión, presentamos 8 casos menores de 5 años sanos y vacunados de VVZ. Aunque se han confirmado casos de reactivaciones de VVZ cepa Oka, estudios recientes no han observado un aumento de la incidencia de HZ en niños vacunados7. No obstante, no se dispone de estudios epidemiológicos que evalúen la verdadera incidencia de HZ en niños tras la introducción de la vacunación sistemática en nuestro medio. La caracterización molecular del virus podría ayudar a obtener más información de la incidencia de HZ tras vacunación frente a VVZ.