Actualmente los fármacos aprobados como adyuvantes en el melanoma avanzado son: interferón, con una efectividad muy limitada, e ipilimumab, con una toxicidad importante y hasta un 1% de mortalidad asociada1. La terapia diana (anti-BRAF, anti-MEK y sus combinaciones) (tabla) y la inmunoterapia con anticuerpos anti-PD1 han modificado el pronóstico del melanoma metastásico2, pero hasta el momento no se tenía evidencia suficiente sobre su eficacia en adyuvancia. Recientemente Long et al.3 han publicado los resultados de un ensayo clínico fase 3 doble ciego en pacientes con melanoma BRAF mutado estadios IIIA-C, comparando placebo (n=432) con terapia diana combinada vía oral (TDC) (n=438) con dabrafenib (anti-BRAF, 300mg/día) y trametinib (anti-MEK, 2mg/día) durante 12 meses. La mediana de seguimiento fue de 2,8 años, momento en que la TDC presentó un reducción del 53% del riesgo de recaídas comparada con placebo. La estimación a 3 años de la supervivencia libre de recaídas fue del 58% en el grupo de TDC versus 39% en el grupo placebo (HR: 0,47; IC 95%: 0,39-0,58; p<0,001). La tasa de supervivencia global estimada fue del 86 y 77%, respectivamente (HR: 0,57; IC 95%: 0,42-0,79; p=0,0006). La tasa de supervivencia libre de metástasis a distancia también fue superior con TDC. En el momento del análisis estadístico habían fallecido 60 pacientes con TDC (14%) y 93 (22%) en el grupo placebo. El porcentaje de efectos adversos graves fue del 36% con TDC (114 pacientes requirieron interrupción del tratamiento y uno falleció por neumonía) y del 10% con placebo.
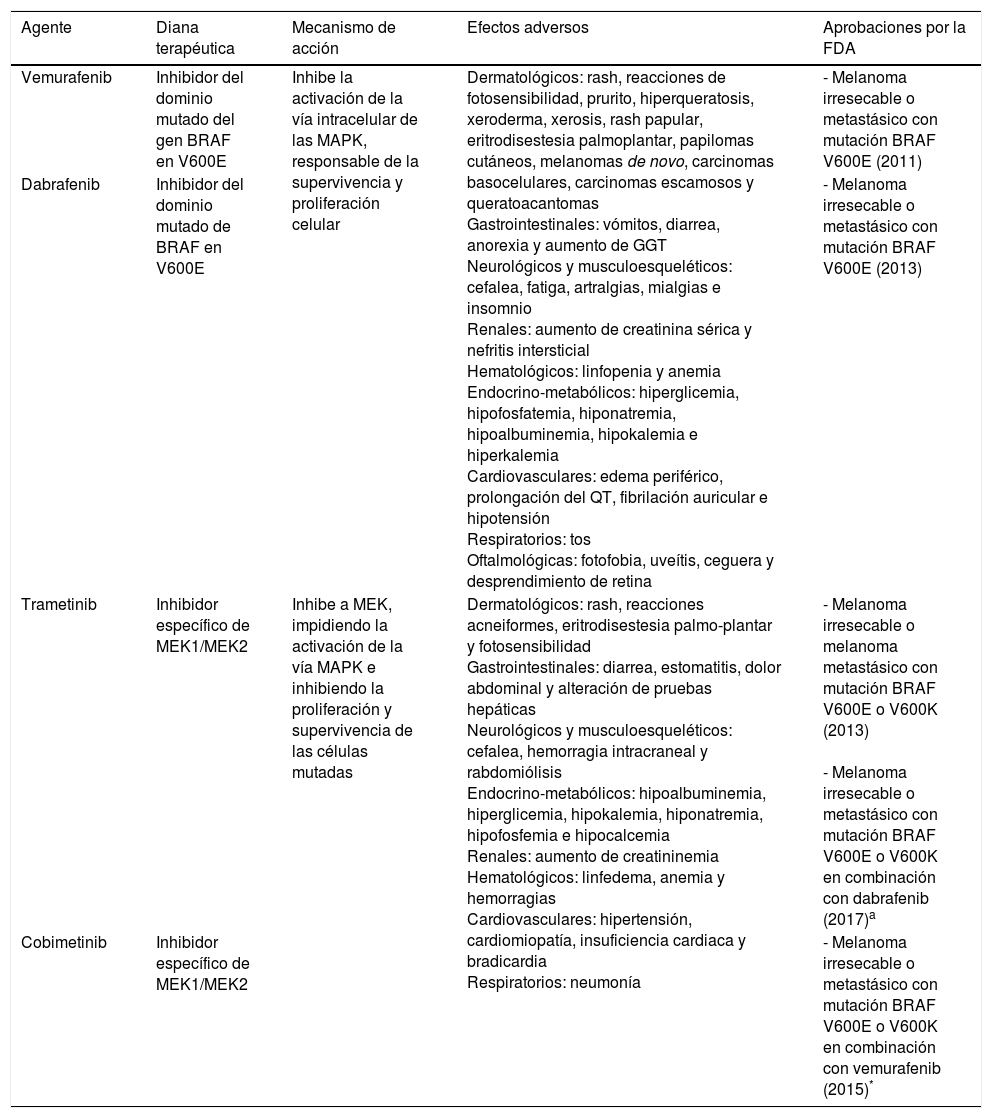
Fármacos anti-BRAF y anti-MEK utilizados en el tratamiento del melanoma
| Agente | Diana terapéutica | Mecanismo de acción | Efectos adversos | Aprobaciones por la FDA |
|---|---|---|---|---|
| Vemurafenib | Inhibidor del dominio mutado del gen BRAF en V600E | Inhibe la activación de la vía intracelular de las MAPK, responsable de la supervivencia y proliferación celular | Dermatológicos: rash, reacciones de fotosensibilidad, prurito, hiperqueratosis, xeroderma, xerosis, rash papular, eritrodisestesia palmoplantar, papilomas cutáneos, melanomas de novo, carcinomas basocelulares, carcinomas escamosos y queratoacantomas Gastrointestinales: vómitos, diarrea, anorexia y aumento de GGT Neurológicos y musculoesqueléticos: cefalea, fatiga, artralgias, mialgias e insomnio Renales: aumento de creatinina sérica y nefritis intersticial Hematológicos: linfopenia y anemia Endocrino-metabólicos: hiperglicemia, hipofosfatemia, hiponatremia, hipoalbuminemia, hipokalemia e hiperkalemia Cardiovasculares: edema periférico, prolongación del QT, fibrilación auricular e hipotensión Respiratorios: tos Oftalmológicas: fotofobia, uveítis, ceguera y desprendimiento de retina | - Melanoma irresecable o metastásico con mutación BRAF V600E (2011) |
| Dabrafenib | Inhibidor del dominio mutado de BRAF en V600E | - Melanoma irresecable o metastásico con mutación BRAF V600E (2013) | ||
| Trametinib | Inhibidor específico de MEK1/MEK2 | Inhibe a MEK, impidiendo la activación de la vía MAPK e inhibiendo la proliferación y supervivencia de las células mutadas | Dermatológicos: rash, reacciones acneiformes, eritrodisestesia palmo-plantar y fotosensibilidad Gastrointestinales: diarrea, estomatitis, dolor abdominal y alteración de pruebas hepáticas Neurológicos y musculoesqueléticos: cefalea, hemorragia intracraneal y rabdomiólisis Endocrino-metabólicos: hipoalbuminemia, hiperglicemia, hipokalemia, hiponatremia, hipofosfemia e hipocalcemia Renales: aumento de creatininemia Hematológicos: linfedema, anemia y hemorragias Cardiovasculares: hipertensión, cardiomiopatía, insuficiencia cardiaca y bradicardia Respiratorios: neumonía | - Melanoma irresecable o melanoma metastásico con mutación BRAF V600E o V600K (2013) - Melanoma irresecable o metastásico con mutación BRAF V600E o V600K en combinación con dabrafenib (2017)a |
| Cobimetinib | Inhibidor específico de MEK1/MEK2 | - Melanoma irresecable o metastásico con mutación BRAF V600E o V600K en combinación con vemurafenib (2015)* |
Fuente: Luke et al.2 y Carlos et al.4.
FDA: Food and Drug Administration; GGT: gamma glutamil transferasa; MAPK: mitogen-activated protein kinase; MEK, MAPK extracellular signal-regulated kinase.
La terapia diana combinada anti-BRAF-anti-MEK (vemurafenib-cobimetinib, dabrafenib-trametinib) presenta mayores respuestas terapéuticas y significativamente menos efectos secundarios que los anti-BRAF o anti-MEK en monoterapia2,4.
Se han publicado también los resultados de un ensayo clínico aleatorizado, doble ciego fase 3 en pacientes con melanoma estadios IIIB-C y IV libre de enfermedad, comparando el anti-PD1 nivolumab (n=453) (3mg/kg cada 2 semanas) e ipilimumab (n=453) (10mg/kg cada 3 semanas, 4 dosis y luego cada 12 semanas). Ambos tratamientos se administraron durante 12 meses con un seguimiento mínimo de 18 meses. La tasa de supervivencia libre de recidiva (TSLR) a los 12 meses fue del 70,5% con nivolumab y del 60,8% con ipilimumab (HR: 0,65; IC 97,56%, 0,51-0,83; p<0,001). La superioridad de nivolumab frente a ipilimumab se observó en prácticamente todos los subgrupos analizados, incluyendo aquellos con expresión de PD-1<5% (TSLR del 64,3 y 53,7%, respectivamente), estadios IIIB-C (TSLR del 72,3 y 61,6%, respectivamente), tumores ulcerados, afectación ganglionar macro o microscópica y en tumores con o sin mutaciones BRAF. La tasa de efectos adversos graves (grados 3 o 4) fue del 14,4% con nivolumab y del 45,9% con ipilimumab, y hubo 2 muertes (por aplasia medular y colitis) secundarias al tratamiento con este último5.
Los resultados presentados en estos ensayos clínicos demuestran un incremento significativo de la supervivencia libre de enfermedad en los pacientes con melanoma avanzado tratados con TDC o nivolumab, con una toxicidad asociada que podría considerarse aceptable si estos resultados son finalmente reproducibles a largo plazo.
Estamos viviendo una época de grandes cambios en el manejo del melanoma y es fundamental para los dermatólogos familiarizarse con estos nuevos fármacos, sus indicaciones y sus efectos adversos.