Vismodegib es el primer inhibidor selectivo de la vía de la señalización Hedgehog aprobado para el tratamiento del carcinoma basocelular (CBC) localmente avanzado y metastásico. Describimos nuestra experiencia en un centro oncológico con el vismodegib en el tratamiento de pacientes con CBC avanzados y/o múltiples durante un periodo de 5 años.
Material y métodosAnalizamos variables como la edad y el sexo del paciente, la localización, el tamaño, el tipo y las características del tumor, el tiempo de evolución, si son tumores primarios o recidivas, la duración del tratamiento, la respuesta a este (completa, parcial, estabilización o ausencia de respuesta), los efectos secundarios observados y las recidivas.
ResultadosUn total de 22 pacientes fueron tratados, 20 con CBC localmente avanzados y 2 con CBC metastásicos con afectación ganglionar. El tratamiento fue administrado durante 11,8 meses de media. El 41% (9) de los pacientes obtuvieron una respuesta completa al tratamiento, un 45% (10) respuesta parcial y en el 14% (3) de los pacientes el tratamiento consiguió estabilizar la enfermedad. Tras una mediana de 21 meses, 2 casos recidivaron. Los principales efectos secundarios observados fueron disgeusia, alopecia y calambres musculares, todos ellos de carácter leve. Ningún paciente desarrolló un carcinoma epidermoide sobre el área tratada con vismodegib, aunque sí cambios metatípicos tras el tratamiento.
ConclusionesEl vismodegib es un fármaco seguro y eficaz para el tratamiento del CBC localmente avanzado, con un porcentaje de respuesta del 86%. Los efectos adversos deben tenerse en cuenta por su alta frecuencia, aunque estos suelen ser de carácter leve.
Vismodegib is the first selective Hedgehog inhibitor approved for the treatment of locally advanced and metastatic basal cell carcinoma (BCC). In this article, we describe our experience with the use of this drug to treat advanced and/or multiple BCCs at a cancer center over 5 years.
Material and methodsWe analyzed the following variables: patient age and sex; tumor location, size, type, and characteristics; time since onset; primary or recurrent status; duration of treatment; response to treatment (complete, partial, stabilization, or absence of response); adverse effects; and recurrences.
ResultsWe treated 22 patients, of whom 20 had locally advanced BCCs and 2 had metastatic BCCs with lymph node involvement. The treatment was administered over a mean of 11.8 months. Nine patients (41%) achieved complete response and 10 (45%) partial response. The disease was stabilized in 3 (14%). Two patients relapsed after a median of 21 months. The main adverse effects were dysgeusia, alopecia, and muscle cramps, all of which were mild. None of the patients developed squamous cell carcinoma in an area treated with vismodegib, although metatypical changes were observed after treatment.
ConclusionsWith a response rate of 96%, vismodegib is a safe and effective treatment for locally advanced BCC. Adverse effects are generally mild but they need to be taken into account owing to their high frequency.
El carcinoma basocelular (CBC) es el tumor cutáneo más frecuente. Aproximadamente el 80% de los tumores cutáneos no melanoma son CBC1, lo que representa una incidencia de 113-253 casos/100.000 personas-año en España2. De estos, se estima una incidencia de CBC avanzado del 0,6-0,8%3, lo que supone aproximadamente unos 300-900 casos al año. Dentro de este grupo se diferencia a los CBC localmente avanzados, donde se incluirían aquellos con lesiones en las que las modalidades de tratamiento actual, como la cirugía o la radioterapia, se consideran potencialmente contraindicadas debido a factores propios del tumor o del paciente4, y a los CBC metastásicos, con diseminación ganglionar o a distancia, situación muy poco frecuente (0,003-0,1% de CBC)5,6.
Diferentes estudios genéticos demuestran la existencia de alteraciones en la vía de señalización Hedgehog en la gran mayoría de los CBC7. En este contexto surge el vismodegib, primer inhibidor selectivo de la vía de la señalización Hedgehog aprobado para el tratamiento del CBC avanzado y metastásico. Este fármaco actúa uniéndose e inactivando específicamente el receptor ligado a la proteína G smoothened (SMO), frenando la activación de la familia de factores de transcripción del oncogén asociado a glioma (GLI), suprimiendo la proliferación y el crecimiento tumoral8.
Vismodegib es un fármaco aprobado desde enero de 2012 en Estados Unidos y desde julio de 2013 en Europa para el tratamiento del CBC avanzado. En junio de 2016, el fármaco recibió la autorización del Ministerio de Sanidad para su financiación en el Sistema Nacional de Salud para su uso en adultos con CBC avanzado o con síntomas de enfermedad metastásica, en la que el médico considera que otras terapias resultan inapropiadas.
ObjetivosEn el presente trabajo describiremos nuestra experiencia en un centro oncológico con el vismodegib en el tratamiento de pacientes con CBC avanzados y/o múltiples durante un periodo de 5 años.
Material y métodosSe realizó un estudio observacional retrospectivo en el que se incluyeron 22 pacientes con CBC tratados en el servicio de dermatología de la Fundación Instituto Valenciano de Oncología entre junio de 2012 y octubre de 2017.
Fueron seleccionados para recibir este tratamiento aquellos pacientes con CBC avanzados y/o múltiples en los que, tras ser evaluados en el comité de tumores de cáncer cutáneo no melanoma, se consideró que otros tratamientos como la cirugía o la radioterapia resultaban inapropiados por el perfil del paciente, la agresividad de la técnica o la probabilidad de éxito de la misma.
Todos los pacientes recibieron vismodegib oral 150mg diarios hasta que presentaron progresión de la enfermedad o toxicidad inaceptable. En algunos pacientes también se interrumpió el tratamiento ante la resolución completa de la enfermedad. Los pacientes fueron seguidos en consultas mensualmente, registrándose la evolución de la lesión, la tolerancia y los efectos secundarios observados.
Las variables analizadas en cada uno de los pacientes fueron: la edad y el sexo del paciente, la localización, el tamaño, el tipo y las características del tumor, el tiempo de evolución, si eran tumores primarios o recidivados, la duración del tratamiento, la respuesta a este (completa, parcial, estabilización o ausencia de respuesta), los efectos secundarios observados y las recidivas posteriores al tratamiento. Consideramos respuesta completa la ausencia de tumor clínico, radiológico y/o histológico. Respuesta parcial, la reducción del 30% del diámetro clínico o radiológico del tumor. Y estabilización cuando el paciente no cumplía criterios de respuesta parcial, respuesta completa o progresión. Por otro lado, consideramos progresión un aumento del tamaño tumoral mayor o igual al 20% del tamaño inicial1.
Para tratar de esclarecer cuánto tarda en aparecer la respuesta al vismodegib, registramos el tiempo de inicio de respuesta, es decir, el tiempo transcurrido desde el inicio del fármaco hasta los primeros indicios de respuesta al mismo. Por otro lado, registramos el tiempo de respuesta máxima, es decir, el tiempo transcurrido hasta la máxima reducción del tumor.
La fuente de recogida de todos los parámetros estudiados fueron las historias clínicas de los pacientes, el archivo de biopsias del servicio de anatomía patológica y el archivo fotográfico de nuestro servicio.
ResultadosEn nuestra serie de casos fueron tratados 22 pacientes, 20 con CBC localmente avanzados y 2 metastásicos con afectación ganglionar. Resumimos las características de estos pacientes en la tabla 1.
Edad y sexo, localización, tamaño, tipo de tumor, años de evolución, tumor primario o recidiva, duración del tratamiento y respuesta al mismo, de los pacientes incluidos en nuestra serie de casos
| Caso | Sexo | Edad | Localización | Tamaño (cm) | Tipo de tumor | Años evolución | Primario o recidiva | Meses tratamiento | Respuesta |
|---|---|---|---|---|---|---|---|---|---|
| 1 | M | 73 | Dorso nasal y 4 en tronco | De 0,5 a 5 | NV | NV | Primario | 5 | RC |
| 2 | F | 70 | Dorso nasal | 4,5×3,5 | CBC infiltrante | 20 | Primario | 7 | RP |
| 3 | M | 68 | Cuero cabelludo | 14×11 | CBC infiltrante ulcerado | 25 | Recidiva | 12 | RP |
| 4 | F | 41 | Mejilla y 4 más (Sdr. Gorlin) | De 2 a 20 | NV | NV | Primario | 18 | RP |
| 5 | F | 97 | Vulva | 13,5×9,5 | CBC infiltrativo | 10 | Primario | 4 | RC |
| 6 | M | 73 | Canto interno ojo derecho y mejilla derecha | De 1,5 a 3 | NV | NV | Primario | 6 | RP |
| 7 | M | 71 | Mejilla y 9 más | De 1 a 7 | NV | NV | Primario | 15 | RP |
| 8 | M | 66 | Canto interno ojo con extensión a órbita | 3,5×2 | CBC infiltrativo | 15 | Primario | 9 | RC |
| 9 | M | 84 | Canto interno ojo con extensión orbitaria y ceja | 5×9 | CBC esclerodermiforme | >3 | Primario | 5 | ES |
| 10 | F | 93 | Canto interno ojo con extensión orbitaria | 3×3 | CBC infiltrante | 24 | Recidiva | 14 | RP |
| 11 | M | 53 | Temporal derecha y órbita derecha+infiltración ganglionar | 14×10 | CBC infiltrante ulcerado | 10 | Primario | 8 | RP |
| 12 | F | 90 | Canto interno del ojo y nariz con infiltración plano óseo | 9×3 | CBC infiltrante | 20 | Recidiva | 17 | RP |
| 13 | M | 50 | Cuero cabelludo con exposición ósea | 8×8 | CBC infiltrante | 15 | Primario | 15 | RC |
| 14 | F | 59 | Canto interno | 3,5×2,5 | CBC basoescamoso | 14 | Recidiva | 22 | ES |
| 15 | F | 50 | Cuero cabelludo | 10×10 | CBC sólido y esclerodermiforme | 11 | Recidiva | 12 | RC |
| 16 | M | 51 | Múltiples CBC (más de 30) (Sdr. Gorlin) | De 0,5 a 5,2 | NV | NV | Primario | 12 | RP |
| 17 | M | 86 | CBC preauricular derecha | 3,5×2 | CBC infiltrativo | 6 | Recidiva | 7 | RC |
| 18 | M | 54 | Canto interno | 2×1,5 | CBC adenoide | 4 | Primario | 19 | RC |
| 19 | M | 76 | Frente con infiltración a plano óseo con infiltración ganglionar | 2×2 | CBC nódulo-quístico | 17 | Recidiva | 10 | RC |
| 20 | M | 64 | Canto interno ojo, y 4 más canto externo | De 1 a 3 | NV | NV | Recidiva | 18 | RP |
| 21 | F | 59 | Nariz y sien izquierda (4) | De 0,5 a 3 | NV | NV | Primario | 6 | RC |
| 22 | F | 72 | Canto interno ojo | 1,5×1,4 | CBC infiltrativo | 14 | Recidiva | 17 | ES |
CBC: carcinoma basocelular; ES: estabilización enfermedad; F: femenino; M: masculino; NV: no valorable; RC: respuesta completa (de todos los tumores en pacientes con múltiples CBC); RP: respuesta parcial.
La mediana de edad de los pacientes al inicio del tratamiento fue de 69 años; 13 eran varones y 9 mujeres. Trece de los tumores tratados eran primarios y 9 recidivas, con una media de 13 años de evolución (1-25 años).
Los tumores se distribuían en su mayoría a nivel periocular (12 casos). Otras localizaciones frecuentemente afectadas fueron: cuero cabelludo (5 casos), nariz (3 casos), frente (2 casos), mejilla (2 casos) y vulva (un caso). Dos de los pacientes incluidos en nuestra serie estaban diagnosticados de síndrome de Gorlin (casos 4 y 16). Los tumores presentaron un tamaño comprendido entre 1,5 y 20cm, con una mediana de 4cm.
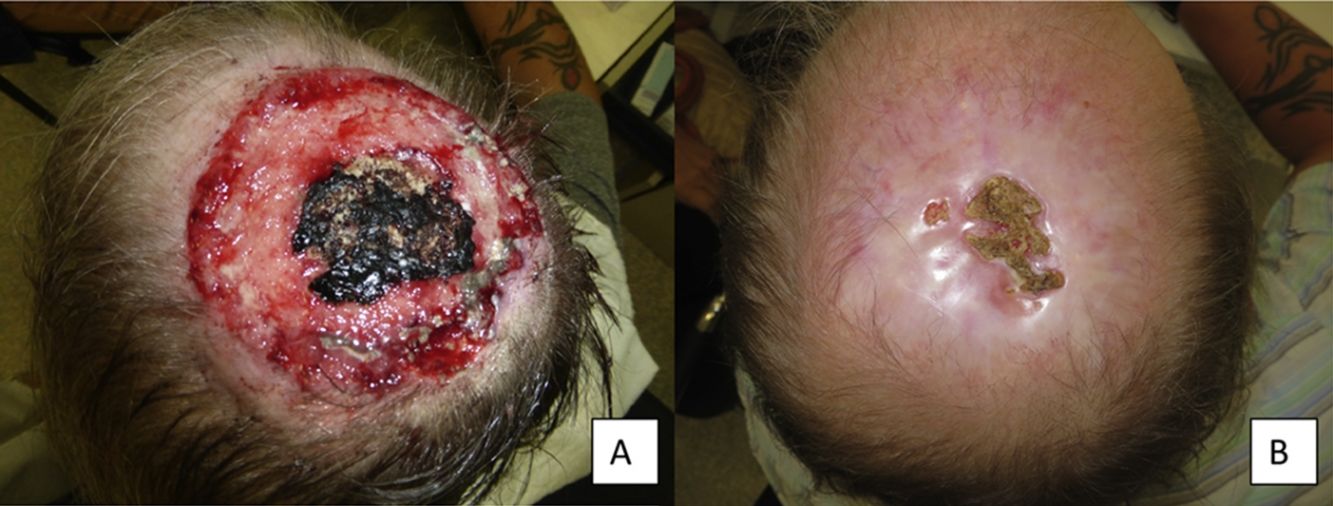
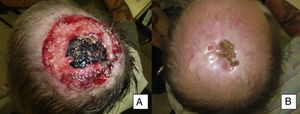
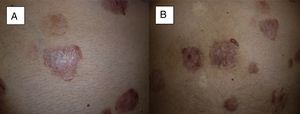
El tratamiento fue administrado durante 11,8 meses de media. En 9 de nuestros pacientes (41% de los casos) se obtuvo una respuesta completa al tratamiento (fig. 1A y B); 10 de nuestros pacientes (45% de los casos) obtuvieron una respuesta parcial (fig. 2A y B, figs. 3 y 4A-D) y en 3 de los pacientes (14% de los casos) vismodegib consiguió estabilizar la enfermedad.
Varón de 50 años con CBC infiltrante de 8×8cm localizado en cuero cabelludo con exposición ósea (A). Recibió vismodegib con inicio de respuesta el primer mes y con respuesta máxima a los 8 meses (B). Actualmente, libre de enfermedad desde hace 13 meses (caso 13 en la tabla 1).
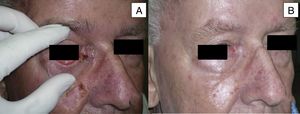
Varón de 73 años con CBC esclerodermiforme de 3×3cm localizado en canto interno (A). Obtiene una respuesta parcial tras 6 meses de tratamiento (B) (caso 6 en la tabla 1).
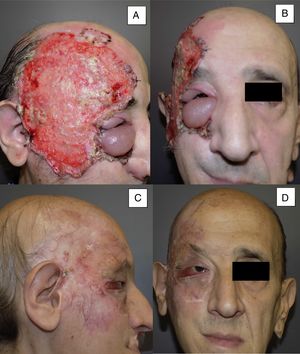
Varón de 53 años con CBC infiltrante ulcerado de 14×10cm localizado en región temporal derecha y órbita derecha con edema palpebral asociado e infiltración de adenopatías (A y B). Tras 8 meses de tratamiento, a nivel clínico parece observarse una respuesta completa al tratamiento (C y D). No obstante, en una biopsia de control realizada durante el seguimiento del paciente, se siguen observando restos tumorales, clasificándose como respuesta parcial (caso 11 en la tabla 1).
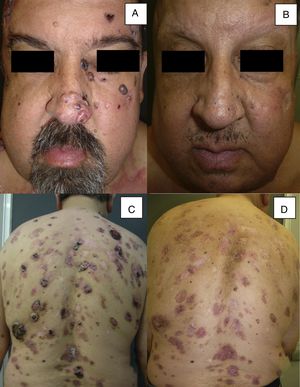
Varón de 51 años afecto de síndrome de Gorlin con múltiples CBC (más de 30) (A y C); obtiene una respuesta parcial al tratamiento tras 12 meses de tratamiento (B y D) (caso 16 en la tabla 1).
Del análisis del tiempo de respuesta al fármaco, obtuvimos un tiempo de inicio de respuesta de un mes de mediana (1-5 meses). Por otro lado, el tiempo de respuesta máxima se observó a los 5 meses de mediana (1-15).
A nivel histológico, en los casos con respuesta completa se observó un remplazamiento del tejido tumoral por dermis con abundante estroma hialino, en ocasiones con leve infiltrado inflamatorio asociado. En las respuestas parciales se observaron dos tendencias: en una el tumor reducía su tamaño y ulceración manteniendo una morfología de CBC; en la otra el tumor se volvía metatípico, con células más grandes y eosinófilas, con núcleos grandes y pleomórficos, es decir, más indiferenciadas. Además, en un caso el tumor cambió su subtipo pasando de CBC infiltrante a CBC basoescamoso.
Los pacientes fueron seguidos durante una media de 38 meses y una mediana de 21 meses (3-59). Entre el total de pacientes que obtuvieron una respuesta completa (9 casos), se produjo recidiva clínica, histológica y/o radiológica en 2 de ellos (22%), con un tiempo hasta la recidiva de 2 y 10 meses (fig. 5A y B). En nuestra serie ningún paciente desarrolló un carcinoma epidermoide sobre el área tratada con vismodegib. No obstante, sí se presentó un carcinoma epidermoide en una localización diferente a la tratada a los 3 años de haber finalizado el tratamiento.
Recurrencia a los 4 meses de la finalización del tratamiento. Se observa en dos de los tumores localizados en el abdomen como se inicia la recurrencia local desde la periferia del tumor (A y B) (caso 16 en la tabla 1).
En cuanto a los pacientes con CBC metastásico, uno de ellos (caso 11) obtuvo una respuesta parcial al tratamiento con reducción del tamaño de la adenopatía cervical afecta por el tumor, según la RMN realizada 3 meses después del inicio del fármaco. El otro paciente con CBC metastásico (caso 19) obtuvo una respuesta completa a nivel de la lesión sin evidenciarse nueva afectación ganglionar en las pruebas de imagen solicitadas durante el seguimiento posterior (la adenopatía afecta localizada en la región parotídea fue extirpada previamente al inicio del fármaco).
Todos los pacientes presentaron algún efecto secundario. Los principales efectos secundarios observados fueron disgeusia, alopecia y calambres musculares. Aunque todos ellos fueron de carácter leve, en 5 casos provocaron la interrupción temporal del tratamiento por intolerancia del paciente.
DiscusiónA pesar de que no existe una definición establecida para los CBC localmente avanzados, se ha propuesto emplear este término para aquellos CBC en estadioII de la American Joint Committee on Cancer (AJCC) (tumores >2cm y con al menos dos factores de alto riesgo, como profundidad de invasión mayor de 2mm, nivel de ClarkIV, invasión perineural, localización en H facial y pobre diferenciación tumoral)9. Posteriores publicaciones, como la de un grupo multidisciplinar británico, apoyan esta definición y añaden una serie de factores dependientes del tumor (tamaño tumoral gigante, localización en H facial, número de tumores elevado, subtipo histológico y posibilidad de tratamiento curativo) y dependientes del paciente (edad, estado general del paciente, reducción de la calidad de vida como consecuencia del tratamiento, opinión del paciente, presencia de genodermatosis o comorbilidades importantes)10.
En este contexto surge vismodegib como terapia dirigida con capacidad de inhibir selectivamente la vía de señalización molecular del CBC, ofreciendo una alternativa terapéutica a la cirugía o radioterapia en el tratamiento de los CBC avanzados.
Sekulic et al. llevaron a cabo el estudio pivotal ERIVANCE, en el que incluyeron a 104 pacientes (71 CBC localmente avanzados y 33 CBC metastásicos) que recibieron vismodegib 150mg diarios. En este primer ensayo, se obtuvieron respuestas del 48,5% en CBC metastásicos y del 60,3% en CBC localmente avanzados1. Posteriormente se diseñaron ensayos como el STEVIE, con un total de 1.232 pacientes, con el objetivo primario de monitorizar la seguridad del fármaco, y MIKIE, en el que se incluían pacientes con múltiples CBC. STEVIE obtuvo una tasa de respuesta del 68,5%11, mientras que MIKIE consiguió porcentajes de respuesta de entre el 54 y el 62%12.
La tasa de respuesta a vismodegib en nuestra serie fue del 41% de respuestas completas y del 45% de respuestas parciales, lo que supone una tasa de respuesta conjunta al fármaco del 86%, considerablemente superior a ERIVANCE (60,3%), STEVIE (68,5%) y MIKIE (54-62%). Por otro lado, el fármaco consiguió estabilizar la enfermedad en el 14% de los casos. Pensamos que esta diferencia de tasa de respuesta entre nuestra serie y los ensayos publicados puede deberse al pequeño tamaño de la muestra de pacientes de nuestra serie (n=22), comparados con los 104 pacientes incluidos en ERIVANCE, los 229 en MIKIE o los 1.232 de STEVIE.
En cuanto al tiempo que necesita el fármaco para obtener los primeros resultados recordamos que, del análisis del tiempo de respuesta al fármaco, obtuvimos un tiempo de inicio de respuesta de un mes de mediana (1-5 meses) y un tiempo de respuesta máxima de 5 meses de mediana (1-15). En este caso resultan similares nuestros resultados y los de ERIVANCE, que describió un tiempo hasta la reducción máxima del tumor de 5,5-6,7 meses1. Con vismodegib, por tanto, obtuvimos resultados clínicamente visibles ya desde las primeras revisiones, alcanzando en muchas ocasiones la respuesta máxima a los pocos meses de inicio del fármaco. Como en nuestro caso 1, un varón de 73 años con múltiples CBC en quien, ya en la primera visita de revisión (1.er mes), todas las lesiones mostraban un aspecto cicatricial con práctica ausencia clínica de tumor residual (tabla 1, caso 1).
El fármaco se toma en forma de comprimidos con una dosis diaria de 150mg. Está contraindicado el embarazo, por lo que hay que establecer un programa de prevención del mismo tanto en el varón como en la mujer. Se debe evitar el embarazo durante el tratamiento y 2 meses después en el varón y hasta 2 años después en la mujer. Siempre que sea posible, debe realizarse una biopsia para asegurar el diagnóstico y una RMN para medir la respuesta radiológica posterior. Así mismo, debemos seguir al paciente mensualmente con controles analíticos con función hepática y muscular.
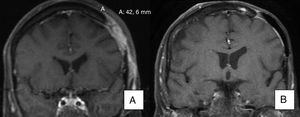
En cuanto a cómo integrar el uso del fármaco con las terapias ya existentes, en nuestra experiencia el uso concurrente de vismodegib parece mostrar un efecto sinérgico con la radioterapia, lo que podría deberse a su efecto radiosensibilizante sobre el tumor. El caso 15 de nuestra serie, una mujer de 50 años con un CBC esclerodermiforme de 10×10cm localizado en cuero cabelludo, intervenida quirúrgicamente en 15 ocasiones por múltiples recidivas, a la cual se le llegó a practicar una craneotomía con tratamiento radioterápico posterior, recibió tratamiento con vismodegib durante 12 meses obteniendo una respuesta completa al mismo (fig. 6A y B), sin recidivas hasta el momento actual (intervalo libre de enfermedad de 17 meses). En este sentido existen casos publicados con experiencias similares en cuanto al uso combinado del fármaco y radioterapia, con excelente respuesta, sin efectos secundarios añadidos a los del propio fármaco y con buena tolerancia por parte del paciente13.
A) RMN previa en la que se observa infiltración ósea del tumor. B) Resolución radiológica tras 12 meses de tratamiento (caso 15 en la tabla 1).
Existen publicaciones que afirman que vismodegib puede incrementar el riesgo de transformación a carcinoma escamoso de los CBC tratados con el fármaco, así como de desarrollo de carcinomas epidermoides en otras localizaciones. Mohan et al. publicaron un artículo en el que describieron un incremento del riesgo de desarrollo de un tumor, diferente del CBC, tras el tratamiento con vismodegib, con un hazard ratio de 6,37, y de 8,12 en el caso de carcinomas epidermoides14. No obstante, este artículo fue ampliamente criticado por autores como Puig et al.15, principalmente por un inadecuado diseño del estudio, al tratarse de un estudio de cohortes retrospectivo en lugar de un estudio de casos y controles, como describieron en el artículo. Además en el estudio se incluyeron todos los tumores aparecidos, alguno de ellos diagnosticado tan solo 15 días después del inicio del fármaco15. Como ya comentamos, en nuestra serie ningún paciente desarrolló un carcinoma epidermoide sobre el área tratada con vismodegib, aunque sí lo hizo uno de nuestros pacientes 3 años después y en una localización diferente a la tratada. Los últimos artículos publicados parecen ir en ese sentido, como el reciente artículo de Bhutani et al., en el que se realiza un estudio retrospectivo de 1.675 pacientes tratados con el fármaco dentro de los ensayos STEVIE y ERIVANCE, llegándose a la conclusión de que el tratamiento con vismodegib no se asocia a un aumento del desarrollo de carcinoma epidermoide16. No obstante, sí puede observarse durante el tratamiento un cambio en la histología a carcinoma basocelular metatípico o incluso basoescamoso.
Respecto al perfil de seguridad y tolerabilidad del fármaco, muchos de los acontecimientos adversos están relacionados con el mecanismo de acción del fármaco. La mayoría de estos son grados 1 y 217. En nuestra experiencia, la práctica totalidad de nuestros pacientes presentaron efectos adversos, siendo los más frecuentes disgeusia, alopecia y calambres musculares, todos ellos de carácter leve. Otros observados fueron la astenia, la anorexia y la pérdida de peso. En 5 pacientes (22,7%) provocaron la interrupción temporal del tratamiento por el carácter invalidante de los mismos, sobre todo disgeusia y ageusia. Porcentaje similar al de ensayos como ERIVANCE, en el que un 21,2% de los pacientes tuvieron que interrumpir el tratamiento18. Un aspecto importante relacionado con lo anterior es que las interrupciones del tratamiento no parecen comprometer su eficacia11; de hecho, en el ensayo ERIVANCE se permitieron interrupciones de hasta 8 semanas sin que estas influyeran en la respuesta al fármaco1.
ConclusionesEl vismodegib es un fármaco seguro y eficaz para el tratamiento de los CBC avanzados, con porcentajes de respuesta de entre el 54-86%. El inicio de respuesta a vismodegib es rápido (un mes de mediana) y se consigue el máximo de respuesta en menos de 6 meses (5 meses de mediana). Ninguno de nuestros pacientes desarrolló un carcinoma epidermoide sobre el área tratada con vismodegib. Sin embargo, es conveniente realizar un seguimiento cuidadoso de los pacientes y biopsiar áreas de aparente resistencia al tratamiento por la posibilidad de cambios metatípicos en la histología. Los efectos adversos deben tenerse en cuenta por su alta frecuencia, aunque estos suelen ser de carácter leve.
Conflicto de interesesB. Llombart, C. Serra-Guillén y O. Sanmartín han impartido charlas remuneradas para Hoffmann-La Roche. El resto de los autores declaran no tener ningún conflicto de intereses.