El uso de los agentes biológicos en el tratamiento de las enfermedades inflamatorias crónicas, principalmente reumatológicas, dermatológicas y digestivas, ha llevado aparejado una actualización en el diagnóstico y el manejo terapéutico de los efectos adversos asociados. Entre ellos se incluye la exacerbación de algunas de las patologías que presentan nuestros pacientes y que, si bien ha habido casos de tratamiento exitoso de las mismas, también se han comunicado reagudizaciones de difícil control1. Presentamos un caso de exacerbación de dermatitis atópica en un paciente con colitis ulcerosa tratado con infliximab, y revisamos los casos previamente publicados en la literatura.
Presentamos el caso de un varón de 30 años, con antecedentes personales de colitis ulcerosa en tratamiento con infliximab (refractaria a tratamiento con mesalazina y azatioprina), y que desde su quinta infusión presentó un cuadro de eccema generalizado, intensamente pruriginoso y que no cedía con corticoides tópicos ni antihistamínicos orales.
El paciente tenía antecedentes de dermatitis atópica (DA) desde la infancia. No refería rinitis ni asma bronquial extrínseca. Las lesiones siempre se habían focalizado en las flexuras (huecos antecubitales y poplíteos) y se habían controlado con corticoides e inhibidores de la calcineurina tópicos, sin necesidad de terapia sistémica o fototerapia.
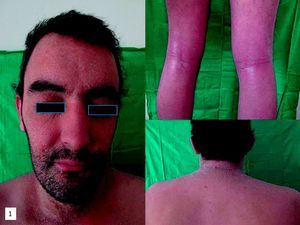
En la exploración física destacaba eritema y fina descamación en la cara, el tronco y las flexuras de los miembros, con afectación de casi el 50% de la superficie corporal (fig. 1). No había alteración de las constantes vitales ni compromiso respiratorio.
Las pruebas complementarias no mostraron eosinofilia, elevación de IgE ni de reactantes de fase aguda (PCR, VSG). El estudio histológico mostró espongiosis moderada e infiltrado perivascular de predominio linfocitario. La ausencia de queratinocitos necróticos, el mínimo daño de la capa basal y el infiltrado linfocitario profundo sin eosinófilos junto con la clínica, favorecía más la posibilidad de una exacerbación de su DA que la de una toxicodermia.
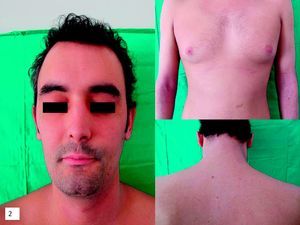
Optamos por la suspensión cautelar de infliximab e iniciamos terapia con prednisona 0,5mg/kg/día y lenta reducción hasta el control del proceso en tres semanas (fig. 2).
La DA desde el punto de vista etiopatogénico se caracteriza en la fase aguda por un patrón Th2 (con elevación de IgE y eosinofilia en numerosos casos), mientras que en la fase crónica2 el patrón inflamatorio es Th1. Por ello sería esperable que los agentes anti-TNF3 utilizados en la psoriasis mejorasen las formas crónicas de la DA sin una respuesta clara en la fase aguda.
En la fase crónica de la DA hay una elevación sérica del TNF-α, el cual es liberado inicialmente por los mastocitos y posteriormente por los linfocitos T colaboradores y los queratinocitos. Su liberación contribuye a estimular la cascada inflamatoria con aumento de los niveles de IL 1, 6, 8 y moléculas de adhesión celular (ICAM-1) y vascular (VCAM). La evolución clínica y patogénica de un patrón de respuesta Th2 a otro Th1 podría explicar el éxito en algunas series de pacientes atópicos crónicos2. Sin embargo, parece probable la implicación adicional de otros factores etiopatogénicos no identificados, porque en la mayoría de los casos publicados la respuesta queda limitada a la fase de inducción3.
En la revisión bibliográfica realizada hemos encontrado 7 casos bien documentados de exacerbación de DA o DA-like con infliximab4–7, lo cual nos ha parecido interesante. Es posible que esto se deba a que algunos casos de exacerbación de DA se hayan podido catalogar como eccema inespecífico (la DA ha sido considerada como factor predictor de aparición de eccemas like en pacientes con psoriasis que reciben infliximab)8, o que se trate de un efecto adverso infradiagnosticado, o finalmente por la escasa incidencia de casos que hayan requerido una terapia más agresiva8,9. Los casos a los que hacemos referencia junto con el nuestro quedan reflejados en la tabla 1.
Características clínicas y evolutivas de pacientes con exacerbacion de dermatitis atópica por infliximab
| Edad | Sexo | Patología basal | AP- atopia | Dosis | Aparición temporal de la reagudización de la DA | Evolución y actitud respecto a IFX | |
| 1 (Wright RC4) | 83 | Varón | Psoriasis | + | 5mg/kg/día | 1.a infusión | Continúa control con terapia tópica |
| 2 (Wright RC4) | 68 | Mujer | Artritis reumatoide | +/- | 5mg/kg/día | No especificado | Continúa control con terapia tópica |
| 3 (Vestergaard C et al.5) | 46 | Varón | Psoriasis suberitrodérmica+artropatía psoriásica | + | 5mg/kg/día | 7.a infusión | Suspendido control con ciclosporina |
| 4 (Vestergaard C et al.5) | 68 | Varón | Psoriasis pustulosa | + | 5mg/kg/día | 8.a infusión | Suspendido control con ciclosporina |
| 5 (Chan JL et al.6) | 45 | Varón | Psoriasis | + | 3mg/kg/día | 2.a infusión | Continúa control con terapia tópica |
| 6 (Chan JL et al.6) | 62 | Mujer | Artritis reumatoide | + | 5mg/kg/día | 7.a infusión | Continúacontrol con terapia tópica |
| 7 (Chan JL et al.6) | 15 | Varón | Enfermedad de Crohn | + | 5mg/kg/día | 3.a infusión | Suspendido control con terapia tópica |
| 8 (Ruiz-Villaverde et al.) | 30 | Varón | Colitis ulcerosa | + | 5mg/kg/día | 5.a infusión | Suspendido control con CTC v.o.+tópicos |
AP: antecedentes personales; CTC v.o.: corticoterapia vía oral; DA: dermatitis atópica; IFX: infliximab.
En relación con los casos comunicados, casi todos presentan antecedentes de dermatitis atópica y tan solo difieren en la patología basal subsidiaria de tratamiento con infliximab. No hay un claro patrón respecto al momento en el que pueden presentarse estas reacciones, si bien en todos los casos aparecen en los dos primeros años de tratamiento. Nuestro paciente requirió tratamiento sistémico y creemos importante reseñar que, a pesar de lo extenso de su afectación, no hubo alteraciones en las pruebas analíticas como en los casos previamente reseñados.
Con independencia de que el aumento en el conocimiento de los factores etiopatogénicos de la DA y las terapias biológicas es cada día mayor, todavía existen lagunas que nos impiden predecir el desarrollo de este tipo de efectos secundarios, a priori no esperables desde el punto de vista fisiopatológico. Así, mediante la presentación de este caso queremos remarcar la importancia de la recogida minuciosa de antecedentes dermatológicos de DA en la anamnesis de pacientes subsidiarios de terapia biológica, especialmente en pacientes reumatológicos y con enfermedad inflamatoria intestinal.
Responsabilidades éticasProtección de personas y animales. Los autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki. Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio. Derecho a la privacidad y consentimiento informado. Los autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.