El manejo de apremilast en la práctica clínica complementa la información procedente de los ensayos clínicos pivotales.
Material y métodoTras una revisión de la literatura se consideraron, por parte de un panel de dermatólogos expertos en el manejo de la psoriasis, 5 áreas donde la evidencia sobre el uso de apremilast en la psoriasis moderada era insuficiente o controvertida, que fueron evaluadas a través de un cuestionario diseñado según la metodología Delphi.
ResultadosSe alcanzó consenso en 96 de los 143 ítems planteados (67%) (85 en el acuerdo y 11 en el desacuerdo). El objetivo terapéutico con apremilast debería ponderarse entre la respuesta clínica, la sintomatología asociada, la calidad de vida y la satisfacción del paciente. El perfil en el que el uso de apremilast se considera con mayores posibilidades de éxito sería el de un paciente con psoriasis moderada estable. La mayoría de los clínicos consideraron que apremilast es adecuado para pacientes en los que hayan fracasado o estén contraindicados los tratamientos convencionales, preferentemente de forma previa a la indicación de terapia biológica. Hubo consenso en reconocer apremilast como una opción terapéutica adecuada para el tratamiento en localizaciones difíciles, como la psoriasis palmoplantar y del cuero cabelludo. La necesidad de cribado, así como de su monitorización durante el seguimiento, se consideró menor que la de otros tratamientos sistémicos, convencionales y biológicos.
ConclusionesApremilast podría representar una opción terapéutica en un perfil de pacientes distinto al presentado en los ensayos clínicos. La ausencia de un consenso sobre la definición de psoriasis moderada, la escasa evidencia acerca del fármaco en la vida real, así como algunos aspectos relacionados con la tolerabilidad representan limitaciones a estas propuestas.
Experience in the use of apremilast in clinical practice complements the information available from pivotal clinical trials.
Material and methodFollowing a review of the literature, a panel of dermatologists with expertise in the management of psoriasis considered 5 scenarios in which the evidence supporting the use of apremilast to treat moderate psoriasis is insufficient or controversial. These scenarios were then assessed using a Delphi questionnaire.
ResultsConsensus was reached on 96 (67%) of the 143 items (positive in 85 and negative in 11). The therapeutic goal for apremilast should be based on 4 outcomes: clinical response, symptoms, quality of life, and patient satisfaction. The scenario in which the use of apremilast was considered to have the greatest possibility of success was in patients with stable moderate psoriasis. Most of the clinicians considered apremilast to be an appropriate treatment when conventional therapies fail or are contraindicated, preferably before the prescription of biologic therapy. Consensus was reached that apremilast is an appropriate treatment for psoriasis in difficult locations, such as the scalp or the palms and soles. It was also agreed that apremilast requires less prescreening and monitoring than other conventional and biologic systemic therapies.
ConclusionsApremilast could be a treatment option for patients with a different profile to that of clinical trial participants. The limitations of this proposal are the absence of consensus on the definition of moderate psoriasis, the lack of real-world evidence on the use of apremilast, and certain aspects related to tolerability.
Apremilast es un inhibidor oral de la fosfodiesterasa 4 que ejerce una acción inmunomoduladora, bloqueando parcialmente la expresión de citocinas proinflamatorias e induciendo la expresión de citocinas antiinflamatorias implicadas en la patogénesis de la psoriasis. Este fármaco está indicado en el tratamiento de la psoriasis moderada a grave1 y en la artritis psoriásica, con un perfil de seguridad y tolerabilidad aceptables a corto y largo plazo. Sin embargo, debido al perfil de los pacientes incluidos en los ensayos clínicos pivotales de este fármaco, muy similar al de pacientes candidatos a terapia biológica2,3, existen deficiencias en el conocimiento de las posibilidades de apremilast en la práctica clínica habitual, tanto en relación con la identificación del paciente candidato a su prescripción como al correcto posicionamiento del fármaco respecto a otras terapias convencionales y biológicas. En este sentido, las recomendaciones consensuadas basadas en la opinión de los expertos y elaboradas a través de metodologías validadas y rigurosas aportan guías de trabajo útiles para estas situaciones, dotando a los expertos de información valiosa en la práctica clínica4.
A fin de complementar la evidencia disponible en la literatura sobre el uso de apremilast, un grupo de expertos llevó a cabo una evaluación de aquellos escenarios y aspectos en los que la información publicada se consideró insuficiente.
Material y métodosComité científicoEl comité científico estaba compuesto por un coordinador nacional (JMC) y 5 coordinadores regionales (RR, IB, MGB, MA, PH). Los miembros regionales propusieron y discutieron escenarios clínicos donde, por la falta actual de evidencia o de consenso, se consideró de interés desarrollar recomendaciones terapéuticas respecto al uso de apremilast. Se escogieron 5 escenarios: i) eficacia en la psoriasis moderada de forma previa al uso de biológicos en pacientes con psoriasis moderada; ii) eficacia en localizaciones especiales: afectación ungueal, cuero cabelludo y palmoplantar; iii) eficacia en pacientes con psoriasis y artritis psoriásica asociada; iv) manejo y despistaje de comorbilidades en la psoriasis, y v) implicaciones de la seguridad en el uso de apremilast.
Revisión de la literaturaSe realizó una búsqueda bibliográfica en las bases de datos Medline y The Cochrane Library con el objetivo de definir una serie de ítems relacionados con escenarios clínicos en psoriasis para los cuales la evidencia clínica no era suficiente para responder las preguntas planteadas en la clínica. Para cada uno de los escenarios propuestos se diseñó una única estrategia de búsqueda, que se complementó con una búsqueda manual. En la selección de la información se dio prioridad a los ensayos clínicos aleatorizados y los estudios de práctica clínica real, aunque también se incluyeron documentos de consenso, artículos de recomendación y guías clínicas actualizados. La búsqueda bibliográfica se realizó en febrero de 2018 y solo se incluyeron artículos publicados originalmente en inglés o español. En el caso de los ensayos clínicos y los estudios de vida real, no se aplicó ninguna restricción temporal (Tabla 1). De forma posterior a la finalización del artículo se realizaron búsquedas adicionales en las mismas bases de datos con la intención de conseguir información actualizada de apremilast en la vida real (búsqueda bibliográfica adicional en mayo de 2019).
Metodología de la revisión bibliográfica
| Las estrategias de búsqueda para cada escenario fueron las siguientes: i) Escenario #1: «(Apremilast OR otezla) AND (psoriasis OR moderate psoriasis OR severe to moderate psoriasis) AND efficacy NOT psoriatic arthritis» (45 citas/12 ensayos clínicos); ii) Escenario #2: «(Apremilast OR otezla) AND (psoriasis OR moderate psoriasis OR severe to moderate psoriasis) AND efficacy AND (scalp OR nail OR palmoplantar OR difficult to treat) NOT psoriatic arthritis» (9 citas/2 ensayos clínicos); iii) Escenario #3: «(Apremilast OR otezla) AND (psoriasis OR moderate psoriasis OR severe to moderate psoriasis) AND psoriatic arthritis AND efficacy» (214 citas/2 ensayos clínicos); iv) Escenario #4: «psoriasis AND comorbid* AND (screening OR management) NOT psoriatic arthritis» (513 citas/8 ensayos clínicos); v) Escenario #5: «(Apremilast OR otezla) AND (psoriasis OR moderate psoriasis OR severe to moderate psoriasis) AND safety NOT psoriatic arthritis» (27 citas/11 ensayos clínicos) |
Los expertos alcanzaron acuerdo positivo en 30 (55,6%; 24 en primera ronda y 6 en segunda) y acuerdo negativo en 3 (5,6%; 2 en primera ronda y uno en segunda) de los 54 ítems incluidos en esta sección del cuestionario. El PASI absoluto y la satisfacción global reportada por el paciente se consideraron los parámetros más apropiados para la valoración de apremilast en la práctica clínica. Se acordó que sería adecuado mantener el tratamiento hasta la semana 24 en los pacientes que alcancen una respuesta parcial en la semana 16 cuando se objetive una respuesta PASI<50 y/o un PASI absoluto>5, siempre que aquellos se mostrasen satisfechos con el tratamiento y no se observase un impacto importante en su calidad de vida (Dermatology Life Quality Index [DLQI]<1). La satisfacción con el tratamiento debería considerarse como justificación para valorar el mantenimiento del tratamiento más allá de la semana 24, aun cuando no se hubiese alcanzado una respuesta PASI 75.
Se acordó que apremilast es una opción terapéutica adecuada para el tratamiento de los pacientes con psoriasis moderada que no respondan o presenten contraindicación a las terapias sistémicas convencionales y que aún no sean candidatos o no respondan o presenten contraindicación a las terapias biológicas. Las circunstancias que influirían en mayor medida en la elección de apremilast serían: i) afectación cutánea moderada; ii) cuadro clínico estable; iii) sintomatología asociada; iv) presencia de psoriasis palmoplantar; v) presencia de comorbilidades; vi) polimedicación; vii) pacientes jóvenes en los que se prevén tratamientos muy prolongados, y viii) pacientes con fobia a las inyecciones. Apremilast no se consideró, por el contrario, una opción adecuada para los pacientes que presenten formas inestables de enfermedad con afectación cutánea extensa ni en aquellos que requieran una resolución rápida de las lesiones cutáneas.
La combinación de apremilast con fototerapia, particularmente ultravioleta B de banda estrecha, se valoró como adecuada en las siguientes circunstancias: i) desde el inicio del tratamiento en pacientes que requieran respuesta cutánea rápida; ii) en pacientes que no hayan alcanzado una respuesta óptima tras 16-24 semanas, pero que estén satisfechos con el tratamiento, y iii) en pacientes en los que se empiece a observar una disminución de la eficacia alcanzada (Tabla 2).
Eficacia en la psoriasis moderada: casos de uso previo a biológicos en pacientes con enfermedad moderada
| Ítem | Mediana | MAD-M | Adecuación | Acuerdo | Resultado | |
|---|---|---|---|---|---|---|
| 1 | Es necesario diferenciar la psoriasis en placas moderada de la psoriasis grave, teniendo en cuenta las distintas estrategias terapéuticas en ambos grupos | 8 | 0,94 | Apropiado | Acuerdo | Consenso en primera ronda |
| 2 | Es necesario definir mejor los criterios para la clasificación de la psoriasis en placas moderada | 9 | 0,47 | Apropiado | Acuerdo | Consenso en primera ronda |
| 3 | Es necesario definir mejor los criterios de respuesta terapéutica en la psoriasis en placas moderada | 8 | 0,76 | Apropiado | Acuerdo | Consenso en primera ronda |
| 4 | Los índices más adecuados para evaluar la respuesta en la psoriasis moderada son: | |||||
| PASI 75/90/100 | 6 | 1,18 | Incierto | Neutral | No consenso | |
| PASI relativo (porcentaje de mejoría) | 7 | 0,94 | Apropiado | Neutral | No consenso | |
| PASI (valor absoluto) | 8 | 1,06 | Apropiado | Acuerdo | Consenso en primera ronda | |
| BSA | 5 | 1,18 | Incierto | Neutral | No consenso | |
| PGA | 8 | 0,71 | Apropiado | Acuerdo | Consenso en segunda ronda | |
| DLQI | 8 | 0,94 | Apropiado | Neutral | No consenso | |
| Satisfacción global reportada por el paciente | 8 | 1,06 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Cuestionarios de satisfacción autorreportados por el paciente (objetivos referidos por el paciente) | 7 | 0,76 | Apropiado | Neutral | No consenso | |
| 7 | Los parámetros terapéuticos más adecuados en la valoración del efecto terapéutico del tratamiento con apremilast son: | |||||
| PASI 75 | 6 | 1,35 | Incierto | Neutral | No consenso | |
| PASI relativo (porcentaje de mejoría) | 7 | 1,00 | Apropiado | Neutral | No consenso | |
| PASI (valor absoluto) | 8 | 0,71 | Apropiado | Acuerdo | Consenso en primera ronda | |
| PGA | 7 | 1,29 | Apropiado | Neutral | No consenso | |
| BSA | 6 | 1,35 | Incierto | Neutral | No consenso | |
| PGA×BSA | 5 | 1,18 | Incierto | Neutral | No consenso | |
| Mejoría de la calidad de vida (DLQI) | 6 | 0,94 | Incierto | Neutral | No consenso | |
| Escala EVA (prurito/dolor) | 7 | 1,24 | Apropiado | Neutral | No consenso | |
| Seguridad | 9 | 1,06 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Tolerabilidad | 7 | 1,18 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Satisfacción global reportada por el paciente | 8 | 0,88 | Apropiado | Acuerdo | Consenso en primera ronda | |
| 8 | El objetivo terapéutico del tratamiento con apremilast debería contemplar tanto la respuesta clínica como la sintomatología asociada y la calidad de vida, en función de las características individuales de los pacientes | 9 | 0,71 | Apropiado | Acuerdo | Consenso en primera ronda |
| 9 | La satisfacción del paciente con el tratamiento con apremilast es una medida especialmente relevante a la hora de evaluar el efecto terapéutico del fármaco | 8 | 1,12 | Apropiado | Acuerdo | Consenso en primera ronda |
| 10 | Es adecuado cambiar el tratamiento con apremilast ante: | |||||
| Ausencia de respuesta PASI 50 durante las primeras 16 semanas de tratamiento | 7 | 1,29 | Apropiado | Neutral | No consenso | |
| Ausencia de respuesta PASI 75 durante las primeras 16 semanas de tratamiento | 4 | 1,35 | Incierto | Neutral | No consenso | |
| PASI absoluto mayor de 7 durante las primeras 16 semanas de tratamiento | 7 | 1,47 | Apropiado | Neutral | No consenso | |
| PASI absoluto mayor de 5 durante las primeras 16 semanas de tratamiento | 7 | 1,29 | Apropiado | Neutral | No consenso | |
| PASI absoluto mayor de 3 durante las primeras 16 semanas de tratamiento | 3 | 1,18 | Inapropiado | Acuerdo | Consenso en segunda ronda | |
| 11 | Es adecuado mantener el tratamiento con apremilast aunque la respuesta PASI sea menor de 50 y/o el PASI absoluto sea mayor de 5 en las primeras 16 semanas de tratamiento si el impacto en la calidad de vida y/o la satisfacción de los pacientes son satisfactorios (DLQI menor de 5) | 6 | 1,29 | Incierto | Neutral | No consenso |
| 12 | Es adecuado mantener el tratamiento con apremilast aunque la respuesta PASI sea menor de 50 y/o el PASI absoluto sea mayor de 5 en las primeras 16 semanas de tratamiento si el impacto en la calidad de vida y/o la satisfacción de los pacientes son satisfactorios (DLQI menor de 1) | 7 | 1,29 | Apropiado | Acuerdo | Consenso en segunda ronda |
| 13 | En los pacientes con una respuesta parcial (50<PASI<75) en las primeras 16 semanas de tratamiento con apremilast es adecuado mantener el tratamiento hasta la semana 24 y realizar una posterior evaluación | 8 | 0,59 | Apropiado | Acuerdo | Consenso en primera ronda |
| 14 | En los pacientes que refieren satisfacción con el tratamiento con apremilast es adecuado mantener el tratamiento, aunque no se alcance una respuesta PASI 75 tras 24 semanas de tratamiento | 8 | 1,53 | Apropiado | Acuerdo | Consenso en primera ronda |
| 19 | La estrategia de combinar apremilast con fototerapia (UVB-BE) es adecuada en los siguientes supuestos: | |||||
| Al iniciar el tratamiento con apremilast, en aquellos pacientes que precisen una respuesta cutánea más rápida | 9 | 0,94 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Durante la administración de apremilast, en aquellos pacientes que no llegan a alcanzar una respuesta óptima tras 16-24 semanas de tratamiento, pero refieren satisfacción con el tratamiento | 8 | 1,53 | Apropiado | Acuerdo | Consenso en primera ronda | |
| En aquellos pacientes en los que se observa una reducción de la eficacia alcanzada durante la administración continuada de apremilast | 8 | 1,29 | Apropiado | Acuerdo | Consenso en primera ronda | |
| 22 | La posibilidad de interrumpir el tratamiento con apremilast, recuperando su eficacia en el retratamiento, es una cualidad adicional de apremilast adecuada a la hora de requerir una interrupción temporal del tratamiento | 8 | 0,76 | Apropiado | Acuerdo | Consenso en primera ronda |
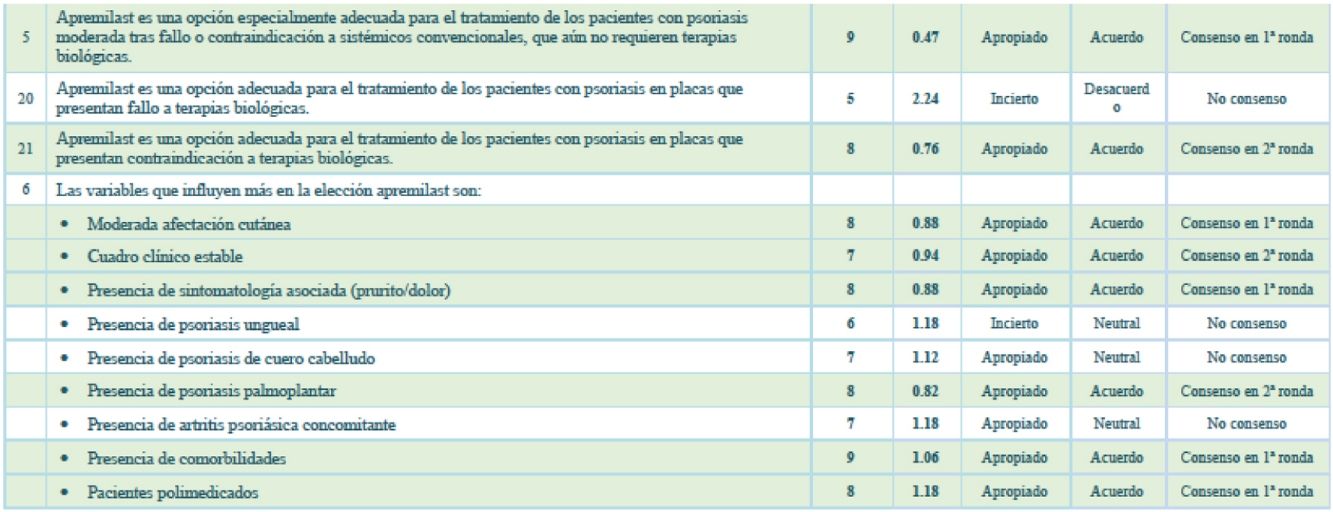
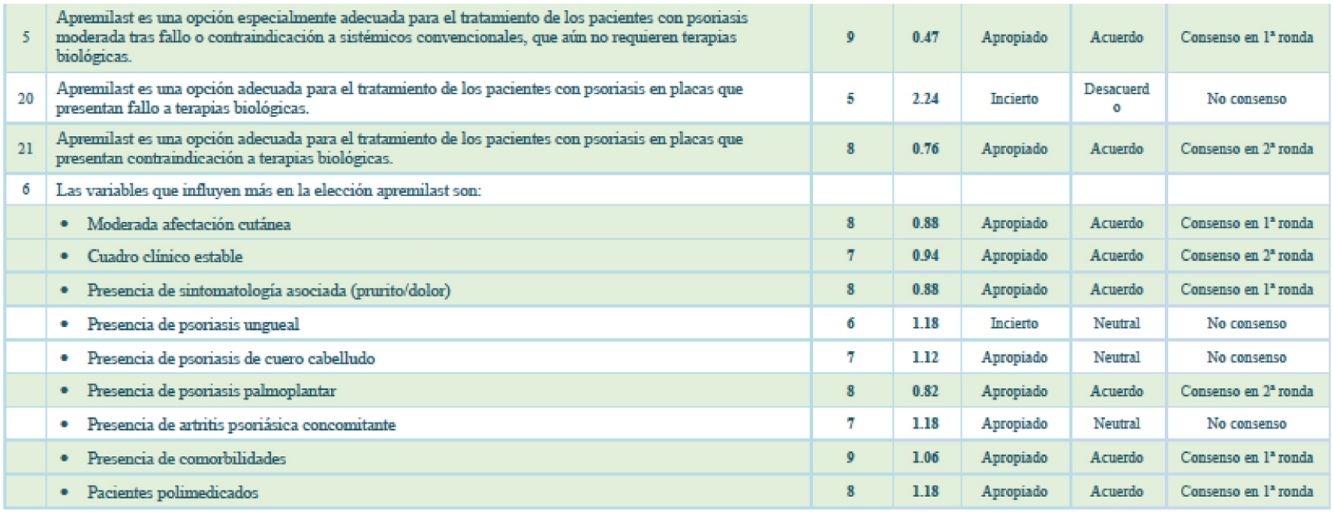
| 5 | Apremilast es una opción especialmente adecuada para el tratamiento de los pacientes con psoriasis moderada tras fallo o contraindicación a sistémicos convencionales, que aún no requieren terapias biológicas | 9 | 0,47 | Apropiado | Acuerdo | Consenso en primera ronda |
| 20 | Apremilast es una opción adecuada para el tratamiento de los pacientes con psoriasis en placas que presentan fallo a terapias biológicas | 5 | 2,24 | Incierto | Desacuerdo | No consenso |
| 21 | Apremilast es una opción adecuada para el tratamiento de los pacientes con psoriasis en placas que presentan contraindicación a terapias biológicas | 8 | 0,76 | Apropiado | Acuerdo | Consenso en segunda ronda |
| 6 | Las variables que influyen más en la elección de apremilast son: | |||||
| Moderada afectación cutánea | 8 | 0,88 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Cuadro clínico estable | 7 | 0,94 | Apropiado | Acuerdo | Consenso en segunda ronda | |
| Presencia de sintomatología asociada (prurito/dolor) | 8 | 0,88 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Presencia de psoriasis ungueal | 6 | 1,18 | Incierto | Neutral | No consenso | |
| Presencia de psoriasis de cuero cabelludo | 7 | 1,12 | Apropiado | Neutral | No consenso | |
| Presencia de psoriasis palmoplantar | 8 | 0,82 | Apropiado | Acuerdo | Consenso en segunda ronda | |
| Presencia de artritis psoriásica concomitante | 7 | 1,18 | Apropiado | Neutral | No consenso | |
| Presencia de comorbilidades | 9 | 1,06 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Pacientes polimedicados | 8 | 1,18 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Pacientes jóvenes, en los que se prevé un largo tiempo de necesidad de tratamientos específicos para la psoriasis | 7 | 0,71 | Apropiado | Acuerdo | Consenso en segunda ronda | |
| Pacientes de edad avanzada con múltiples comorbilidades | 8 | 0,71 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Formas inestables con afectación cutánea extensa | 1 | 1,24 | Inapropiado | Acuerdo | Consenso en primera ronda | |
| Pacientes que demandan un rápido aclarado de las lesiones cutáneas | 1 | 1,18 | Inapropiado | Acuerdo | Consenso en primera ronda | |
| Pacientes que prefieren medicación oral | 9 | 0,94 | Apropiado | Acuerdo | Consenso en primera ronda |
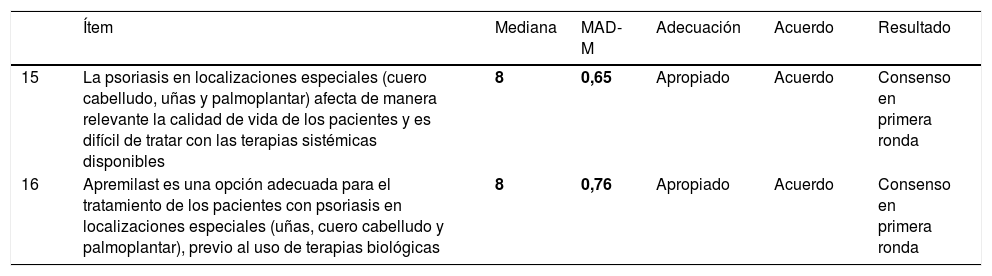
Apremilast fue consensuado en primera ronda como una opción terapéutica adecuada para el manejo de los pacientes con psoriasis y afectación de localizaciones especiales, tales como las uñas, el cuero cabelludo y la psoriasis palmoplantar (Tabla 3).
Eficacia en localizaciones especiales: casos en uñas, cuero cabelludo y palmoplantar
| Ítem | Mediana | MAD-M | Adecuación | Acuerdo | Resultado | |
|---|---|---|---|---|---|---|
| 15 | La psoriasis en localizaciones especiales (cuero cabelludo, uñas y palmoplantar) afecta de manera relevante la calidad de vida de los pacientes y es difícil de tratar con las terapias sistémicas disponibles | 8 | 0,65 | Apropiado | Acuerdo | Consenso en primera ronda |
| 16 | Apremilast es una opción adecuada para el tratamiento de los pacientes con psoriasis en localizaciones especiales (uñas, cuero cabelludo y palmoplantar), previo al uso de terapias biológicas | 8 | 0,76 | Apropiado | Acuerdo | Consenso en primera ronda |
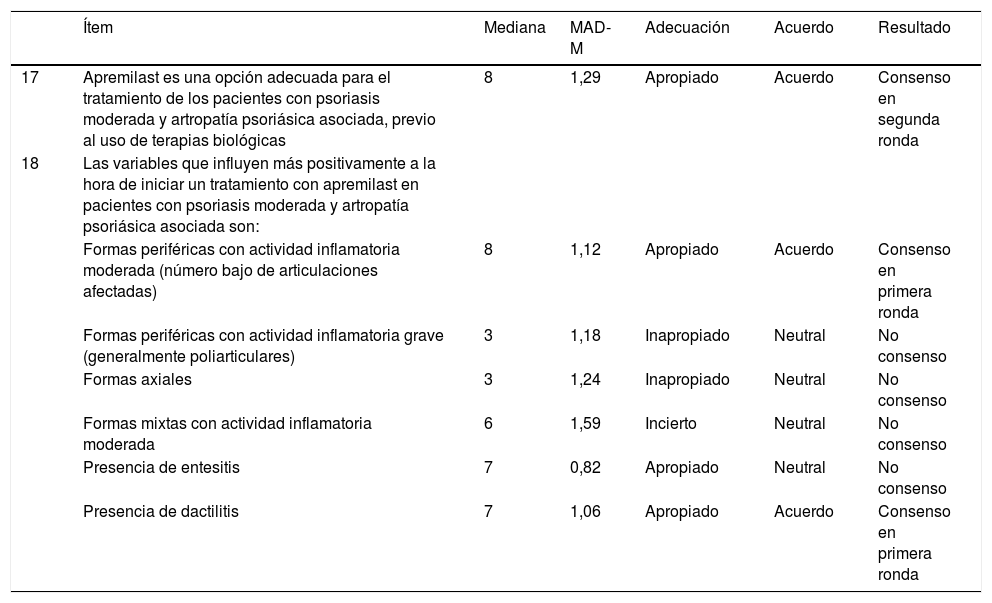
El comité de expertos alcanzó consenso positivo en 3 (42,9%; 2 en primera ronda y uno en segunda) de los 7 ítems incluidos en esta sección del cuestionario. Apremilast fue consensuado como una opción terapéutica adecuada, previa al uso de fármacos sistémicos biológicos, para el tratamiento de los pacientes con psoriasis moderada a grave que presenten artropatía psoriásica asociada, en presencia de formas periféricas con actividad inflamatoria moderada (número limitado de articulaciones afectadas) y dactilitis (Tabla 4).
Eficacia en pacientes con psoriasis y artritis psoriásica asociada
| Ítem | Mediana | MAD-M | Adecuación | Acuerdo | Resultado | |
|---|---|---|---|---|---|---|
| 17 | Apremilast es una opción adecuada para el tratamiento de los pacientes con psoriasis moderada y artropatía psoriásica asociada, previo al uso de terapias biológicas | 8 | 1,29 | Apropiado | Acuerdo | Consenso en segunda ronda |
| 18 | Las variables que influyen más positivamente a la hora de iniciar un tratamiento con apremilast en pacientes con psoriasis moderada y artropatía psoriásica asociada son: | |||||
| Formas periféricas con actividad inflamatoria moderada (número bajo de articulaciones afectadas) | 8 | 1,12 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Formas periféricas con actividad inflamatoria grave (generalmente poliarticulares) | 3 | 1,18 | Inapropiado | Neutral | No consenso | |
| Formas axiales | 3 | 1,24 | Inapropiado | Neutral | No consenso | |
| Formas mixtas con actividad inflamatoria moderada | 6 | 1,59 | Incierto | Neutral | No consenso | |
| Presencia de entesitis | 7 | 0,82 | Apropiado | Neutral | No consenso | |
| Presencia de dactilitis | 7 | 1,06 | Apropiado | Acuerdo | Consenso en primera ronda |
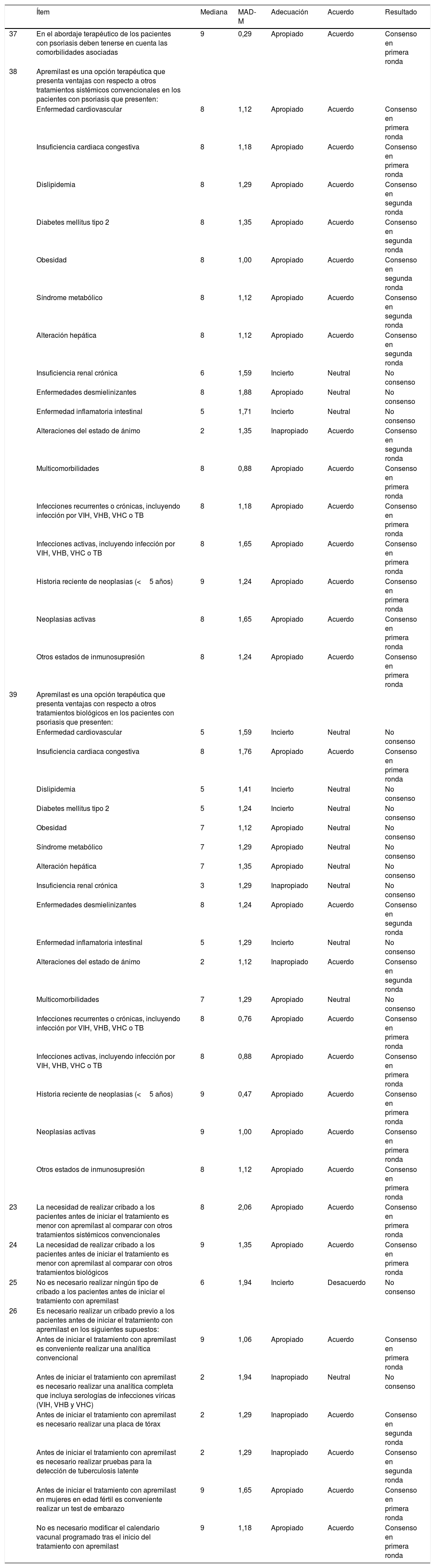
Los expertos alcanzaron consenso positivo en 26 (59,1%; 20 en primera ronda y 6 en segunda) y consenso negativo en 4 (9,1%; los 4 en segunda ronda) de los 44 ítems incluidos en esta sección del cuestionario. Se alcanzó acuerdo en que apremilast presenta ventajas con respecto a los fármacos convencionales en relación con el impacto en las comorbilidades en comparación a otros tratamientos sistémicos convencionales y biológicos, en pacientes con psoriasis que presenten infecciones recurrentes, crónicas o activas, historia reciente de neoplasias (menos de 5 años), neoplasias activas u otros estados de inmunosupresión, así como en comorbilidades del ámbito metabólico. Con respecto a los fármacos biológicos, se consideró que apremilast presentaba ventajas en seguridad en pacientes con insuficiencia cardiaca congestiva o enfermedades desmielinizantes. Por el contrario, se acordó que apremilast no es buena opción terapéutica para pacientes con alteraciones del estado de ánimo (Tabla 5).
Manejo y cribado de comorbilidades en la psoriasis
| Ítem | Mediana | MAD-M | Adecuación | Acuerdo | Resultado | |
|---|---|---|---|---|---|---|
| 37 | En el abordaje terapéutico de los pacientes con psoriasis deben tenerse en cuenta las comorbilidades asociadas | 9 | 0,29 | Apropiado | Acuerdo | Consenso en primera ronda |
| 38 | Apremilast es una opción terapéutica que presenta ventajas con respecto a otros tratamientos sistémicos convencionales en los pacientes con psoriasis que presenten: | |||||
| Enfermedad cardiovascular | 8 | 1,12 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Insuficiencia cardiaca congestiva | 8 | 1,18 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Dislipidemia | 8 | 1,29 | Apropiado | Acuerdo | Consenso en segunda ronda | |
| Diabetes mellitus tipo 2 | 8 | 1,35 | Apropiado | Acuerdo | Consenso en segunda ronda | |
| Obesidad | 8 | 1,00 | Apropiado | Acuerdo | Consenso en segunda ronda | |
| Síndrome metabólico | 8 | 1,12 | Apropiado | Acuerdo | Consenso en segunda ronda | |
| Alteración hepática | 8 | 1,12 | Apropiado | Acuerdo | Consenso en segunda ronda | |
| Insuficiencia renal crónica | 6 | 1,59 | Incierto | Neutral | No consenso | |
| Enfermedades desmielinizantes | 8 | 1,88 | Apropiado | Neutral | No consenso | |
| Enfermedad inflamatoria intestinal | 5 | 1,71 | Incierto | Neutral | No consenso | |
| Alteraciones del estado de ánimo | 2 | 1,35 | Inapropiado | Acuerdo | Consenso en segunda ronda | |
| Multicomorbilidades | 8 | 0,88 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Infecciones recurrentes o crónicas, incluyendo infección por VIH, VHB, VHC o TB | 8 | 1,18 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Infecciones activas, incluyendo infección por VIH, VHB, VHC o TB | 8 | 1,65 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Historia reciente de neoplasias (<5 años) | 9 | 1,24 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Neoplasias activas | 8 | 1,65 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Otros estados de inmunosupresión | 8 | 1,24 | Apropiado | Acuerdo | Consenso en primera ronda | |
| 39 | Apremilast es una opción terapéutica que presenta ventajas con respecto a otros tratamientos biológicos en los pacientes con psoriasis que presenten: | |||||
| Enfermedad cardiovascular | 5 | 1,59 | Incierto | Neutral | No consenso | |
| Insuficiencia cardiaca congestiva | 8 | 1,76 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Dislipidemia | 5 | 1,41 | Incierto | Neutral | No consenso | |
| Diabetes mellitus tipo 2 | 5 | 1,24 | Incierto | Neutral | No consenso | |
| Obesidad | 7 | 1,12 | Apropiado | Neutral | No consenso | |
| Síndrome metabólico | 7 | 1,29 | Apropiado | Neutral | No consenso | |
| Alteración hepática | 7 | 1,35 | Apropiado | Neutral | No consenso | |
| Insuficiencia renal crónica | 3 | 1,29 | Inapropiado | Neutral | No consenso | |
| Enfermedades desmielinizantes | 8 | 1,24 | Apropiado | Acuerdo | Consenso en segunda ronda | |
| Enfermedad inflamatoria intestinal | 5 | 1,29 | Incierto | Neutral | No consenso | |
| Alteraciones del estado de ánimo | 2 | 1,12 | Inapropiado | Acuerdo | Consenso en segunda ronda | |
| Multicomorbilidades | 7 | 1,29 | Apropiado | Neutral | No consenso | |
| Infecciones recurrentes o crónicas, incluyendo infección por VIH, VHB, VHC o TB | 8 | 0,76 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Infecciones activas, incluyendo infección por VIH, VHB, VHC o TB | 8 | 0,88 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Historia reciente de neoplasias (<5 años) | 9 | 0,47 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Neoplasias activas | 9 | 1,00 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Otros estados de inmunosupresión | 8 | 1,12 | Apropiado | Acuerdo | Consenso en primera ronda | |
| 23 | La necesidad de realizar cribado a los pacientes antes de iniciar el tratamiento es menor con apremilast al comparar con otros tratamientos sistémicos convencionales | 8 | 2,06 | Apropiado | Acuerdo | Consenso en primera ronda |
| 24 | La necesidad de realizar cribado a los pacientes antes de iniciar el tratamiento es menor con apremilast al comparar con otros tratamientos biológicos | 9 | 1,35 | Apropiado | Acuerdo | Consenso en primera ronda |
| 25 | No es necesario realizar ningún tipo de cribado a los pacientes antes de iniciar el tratamiento con apremilast | 6 | 1,94 | Incierto | Desacuerdo | No consenso |
| 26 | Es necesario realizar un cribado previo a los pacientes antes de iniciar el tratamiento con apremilast en los siguientes supuestos: | |||||
| Antes de iniciar el tratamiento con apremilast es conveniente realizar una analítica convencional | 9 | 1,06 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Antes de iniciar el tratamiento con apremilast es necesario realizar una analítica completa que incluya serologías de infecciones víricas (VIH, VHB y VHC) | 2 | 1,94 | Inapropiado | Neutral | No consenso | |
| Antes de iniciar el tratamiento con apremilast es necesario realizar una placa de tórax | 2 | 1,29 | Inapropiado | Acuerdo | Consenso en segunda ronda | |
| Antes de iniciar el tratamiento con apremilast es necesario realizar pruebas para la detección de tuberculosis latente | 2 | 1,29 | Inapropiado | Acuerdo | Consenso en segunda ronda | |
| Antes de iniciar el tratamiento con apremilast en mujeres en edad fértil es conveniente realizar un test de embarazo | 9 | 1,65 | Apropiado | Acuerdo | Consenso en primera ronda | |
| No es necesario modificar el calendario vacunal programado tras el inicio del tratamiento con apremilast | 9 | 1,18 | Apropiado | Acuerdo | Consenso en primera ronda |
Los requisitos tanto en las pruebas de cribado como en el seguimiento durante el tratamiento con apremilast se consideraron más sencillos que en otros tratamientos convencionales o biológicos. De igual forma, se consensuó la conveniencia de realizar siempre, antes del tratamiento, una analítica convencional y un test de embarazo en mujeres en edad fértil. Por el contrario, no se consideró necesario incluir radiografías de tórax, pruebas para la detección de tuberculosis latente o modificar el calendario vacunal programado tras el inicio del tratamiento (Tabla 5).
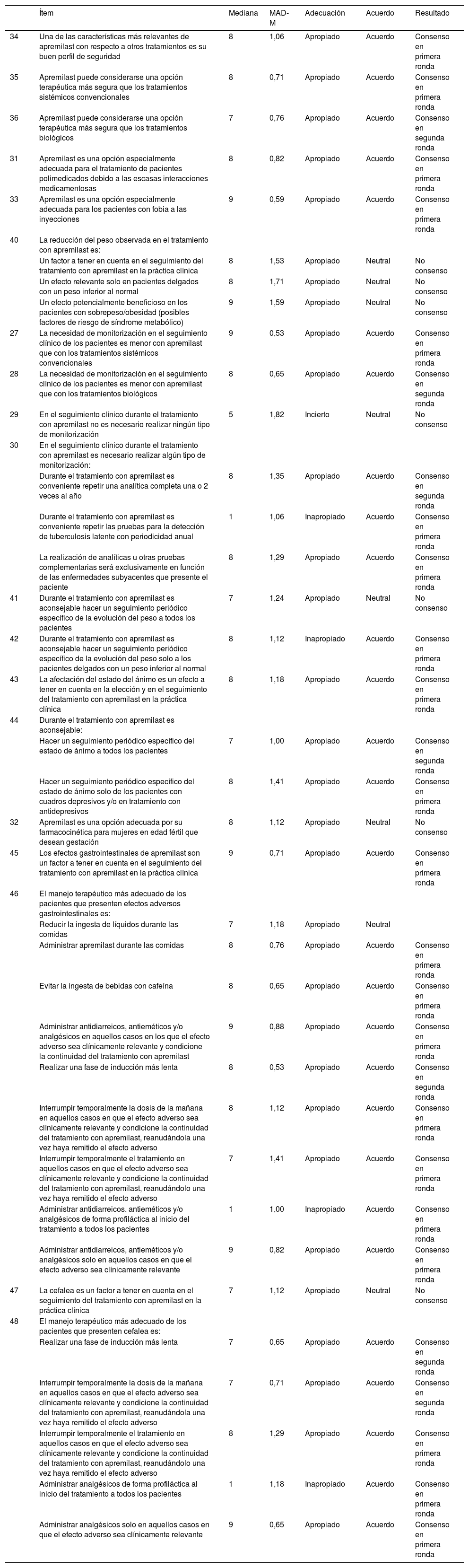
Implicaciones de la seguridad en el uso de apremilastLos expertos alcanzaron consenso positivo en 24 (66,7%; 17 en primera ronda y 7 en segunda) y consenso negativo en 4 (11,1%; las 4 en primera ronda) de los 36 ítems incluidos en esta sección del cuestionario. La necesidad de monitorización de apremilast se consideró menor a la habitual en las terapias sistémicas convencionales e incluso respecto a algunas biológicas (convencionales, consenso en primera ronda o biológicas, consenso en segunda ronda). Se acordó conveniente hacer una analítica completa una o 2 veces al año, mientras que cualquier otro tipo de prueba complementaria se haría en función de la enfermedad subyacente del paciente. Se alcanzó acuerdo en que apremilast es una opción adecuada para el tratamiento de pacientes polimedicados, así como en aquellos con fobia a las inyecciones.
En relación con los efectos adversos potenciales asociados al fármaco, se alcanzó consenso en que la pérdida de peso, la alteración del estado de ánimo y los trastornos gastrointestinales son factores importantes a tener en cuenta antes y durante el tratamiento con apremilast, y que requieren un seguimiento periódico específico. También se acordó recomendar un seguimiento de la evolución del peso en pacientes con peso inferior al normal y se remarcó la importancia de detectar precozmente y monitorizar periódicamente posibles alteraciones del estado de ánimo tanto durante la elección de la terapia como durante el tratamiento. Las medidas consensuadas para la minimización y el manejo práctico de los posibles efectos adversos asociados al fármaco se pueden consultar en la Tabla 6.
Implicaciones de la seguridad en el uso de apremilast
| Ítem | Mediana | MAD-M | Adecuación | Acuerdo | Resultado | |
|---|---|---|---|---|---|---|
| 34 | Una de las características más relevantes de apremilast con respecto a otros tratamientos es su buen perfil de seguridad | 8 | 1,06 | Apropiado | Acuerdo | Consenso en primera ronda |
| 35 | Apremilast puede considerarse una opción terapéutica más segura que los tratamientos sistémicos convencionales | 8 | 0,71 | Apropiado | Acuerdo | Consenso en primera ronda |
| 36 | Apremilast puede considerarse una opción terapéutica más segura que los tratamientos biológicos | 7 | 0,76 | Apropiado | Acuerdo | Consenso en segunda ronda |
| 31 | Apremilast es una opción especialmente adecuada para el tratamiento de pacientes polimedicados debido a las escasas interacciones medicamentosas | 8 | 0,82 | Apropiado | Acuerdo | Consenso en primera ronda |
| 33 | Apremilast es una opción especialmente adecuada para los pacientes con fobia a las inyecciones | 9 | 0,59 | Apropiado | Acuerdo | Consenso en primera ronda |
| 40 | La reducción del peso observada en el tratamiento con apremilast es: | |||||
| Un factor a tener en cuenta en el seguimiento del tratamiento con apremilast en la práctica clínica | 8 | 1,53 | Apropiado | Neutral | No consenso | |
| Un efecto relevante solo en pacientes delgados con un peso inferior al normal | 8 | 1,71 | Apropiado | Neutral | No consenso | |
| Un efecto potencialmente beneficioso en los pacientes con sobrepeso/obesidad (posibles factores de riesgo de síndrome metabólico) | 9 | 1,59 | Apropiado | Neutral | No consenso | |
| 27 | La necesidad de monitorización en el seguimiento clínico de los pacientes es menor con apremilast que con los tratamientos sistémicos convencionales | 9 | 0,53 | Apropiado | Acuerdo | Consenso en primera ronda |
| 28 | La necesidad de monitorización en el seguimiento clínico de los pacientes es menor con apremilast que con los tratamientos biológicos | 8 | 0,65 | Apropiado | Acuerdo | Consenso en segunda ronda |
| 29 | En el seguimiento clínico durante el tratamiento con apremilast no es necesario realizar ningún tipo de monitorización | 5 | 1,82 | Incierto | Neutral | No consenso |
| 30 | En el seguimiento clínico durante el tratamiento con apremilast es necesario realizar algún tipo de monitorización: | |||||
| Durante el tratamiento con apremilast es conveniente repetir una analítica completa una o 2 veces al año | 8 | 1,35 | Apropiado | Acuerdo | Consenso en segunda ronda | |
| Durante el tratamiento con apremilast es conveniente repetir las pruebas para la detección de tuberculosis latente con periodicidad anual | 1 | 1,06 | Inapropiado | Acuerdo | Consenso en primera ronda | |
| La realización de analíticas u otras pruebas complementarias será exclusivamente en función de las enfermedades subyacentes que presente el paciente | 8 | 1,29 | Apropiado | Acuerdo | Consenso en primera ronda | |
| 41 | Durante el tratamiento con apremilast es aconsejable hacer un seguimiento periódico específico de la evolución del peso a todos los pacientes | 7 | 1,24 | Apropiado | Neutral | No consenso |
| 42 | Durante el tratamiento con apremilast es aconsejable hacer un seguimiento periódico específico de la evolución del peso solo a los pacientes delgados con un peso inferior al normal | 8 | 1,12 | Inapropiado | Acuerdo | Consenso en primera ronda |
| 43 | La afectación del estado del ánimo es un efecto a tener en cuenta en la elección y en el seguimiento del tratamiento con apremilast en la práctica clínica | 8 | 1,18 | Apropiado | Acuerdo | Consenso en primera ronda |
| 44 | Durante el tratamiento con apremilast es aconsejable: | |||||
| Hacer un seguimiento periódico específico del estado de ánimo a todos los pacientes | 7 | 1,00 | Apropiado | Acuerdo | Consenso en segunda ronda | |
| Hacer un seguimiento periódico específico del estado de ánimo solo de los pacientes con cuadros depresivos y/o en tratamiento con antidepresivos | 8 | 1,41 | Apropiado | Acuerdo | Consenso en primera ronda | |
| 32 | Apremilast es una opción adecuada por su farmacocinética para mujeres en edad fértil que desean gestación | 8 | 1,12 | Apropiado | Neutral | No consenso |
| 45 | Los efectos gastrointestinales de apremilast son un factor a tener en cuenta en el seguimiento del tratamiento con apremilast en la práctica clínica | 9 | 0,71 | Apropiado | Acuerdo | Consenso en primera ronda |
| 46 | El manejo terapéutico más adecuado de los pacientes que presenten efectos adversos gastrointestinales es: | |||||
| Reducir la ingesta de líquidos durante las comidas | 7 | 1,18 | Apropiado | Neutral | ||
| Administrar apremilast durante las comidas | 8 | 0,76 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Evitar la ingesta de bebidas con cafeína | 8 | 0,65 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Administrar antidiarreicos, antieméticos y/o analgésicos en aquellos casos en los que el efecto adverso sea clínicamente relevante y condicione la continuidad del tratamiento con apremilast | 9 | 0,88 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Realizar una fase de inducción más lenta | 8 | 0,53 | Apropiado | Acuerdo | Consenso en segunda ronda | |
| Interrumpir temporalmente la dosis de la mañana en aquellos casos en que el efecto adverso sea clínicamente relevante y condicione la continuidad del tratamiento con apremilast, reanudándola una vez haya remitido el efecto adverso | 8 | 1,12 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Interrumpir temporalmente el tratamiento en aquellos casos en que el efecto adverso sea clínicamente relevante y condicione la continuidad del tratamiento con apremilast, reanudándolo una vez haya remitido el efecto adverso | 7 | 1,41 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Administrar antidiarreicos, antieméticos y/o analgésicos de forma profiláctica al inicio del tratamiento a todos los pacientes | 1 | 1,00 | Inapropiado | Acuerdo | Consenso en primera ronda | |
| Administrar antidiarreicos, antieméticos y/o analgésicos solo en aquellos casos en que el efecto adverso sea clínicamente relevante | 9 | 0,82 | Apropiado | Acuerdo | Consenso en primera ronda | |
| 47 | La cefalea es un factor a tener en cuenta en el seguimiento del tratamiento con apremilast en la práctica clínica | 7 | 1,12 | Apropiado | Neutral | No consenso |
| 48 | El manejo terapéutico más adecuado de los pacientes que presenten cefalea es: | |||||
| Realizar una fase de inducción más lenta | 7 | 0,65 | Apropiado | Acuerdo | Consenso en segunda ronda | |
| Interrumpir temporalmente la dosis de la mañana en aquellos casos en que el efecto adverso sea clínicamente relevante y condicione la continuidad del tratamiento con apremilast, reanudándola una vez haya remitido el efecto adverso | 7 | 0,71 | Apropiado | Acuerdo | Consenso en segunda ronda | |
| Interrumpir temporalmente el tratamiento en aquellos casos en que el efecto adverso sea clínicamente relevante y condicione la continuidad del tratamiento con apremilast, reanudándolo una vez haya remitido el efecto adverso | 8 | 1,29 | Apropiado | Acuerdo | Consenso en primera ronda | |
| Administrar analgésicos de forma profiláctica al inicio del tratamiento a todos los pacientes | 1 | 1,18 | Inapropiado | Acuerdo | Consenso en primera ronda | |
| Administrar analgésicos solo en aquellos casos en que el efecto adverso sea clínicamente relevante | 9 | 0,65 | Apropiado | Acuerdo | Consenso en primera ronda |
La eficacia de apremilast en el tratamiento de la psoriasis en placas moderada a grave se ha evaluado en diferentes ensayos clínicos aleatorizados de fase ii y de fase iii.
En los estudios de fase iii ESTEEM-1 y ESTEEM-22,3, un tercio de los pacientes tratados con apremilast alcanzaron una respuesta PASI 75 a la semana 16, frente a menos del 6% en la rama de placebo. En la semana 50, la mitad de los pacientes en tratamiento mantenían una respuesta PASI 75 y más del 75% una respuesta≥PASI 70.
Sin embargo, los datos obtenidos de los ensayos clínicos, aun cuando resultan significativos, no reflejan necesariamente, debido al perfil de selección, las perspectivas de un fármaco convencional de nueva generación como apremilast en la práctica clínica real.
El perfil en el que los clínicos consideraron que el uso de apremilast permite predecir mayores posibilidades de éxito sería el de un paciente con psoriasis moderada y estable. El concepto de psoriasis moderada no se encuentra definido ni aceptado de forma uniforme. Las directrices de la Academia Americana de Dermatología definen en 2011 3 categorías de enfermedad en función de la superficie corporal implicada y consideran psoriasis moderada aquella que afecta a una superficie corporal implicada de entre el 5 y el 10%8.
Knuckles et al. encontraron, a través de la realización de encuestas a dermatólogos norteamericanos, que aunque con notable dispersión, la mediana de aquellos consideraba psoriasis moderada aquella con una mediana de superficie corporal implicada del 5-10%9. Llamas-Velasco et al. proponen un valor de PASI para la psoriasis moderada<7 y DLQI≥5 o de 7-15 con independencia del valor del DLQI, que se solapa con los valores de PASI que claramente serían candidatos a terapia biológica10. En el estudio prospectivo LAPIS-PSO, que incluía 500 pacientes tratados en la práctica clínica real, se comprobó como las perspectivas de respuesta en cuanto a los pacientes que alcanzan la respuesta PASI 75 o PGA 0/1 fueron mayores en pacientes con PASI basal menor al de los estudios pivotales11,12. Papadavid et al. presentaron una serie de 51 pacientes en la práctica clínica real en los que el PASI medio fue de 10,8, de los que el 59,3% alcanzó una respuesta de al menos PASI 75 a las 16 semanas13. También fueron inferiores los valores de PASI presentados por Aragón-Miguel et al.14, 9,37, o Lukoviek et al.15, 9,01. En el estudio APRIL16, también sobre práctica real, los pacientes que continuaban en tratamiento a los 6 meses desde la primera prescripción presentaban un menor PASI inicial medio ?9,4? frente a aquellos que lo habían suspendido por falta de respuesta, 11,8.
La mayoría de los clínicos consideraron en este trabajo que apremilast, por sus características, es un tratamiento adecuado para pacientes en que hayan fracasado o estén contraindicados los tratamientos convencionales, pero preferentemente de forma previa a la indicación de terapia biológica. Esta consideración se aleja del perfil de los pacientes que se incluyeron en los ensayos pivotales, en gran medida con psoriasis muy grave y extensa, en donde con frecuencia habían fracasado los tratamientos biológicos, y puede modificar las perspectivas de respuesta. Por ejemplo, en el estudio ESTEEM-2 el porcentaje de pacientes tratados con apremilast que alcanzó una respuesta PASI 75 fue significativamente menor entre los que habían recibido tratamiento previo con terapias biológicas (22,8%) que entre los que no habían recibido ninguna terapia sistémica, biológica (31,9%) o convencional (33,3%)3.
El conjunto de pacientes que persistían en tratamiento activo también presentaban un menor valor medio de tratamientos sistémicos (media 1,47) y biológicos (0,20) que aquellos que no continuaban a los 6 meses (1,96 y 0,70, respectivamente). El 27% de los pacientes incluidos en este grupo había realizado tratamiento biológico previamente. Este posicionamiento de los clínicos, razonable teniendo en cuenta tanto la naturaleza de apremilast como fármaco convencional como sus perspectivas terapéuticas, ha quedado probablemente distorsionado en el acceso en la práctica clínica por cuestiones relacionadas con el reembolso, que lo han acercado al grupo de terapias biológicas17. A pesar de todas estas consideraciones, es cierto que no existen ensayos clínicos controlados que permitan perfilar de forma certera las perspectivas de apremilast en los pacientes con psoriasis moderada.
En este trabajo se puso de manifiesto que los clínicos participantes no exigen criterios objetivos de respuesta completa o casi completa ?medidas por el PASI absoluto? como criterio de respuesta al fármaco, ponderándose aquellos en gran medida con la satisfacción global reportada por el paciente, junto a la tolerabilidad y la seguridad del fármaco. Asimismo, se consideró que, en general, se puede asumir un margen de 24 semanas antes de decidir si continuar o no con el tratamiento. Esta consideración contrasta con los objetivos terapéuticos definidos en los ensayos clínicos y pone de manifiesto el camino por desarrollar todavía en la psoriasis en cuanto a objetivos terapéuticos e intervalos de evaluación, así como el papel del empoderamiento del usuario, reflejado en los objetivos referidos por el paciente18. Sin embargo, también hace difícil una evaluación objetiva de las perspectivas del fármaco con respecto a otras opciones disponibles en el mercado y la valoración de su eficiencia.
Aun cuando la evidencia disponible es limitada, los panelistas consideraron que las perspectivas terapéuticas de apremilast en áreas difíciles de tratar (palmas/plantas, uñas y cuero cabelludo) hacen del fármaco una opción terapéutica útil en pacientes con formas recalcitrantes en estas localizaciones. Esta consideración coincide con las observaciones, limitadas por el número de pacientes, en los ensayos clínicos de fase ii y de fase iii con apremilast19–21. También en estudios observacionales, como el estudio LAPIS-PSO, sobre práctica clínica real, se observó que a los 4 meses de tratamiento con apremilast un 62% de los pacientes había alcanzado una respuesta NAPSI-50, alrededor del 60% una puntuación de 0 o 1 en el índice ScPGA, y casi un 70% una puntuación de 0 o 1 en el índice PPPGA11,22 (Tabla S2. Ver material suplementario).
En el único estudio aleatorizado en el que se evalúa de forma específica el efecto de apremilast en la psoriasis palmoplantar, Bissonnette et al. no encontraron diferencias significativas en el PPPGA 0/1 en la semana 16 entre los pacientes tratados con apremilast y el placebo (4%; p=0,1595). Sin embargo, el 24% de los pacientes tratados con apremilast alcanzaron este objetivo en la semana 32, y también fueron superiores los valores de PPPASI 75 (apremilast 22%; placebo 8%; p=0,0499) o el impacto en la calidad de vida (DLQI, apremilast −4,3± 5,1; placebo −0,8±4,5; p=0,0004)19. En el estudio STYLE, el primer ensayo fase iii multicéntrico, aleatorizado, controlado con placebo para evaluar la eficacia clínica y la seguridad de apremilast, en pacientes con psoriasis en placa de cuero cabelludo moderada-grave, el 43,4% de los pacientes tratados con apremilast vs. PBO (13,8%) alcanzó el objetivo primario, respuesta de ScPGA 0 o 1 con una reducción de≥2 puntos desde momento basal a las 16 semanas23.
La presencia simultánea de artropatía psoriásica representa, en opinión de los panelistas, una razón añadida para el uso del fármaco, en particular en aquellos casos de afectación moderada, oligoarticular o con dactilitis. La eficacia de apremilast en la artritis psoriásica se evaluó en los ensayos de fase iii PALACE-1-324–26. En la semana 16, alrededor del 40% de los pacientes tratados con apremilast (30mg BID) presentó una respuesta ACR20, frente a un 20% en la rama de placebo.
A largo plazo (260 semanas), algo más del 70% de los pacientes tratados con apremilast mantenían una respuesta ACR20. Por otro lado, el porcentaje de pacientes que alcanzaron una resolución completa de la entesitis y la dactilitis basal se mantuvo estable con el tratamiento continuado con apremilast (30mg BID), en aproximadamente el 55 y el 80%, respectivamente26.
En su conjunto, el perfil de seguridad de apremilast fue percibido por los clínicos como uno de los activos más apreciados del fármaco. En la Tabla S3 del material suplementario se resumen los efectos adversos más frecuentemente observados con apremilast (≥5% de los pacientes)27,28. En la evaluación de los estudios ESTEEM-1 y 2, la incidencia de efectos adversos a las 156 semanas en relación con eventos cardiovasculares (incidencia relacionada con la exposición de 0,5/100 pacientes-año), neoplasias (1,2/100 pacientes-año), depresión (1,8/100 pacientes-año) o intentos de suicidio (0,1/100 pacientes-año) no se incrementó con respecto a las observadas en el primer año28. Los datos del estudio LAPIS-PSO indicaban que en la práctica clínica real la incidencia global de efectos adversos con apremilast podría ser menor que la registrada durante los ensayos clínicos22.
Las necesidades de cribado y monitorización se consideraron menores a las habituales en el tratamiento sistémico convencional o el biológico. Todo ello representa, a priori, ciertas ventajas con respecto al protocolo habitual en terapia sistémica en la psoriasis, lo que podría incrementar su prescripción en aquellos centros en los que el acceso a estos procedimientos fuese lento o complejo. En la ficha técnica de apremilast no se refiere la necesidad de realizar ningún tipo de prueba antes o durante el tratamiento27.
A las contraindicaciones descritas en la ficha técnica, las guías europeas S3 incluyen las infecciones agudas graves como contraindicación absoluta al uso de apremilast. Asimismo, se incluyen como contraindicaciones relativas las infecciones agudas y crónicas, el cáncer y las enfermedades linfoproliferativas, y la depresión29. Los pacientes con cáncer fueron excluidos de los ensayos clínicos aleatorizados (a excepción de las neoplasias cervicales intraepiteliales y los carcinomas de células escamosas), por lo que no existe evidencia del uso del fármaco en estos pacientes. La depresión, además de ser una comorbilidad frecuentemente asociada a la psoriasis30,31, aparece en la ficha técnica de apremilast como un efecto adverso potencial del fármaco. En los ensayos clínicos de fase iii controlados con placebo se registró depresión en algo más del 1% de los pacientes tratados con el fármaco, frente al 0,5% de los tratados con placebo27.
En cuanto al seguimiento, la opinión de los panelistas, que consideraron suficiente la práctica de una analítica de control anual (restringiéndose otras exploraciones a los requerimientos de cada paciente en función de su perfil), resulta coherente con las recomendaciones realizadas desde la EADV29.
Los eventos adversos considerados más relevantes fueron los efectos secundarios gastrointestinales, la afectación del estado de ánimo y la eventual pérdida de peso. En general, se considera que su conocimiento y el manejo precoz pueden permitir minimizarlos y continuar el tratamiento en la mayoría de los pacientes, circunstancia ya descrita en la literatura32. Sin embargo, un porcentaje mayor de pacientes podría abandonar el tratamiento en la práctica real con respecto a lo observado en los ensayos clínicos debido a problemas de tolerabilidad, probablemente debido a la existencia de alternativas en la práctica clínica real. Por ejemplo, Lee et al. detectaron un abandono del fármaco en un 23% de los pacientes debido fundamentalmente a efectos adversos después de un periodo medio de 123 días en una serie de 77 pacientes en práctica clínica real, frente al 5,3% observado en los ensayos clínicos33.
En definitiva, los clínicos perciben apremilast como una opción apreciable en el contexto de la individualización terapéutica del paciente con psoriasis, en el que la efectividad objetiva debe ponderarse con la seguridad, conveniencia y satisfacción del paciente. En particular, se aprecia la versatilidad del fármaco en perfiles de pacientes en los que no son posibles otros tratamientos, así como sus efectos positivos en la sintomatología, en la calidad de vida y en algunas localizaciones especiales, así como su perfil de seguridad. Como inconvenientes, deben tenerse en cuenta las limitaciones en cuanto a las perspectivas de efectividad del fármaco en comparación con otras alternativas de nueva generación, y algunos aspectos relacionados con la tolerabilidad al fármaco que pueden condicionar la eficiencia de este en un contexto muy competitivo.
Del trabajo se extrae la conveniencia de definir el concepto de psoriasis moderada que permita obtener evidencia ponderada de este y otros fármacos en este ámbito, así como la necesidad de disponer de una mayor evidencia publicada, procedente de ensayos clínicos o de vida real, que permita contrastar las opiniones reflejadas por los expertos.
Conflicto de interesesJose Manuel Carrascosa ha sido asesor y ponente, ha participado en ensayos clínicos y ha asistido a reuniones y congresos con el apoyo económico de AbbVie, Celgene, Janssen-Cilag, Leo-Pharma, Lilly, Novartis, Pfizer, Biogen, Sandoz, Milan, Sanofi-Aventis, Almirall.
Mariano Ara ha impartido ponencias y ha asistido a reuniones de asesoría patrocinadas por AbbVie, Pfizer, MSD, Janssen, Celgene, Almirall, Amgen, Novartis, Lilly, Leo.
Pedro Herranz ha sido asesor/ponente/investigador para AbbVie, Celgene, Lilly, Janssen-Cilag, MSD, Novartis, Pfizer, Regeneron, Sanofi-Aventis.
Isabel Belinchon ha participado en ensayos clínicos, ha percibido honorarios como consultora o por la participación en conferencias por parte de AbbVie, Janssen, MSD, Pfizer-Wyeth, Leo, Celgene, Novartis y Lilly.
Marta García-Bustínduy ha sido asesora y ponente, ha participado en ensayos clínicos y ha asistido a reuniones y congresos con el apoyo económico de AbbVie, Celgene, Janssen-Cilag, Leo, Lilly, Novartis, MSD, Pfizer-Wyeth, Sanofi-Aventis.
Celgene colaboró para la organización de reuniones de trabajo y soporte bibliográfico y elaboración y desarrollo del Delphi llevado a cabo por la consultoría científica independiente. Ninguna persona relacionada con Celgene ha participado en la elaboración de propuestas, otros contenidos llevados a cabo por este grupo de trabajo, ni en la redacción de este manuscrito.