El metotrexato (MTX) es un fármaco de uso frecuente en Dermatología con un buen perfil de seguridad. A pesar de que las complicaciones graves por toxicidad aguda suelen ocurrir en el contexto de dosis antineoplásicas (hasta 1-3g/m2 en algunos tumores), ocasionalmente aparecen en pacientes tratados con dosis considerablemente menores, siendo fundamental su identificación precoz. Presentamos 3 pacientes con mielosupresión aguda por MTX que comenzaron con lesiones cutáneas similares, observación clínica que puede ser clave en el diagnóstico precoz de esta importante entidad.
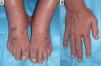
La primera paciente era una mujer de 65 años con artritis reumatoide (AR) en tratamiento desde hacía un mes con MTX (20mg/24h), ibuprofeno (600mg/8h) y prednisona (10mg/24h), que acudió a urgencias por un cuadro de 3 días de fiebre y mucositis, junto a la aparición brusca de edema doloroso de las manos y úlceras en ambos pies (fig. 1). Tras 48h de observación hospitalaria desarrolló una pancitopenia grave con 400 neutrófilos/mm3 (1.800-7.600), 9g/dl de Hb (11,4-15,1) con VCM 100ft y 66.000 plaquetas/mm3 (140.000-450.000). Los hemocultivos, urocultivos, estudio microbiológico de mucosas y serologías de VIH, lúes, VHB, VHC, parvovirus B19, CMV, VEB y toxoplasma fueron negativos.
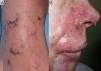
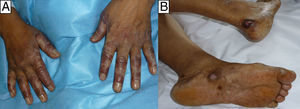
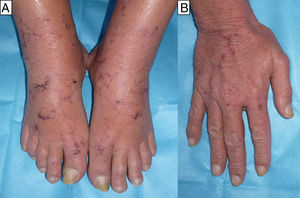
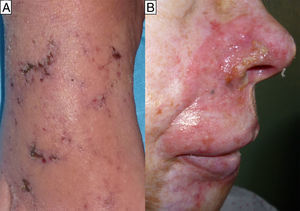
El segundo y tercer caso correspondían a un varón de 60 años y a una mujer de 55, ambos con antecedentes de micosis fungoide (MF) en tratamiento desde hacía 4 y 6 meses con 20 y 25mg/semanales de MTX, respectivamente, y desde hacía un mes con 800/160mg/día 3 veces/semana de sulfametoxazol/trimetoprim (SMX/TMP) como profilaxis de una sepsis de origen cutáneo, que consultaron por erosiones acrales muy dolorosas de una semana de evolución (figs. 2 y 3). En el varón se objetivó anemización grave (de 11,7 a 7,9g/dl de Hb) respecto al control previo 2 semanas antes, y en la mujer una bicitopenia moderada no conocida previamente (Hb de 10g/dl y 2.000 leucocitos/mm3 con 600 neutrófilos/mm3). Los cultivos de las lesiones cutáneas fueron negativos para virus y bacterias en ambos casos.
En los 3 pacientes la biopsia mostró hiperplasia epidérmica reactiva con áreas ulceradas de fondo fibrinoso y eosinofilia dérmica. Se suspendió MTX y se iniciaron medidas sintomáticas, con resolución de las lesiones cutáneas en menos de un mes en todos los casos. Además, en la primera paciente fue necesario añadir tratamiento específico (ácido folínico y estimulador de las colonias de neutrófilos) debido a pancitopenia grave, que evolucionó favorablemente.
El MTX es un antimetabolito análogo del ácido fólico que inhibe de forma competitiva y reversible la enzima dihidrofolato reductasa (DHFR), indispensable para la síntesis celular de ADN. Este mecanismo justifica su acción antiproliferativa y el perfil de efectos adversos a dosis altas, siendo la mielosupresión aguda su manifestación más letal1. Utilizado como antiinflamatorio, la cantidad de moléculas de fármaco en contacto con la enzima es insuficiente para mantener su inhibición, postulándose que el efecto a dosis bajas pueda estar en relación con la formación de poliglutamatos intracelulares2. No obstante, la gran variabilidad inter e intraindividual en su metabolismo3 y la posible coexistencia con factores que aumenten su disponibilidad a nivel celular hace que, en la práctica, debamos considerar a todo paciente en tratamiento con MTX susceptible de desarrollar una complicación grave. Nuestros 3 casos presentaban factores facilitadores de citotoxicidad: en el primero sobredosificación por error en la posología indicada (semanal en vez de diaria) y toma de ibuprofeno, los cuales interfieren con la eliminación renal de MTX y aumentan su fracción libre en plasma por desplazamiento de la unión a proteínas; en los siguientes profilaxis con SMX/TMP, que impide la transformación del ácido paraaminobenzoico (PABA) en ácido fólico (SMX) e inhibe directamente la DHFR (TMP).
La aparición de erosiones y/o úlceras cutáneas como manifestación de citotoxicidad aguda por MTX es excepcional. En la literatura médica revisada solo hemos encontrado 5 casos en pacientes sin dermatosis previa4–8, todos varones en tratamiento a dosis bajas por AR y solo uno de ellos cursó con afectación general, fiebre, mucositis y pancitopenia aguda grave, similar a nuestra primera paciente7. En pacientes con psoriasis y/o MF existe un recambio celular elevado que aumentaría el tropismo cutáneo del MTX9,10. Lawrence et al. diferencian 2 patrones clínicos de distinto pronóstico en pacientes con psoriasis: el tipo i con erosiones y/o úlceras sobre placas que curan en pocos días tras retirar MTX y el tipo ii con lesiones sobre piel sana que tardan semanas en resolverse pese al cese del tratamiento9. Su reconocimiento en consulta es importante, pues plantean el diagnóstico diferencial con la ineficacia del tratamiento o rebrote de la dermatosis, al ser característica su aparición al inicio/finalización del tratamiento, pudiendo inducir erróneamente al aumento de dosis o a la reintroducción del MTX, respectivamente. El factor común en todos los casos descritos, tanto en individuos con enfermedad cutánea de base como en sanos, es el dolor desproporcionado de las lesiones y su típica distribución acral, hallazgos presentes en nuestros pacientes.
En función de lo expuesto, consideramos que la aparición de erosiones y/o úlceras acrales dolorosas en pacientes en tratamiento con MTX debe hacernos pensar y descartar citotoxicidad grave subyacente. Realizar una minuciosa valoración de toda la medicación concomitante y asegurarse de que el paciente entienda la pauta de MTX indicada son 2 aspectos fundamentales para prevenir el desarrollo de efectos adversos potencialmente letales.