La terapia fotodinámica con luz de día (TFDLD) es una nueva modalidad de terapia fotodinámica (TFD) que, manteniendo la misma eficacia en queratosis actínicas (QA) grado i y ii que la técnica convencional, disminuye sus efectos adversos y la hace más eficiente. Los condicionantes meteorológicos propios de la España y Portugal hacen necesario el establecimiento de un protocolo adecuado y consensuado por expertos adaptado a los mismos.
ObjetivoEstablecer un protocolo para la TFDLD con metil-aminolevulinato (MAL) para el tratamiento de las QA grado i y ii adecuado y consensuado a las características epidemiológicas, meteorológicas y clínicas que se dan en España y Portugal.
MétodoDoce dermatólogos de diferentes áreas geográficas de ambos países, con experiencia en el tratamiento de las QA con TFD, se reunieron para elaborar un documento de consenso para la realización de TFDLD con MAL. De la revisión de la bibliografía y de su experiencia se elaboró el procedimiento recomendado para su realización.
ResultadosLas recomendaciones adoptadas establecen que los pacientes con QA grado i y ii múltiples, especialmente en el contexto de campo de cancerización, son los candidatos a realizar este tratamiento. La TFDLD se puede realizar durante todo el año, siendo limitaciones las temperaturas menores de 10°C o las excesivamente elevadas, así como los días de lluvia, nieve o niebla. El procedimiento es sencillo y requiere la aplicación de un fotoprotector FPS>30 que solo contenga filtros orgánicos, la preparación adecuada de las lesiones, la aplicación del MAL sin oclusión y su activación con la luz del día durante 2h.
ConclusiónEste documento de consenso supone una guía práctica y detallada para la realización de la TFDLD con MAL en España y Portugal destinada a la consecución de la máxima efectividad con mínimos efectos adversos.
Daylight-mediated photodynamic therapy (PDT) is a new type of PDT that is as effective as conventional PDT in grade 1 and 2 actinic keratosis but with fewer adverse effects, resulting in greater efficiency. The climatic conditions in the Iberian Peninsula require an appropriately adapted consensus protocol.
ObjectiveWe describe a protocol for the treatment of grade 1 and 2 actinic keratosis with daylight-mediated PDT and methyl aminolevulinate (MAL) adapted to the epidemiological and clinical characteristics of Spanish and Portuguese patients and the climatic conditions of both countries.
MethodsTwelve dermatologists from different parts of Spain and Portugal with experience in the treatment of actinic keratosis with PDT convened to draft a consensus statement for daylight-mediated PDT with MAL in these countries. Based on a literature review and their own clinical experience, the group developed a recommended protocol.
ResultsAccording to the recommendations adopted, patients with multiple grade 1 and 2 lesions, particularly those at risk of developing cancer, are candidates for this type of therapy. Daylight-mediated PDT can be administered throughout the year, although it is not indicated at temperatures below 10°C or at excessively high temperatures. Likewise, therapy should not be administered when it is raining, snowing, or foggy. The procedure is simple, requiring application of a sunscreen with a protection factor of at least 30 based exclusively on organic filters, appropriate preparation of the lesions, application of MAL without occlusion, and activation in daylight for 2hours.
ConclusionThis consensus statement represents a practical and detailed guideline to achieve maximum effectiveness of daylight-mediated PDT with MAL in Spain and Portugal with minimal adverse effects.
Las queratosis actínicas (QA) son unas lesiones cutáneas muy frecuentes, consideradas precancerosas por unos autores o carcinomas escamosos in situ por otros, que aparecen en áreas crónicamente expuestas a la radiación ultravioleta1. En España la tasa de prevalencia total se estima en el 28,6% de los mayores de 45 años (IC 95%: 27,2; 30,1%)2. Un porcentaje de estas lesiones, que oscila entre el 0,60% en el primer año y el 2,57% en 4 años, evolucionan a un carcinoma escamoso invasivo, por lo que su tratamiento se considera obligado3.
En los últimos años el desarrollo de la actividad clínica, apoyado por los múltiples datos procedentes de la investigación científica, han hecho de la terapia fotodinámica (TFD) uno de los tratamientos consolidados para las QA (grado de evidencia IA)4. Independientemente de su eficacia, este tipo de terapia se ha relacionado con una muy limitada aparición de efectos adversos y un buen resultado cosmético5-8. No obstante, uno de sus principales inconvenientes es el dolor intenso durante la irradiación, asociado incluso con incremento de la tensión arterial en algunos pacientes, y que obliga, en ocasiones, a la utilización de analgesia, anestesia local, troncular o sedación9-11. Por otro lado, el procedimiento convencional de la TFD requiere una preparación especial en un centro dotado de lámpara específica, y un personal sanitario especialmente entrenado. Para la TFD convencional (TFDc) se requiere un tiempo de incubación del fotosensibilizante (metil aminolevulinato [MAL] o ácido aminolevulínico [ALA]) de 3h, y su posterior iluminación con una fuente de luz adecuada administrando entre 37 y 100J/cm2 dependiendo de la lámpara utilizada. Por todo ello, la principal aportación de la terapia fotodinámica con luz de día (TFDLD) en este contexto es la simplificación de la técnica convencional y la disminución de los efectos adversos, principalmente el dolor.
La TFDLD con MAL (Metvix®; Galderma, París, Francia) es un nuevo procedimiento para realizar TFD que, manteniendo la misma efectividad de la TFDc, es más tolerable y eficiente12,13. La TFDLD permite aprovechar la luz visible como fuente de iluminación. En este caso, al mismo tiempo que el MAL se metaboliza en protoporfirina ix (PpIX) se va produciendo su fotoactivación dando lugar a un efecto fotodinámico continuo. Esto condiciona que la PpIX no se acumule en la piel y, por lo tanto, que el procedimiento no sea doloroso14.
El primer consenso europeo sobre el uso de la TFDLD en QA fue publicado en 201115. En este documento se exponían los resultados de 4 ensayos clínicos aleatorizados fase iii que mostraban a la TFDLD como un tratamiento eficaz para las QA. Las tasas de respuesta completa por lesión a los 3 meses fueron similares a la TFDc (79% versus 71% respectivamente), una práctica ausencia de dolor (puntuación de 2 versus 6,7 en una escala analógica de 0 a 10) y una mayor facilidad de uso tanto para el paciente como para el clínico13,14,16,17.
No obstante, desde esta fecha se han publicado algunos estudios y realizado 2 ensayos clínicos de interés en diferentes partes del mundo. El más relevante, hasta ahora publicado, es un ensayo clínico, multicéntrico y aleatorizado llevado a cabo en Australia que ha demostrado que la TFDLD no es inferior a la TFDc en cuanto a eficacia en el tratamiento de QA principalmente leves (tasa de lesiones con respuesta completa a los 3 meses 89% versus 93% respectivamente; IC 95%: –6,8 a –0,3) y mejor tolerada por los pacientes. Además la respuesta se mantenía en el 96% de las lesiones a los 6 meses de seguimiento18.
También se ha llevado a cabo un ensayo clínico multicéntrico, con una metodología similar al anterior, en 5 países del norte y sur de Europa. En este caso tampoco se evidenciaron diferencias en la tasa de respuesta de las QA leves y moderadas entre la TFDc (75%) y la TFDLD (70%). Dicha respuesta no se vio influida por las distintas condiciones meteorológicas del día del tratamiento (soleado, nublado o parcialmente nublado). El dolor experimentado por los pacientes fue significativamente inferior en el grupo tratado con TFDLD versus TFDc (0,7 versus 4,4, p<0,001)19. Otros estudios clínicos en diferentes zonas geográficas, como Brasil, Italia, España, o utilizando ALA como fotosensibilizante, han presentado resultados similares siendo una constante la disminución de los efectos adversos respecto a la TFDc, especialmente el dolor20-25.
A la luz, por tanto, de todos estos nuevos estudios, y a la vista de las importantes ventajas, tanto para el paciente como para el dermatólogo, que tiene esta nueva modalidad de TFD para tratar las QA, surgió la necesidad de redactar un nuevo documento de consenso europeo que ya ha sido recientemente publicado26. Sin embargo, el hecho de que la TFDLD esté supeditada a las condiciones de luz y clima del lugar del tratamiento, y al momento del año en el que se realice, justifica la realización de documentos de consenso propios de determinadas áreas geográficas. Considerando las importantes variaciones climatológicas que se producen a lo largo del año en España y Portugal, se realizó una reunión de dermatólogos expertos en TFD de ambos países para consensuar el uso de TFDLD en QA.
Este artículo recoge las principales recomendaciones acordadas en esta reunión, las cuales se basan en la revisión de la bibliografía existente y la experiencia de los expertos en lo que se refiere a la selección de los pacientes y la realización del procedimiento.
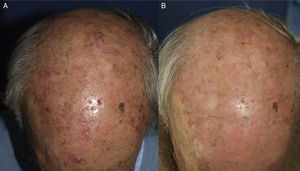
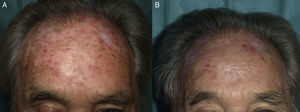
Procedimiento de la terapia fotodinámica con luz de díaSelección del pacienteDe acuerdo a los datos científicos disponibles, y en consonancia con el documento de consenso europeo26, se establece que el paciente tipo para la aplicación de la TFDLD es aquel que presenta QA grado i-ii múltiples, especialmente aquellos que presentan una afectación amplia en áreas fotoexpuestas, y de forma muy preferente quienes no toleran la TFDc. La TFDLD es especialmente ventajosa en los pacientes con campo de cancerización, ya que permite el tratamiento tanto de las lesiones clínicamente visibles como de las subclínicas (fig. 1). La TFDLD puede usarse tanto en pacientes que no han recibido ningún tratamiento previo como en los que han sido tratados con cualquiera de los métodos en la actualidad disponibles para las QA, incluida la TFDc (fig. 2). La TFDLD puede repetirse sin que se haya establecido la periodicidad más adecuada.
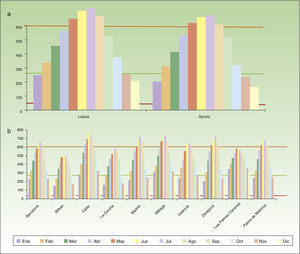
Basándonos en los resultados de los 2 principales ensayos clínicos realizados, 2h de exposición a la luz solar es lo recomendable para llevar a cabo la TFDLD. Este tiempo es necesario para que se sintetice la cantidad suficiente de PpIX para llevar a cabo el tratamiento fotodinámico. En cuanto a la intensidad de la luz solar, considerando que esta varía a lo largo del año, se ha calculado la media de la intensidad de luz diaria recibida desde las 9 a las 18h medida a lo largo de todo el año en diferentes ciudades del territorio español y portugués, usando un software meteorológico (meteonomr; METEOTEST, Berna, Suiza) (fig. 3a,3b). Considerando que el nivel mínimo de intensidad de la luz para poder llevar a cabo la TFDLD se ha establecido en 130W/m2, los niveles de intensidad de la luz mínimos, medios y máximos obtenidos en el ensayo clínico europeo con TFDLD comparados con los niveles de intensidad de luz solar recibidos en los distintos meses del año en todas las ciudades españolas y portuguesas están por encima de dicha intensidad utilizada. Por tanto, en España y Portugal, por nuestras características geográficas, se alcanza fácilmente el umbral de radiación suficiente para realizar TFDLD en todos los puntos geográficos en cualquier momento del año.
Medidas diarias de intensidad de luz a lo largo del año de 9h a 18h (Watts/m2). Se representa la media diaria global para cada mes (meteonorm data 1986-2005) en ciudades portuguesas (a) y ciudades españolas (b). Las líneas horizontales indican los niveles de intensidad de la luz del estudio europeo de TFD con luz de día25 (rojo: min. 44W/m2; naranja: máx. 601W/m2; verde: media 267W/m2).
El paciente debe exponerse a la luz del día entre las 10 y las 18h, que es la franja horaria en la que se han realizado las mediciones previamente expuestas. No obstante, en los días centrales del invierno, con pocas horas de luz, no se iniciará la iluminación más tarde de las 15h, mientras que en los meses de verano se podría realizar hasta las 19h.
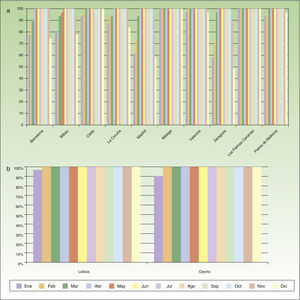
Temperatura más aconsejable para la terapia fotodinámica con luz de díaLa temperatura baja está relacionada con menor producción de PpIX en estudios preclínicos, dificultando a su vez la permanencia del paciente en el exterior. Distintos autores han recomendado una temperatura mínima de 10°C por la comodidad del paciente26. De acuerdo a las temperaturas medias registradas en diferentes ciudades de España y Portugal, la mayoría de ellas alcanzan dicha temperatura el 100% de los días (fig. 4a,4b). No obstante, ciudades de la mitad norte de España durante los meses de diciembre y enero pueden tener hasta un 40% de los días con temperaturas inferiores (como por ejemplo Madrid o Zaragoza). Por otro lado, hay que tener en cuenta que temperaturas extremadamente altas, registradas en algunas zonas durante los meses de verano, pueden alterar la realización de este tratamiento por 2 razones: la sudoración puede contribuir a la realización de un tratamiento inadecuado y, por otro lado, existe el riesgo de que pacientes ancianos puedan sufrir un golpe de calor. No obstante, hay que considerar que, en estos casos, el paciente puede realizar la TFD en un área de sombra no muy oscura.
En cuanto a las condiciones meteorológicas, todas salvo la lluvia permiten llevar a cabo la TFDLD.
Protocolo recomendadoEn la tabla 1 se esquematiza este procedimiento de TFDLD con MAL.
Esquema de la TFD con metil-aminolevulinato y luz de día
| Paso | Procedimiento | Detalles | Imagen |
|---|---|---|---|
| Protección solar | Aplicación de un fotoprotector FPS 30 o 50+ en todas las áreas fotoexpuestas antes de acudir a la consulta o unos 15min antes de aplicar el MAL | Fotoprotector sin filtros físicos (sin dióxido de titanio, óxido de cinc) | |
| Preparación de la piel | Las escamas e hiperqueratosis deben ser eliminadas de la zona del tratamiento | Curetaje, lijas, urea o ácido salicílico, láser, microdermoabrasión | |
| Aplicación de MAL | Aplicar una capa fina sobre las queratosis actínicas | Sin oclusión; 1g para tratar un cuero cabelludo o una cara completa | |
| Exposición a la luz de día | El paciente sale al exterior en los siguientes 30min después de la aplicación de MALPermanece durante 2h, bien en una zona de total exposición solar o en una zona con áreas de semisombraEn invierno hasta las 15hEn verano hasta las 19h (evitando horas de excesivo calor) | Misma eficacia en días soleados y nubladosTemperatura superior a 10°CEvitar sombras de edificiosEs importante que en menos de 30min salga a la calle para evitar acumulación de PPIX y dolor durante la iluminación | |
| Retirada de MAL y precauciones | Tras 2h de exposición, retirar MAL mediante lavado de la zonaCubrir las zonas tratadas durante 24h físicamente, o si no fuera posible aplicar un fotoprotector SPF 50+ | La retirada de la crema puede realizarse en la clínica o puede hacerla el propio pacienteEl fotoprotector deberá contener filtros físicosHidratar la piel durante una semana para aliviar la aparición de costras | |
| Seguimiento | Las lesiones tratadas deberían ser evaluadas después de 3 meses | Si fuera necesario, se realizará otra sesión |
La recomendación de fotoprotección solar tiene como función evitar la acción nociva de la radiación ultravioleta (UV) durante la fase de exposición a la luz de la TFDLD y la aparición del eritema solar. El fotoprotector utilizado debe contener solo filtros orgánicos o químicos, evitando aquellos que contengan filtros físicos o inorgánicos. Esto es debido a que estos últimos no solo bloquean la radiación UV, efecto deseado, sino también la radiación visible, necesaria para excitar la PpIX durante la reacción fotodinámica.
En cuanto al factor de protección solar (FPS), en los estudios realizados se han utilizado diferentes FPS (15-50) con resultados de eficacia similares y sin diferencias en los efectos adversos. Basado en esto y en las recomendaciones de fotoprotección que habitualmente se establecen para estos pacientes, el FPS aconsejado será 30 o superior. Para una adecuada absorción y actuación del mismo, es recomendable que el paciente se lo aplique en todas las áreas que van a estar fotoexpuestas antes de acudir a la consulta. De no haberlo hecho así, se le aplicará en la consulta y se esperará unos 15min, hasta su absorción.
Preparación de las lesionesLas escamas deberán eliminarse en la zona de tratamiento previamente a la aplicación del fotosensibilizante. Existen diversos procedimientos para ello, desde el uso de papel de lija, cremas queratolíticas con urea o ácido salicílico, micropunciones e incluso láser20,27. El método elegido por la mayoría de los expertos fue el curetaje, método también utilizado en los 2 ensayos clínicos realizados en Australia y Europa18.
Administración del fármacoSe aplicará una fina capa de crema con MAL en las áreas de tratamiento, lesión o campo. Como recomendación se puede utilizar 1g para tratar todo el cuero cabelludo o toda la cara. No se necesita oclusión. El paciente deberá salir al aire libre en la próxima media hora y no más tarde, ya que si permaneciera más en el interior podría dar lugar a la acumulación de PpIX en su piel incrementando así la posibilidad de que al exponerse a la luz del día experimente dolor.
Exposición a la luz del díaEl paciente debe permanecer 2h al aire libre para permitir una suficiente síntesis de PpIX en sus lesiones y un tratamiento fotodinámico satisfactorio. Esta exposición se realiza de forma directa a la luz del sol, aunque en días calurosos puede hacerse en áreas de sombra para preservar la comodidad del paciente, siempre que no sean sombras demasiado oscuras, ni cerca de edificios altos.
Cuidados tras el tratamientoFinalizadas las 2h de exposición se deben retirar de la piel los restos de MAL con agua o suero fisiológico, y cubrir la zona tratada durante al menos 24h. Si esto no fuera posible se aplicará un fotoprotector con FPS 50+ con filtros inorgánicos o físicos; de hecho algunos expertos solo recomiendan esta medida, sin haber observado mayor frecuencia o intensidad de efectos secundarios. En la siguiente semana se puede recomendar la aplicación de hidratantes para aliviar la aparición de costras.
SeguimientoLos pacientes deben ser seguidos de igual manera que con la TFDc. Generalmente se revisan a los 3 meses, salvo que el dermatólogo estime oportuno una visita anterior.
ConclusionesEl presente consenso constituye una guía para el uso de la TFDLD en las QA en España y Portugal. Esta nueva forma de hacer TFD presenta importantes ventajas respecto a la TFDc en el tratamiento de las QA y el campo de cancerización. Es beneficiosa para el paciente por sus menores efectos secundarios, especialmente el dolor; ahorra tiempo al personal sanitario, ya que no hace falta anestesiar a los pacientes ni controlarlos durante la iluminación; y supone un ahorro tanto en personal como en instalaciones y equipamiento específico. Sin embargo, la TFDLD no debe ser considerada como un sustituto de la TFDc, sino como una alternativa especialmente indicada para el tratamiento de áreas extensas y pacientes con mala tolerancia a esta. Por otro lado, la TFDc sigue siendo la única con indicación en la enfermedad de Bowen y el carcinoma basocelular superficial y nodular menor de 2mm de profundidad4.
En conclusión, la TFDLD es una alternativa más en el tratamiento de las QA grado i y ii, eficaz, segura y mejor tolerada, además de ser técnicamente más sencilla para el personal sanitario y más cómoda para los pacientes.
FinanciaciónEl laboratorio Galderma ha promovido la elaboración de este documento sin interferir en las decisiones del grupo de expertos.
Conflicto de interesesLa Dra. Yolanda Gilaberte ha participado como ponente y/o en estudios clínicos patrocinados por los laboratorios Galderma S.A., Leo Pharma, Almiral y Novartis; el Dr. Carlos Serra ha participado como ponente para los laboratorios IFC, MEDA, Leo Pharma y en ensayos clínicos para Laboratorios Galderma, S.A. y Leo Pharma; el Dr. Carlos Guillén ha participado como ponente para los laboratorios IFC, MEDA, Leo Pharma y en ensayos clínicos para Laboratorios Galderma, S.A. y Leo Pharma; la Dra. Bibiana García ha participado como ponente y en estudios clínicos patrocinados por laboratorios Galderma S.A.; el Dr. Antonio Harto ha recibido honorarios por comunicaciones científicas y seminarios de formación para laboratorios Galderma S.A.; el Dr. Pedro Redondo ha participado como ponente y como investigador de un ensayo clínico para Laboratorios Galderma S.A.; la Dra. Lidia Pérez Pérez ha asistido a reuniones nacionales e internacionales sobre terapia fotodinámica invitada por Laboratorios Galderma S.A; los Dres. Miguel Aguilar, Luis Miguel Valladares y Manuel Almagro declaran no tener ningún conflicto de intereses.