Los agentes tópicos representan la primera línea de tratamiento para la psoriasis leve y moderada. Sin embargo, factores como la frecuencia de administración, las características organolépticas o los resultados limitados a corto plazo pueden disminuir la adherencia al tratamiento y su efectividad.
Las innovaciones en los tratamientos tópicos se basan en descubrir nuevas moléculas, pero también en la reformulación de principios activos ya conocidos, mejorando su administración, características organolépticas, biodisponibilidad y comodidad de uso. La espuma en aerosol de calcipotriol y dipropionato de betametasona es una nueva formulación donde los principios activos están disueltos en una mezcla de propelentes volátiles que se evaporan rápidamente dejando una solución sobresaturada de calcipotriol y dipropionato de betametasona, que aumenta la penetración de los fármacos en la epidermis.
En este artículo se hace un breve repaso de las principales evidencias sobre los tratamientos tópicos disponibles para la psoriasis y de la nueva formulación en espuma de calcipotriol y dipropionato de betametasona.
Topical agents are the first-line treatment for mild and moderate psoriasis, but factors such as frequency of administration, organoleptic properties, and the limited short term results can reduce treatment adherence and effectiveness.
Innovations in topical treatments are linked not only to the discovery of new molecules, but also to the reformulation of existing active ingredients based on improvements to administration, organoleptic properties, bioavailability, and ease of use. Calcipotriol and betamethasone dipropionate aerosol foam is a new formulation in which the active ingredients are dissolved in a mixture of volatile propellants that evaporate quickly, leaving a supersaturated solution of calcipotriol and betamethasone dipropionate that enhances penetration into the epidermis.
In this article, we take a look at the new calcipotriol and betamethasone dipropionate aerosol formulation and briefly review the main evidence supporting the use of topical treatments for psoriasis.
La psoriasis es un trastorno inflamatorio crónico, mediado inmunológicamente y de base genética. En España, su prevalencia se estima en un 2,3% de la población; en el 55,6% de los pacientes la enfermedad se clasifica como leve, en el 37,6% como moderada y en el 6,6% como grave1–3. Generalmente la psoriasis leve puede tratarse de forma exclusivamente tópica, mientras que en la psoriasis moderada-grave el tratamiento tópico es casi siempre coadyuvante del tratamiento sistémico y/o la fototerapia4.Las ventajas del tratamiento tópico se derivan, por lo general, de su limitada absorción sistémica, aunque la frecuencia de administración, la conveniencia del tratamiento, las cualidades organolépticas y su limitada eficacia a corto plazo pueden limitar la adherencia al tratamiento y, por lo tanto, su efectividad5.
Las opciones terapéuticas tópicas actuales incluyen varias terapias con una amplia gama de formulaciones, combinaciones y potencias (tabla 1)6,7. No obstante, la elección del tratamiento debe adaptarse a las necesidades y características del paciente8.
Resumen de las principales características de los tratamientos tópicos
| Mecanismo de acción | Eficacia frente a placeboa | Eficacia frente a otros | Recomendaciones | Inconvenientes | |
|---|---|---|---|---|---|
| Corticosteroides tópicos muy potentes | Antiinflamatorio e inmunomodulador: modula transcripción genética de moléculas antiinflamatorias y ↓citocinas proinflamatorias Efectos no génicos sobre fibroblastos y vasos en la dermis | Metaanálisis: 10 estudios (n=1.264) Tamaño efecto (IC95%): −1,56 Puntuación IAGI: 1,81 | >Corticosteroides potentes <Corticosteroide+análogos vitamina D >Análogos de la vitamina D | No usar en pliegues ni cara PsO cuerpo+cuero cabelludo Dosis: 1 vez/día Duración corta: 4 semanas Pauta intermitente a largo plazo | Efecto rebote Taquifilaxia Atrofia cutánea Estrías Telangiectasias Posibilidad de efectos sistémicos |
| Corticosteroides tópicos potentes | Metaanálisis: 13 estudios (n=2.216) Tamaño efecto (IC95%): −0,89 Puntuación IAGI: 1,02 | <Corticosteroides muy potentes<Corticosteroide+análogos de la vitamina D <>Análogos de la vitamina D >Análogos de la vitamina D en cuero cabelludo | |||
| Análogos de la vitamina D | Efecto génico queratinocitos: ↓hiperproliferación celular ↑diferenciación celular ↓producción citocinas proinflamatorias | Metaanálisis: 30 estudios (n=4.986) Tamaño efecto (IC95%): −0,90 Puntuación IAGI: 1,03 | <Corticosteroides muy potentes <Corticosteroide+análogos de la vitamina D <Corticosteroides potentes o muy potentes en cuero cabelludo <>Corticosteroides potentes <>Ditranol | PsO cuerpo Dosis: 1 o 2 veces/día Duración: no limitada No en menores de 6 años | Irritación cutánea: dolor y prurito lugar de la aplicación |
| Combinación corticosteroide+análogo de la vitamina D (Cal/BD) | Efectos antiinflamatorios e inmunomoduladores complementarios: ↑rapidez ↑durabilidad efecto postratamiento ↓efecto rebote | Metaanálisis: 5 estudios (n=2.058) Tamaño efecto (IC95%): −1,44 Puntuación IAGI: 2,18 (2 vez/día); 1,39 (1 vez/día) | >Corticosteroides muy potentes <Corticosteroides potentes o muy potentes en cuero cabelludo >Corticosteroides potentes >Análogos de la vitamina D >Ditranol | PsO cuerpo+cuero cabelludo Dosis: 1 o 2 veces/día Combinación fija o por separado Duración: no limitada | Efectos secundarios (menos que por separado): dolor y prurito lugar de la aplicación |
| Ditranol | ↓ hiperproliferación queratinocitos ↓función granulocítica Efecto inmunosupresor | Metaanálisis: 3 estudios (n=47) Tamaño efecto (IC95%): −1,06 Puntuación IAGI: 1,22 | <Corticosteroides muy potentes <Corticosteroides potentes <>Análogos de la vitamina D | Mejor combinado (corticosteroides, análogos de la vitamina D, fototerapia) Dosis: 1-2 veces/día Uso en centros especializados | Irritación local Manchas en ropa y muebles |
| Tazaroteno | Regula proliferación y diferenciación queratinocitos | Metaanálisis: un estudio (n=318) Tamaño efecto (IC95%): −0,86 Puntuación TSS: 3,8 vs. 5,3 | <Corticosteroides muy potentes <Corticosteroides potentes <Análogos de la vitamina D <Ditranol | Formulación en gel Efecto persistente postratamiento Dosis 1 vez/día Uso combinado con corticosteroides Indicación: plantas pies, palmas y uñas | Baja eficacia Irritación local |
Cal/BD: calcipotriol más dipropionato de betametasona; IAGI: evaluación del investigador de la mejora general global (Investigator's Assessment of Overall Global Improvement); TSS: puntuación total de gravedad (Total Severity Score).
aInformación adaptada de Mason et al. y Samarasekera et al.6,7.
Una revisión Cochrane concluye que los tratamientos combinados de vitamina D y corticosteroides tópicos son por lo general más efectivos que la monoterapia con los mismos principios activos por separado6. La probabilidad de respuesta al tratamiento combinado (70,9%) es similar a la de los corticosteroides muy potentes (67,9%) cuando ambos se emplean en aplicación única diaria7.
La combinación calcipotriol y dipropionato de betametasona (Cal/BD) según diferentes estudios consigue una reducción media del PASI del 65-74% a las 4 semanas, siendo la irritación y el prurito los efectos adversos más frecuentes8. Esta combinación, además, ha demostrado evitar la reducción del grosor de la epidermis y de la dermis que produce el uso prolongado de BD en monoterapia9.
Las recomendaciones actuales de guías terapéuticas y consensos6,7 consideran los corticosteroides tópicos y los análogos de la vitamina D, solos o en combinación, la mejor opción de tratamiento tópico para la psoriasis6,10–12.
Estrategias de innovación en tratamientos tópicos para la psoriasis: aportación del calcipotriol y dipropionato de betametasona en espumaLa falta de adherencia es un problema asociado al tratamiento tópico, que afecta del 39% al 73% de los pacientes con psoriasis13,14. Por ello, en los últimos años muchas investigaciones se han centrado en mejorar la administración de fármacos tópicos ya conocidos15, aumentando la biodisponibilidad de sus principios activos16,17, con el fin de mejorar su eficacia, rapidez de acción y su perfil de seguridad, permitiendo reducir la posología y facilitando su aplicación para aumentar la adherencia5.
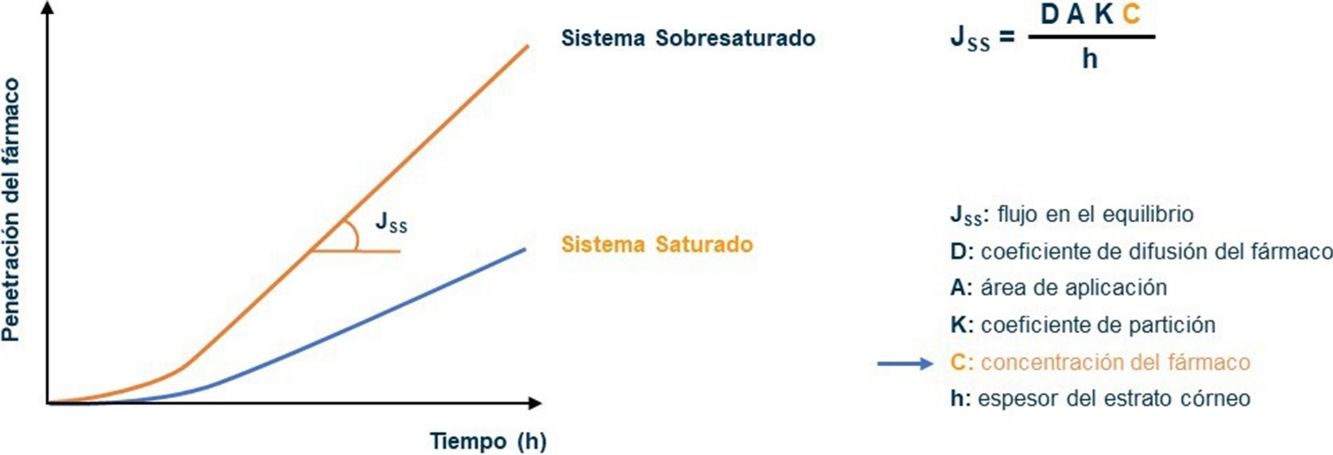
En los tratamientos tópicos, la biodisponibilidad de los fármacos está determinada por su capacidad de penetración a través de la epidermis que depende, entre otros factores, de la concentración de principios activos en el vehículo16–18. La espuma en aerosol de Cal/BD es un tratamiento basado en la reformulación de 2 principios activos ya conocidos, disueltos en una mezcla de propelentes volátiles, butano y dimetiléter. Tras ser aplicada sobre la piel, los propelentes volátiles se evaporan rápidamente formándose una fina capa de espuma de una solución sobresaturada de Cal/BD que, al tener mayor concentración de principio activo biodisponible, tiene una mayor tasa de penetración a través del estrato córneo (Ley de Fick, fig. 1)17–23. Esta técnica se conoce como de disolución con co-disolvente volátil y permite tener los principios activos disueltos por encima de su grado de solubilidad máxima, evitando que estos precipiten. Dos ensayos, uno in vitro y otro de fase I han demostrado una mayor tasa de penetración y potencial vasoconstrictor respectivamente de la espuma en comparación a la misma combinación fija formulada en pomada20,23.
Ley de Fick. La ley de Fick, modelo del paso de sustancias a través de membranas, relaciona el flujo de difusión con la concentración. La ley postula que el flujo va desde una región de alta concentración a las regiones de baja concentración, con una magnitud proporcional al gradiente de concentración. Es decir, a mayor concentración, mayor difusión a través de la membrana, y por similitud, a través de la epidermis.
Un primer estudio exploratorio mostró cómo la espuma de Cal/BD lograba una reducción del score TCS (suma de eritema, descamación y grosor de la lesión) significativamente mayor que la pomada de Cal/BD (p=0,038), la espuma de BD (p=0,005) o el vehículo de la espuma (p<0,001). Las mediciones ecográficas confirmaron una mayor reducción del grosor de la piel y la inflamación asociadas a la psoriasis22.
El desarrollo clínico posterior ha permitido demostrar la superioridad en eficacia de la espuma frente a los monocomponentes por separado, a la pomada de Cal/BD, al gel de Cal/BD y a su vehículo14,24–28 (tabla 2).
Resumen de las principales evidencias del desarrollo de la nueva formulación: espuma en aerosol de Cal/BD
| Referencia | Diseño | N | Tratamientos | Pauta/Duración | Resultados | |
|---|---|---|---|---|---|---|
| Farmacocinética y biodisponibilidad | ||||||
| Estudio de penetración | Hollesen Basse et al. J Invest Dermatol. 2014 (ref.20) | In vitro, fase i, piel oreja de cerdo | Espuma Cal/BD vs. pomada Cal/BD | 1 aplicación simple Control 2h/6h/21h | Mayor penetración con espuma vs. pomada (p<0,05) Niveles constantes de 2h a 21h (estabilidad de la espuma) | |
| Potencial vasoconstrictor | Queille-Roussel et al. J Eur Acad Dermatol Venereol. 2016 (ref.23) | Fase I, unicéntrico, investigador ciego, controlado, comparaciones intraindividuales | 35 voluntarios sanos | Espuma Cal/BD vs. pomada Cal/BD vs. crema clobetasol vs. pomada fluocinolona vs. espuma BD vs. vehículo espuma vs. control negativo | 1 aplicación simple en diferentes zonas 6-32h postaplicación | Potencia vasoconstrictora: crema clobetasol>espuma Cal/BD>pomada Cal/BD y pomada fluocinolona |
| Eficacia | ||||||
| Estudio exploratorio | Queille-Roussel et al. Clin Drug Investig. 2015 (ref.22) | Fase IIa, exploratorio, unicéntrico, investigador ciego, controlado Comparaciones intraindividuales | 24 pacientes | Espuma Cal/BD vs. pomada Cal/BD vs. espuma BD vs. vehículo espuma | 1 aplicación/día 4 semanas | Puntuación clínica total (TCS): Espuma Cal/BD:−6±1,27 vs. poma Cal/BD: −5,25 (p<0,05) vs. espuma BD: −4,96 (p<0,05) vs. vehículo espuma: −1,88 (p<0,0001) |
| Frente a monocomponentes | Lebwohl et al. J Clin Aesthet Dermatol. 2016 (ref.14) | Fase II, multicéntrico, aleatorizado, doble ciego | 302 pacientes | Espuma Cal/BD vs. espuma Cal vs. espuma BD | 1 aplicación/día 4 semanas | Tasa éxito/mPASI75 (semana 4) Espuma Cal/BD: 45%/49% vs. espuma Cal: 14,9%/18% (p<0,001) vs. espuma BD: 30,7% (p<0,05)/34% |
| Frente a pomada Cal/BD | Koo et al. J Dermatolog Treat. 2016 (ref.25) | Fase II, multicéntrico, aleatorizado, investigador ciego | 376 pacientes | Espuma Cal/BD vs. pomada Cal/BD vs. vehículo espuma vs. vehículo pomada | 1 aplicación/día 4 semanas | Tasa de éxito/↓mPASI (semana 4): Espuma Cal/BD: 54,6%/↓74,2% vs. pomada Cal/BD: 43%/↓63,2% (p<0,05) |
| Frente al vehículo Estudio PSO-FAST | Leonardi et al. J Drugs Dermatol. 2015 (ref.26) J Drugs Dermatol. 2016 (ref.29) | Fase III, multicéntrico, aleatorizado, doble ciego | 426 pacientes | Espuma Cal/BD vs. vehículo espuma | 1 aplicación/día 4 semanas | Resultados (semana 4): Éxito: 53,3 vs. 4,8% (p<0,001) mPASI: 2 vs. 5,5 (p<0,001) mPAS75: 52,9 vs. 8,2% (p<0,001) ↓70% prurito: 83,5 vs. 40,6% (p<0,001) DLQI (0/1): 48,1 vs. 21,2% (p<0,001) |
| Frente al gel Cal/BD Estudio PSO-ABLE | Paul et al. J Eur Acad Dermatol Venereol. 2017 (ref.27) | Fase III, multicéntrico, aleatorizado, investigador ciego | 463 pacientes | Espuma Cal/BD vs. gel Cal/BD vs. vehículo espuma vs. vehículo gel | 1 aplicación/día 12 semanas | Resultados (semana 4 vs. semana 8): Éxito: 38 vs. 22% (p<0,001) mPASI75: 52 vs. 35% (p<0,001) mPASI90: 22 vs. 11% (p<0,001) Éxito (semana 12): 44 vs. 34% |
| Paul et al. Am J Clin Dermatol. 2017 (ref.30) | Análisis sub-grupo estudio PSO-ABLE | 159 pacientes psoriasis moderada-severa | Espuma Cal/BD (n=77) vs. gel Cal/BD (n=82) | 1 aplicación/día 12 semanas | Éxito (semana 4): 32 vs. 19% Éxito (semana 8): 36 vs. 17% (p<0,05) Éxito (semana 12): 38 vs. 32% mPASI75 (semana 4): 40 vs. 17% (p=0,001) mPASI75 (sem 8): 53 vs. 22% (p<0,001) mPASI75 (semana 12): 57 vs. 35% (p<0,01) | |
| Análisis combinado | Stein Gold et al. J Drugs Dermatol. 2016 (ref.28) | Análisis combinado de: Koo et al. (ref.25) Lebwohl et al. (ref.14) Leonardi et al. (ref.26) | 1.104 pacientes | Espuma Cal/BD vs. espuma Cal vs. espuma BD vs. pomada Cal/BD vs. vehículo espuma | 1 aplicación/día 4 semanas | Tasa éxito/↓ mPASI/PASI75 (semana 4): Espuma Cal/BD: 51%/↓72%/51% vs. pomada Cal/BD: 43%/↓63%/41% vs. espuma BD: 31%/↓53%/34% vs. espuma Cal: 15%/↓43%/18% vs. vehículo espuma: 5%/↓32%/7% vs. vehículo pomada: 8%/↓33%/10% |
| Seguridad | ||||||
| Datos de tolerabilidad de los estudios de eficacia | Menter et al. Skinmed 2017 (ref.33) | Análisis combinado de: Koo et al. (ref.25) Lebwohl et al. (ref.14) Leonardi et al. (ref.26) | 1.104 pacientes | Espuma Cal/BD vs. espuma Cal vs. espuma BD vs. pomada Cal/BD vs. vehículo espuma | 1 aplicación/día 4 semanas | EA espuma Cal/BD: 13,8% (n.s. vs. otros) RAM espuma Cal/BD: 2,7 vs. 3% pomada Cal/BD vs. 6,1% espuma Cal vs. 7,1% espuma BD RAM más frecuentes espuma Cal/BD: dolor (4/564) y prurito (2/564) en el lugar de aplicación |
| Potencial de irritación y sensibilización | Queille-Roussel et al. J Am Acad Dermatol. 2015 (ref.32) | Fase I, unicéntrico, aleatorizado, controlado | 213 voluntarios sanos | Espuma Cal/BD vs. vehículo espuma vs. vaselina blanca (control negativo) | 5 aplicaciones/semanas parches (semioclusivo) durante 3 semanas+2 sem. descanso+1 aplicación | Potencial irritativo bajo Puntuación máxima 2 (eritema con edema leve-moderado) en 3/213 voluntarios |
| Estudio MUSE (máximo uso y exposición sistémica) | Taraska et al. J Cutan Med Surg. 2016 (ref.34) | Fase II, multicéntrico, abierto, no controlado | 35 pacientes psoriasis moderada-grave BSA: 15%-30% | Espuma Cal/BD | 1 aplicación/día 4 semanas 13,5-113g/semana | Prueba estimulación con ACTH: normal Calcio sérico corregido Albúmina: normal Calcio en orina de 24h: normal Ratio calcio/creatinina en orina: normal |
EA: efectos adversos, mPASI: PASI modificado (PASI modificado que no considera la afectación en la cabeza); RAM: reacciones adversas asociadas a medicamento.
Los análisis combinados de Stein Gold y Menter et al. agrupan los datos de los 3 ensayos de 4 semanas de duración: Leonardi et al.26; Lebwohl et al.14; Koo et al.25.
En el ensayo de fase ii frente a los monocomponentes, el porcentaje de pacientes que alcanzó el éxito terapéutico (piel «limpia o casi limpia» [PGA 0/1], con al menos una mejora de 2 puntos21) tras 4 semanas fue significativamente mayor con la espuma Cal/BD (45%) que con la espuma de Cal (14,9%; p<0,001) y la espuma de BD (30,7%; p=0,047). También la reducción del mPASI y el porcentaje de pacientes con respuesta mPASI75 (p<0,001 para Cal) fue mayor con la espuma de Cal/BD14.
En el ensayo de fase ii frente a la misma combinación en pomada, la proporción de éxito terapéutico (PGA 0/1) de la espuma Cal/BD fue significativamente superior a la pomada de Cal/BD (54,6% vs. 43%; p<0,05) y a los vehículos en pomada y espuma, con un perfil de seguridad similar. La reducción del mPASI también fue significativamente superior con la espuma de Cal/BD respecto a pomada, desde la semana 1 (−43,4 vs. −30,5%; p<0,001) hasta la semana 4 (−74,2 vs. −63,2%; p<0,01)25.
El estudio PSO-FAST26, de fase iii que comparó el Cal/BD en espuma frente a su vehículo, confirmó la eficacia del brazo activo con una tasa de éxito terapéutico del 53,3 vs. 4,8% del vehículo (p<0,001) y una puntuación de mPASI final de 2 vs. 5,5 (p<0,001) tras 4 semanas de tratamiento. El 83,5% de pacientes refirieron una rápida y significativa disminución del prurito. También hubo mejora de la calidad de vida, con reducción del DLQI de 7 puntos vs. 4,4 (p<0,001), y un 48,1 vs. 21,2% (p<0,001) de los pacientes reportaron poca o ninguna afectación en su calidad de vida (DLQI 0/1) tras 4 semanas29.
En el estudio PSO-ABLE27, la espuma de Cal/BD mostró una mayor eficacia después de 4 semanas en comparación con el Cal/BD en gel en la semana 8, tanto en el porcentaje de éxito terapéutico (38 vs. 22%; p<0,001), como en el porcentaje de pacientes que alcanzaron respuesta mPASI75 (52 vs. 35%; p<0,001) y mPASI90 (22,2 vs. 10,7%; p<0,001). En la semana 12, la tasa de éxito del tratamiento fue del 44,1% con la espuma de Cal/BD frente al 34,3% con el gel. En el cuestionario de preferencias, el 83,7% de los pacientes tratados con espuma Cal/BD prefería este tratamiento respecto a otras terapias tópicas previas, percibiéndola como más eficaz (88,3%), más fácil de aplicar (76,5%) y con mejor tolerabilidad (81,0%)27. En un subanálisis de este estudio donde se seleccionaron los pacientes con psoriasis moderada-grave (BSA≥10% o mPASI>10 o DLQI>10), se demostró una mayor proporción de pacientes con respuesta mPASI75 en las semanas 4, 8 y 12 con la espuma Cal/BD respecto al gel Cal/BD (57,1 vs. 35,4%; p=0,006 en la semana 12). La tasa de éxito terapéutico (PGA 0/1) fue mayor con la espuma en la semana 4 (32 vs. 19%; n.s.), en la semana 8 (35,6 vs. 16,9%; p<0,05) y en la semana 12 (38 vs. 31,6%; n.s.)30. En otro subestudio de biomarcadores con los pacientes más graves del PSO-ABLE se observó que, tras 12 semanas de tratamiento, hubo una reducción significativa de los niveles de biomarcadores proinflamatorios como la interleucina 17A y la quimiocina derivada de macrófagos CCL22 (p<0,0001); mientras que los niveles de adiponectina, marcador cardioprotector, se incrementaron (p=0,03). Estudios prospectivos controlados por placebo serían necesarios para confirmar estos resultados31.
Seguridad de la espuma en aerosol de calcipotriol y dipropionato de betametasonaLa espuma de Cal/BD ha demostrado un bajo potencial irritativo y de sensibilización32. Los estudios de eficacia fase ii y iii demostraron un perfil de seguridad aceptable y una buena tolerabilidad hasta 12 semanas de tratamiento14,25–27. El análisis combinado de 3 ensayos con un total de 1.104 pacientes tratados durante 4 semanas mostró que los eventos adversos más frecuentes asociados con la espuma de Cal/BD fueron nasofaringitis (n=6; 1,1%) y dolor en el sitio de aplicación (n=4; 0,7%). La tasa de reacciones adversas asociadas a medicamento fue del 2,7%, siendo los más frecuentes: dolor (n=4; 0,7%) y prurito (n=2; 0,4%) en el lugar de aplicación33. Globalmente, el perfil de seguridad del Cal/BD en espuma fue similar a la misma combinación en gel y pomada. No se detectaron efectos adversos locales ni sistémicos con el uso prolongado de la espuma en el estudio PSO-ABLE27.
Finalmente, el estudio de fase ii (MUSE)34 evaluó la función del eje hipotálamo-hipófisis suprarrenal y la homeostasis del calcio en condiciones de uso máximo de la espuma de Cal/BD (13,5-113g/semana) durante 4 semanas. Este estudio no mostró efectos clínicamente relevantes sobre el eje hipotálamo-hipófisis suprarrenal ni sobre el calcio sérico corregido con albúmina, el calcio en orina de 24h ni la ratio calcio/creatinina en orina.
DiscusiónEl tratamiento tópico sigue siendo la piedra angular del manejo diario de la psoriasis, especialmente en casos de enfermedad leve, o como complemento del tratamiento sistémico. Sus principales ventajas son la reducción de los riesgos de toxicidad farmacológica y el de conferir autonomía al paciente con psoriasis en cuanto a su tratamiento, mientras que los principales inconvenientes son la menor eficacia frente a tratamientos sistémicos, aunque no haya ensayos clínicos al respecto, y la menor adherencia potencial por parte de los pacientes.
Disponer de nuevos fármacos de aplicación tópica de mayor eficacia en psoriasis y mayor comodidad de aplicación es un reto prioritario en el desarrollo de nuevos productos. Una de las estrategias de innovación actuales radica en la reformulación de fármacos ya conocidos15 que permite mejorar la biodisponibilidad de los principios activos sobre la piel, mejorando así su potencial terapéutico y sus características organolépticas. Estos 2 factores tienen impacto en las preferencias de los pacientes e incrementan la adherencia terapéutica.
En esta revisión se han evaluado los datos del desarrollo clínico del Cal/BD en un nuevo vehículo (espuma) y dispositivo (aerosol) a través del que se demuestra un nivel de eficacia adecuado, mejorando los preparados ya existentes (gel y pomada) y permitiendo un tratamiento tópico cómodo y prolongado de la psoriasis.
Esto es posible gracias a la galénica en espuma que, tras su aplicación sobre la piel, permite la creación de una solución de Cal/BD sobresaturada estable y totalmente biodisponible que aumenta la tasa de penetración a través del estrato córneo, sin comprometer la seguridad.
Se están llevando a cabo otros estudios con la espuma de Cal/BD para evaluar su eficacia como terapia de mantenimiento a largo plazo (NCT02899962) y su seguridad y eficacia en población pediátrica (NCT02387853)35.
Actualmente están en fase de desarrollo diversas moléculas para el tratamiento tópico de la psoriasis36. En fase ii se encuentran crisaborol –un antiinflamatorio inhibidor de la fosfodiesterasa 4 aprobado por la FDA para el tratamiento de la dermatitis atópica– (NCT01300052), lPH-10 (Rosa de Bengala) en hidrogel (NCT01247818), SNA-120 (Pegcantratinib) en pomada (NCT03322137) y tofacitinib en pomada (NCT01831466). En fase 3 se están estudiando IDP-118, una combinación de propionato de halobetasol y tazaroteno en loción (NCT02462083), M518101 (NCT01908595) y MC2-01, calcipotrieno y dipropionato de betametasona en crema (NCT03308799).
Conflicto de interesesEste manuscrito ha sido redactado con ayuda de BlueBliss, financiado por LEO Pharma.
El Dr. Puig ha percibido honorarios como consultor, y su institución ha percibido ingresos por su participación como investigador en ensayos clínicos de LEO Pharma. El Dr. Carretero ha participado como consultor o ha impartido charlas en nombre de LEO Pharma y Gebro Pharma.
A Lidia Rodriguez, Cluster Medical Advisor Dermatology (Southern Europe) de LEO Pharma, por su ayuda en la edición del manuscrito.