El eczema de manos (ECM) afecta a cerca del 10% de la población, presentándose entre el 5 y el 7% de los casos como una enfermedad crónica grave y siendo refractario al tratamiento con corticoides tópicos entre el 2 y el 4% de las veces. El propósito del artículo es describir el uso de la alitretinoína oral en pacientes con ECM refractario a corticoides tópicos potentes en el ámbito sanitario público español.
Material y métodosEstudio observacional descriptivo, exploratorio, transversal, basado en la revisión retrospectiva de historias clínicas de pacientes con ECM en tratamiento con alitretinoína en el ámbito sanitario público español.
ResultadosSe revisaron 62 historias clínicas de pacientes de 13 centros distribuidos en 5 comunidades autónomas del territorio español. Alitretinoína se utilizó predominantemente a dosis de 30mg/día, principalmente en un único ciclo, tras el cual la mayoría de pacientes lograron una respuesta clínica satisfactoria según el juicio médico. Los eventos adversos fueron todos previsibles y en línea con los tratamientos sistémicos con retinoides. Los dermatólogos estuvieron de acuerdo en que los beneficios clínicos logrados con alitretinoína favorecían la adherencia al tratamiento y una reincorporación más rápida de los pacientes al trabajo.
ConclusiónLos resultados muestran un uso de alitretinoína oral en línea con las recomendaciones establecidas así como la buena respuesta al tratamiento asociado y los pocos efectos adversos. Los dermatólogos coinciden que los beneficios alcanzados favorecen la adherencia al tratamiento y mejoran la calidad de vida relacionada con la salud de los pacientes.
Hand eczema affects nearly 10% of the population. The condition becomes severe and chronic in 5% to 7% of cases and is refractory to topical corticosteroids in 2% to 4%. This study aimed to describe the current use of oral alitretinoin in treating Spanish national health system patients with hand eczema that is refractory to potent topical corticosteroids.
Materials and methodsObservational, descriptive, exploratory, cross-sectional study based on the retrospective analysis of records for patients with hand eczema treated with alitretinoin in the Spanish national health system.
ResultsWe reviewed the records for 62 patients in 13 hospitals in 5 different administrative areas (autonomous communities) of Spain. Alitretinoin was usually used at a dosage of 30mg/d. In most cases the physician judged the clinical response to be satisfactory after a single cycle. The recorded adverse effects were foreseeable and of the type reported for systemic retinoids. The dermatologists agreed that the clinical benefits achieved with alitretinoin favored adherence to treatment and an early return to work.
ConclusionsThe results show that oral alitretinoin is being used according to established recommendations and that response is good, with few adverse effects. The dermatologists agreed that the benefits favored adherence and improved the patients’ health related quality of life.
El eczema crónico de manos (ECM) es aquel que persiste durante más de 3 meses o reaparece 2 o más veces en un periodo de 12 meses a pesar de la aplicación de medidas terapéuticas1. Se caracteriza por la presencia de eritema, vesículas, pápulas, grietas, hiperqueratosis, prurito y dolor que pueden variar en gravedad, desde un compromiso leve hasta una afección incapacitante2,3. El eczema de manos afecta a alrededor del 10% de la población4,5, de esta, entre el 5 y el 7% tiene una enfermedad crónica grave, y entre el 2 y el 4% son refractarios al tratamiento con corticoesteroides tópicos1.
Se estima que en España hay alrededor de 5.000 personas afectadas por la enfermedad grave refractaria al tratamiento, siendo la mayoría adultos en edad laboral6,7. El ECM puede llegar a convertirse en un estigma social que podría provocar rechazo y afectar la calidad de vida relacionada con la salud (CVRS) de los pacientes, así como comprometer su vida laboral8,9.
El tratamiento para el ECM grave son los corticoesteroides tópicos potentes1. También se utilizan inhibidores de la calcineurina tópicos, fototerapia con psoralenos y radiación ultravioleta de longitud de onda larga (PUVA), así como tratamientos sistémicos con corticoesteriodes o inmunosupresores como la ciclosporina10–12.
La alitretinoína es el único tratamiento oral aprobado por la Agencia Española de Medicamentos y Productos Sanitarios para el tratamiento del ECM grave resistente a los corticoesteroides tópicos potentes13. Es un panagonista de los receptores intracelulares de los retinoides que regula la multiplicación y la diferenciación celular, así como la apoptosis celular, además de tener efectos inmunomoduladores y antiinflamatorios relevantes para la inflamación de la piel14. Su eficacia y seguridad en el tratamiento del ECM grave y refractario se ha evaluado en pacientes adultos a dosis diarias de 10-30mg administradas durante 12-24 semanas4,15–17.
El objetivo principal de este estudio es describir el uso de alitretinoína en pacientes con ECM en el ámbito sanitario público español proporcionando una descripción detallada de las características sociodemográficas y clínicas de los pacientes, la respuesta obtenida con el tratamiento, la adherencia y la CVRS de los pacientes y la satisfacción global de los médicos con el tratamiento.
MetodologíaDiseñoSe llevó a cabo un estudio observacional, descriptivo, exploratorio y transversal basado en la revisión de historias clínicas de pacientes con ECM tratados con alitretinoína en el ámbito sanitario público español entre julio y septiembre de 2012.
Población del estudioEn el momento del estudio, alitretinoína solo podía dispensarse en ámbitos hospitalarios, en servicios especializados de dermatología y a petición de las farmacias de hospital a la Agencia Española del Medicamento (AEMPS). Todos los pacientes tratados con alitretinoína fueron identificados a partir de historias clínicas. El estudio incluía pacientes mayores de 18 años de edad, con diagnóstico de ECM, que habían recibido tratamiento con alitretinoína y con al menos una visita de seguimiento documentada en la historia clínica en el momento de la recopilación de datos. Se excluyó a pacientes con diagnóstico distinto del ECM, con infecciones u otras afecciones cutáneas, de cualquier etiología, documentadas en la historia clínica, que pudieran interferir en la evaluación de la respuesta a alitretinoína. La selección e inclusión de las historias clínicas en el estudio fue secuencial y no aleatorizada.
Se invitó a participar a un total de 21 centros hospitalarios pertenecientes al ámbito sanitario español.
Variables recopiladasMediante un cuaderno de recogida de datos (CRD) específico para este estudio, se recopilaron datos de los pacientes referentes a las características sociodemográficas (edad, sexo, situación y sector laboral, contacto con sustancias asociadas al ECM) y clínicas: patología concomitante asociada a ECM (dermatitis atópica, alergia, asma, rinoconjuntivitis u otras), antecedentes patológicos (diabetes, patología tiroidea, insuficiencia hepática, insuficiencia renal, hipercolesterolemia, hipertrigliceridemia, hipervitaminosis A, hipertensión arterial, obesidad, otras enfermedades dermatológicas o sistémicas), fecha del diagnóstico y pruebas diagnósticas realizadas, tipo, localización y grado de afectación del ECM, síntomas y signos asociados; dosis, frecuencia y duración del tratamiento con alitretinoína, del tratamiento previo recibido para el ECM, del tratamiento concomitante no relacionado con el ECM y del tratamiento concomitante para el ECM; acontecimientos adversos y gravedad documentados; respuesta a los criterios de tratamiento aplicados por el médico responsable (incluidos Physician Global Assessment [PGA, Evaluación global del médico], Patient Global Assessment [PaGA, Evaluación global del paciente] o modified Total Lesion Symptom Score [mTLSS, Marcador Modificado de Síntomas de la Lesión Total]18); respuesta al tratamiento; pruebas analíticas y resultados solicitados durante el diagnóstico y el seguimiento; y plan de prevención de embarazos (si corresponde).
Para definir la satisfacción de los médicos con la respuesta al tratamiento, en el momento de la recogida de datos los médicos cumplimentaron un cuestionario ad hoc que contenía preguntas relativas a su satisfacción con el uso de alitretinoína en la población estudiada, el tipo de respuesta clínica obtenida tras su indicación y el nivel de adherencia y cumplimiento terapéutico que observaron, así como las condiciones de prescripción habituales y el seguimiento de las recomendaciones para su uso (cuestionario disponible como material suplementario). Las preguntas se respondieron mediante una escala tipo Likert de 5 puntos (1=muy insatisfecho, 2=insatisfecho, 3=satisfecho, 4=muy satisfecho y 5=completamente satisfecho).
Requisitos éticosEl diseño retrospectivo del estudio requirió la existencia de una política en vigor en el centro sanitario correspondiente, que cumpliese las condiciones de confidencialidad y no trazabilidad establecidas en la Ley Orgánica de Protección de Datos de Carácter Personal (LOPD). El protocolo del estudio fue aprobado por el Comité Ético de Investigación Clínica del Hospital Puerta de Hierro (Madrid).
ResultadosCentros participantes y número final de historias clínicas revisadasDe los 21 centros hospitalarios identificados inicialmente, 13 aceptaron participar en el estudio, distribuidos en 5 comunidades autónomas del territorio español (Andalucía n=1; Aragón n=1; Castilla la Mancha n=2; Catalunya n=2 y Madrid n=7). Se identificaron 72 historias clínicas, de las cuales 62 (86%) cumplían los criterios de selección. Los motivos de exclusión fueron cambio en el diagnóstico de ECM por diagnóstico de psoriasis durante el tratamiento (n=1), tratamiento indicado para psoriasis (n=1), diagnóstico exclusivo de eczema crónico en los pies (n=2), historia clínica no disponible (n=1) y ausencia de seguimiento clínico (n=5).
Características sociodemográficas de los pacientesLa tabla 1 muestra las características sociodemográficas y situación laboral de los pacientes incluidos en el estudio. La media de edad era de 53 años (DE 13) con una proporción similar de hombres (46,8%) y de mujeres (53,2%). Alrededor del 40,3% (n=25) eran trabajadores activos, 9,7% eran amas de casa, 9,7% pensionistas y 1,6% desempleados. La mayoría de pacientes pertenecían a la industria textil, química y de plásticos (11,3%), seguida de trabajo doméstico (9,7%), construcción (8,1%) y hostelería y restauración (8,1%). Dos pacientes hacían referencia al ECM como factor determinante de la modificación en la actividad profesional, y 6 especificaban el ECM como causa de incapacidad laboral transitoria.
Diagnóstico de eczema crónico de manosEn el 75,8% (n=47) de los pacientes se realizaron pruebas para el diagnóstico del ECM (promedio de 1,7 [DE 0,6]), siendo las más utilizadas las pruebas del parche (66,1%; n=41) y las biopsias (29,0%; n=18).
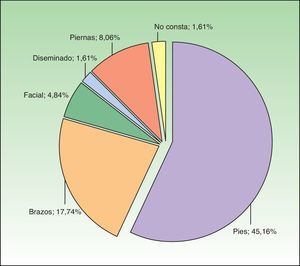
El subtipo de ECM más frecuente era el fisurado hiperqueratósico (29,0%; n=18), mientras que en el 12,9% (n=8) de los pacientes coexistía más de un subtipo. El ECM se observó con más frecuencia en las palmas (69,35%, n=43) y en el dorso de las manos (16,13%, n=10). Aunque en el 67,74% de los pacientes (n=42) el ECM se observó en una sola localización (manos), en el 19,35% (n=12) y en el 11,29% (n=7) se observó en 2 o 3 localizaciones diferentes, respectivamente. La figura 1 muestra diferentes ubicaciones descritas además de las manos.
Respecto a los síntomas asociados al ECM, se documentó al menos un síntoma en el 62,9% (n=39) de los pacientes. Estos síntomas incluían prurito (61,3%: leve n=2; moderado n=3; intenso n=17; sin definición de la intensidad n=16), dolor (16,1%: moderado n=2; intenso n=4; sin definición de la intensidad n=4) y escozor (3,2%: moderado n=2). En el 90,3% (n=56) de los pacientes se registraron signos asociados al ECM como enrojecimiento, descamación, vesículas, edema y grietas, siendo los más frecuentes descamación (62,9%; n=39), enrojecimiento (45,2%; n=28) y grietas (38,7%; n=24).
En el 69,3% de los pacientes, la intensidad del ECM se documentó en el momento del diagnóstico. El grado de intensidad se recogió en la historia con diferentes términos como «severo», «intenso» e «importante», considerándose equivalentes para el análisis. Se documentó ECM grave en 9 pacientes, mientras que, asumiendo que los términos brote, «moderado» y «moderado a intenso» representaban una intensidad moderada, 21 pacientes tuvieron este grado intermedio de intensidad.
El 87,1% (n=54) de las historias hizo referencia a la resistencia del ECM al tratamiento con corticoesteroides tópicos potentes, usando términos como «falta de respuesta» (69,4% [n=43]) o «corticodependiente» (9,7% [n=6]). En 5 pacientes (8,1%), el «impacto en la calidad de vida» se describió, junto con la resistencia al tratamiento, como un aspecto complementario de la evaluación del ECM. No se documentó el uso de escalas de medida recomendadas para estas características de la enfermedad.
Más de la mitad de las 62 historias (58,1%; n=36) describían una o más enfermedades concomitantes asociadas al ECM, siendo la dermatitis atópica (22,6%, n=14), la alergia (16,1%, n=10) y la rinitis (9,7%, n=6) las más comunes.
Tratamiento previo al inicio de alitretinoínaAntes de la introducción de alitretinoína los pacientes habían recibido una media de 3 (DE 1,6) medicamentos. Entre los tratamientos tópicos, el 83,9% (n=52) fueron corticoides, el 33,9% (n=21) inmunomoduladores, mientras que el 25,8% (n=16) fueron retinoides tópicos. La fototerapia se utilizó en el 16,1% (n=10) de los casos.
Más de la mitad de los pacientes (56,4%, n=35) recibieron medicamentos sistémicos para el ECM en algún momento de la enfermedad, incluidos los corticoesteroides orales (43,5%, n=27), inmunosupresores (33,9%, n=21), analgésicos y antibióticos (1,6%, n=1). El 22,6% (n=14) de los pacientes fueron tratados con antihistamínicos y la misma proporción de pacientes (4,8%, n=3) fueron tratados con antigotosos como la colchicina o antipalúdicos.
Tratamiento con alitretinoínaDe los 62 pacientes incluidos, el 83,9% (n=52) recibió un único ciclo de tratamiento con alitretinoína, el 14,5% (n=9) recibió 2 ciclos y solo un paciente (1,6%) recibió 3 ciclos.
El tiempo medio transcurrido entre los ciclos de tratamiento fue de 6,7 meses (DE 8,9) para el primer y el segundo ciclo, y de 16 meses entre el segundo y el tercer ciclo. Se utilizó alitretinoína 30mg/día en el 83,8% (n=52) de los pacientes durante el ciclo 1, en el 66,7% (n=6) durante el ciclo 2 y en el 100% (n=1) en el tercer ciclo. En un paciente (1,6%) se utilizó una dosis inicial de 30mg que posteriormente se redujo a 10mg debido a las cefaleas, mientras que en otro paciente una dosis inicial de 10mg se aumentó posteriormente a 30mg el día 20. A los pacientes que recibieron un segundo ciclo de tratamiento se les cambió la dosis respecto a la aprobada en el 22,2% (n=2) de los casos, siendo prescrita una dosis de 30mg cada 48 horas. La duración del primer ciclo de tratamiento tuvo una mediana de 15,9 semanas (rango 2-82 semanas) mientras que la duración del segundo ciclo de tratamiento fue de mediana 8,3 semanas (rango 4-65). Finalmente, en el único paciente que recibió un tercer ciclo de tratamiento, la duración fue de 65 semanas.
El tiempo transcurrido desde el inicio del tratamiento con alitretinoína hasta la primera evaluación de la respuesta presentó una mediana de 35 días (rango 0-607), 42 días (rango 0-61) y 90 días para el primero, segundo y tercer ciclo, respectivamente.
El uso de alguna herramienta recomendada usualmente para la evaluación de la respuesta al tratamiento se documentó en el 35,5% de los pacientes. Respecto a la respuesta al tratamiento, la tabla 2 muestra la evaluación obtenida según el ciclo. En la mayoría de los casos, la respuesta al tratamiento («manos limpias o casi limpias») fue establecida según el juicio clínico del médico.
Distribución de la muestra con base en la evaluación de la respuesta al tratamiento con alitretinoína oral después de cada ciclo
| Evaluaciones | Ciclo 1 | Ciclo 2 | Ciclo 3 | |||
|---|---|---|---|---|---|---|
| n | % | n | % | n | % | |
| Manos limpias | 8 | 12,9 | 1 | 11,1 | – | – |
| Manos casi limpias | 2 | 3,2 | – | – | – | – |
| Mejoría clínica | 31 | 50 | 3 | 33,3 | 1 | 100 |
| Buena evolución | 8 | 12,9 | – | – | – | – |
| Falta de respuesta | 9 | 14,5 | 1 | 11,1 | – | – |
| Sin valoración descrita | 4 | 6,45 | 4 | 44,4 | – | – |
| Total | 62 | 100 | 9 | 100 | 1 | 100 |
Teniendo en cuenta los datos arriba mencionados, 49 (79%) pacientes mostraron una mejoría del ECM (10 de ellos lograron «manos limpias o casi limpias»), mientras que 9 (14,5%) no refirieron ninguna respuesta al tratamiento y 4 (6,4%) no registraron datos de valoración. Se observó una mejoría de la enfermedad en 4 (44,4%) de los 9 pacientes que recibieron un segundo ciclo de tratamiento, mientras que uno (11,1%) no tuvo ninguna respuesta al tratamiento y 4 (44,4%) no registraron datos de valoración. En el paciente en el que se indicó un tercer ciclo de tratamiento se observó mejoría clínica en la primera evaluación de seguimiento realizada.
Alrededor del 43,5% (n=27) de los pacientes recibieron un tratamiento tópico concomitante, como emolientes (22,6%; n=14), corticoesteroides muy potentes (19,4%; n=12) y corticoesteroides potentes (3,2%; n=2). Además, el 6,5% (n=4) usaron corticoesteroides sistémicos.
Control y seguridad del tratamiento con alitretinoínaSe dispuso de información sobre la realización de pruebas clínicas como parte del seguimiento del tratamiento con alitretinoína de casi todos los pacientes (98,4%). Se requirió una mediana de 2 (rango 0-13) pruebas analíticas por paciente. La mayoría de participantes (93,4%) mostraron alteraciones bioquímicas durante diferentes ciclos de tratamiento, siendo la alteración del perfil lipídico la más frecuente (hipercolesterolemia [32,3%], hipertrigliceridemia [3,2%] o ambas [6,5%]), seguida de cambios en el recuento de glóbulos blancos (3,2%), aumento de TSH (3,2%) e hiperglucemia (1,6%). No obstante en ningún caso estas alteraciones produjeron una interrupción del tratamiento.
Plan de prevención de embarazosDe las 33 mujeres incluidas, 20 (60,6%) estaban en edad fértil, por lo cual, debían seguir un plan de prevención de embarazos mientras siguieran el tratamiento. No obstante en 14 (70,0%) de estas no se hacía referencia al uso de métodos anticonceptivos en las historias clínicas. Se recomendó el uso de anticonceptivos orales en 4 de las 6 pacientes restantes, mientras que en las otras 2 no se requerían medidas anticonceptivas (un caso con antecedente de histerectomía y en el otro caso la pareja había recibido tratamiento de esterilización definitiva [vasectomía]).
SeguridadDe los 62 pacientes estudiados, el 29% (n=18) no contaba con datos referentes a efectos adversos, 17 (27,4%) no presentaron efectos adversos y 27 (43,5%) presentaron al menos un efecto adverso relacionado con el tratamiento con alitretinoína. El efecto adverso más frecuente fue cefalea (25,8%), seguida de xeroftalmia y xerosis (4,8%), que aparecieron en la misma proporción de pacientes.
Diecinueve pacientes interrumpieron el tratamiento con alitretinoína (5 abandonos por falta de respuesta, 2 debidos al empeoramiento del ECM y 2 debidos a los acontecimientos adversos [cefalea e hinchazón nocturna]).
Satisfacción de los dermatólogos con el tratamiento con alitretinoínaEl 100% de los expertos estaba satisfecho con la eficacia, tiempo, tipo y duración de la respuesta, perfil de seguridad y tolerabilidad de alitretinoína. Todos ellos afirmaron que recomendarían alitretinoína para el tratamiento del ECM.
El 91,7% de los dermatólogos estaban satisfechos, muy satisfechos o completamente satisfechos con la proporción de «pacientes respondedores al tratamiento» observada en su práctica habitual. El 91,7% de los especialistas señalaron que la adherencia (sinónimo de cumplimiento, definida como «grado en que un paciente actúa de acuerdo con el intervalo y dosis prescritos de un régimen de tratamiento»19) con alitretinoína fue mejor en comparación con otros tratamientos para el ECM. Además, el 83,3% observaron una mejor adherencia al tratamiento que con otros tratamientos habitualmente usados para el ECM. Asimismo, el 75% de los médicos consideró que los pacientes que recibieron tratamiento con alitretinoína pudieron regresar antes a su trabajo. Respecto a las condiciones de dispensación y prescripción en vigor en el momento del estudio (uso compasivo), el 66,7% de los dermatólogos reportaron no estar satisfechos con las mismas.
DiscusiónLa Organización Mundial de la Salud promueve estudios relacionados con el uso de medicamentos en la práctica clínica habitual18. Según sus estadísticas, más del 50% de los medicamentos se prescriben, dispensan o venden inadecuadamente, mientras que la mitad de los pacientes no los toman correctamente. Las consecuencias directas conllevan riesgos asociados a los efectos no deseados, pobres resultados y repercusión sobre los recursos sanitarios. En este contexto, este estudio describe cómo la alitretinoína se utiliza en la práctica clínica por parte de médicos especialistas con experiencia tanto en el tratamiento del ECM como en el uso de los retinoides orales. Los presentes resultados ponen de manifiesto que su uso no está del todo acorde con las recomendaciones presentadas en el resumen de las características del producto14. Sin embargo, la documentación de las historias clínicas no es homogénea cuando se comparan distintos hospitales, lo que dificulta la recopilación de datos. Lo mismo ocurre con el seguimiento de las recomendaciones sugeridas en la literatura médica sobre cómo documentar la respuesta al tratamiento, teniendo en cuenta que han de ser el elemento clave en la decisión de continuar, o no, con el tratamiento9.
Con las limitaciones propias del estudio, se puede observar una buena respuesta al tratamiento del ECM con alitretinoína, así como una tolerabilidad aceptable. Los hallazgos en cuanto a la eficacia y la seguridad de alitretinoína, así como las características de la población estudiada y la manifestación clínica del ECM en este informe coinciden con un estudio observacional, prospectivo y descriptivo realizado previamente en España4. A excepción del subtipo de ECM documentado con más frecuencia (en nuestro estudio es el subtipo hiperqueratósico-fisurado, 29,03%), las tasas de respuesta con «manos limpias o casi limpias», el perfil de acontecimientos adversos con predominancia de cefaleas y el tipo de tratamiento recibido son muy similares. Sin embargo, la definición y el registro en las historias clínicas de los criterios de intensidad, cronicidad y resistencia al tratamiento previo, así como la recogida de datos del tratamiento concomitante empleado ha sido una de las limitaciones de este estudio.
El uso de alitretinoína, junto con la información clínica disponible en el momento del estudio se llevó a cabo en un contexto de incertidumbre. Este contexto generalmente prevalece en el tratamiento de enfermedades recurrentes e incapacitantes como el ECM, para las cuales las alternativas de tratamiento existentes son muy limitadas, empleadas «off-label», y con una respuesta clínica indeterminada. Estas circunstancias contrastan con alitretinoína, un medicamento aprobado para el ECM grave y resistente al tratamiento y con una respuesta clínica estudiada15–17.
El ECM grave y refractario al tratamiento es relativamente poco frecuente en España, un hecho que junto con la dificultad del acceso a alitretinoína, debido a sus condiciones de dispensación, supuso un número muy limitado de pacientes susceptibles de ser incluidos en el estudio. No obstante, los hallazgos de este trabajo tienen una validez importante debido a su descripción del uso de un medicamento concreto en la práctica habitual en una enfermedad presente en el sistema sanitario público, aunque los resultados no pueden extrapolarse a otras áreas de la asistencia sanitaria.
Los datos recogidos han permitido describir una tendencia de uso y la necesidad de unificar la recopilación de información del paciente en las historias clínicas, así como normalizar el uso de las herramientas de evaluación para medir la respuesta clínica al tratamiento y los objetivos terapéuticos que se quieren conseguir. Igualmente, los resultados obtenidos sobre la satisfacción de los dermatólogos con el uso de alitretinoína se deben interpretar en el contexto del número de expertos que respondieron al cuestionario.
En conclusión, la alitretinoína se utiliza para el tratamiento del ECM grave y refractaria al tratamiento, predominantemente a dosis de 30mg/día, principalmente en un único ciclo, tras el cual la mayoría de pacientes lograron una respuesta clínica satisfactoria según el juicio médico. Los eventos adversos fueron todos previsibles y en línea con los tratamientos sistémicos con retinoides. Finalmente, los especialistas en dermatología estuvieron de acuerdo en que los beneficios clínicos logrados con alitretinoína favorecen la adherencia al tratamiento y una reincorporación más rápida al trabajo por parte de los pacientes.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónEste estudio ha sido patrocinado por Almirall, SA.
Conflicto de interesesLos Dres. S. Urrutia y G. Roustan declaran haber recibido honorarios por su contribución como expertos en el tema de interés. S. Paz y L. Lizán trabajan para una entidad independiente de investigación y han recibido honorarios por su contribución para el desarrollo y coordinación del proyecto de investigación original así como para la redacción inicial de este manuscrito. Todos los honorarios han sido asumidos por el promotor del estudio, Almirall SA. Las Dras. M.J. Plazas y S. Armengol trabajan en Almirall SA.
No obstante, los autores declaran que los resultados de la investigación descritos en este manuscrito así como el análisis e interpretación de los mismos derivan de la libre opinión y acuerdo de los coautores de la publicación no habiendo existido conflictos ni para la obtención ni para la divulgación de tales resultados.
Los autores desean agradecer a Stiefel/GSK por revisar la exactitud de la información sobre el producto incluida en este manuscrito.