Varón de 81 años de edad con antecedentes de leucemia linfática crónica en estadio A, artritis reumatoide en tratamiento con metotrexato 7,5mg semanales, prednisona y diclofenaco y cardiopatía isquémica.
Consulta por la aparición de una úlcera escrotal dolorosa de pocas semanas de evolución que se trató con sulfadiazina argéntica tópica. Un mes después la lesión había empeorado y el paciente presentaba además deterioro del estado general con fiebre, disnea, palidez cutáneo-mucosa y adenopatías axilares e inguinales.
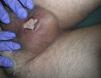
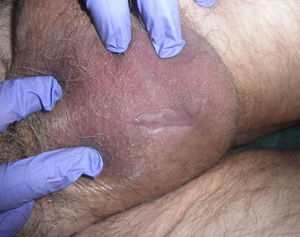
Exploración físicaEn el escroto se observaba una úlcera de 2×4cm de diámetro con los bordes discretamente infiltrados y un fondo fibrinoso (fig. 1).
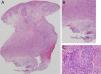
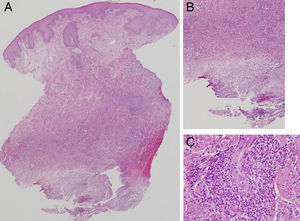
HistopatologíaEn la biopsia cutánea se objetivaba una epidermis con mínima hiperqueratosis. En profundidad existía una zona de necrosis geográfica rodeada por un intenso componente inflamatorio mixto de predominio linfomonocitario con células plasmáticas, histiocitos y eosinófilos. No se observaban infiltrados granulomatosos (fig. 2).
Pruebas complementariasEn la analítica destacaba pancitopenia, deterioro de la función renal, aumento de LDH y de proteína C reactiva. Los cultivos del exudado de la úlcera y del tejido fueron negativos.
¿Cuál es su diagnóstico?
DiagnósticoÚlcera cutánea secundaria a metotrexato.
Evolución y tratamientoSe suspendió metotrexato y se administró ácido folínico intravenoso.
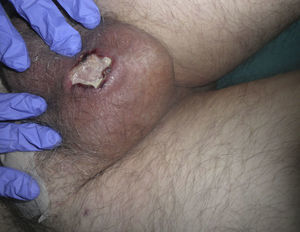
El hemograma se normalizó paulatinamente, observándose disminución progresiva de la úlcera. Un mes después la úlcera cutánea estaba totalmente reepitelizada (fig. 3).
DiscusiónEl metotrexato es un análogo sintético del ácido fólico utilizado como agente quimioterápico y en el tratamiento de enfermedades inflamatorias1.
Las reacciones adversas más comunes incluyen molestias gastrointestinales, artromialgias y malestar general, siendo en general dosis dependientes y atenuadas por el uso de ácido fólico. Además pueden observarse efectos secundarios más graves como alteraciones hepáticas y hematológicas1.
Dentro de los efectos adversos cutáneos la estomatitis y las aftas orales son relativamente frecuentes, y suelen representar un signo precoz de toxicidad. Otras alteraciones cutáneas como fotosensibilidad, exantemas, vasculitis, eritema, descamación y necrólisis epidérmica tóxica2,3 son raras y se presentan a dosis altas del fármaco.
A diferencia de las úlceras mucosas las úlceras cutáneas constituyen un efecto secundario infrecuente2,4, descrito fundamentalmente en pacientes con psoriasis2. En pacientes sin antecedentes de esta dermatosis son excepcionales, encontrándose pocos casos reflejados en la bibliografía5,6 y observándose la asociación con pancitopenia como signo de toxicidad medicamentosa5.
Según una revisión de la literatura, realizada por Pearce y Wilson entre 1967 y 1996, solo 17 pacientes experimentaron dicho efecto secundario7.
Lawrence et al.7 dividen estas úlceras cutáneas en 2 tipos: las de tipo i se presentan como necrosis de las placas de psoriasis y las de tipo ii se describieron en la piel no afectada por psoriasis, pero con alteraciones previas o concurrentes como dermatitis de estasis1,2. El mecanismo subyacente en los 2 tipos parecía ser la toxicidad directa2,8.
El estudio histológico suele ser inespecífico, aunque se han descrito cambios dismadurativos epidérmicos y siringometaplasia escamosa3.
Entre los factores de riesgo más importantes para desarrollar úlceras por metotrexato se encuentran el cambio de la dosis, el tratamiento concomitante con AINE, la insuficiencia renal, las infecciones concomitantes, los brotes de psoriasis pustulosa y la edad avanzada7. La observación de este y otros efectos adversos recuerda que el tratamiento con metotrexato requiere seguimiento prolongado incluso con dosis bajas y estables. Los medicamentos, especialmente los AINE y la insuficiencia renal, pueden potenciar su toxicidad.
Hemos aportado un nuevo caso de una úlcera cutánea secundaria a metotrexato en un paciente sin diagnóstico de psoriasis, acompañada de pancitopenia. El mecanismo patogénico parecía ser multifactorial influyendo la edad, la falta del ácido fólico, la ingesta de AINE y el deterioro de la función renal.
Conflicto de interesesLos autores declaran que no tienen ningún conflicto de intereses.