En caso de fracaso secundario del tratamiento con fármacos biológicos de la psoriasis en placas moderada a grave se puede cambiar de fármaco o intensificarlo de inicio (generalmente aumentando la frecuencia de administración). Conocer el impacto económico de ambas alternativas puede resultar de gran utilidad en la toma de decisiones terapéuticas.
ObjetivoEl presente análisis pretende orientar sobre el momento en que el sobrecoste anualizado de la intensificación supera un umbral de sobrecoste predeterminado.
Material y métodosEn función de los costes de adquisición (precio de venta de laboratorio) de los agentes biológicos aprobados para el tratamiento de la psoriasis moderada a grave se ha estimado el número de semanas que podría intensificarse el biológico de inicio hasta alcanzar un sobrecoste anualizado de 1.000€ con respecto al cambio a otro biológico para un paciente tipo de 80kg de peso.
ResultadosSegún este modelo el cambio de fármaco biológico siempre es más coste efectivo, siendo adalimumab, seguido de ustekinumab, las opciones más eficientes; en caso de intensificación ustekinumab permite una mayor duración del período de prueba (entre 2 y 4 inyecciones) antes de alcanzar el umbral de sobrecoste definido, mientras que este se alcanza al cabo de una infusión en el caso de infliximab.
ConclusiónSi bien este estudio no contempla la eficacia diferencial de las diferentes terapias biológicas como tratamiento de rescate frente a fallo secundario, por existir escasa evidencia científica al respecto, los resultados muestran importantes diferencias en el periodo de tiempo durante el cual se podría intensificar el tratamiento hasta alcanzarse el umbral de sobrecoste definido.
In the event of failure of maintenance therapy with biologic agents for moderate to severe plaque psoriasis, the possible approaches are to switch to another agent or escalate the dose (generally by increased dosing frequency). Knowledge of the economic impact of the 2 alternatives would be extremely useful for therapeutic decision making.
ObjectiveThe present analysis aimed to determine the moment in which the annualized additional cost of escalation exceeds a specified cost overrun.
Materials and methodsBased on the purchase cost (average wholesale price) of approved biologics for the treatment of moderate to severe psoriasis, the number of weeks of escalation of the initial biologic until the annualized cost of dose escalation ran €1000 over the cost of switching to another biologic was calculated for a typical patient weighing 80kg.
ResultsAccording to this model, switching to another biologic is always cost effective, with adalimumab followed by ustekinumab the best choices in this respect. Ustekinumab allows for a longer trial escalation period (2 to 4 injections) before the cost overrun threshold is reached, whereas the threshold is reached in a single infusion if a patient is on infliximab.
ConclusionThe study does not take into account the differential efficacy of the various biologic therapies as rescue treatment for failure of maintenance therapy given the lack of scientific evidence. The results nevertheless show substantial differences in the period during which treatment can be intensified before reaching the preset cost overrun.
En caso de fracaso secundario durante el tratamiento de la psoriasis en placas moderada a grave con fármacos biológicos se presenta la incertidumbre sobre cambiar a otro tratamiento o intensificar el biológico de inicio (generalmente aumentando la frecuencia de administración), práctica que si bien no se encuentra registrada en la ficha técnica, es habitual en práctica clínica y está contemplada en las fases de extensión de los ensayos clínicos y en diversas directrices1 y documentos de consenso2.
Conocer el impacto económico de las alternativas disponibles en caso de fracaso secundario al tratamiento puede resultar de gran utilidad en la toma de decisiones terapéuticas. La mayoría de los estudios económicos realizados hasta el momento no proporcionan información sobre la eficiencia de la intensificación con respecto al cambio a otro tratamiento biológico. A pesar de que la intensificación (aumento de la dosis o reducción de la frecuencia) no se encuentra registrada en la ficha técnica, su efecto ha sido evaluado en los ensayos clínicos y/o en sus fases de extensión abiertas3–7.
A la hora de determinar cuál de las 2 opciones es más eficiente, además de criterios clínicos como la causa de modificación del tratamiento (pérdida de respuesta progresiva, un brote de la enfermedad, etc.) o la probabilidad de respuesta, hay que tener en consideración el criterio económico.
El coste de la intensificación dependerá de la cuantía y duración de la misma, mientras que el coste del tratamiento con un nuevo biológico requerirá una nueva inducción y tendrá asociado un coste adicional de visitas, pruebas diagnósticas, etc. En un análisis preliminar8 se evaluó el coste incremental de la inducción con los diferentes agentes biológicos a las 16 semanas, tomando como referencia el coste promedio diario de los diferentes biológicos disponibles en la fase de mantenimiento, y considerando solo el coste de adquisición de los diversos fármacos (sin tener en cuenta posibles bonificaciones o descuentos). La estrategia de intensificación se asocia a un incremento de coste por un factor comprendido entre 1,2 (ustekinumab, acortando el intervalo entre administraciones de 12 a 10 semanas) y 2 (adalimumab, etanercept), mientras que el cambio de biológico, con la pauta de inducción, se asociaba a un incremento por un factor comprendido entre 1,18 (adalimumab) y 1,75 (etanercept) a las 16 semanas. En este primer análisis no se tuvieron en cuenta los costes asociados al cambio (directos e indirectos, tangibles e intangibles), debidos al posible mayor número de controles y determinaciones analíticas en la fase de inducción. Por otra parte, en algunos pacientes la pérdida de respuesta puede ser un fenómeno transitorio, por lo que la intensificación permitiría mantener el biológico inicial, evitando el «agotamiento» de alternativas terapéuticas.
Por este motivo en este nuevo análisis hemos establecido un valor arbitrario de 1.000€ (correspondiente aproximadamente al coste promedio de adquisición mensual de los biológicos disponibles en fase de mantenimiento según la ficha técnica, y al coste de inducción de adalimumab, que es el tratamiento biológico con menor coste de inducción: 2 inyecciones de 40mg: 1.028,29€) como límite de sobrecoste anual asumible al intensificar temporalmente el biológico frente a la alternativa del cambio, y hemos calculado los costes anualizados de las diferentes alternativas a partir del momento de la decisión clínica (con intensificación o cambio de fármaco en el momento correspondiente a la siguiente administración).
El modelo teórico empleado se aparta de la realidad clínica en diversos aspectos que no pueden de momento ser cuantificados por falta de evidencia científica. En particular, carecemos de datos referentes a la probabilidad de respuesta (basada en la mejoría del Psoriasis Area and Severity Index [PASI] o la Physician's Global Asessment [PGA]) para cada una de las posibles alternativas de intensificación o sustituciones, y desconocemos en gran medida la posible influencia del tratamiento previo sobre la posibilidad de respuesta o la retención del tratamiento con anticuerpos dirigidos contra la subunidad p40 común a la interleucina 12 (IL-12) y la IL-239 o los antagonistas del factor de necrosis tumoral alfa (anti-TNF)10.
Los datos disponibles sobre la eficacia de la intensificación o el cambio de tratamiento son muy limitados. En pacientes con fallo terapéutico primario o secundario frente a adalimumab se ha propuesto aumentar la dosis de este fármaco a 40mg/semana, lo que permite o bien alcanzar la respuesta PASI 75 o bien reducir esta dosis a la habitual (40mg cada 15 días) en el 27% de los pacientes a las 12 semanas y en el 38% a las 24 semanas4. Los pacientes con mayor probabilidad de respuesta (48%) a la intensificación de la dosis son los que presentan un fallo terapéutico secundario, con relativamente bajo peso y enfermedad de corta evolución. En una cohorte observacional prospectiva de pacientes con fallo terapéutico a adalimumab en los que se intensificó la dosis el 25% de los pacientes alcanzó una respuesta PASI 50 a las 12 semanas y el 35% a las 24 semanas, mientras que los porcentajes correspondientes al resultado del tratamiento combinado con metotrexato sin aumentar la dosis fueron del 9 y 18%, respectivamente11.
La evidencia científica actualmente disponible es insuficiente para establecer ninguna preferencia cuando se plantea el empleo de un biológico como segunda línea terapéutica en pacientes con fracaso primario o secundario a un tratamiento previo con otro agente biológico. Se ha demostrado que en pacientes con fallo primario o secundario tras 3-6 meses de tratamiento con etanercept se consigue alcanzar una respuesta PGA<2 en el 49% de los tratados con adalimumab durante 16 semanas12 y en el 65% de los tratados con infliximab durante 10 semanas13, mientras que un 49% de los pacientes tratados con ustekinumab 90mg consiguieron una respuesta PASI 75 a las 12 semanas de la sustitución de etanercept por ustekinumab14. También existen series de casos que indican buena respuesta (no cuantificada) tras el cambio de infliximab a etanercept15 o de anti-TNF a ustekinumab16. Se ha sugerido que la respuesta en pacientes previamente tratados con biológicos es algo inferior en el caso de etanercept, ustekinumab y adalimumab, mientras que la respuesta a infliximab no depende de la exposición previa a otro biológico17.
Por otra parte, por razones de simplificación hemos asumido que en todos los casos la retención del tratamiento después del cambio o la intensificación temporal será del 100% a un año, sin tener en cuenta la posibilidad de un nuevo fracaso terapéutico (fallo primario o secundario). Esta aproximación deja de lado la eficacia y asume que tanto tras la intensificación como tras el cambio de tratamiento los pacientes responden, por lo que el presente estudio representa un análisis de minimización de costes.
A continuación se presentan los resultados de un análisis comparativo del sobrecoste anualizado de la intensificación temporal frente al cambio a otro biológico a la dosis estándar en caso de fracaso secundario (en la fase de mantenimiento) del primer biológico.
Material y métodosSe han efectuado diversas simulaciones mediante hoja de cálculo Excel del coste anual del tratamiento a partir del momento en que se intensifica el primer biológico o se sustituye por otro fármaco, teniendo en cuenta las pautas habituales de tratamiento de la psoriasis moderada a grave con agentes biológicos (adalimumab, etanercept, infliximab, ustekinumab) y los costes de adquisición (precio de venta de laboratorio) de cada uno de ellos en España en junio de 201318.
En el caso de infliximab el coste depende directamente del peso del paciente debido a la pauta posológica en función del mismo (5mg/kg), y debe tenerse asimismo en cuenta la habitual optimización de viales, cuyas fracciones se reparten entre varios pacientes. Con fines de simplificación se han calculado únicamente los costes para un paciente con un peso de 80kg (4 viales). Para este análisis se han incluido los costes publicados asociados a la infusión IV de infliximab en hospital de día en nuestro medio (247,50€)19.
El coste del cambio de biológico se ha estimado teniendo en consideración el coste de la inducción, en función de las recomendaciones registradas en la ficha técnica. En el caso de etanercept se ha considerado la dosis de inducción de 50mg 2 veces por semana durante un periodo de 12 semanas, por ser la pauta más común en la práctica clínica.
Los costes anualizados (precio de venta de laboratorio más coste de la infusión en el caso de infliximab, prorrateando la última dosis anual al intervalo de semanas restante hasta la semana 52) de inducción y mantenimiento para cada uno de los biológicos disponibles, administrados en múltiplos de semanas son: adalimumab, 13.602€ (27,5 inyecciones) frente a 12.860€ (26 inyecciones); etanercept, 14.580€ (64 inyecciones) frente a 11.846€ (52 inyecciones); infliximab, 17.911€ (7,75 infusiones de 4 viales) frente a 15.022€ (6,5 infusiones) y ustekinumab 14.681€ (5 inyecciones) frente a 12.724€ (4,33 inyecciones).
En el caso de los biológicos con una pauta posológica recomendada según la ficha técnica, con frecuencias múltiplo de 4 semanas (ustekinumab e infliximab), se ha observado que en la práctica es muy frecuente que se administren en múltiplos de meses, lo que desde el punto de vista económico tiene un impacto significativo (un año tiene 12 meses y 52 semanas, por lo que la administración por meses implica un ahorro de un 7,7% anual). Aunque no se ha incluido en los cálculos hay que tener en cuenta que en el caso de adalimumab también es frecuente administrarlo 2 veces al mes, lo que implicaría el mismo porcentaje de ahorro (2 inyecciones de 26) sobre los costes calculados de adquisición. Al igual que la intensificación, la administración en múltiplos de meses tampoco está recomendada en la ficha técnica pero se realiza en la práctica clínica habitual, por lo que el presente análisis de la eficiencia de la intensificación frente al cambio se ha realizado contemplando ambas posibilidades con objeto de reflejar lo que sucede en la realidad clínica cotidiana.
No se ha estudiado si tras la intensificación los pacientes mantienen una respuesta óptima al retornar a la dosis normal, por lo que no es posible determinar un número fijo de semanas tras las cuales el paciente volvería a la dosis recomendada en la ficha técnica. La intensificación, manteniendo el fármaco, puede tener ventajas que justifiquen un sobrecoste de unos 1.000€ (el coste aproximado de un mes de mantenimiento con cualquier fármaco biológico), y en este modelo 1.000€ es el «umbral de sobrecoste anualizado asumible» si se desea evitar el cambio de agente terapéutico.
Por lo general, resulta más caro intensificar la dosis del fármaco biológico que sustituirlo por otro: la intensificación, mientras dura, implica generalmente un incremento del coste del 100% en el caso de adalimumab y etanercept, un 33,3% en el caso de infliximab y entre un 20 y un 33,3% en el caso de ustekinumab, mientras que el sobrecoste anualizado de la inducción con respecto al mantenimiento es de aproximadamente un 5,8% en el caso de adalimumab (27,5 inyecciones frente a 26 en 52 semanas), un 15,4% en el caso de adalimumab (27,5 frente a 26 inyecciones), un 19,2% en el caso de infliximab (7,75 frente a 6,5 infusiones) y un 23,1% en el caso de etanercept a la dosis de 50mg 2 veces por semana (64 frente a 52 inyecciones en 52 semanas).
En este modelo se ha calculado el número de semanas que se podría intensificar hasta alcanzar un sobrecoste de 1.000€ con respecto al cambio de biológico, asumiendo que a partir de entonces sería posible volver a la dosis según la ficha técnica; prolongando la primera parte de las líneas de intensificación en los correspondientes gráficos puede estimarse el sobrecoste de mantener la intensificación.
ResultadosLos resultados se presentan en forma de tablas y figuras para cada fármaco biológico.
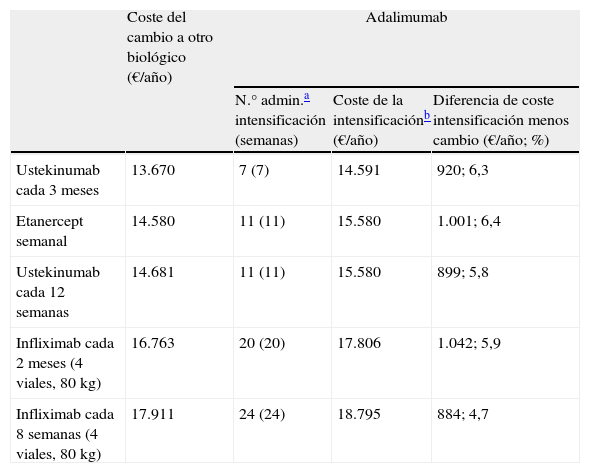
Intensificación de adalimumab frente a cambio a otro biológico (tabla 1)En caso de fracaso secundario durante el tratamiento con adalimumab 40mg cada 2 semanas en mantenimiento, las alternativas de cambio con un coste de aproximadamente 1.000€/año inferior a la intensificación serían, por orden decreciente de eficiencia (coste anualizado creciente):
- 1.
Cambio a ustekinumab cada 3 meses: a partir de la 8.a administración de adalimumab semanal.
- 2.
Cambio a etanercept semanal o ustekinumab cada 12 semanas: en ambos casos, a partir de la 12.a administración. En este caso, la diferencia entre ambos sería mínima (102€/año) por lo que habría que considerar otros factores como una diferente probabilidad de respuesta en el caso de ustekinumab al presentar una diana terapéutica diferente (IL-12/23), la frecuencia de administración (ustekinumab cada 12 semanas frente a etanercept semanal), etc.
- 3.
Cambio a infliximab: a partir de la semana 25.a si en la fase de mantenimiento se administran las infusiones cada 8 semanas, o la 21.a administración si se administra cada 2 meses.
Intensificación de adalimumab (semanal) frente a cambio a otro biológico
| Coste del cambio a otro biológico (€/año) | Adalimumab | |||
| N.° admin.a intensificación (semanas) | Coste de la intensificaciónb (€/año) | Diferencia de coste intensificación menos cambio (€/año; %) | ||
| Ustekinumab cada 3 meses | 13.670 | 7 (7) | 14.591 | 920; 6,3 |
| Etanercept semanal | 14.580 | 11 (11) | 15.580 | 1.001; 6,4 |
| Ustekinumab cada 12 semanas | 14.681 | 11 (11) | 15.580 | 899; 5,8 |
| Infliximab cada 2 meses (4 viales, 80kg) | 16.763 | 20 (20) | 17.806 | 1.042; 5,9 |
| Infliximab cada 8 semanas (4 viales, 80kg) | 17.911 | 24 (24) | 18.795 | 884; 4,7 |
N.° de administraciones que se podría intensificar hasta una diferencia lo más cercana posible a 1.000€/año entre coste de intensificación y coste del cambio a otro biológico.
Coste de la intensificación con el biológico para la duración correspondiente al número de administraciones de la columna 3, expresado en €/año. Este valor incluye el coste correspondiente a las semanas en intensificación, reflejadas en la columna 3, y el coste en mantenimiento correspondiente a las semanas restantes hasta completar el año de tratamiento.
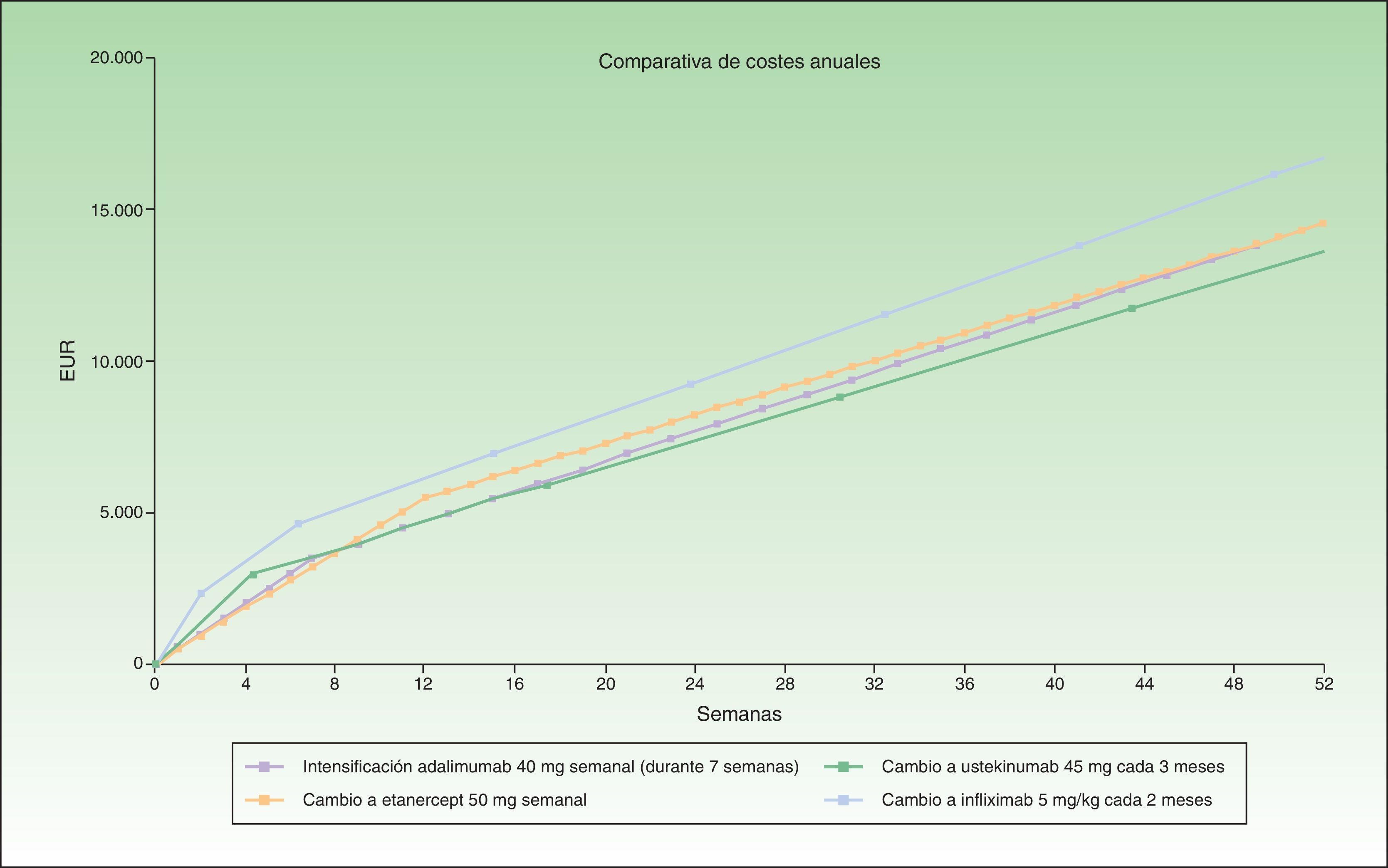
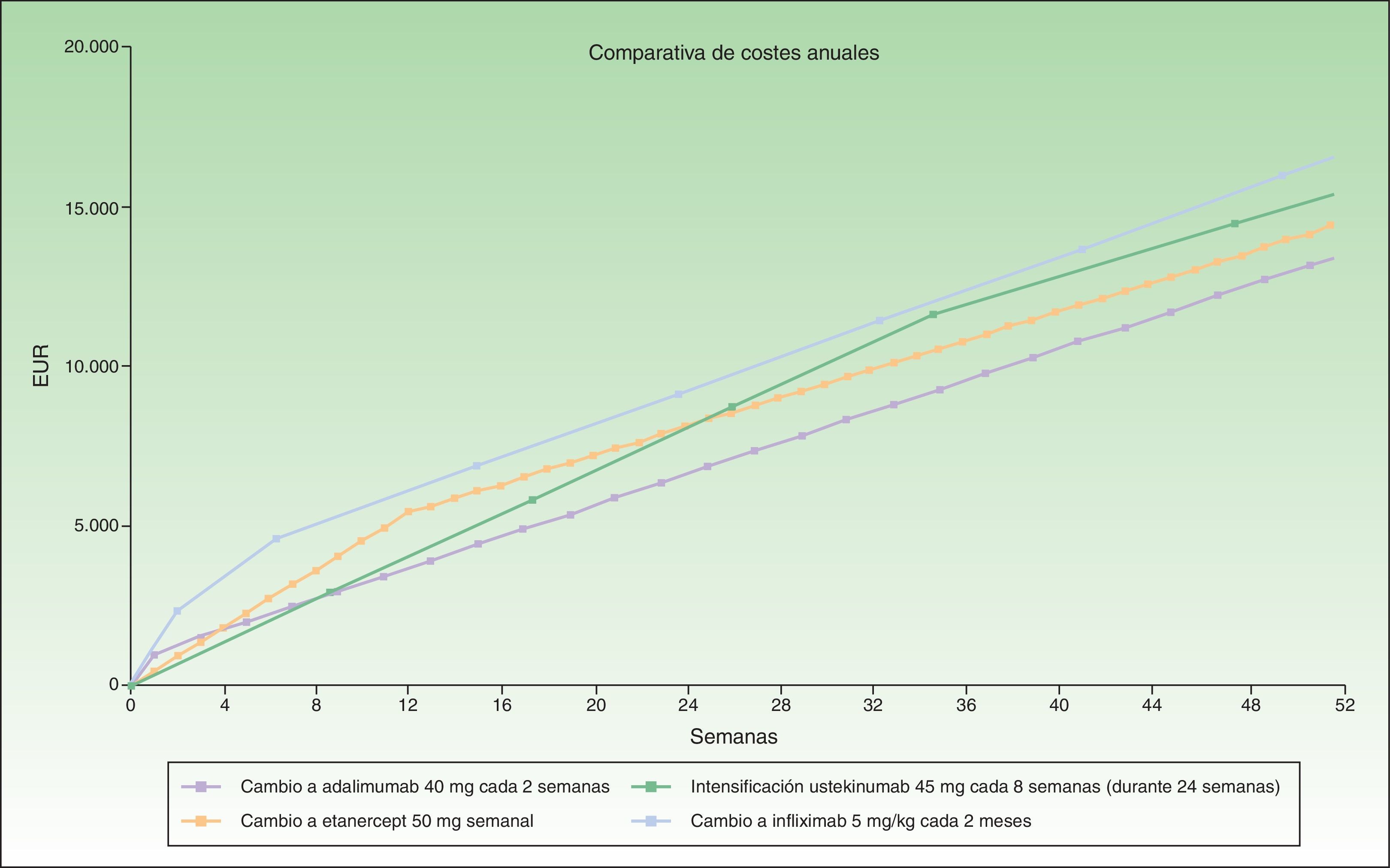
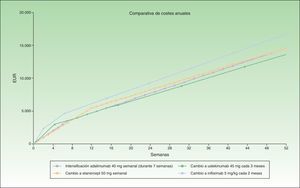
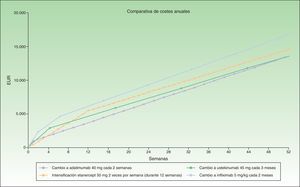
Durante las primeras 8 semanas el coste del cambio a ustekinumab es superior al de la intensificación de adalimumab o al cambio a etanercept, para acabar al final del primer año igualándose con el coste de etanercept en el caso de ustekinumab administrado cada 12 semanas, o siendo inferior al coste de etanercept en el caso de ustekinumab administrado cada 3 meses (fig. 1). El cambio a ustekinumab cada 3 meses sería la alternativa más eficiente después de 7 semanas de intensificación. A continuación la alternativa más eficiente sería el cambio a ustekinumab cada 12 semanas o etanercept, con un coste similar. Incluso asumiendo que no hubiera diferencias de eficacia en pacientes con fallo secundario a un anti-TNF, etanercept tendría el inconveniente relativo de una mayor frecuencia de administración. Por último, la alternativa de cambio a infliximab sería la menos eficiente.
En la figura 1 se ha representado el coste correspondiente a intensificar adalimumab durante 7 semanas en comparación con el coste del cambio a otro biológico, considerándose el coste de cambio a infliximab y ustekinumab con una pauta mensual en mantenimiento. Se observa cómo en este caso el coste anualizado (a las 52 semanas) es menor para ustekinumab (13.670€), seguido de etanercept (14.580€), adalimumab (14.591€) e infliximab (16.763€).
Intensificación de etanercept frente a cambio a otro biológico (tabla 2)- 1.
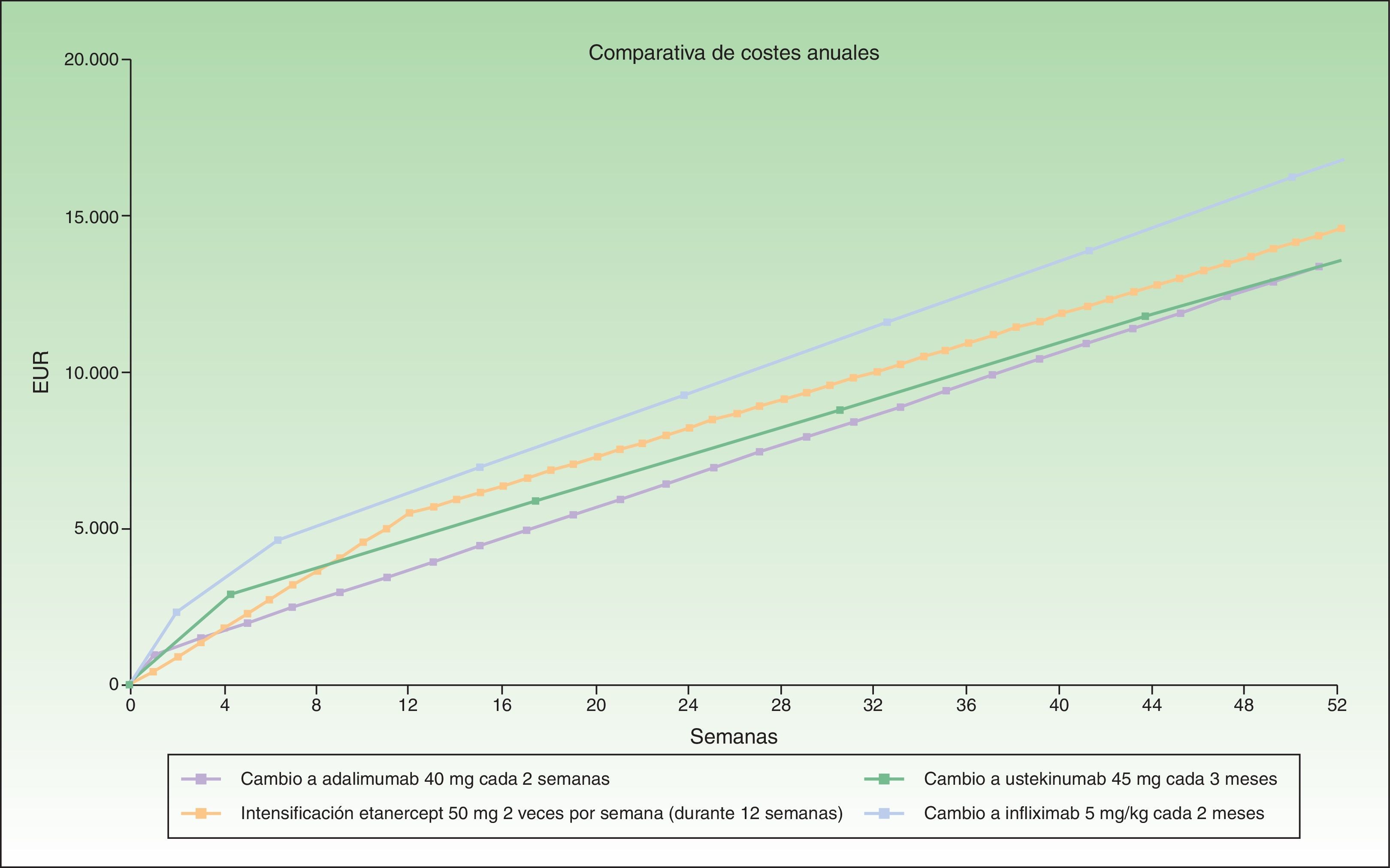
En caso de fracaso secundario durante el tratamiento con etanercept 50mg semanal en mantenimiento, la intensificación a etanercept 50mg 2 veces por semana durante un periodo de hasta 12 semanas (12×2 unidades administradas) sería una alternativa con un sobrecoste aceptable (≈1.000€/año) con respecto al cambio a otro biológico (tabla 2 y fig. 2). Las alternativas de cambio serían, por orden decreciente de eficiencia: cambio a adalimumab cada 2 semanas o ustekinumab cada 3 meses a partir de la 13.a semana. La diferencia entre ambas opciones sería mínima (68€/año), por lo que habría que considerar otros factores tales como una mayor probabilidad de respuesta en el caso de ustekinumab al tratarse de una diferente diana terapéutica (IL-12/23), diferente frecuencia de administración (ustekinumab cada 3 meses vs adalimumab cada 2 semanas), diferente coste en la fase de mantenimiento (ustekinumab cada 3 meses, 11.745€/año frente a adalimumab cada 2 semanas, 12.860€/año), etc.
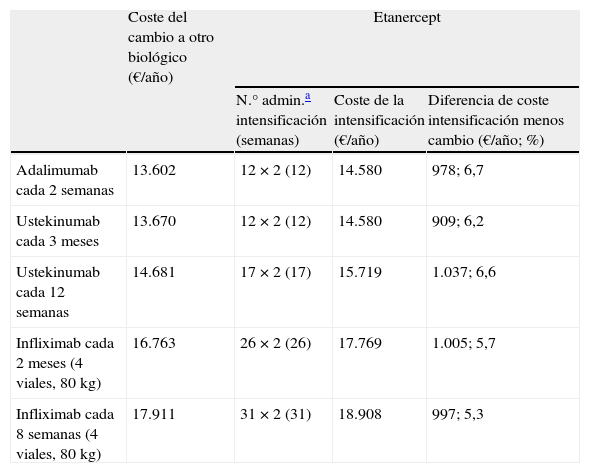
Tabla 2.Intensificación de etanercept (50mg 2 veces por semana) frente a cambio a otro biológico
Coste del cambio a otro biológico (€/año) Etanercept N.° admin.a intensificación (semanas) Coste de la intensificación (€/año) Diferencia de coste intensificación menos cambio (€/año; %) Adalimumab cada 2 semanas 13.602 12×2 (12) 14.580 978; 6,7 Ustekinumab cada 3 meses 13.670 12×2 (12) 14.580 909; 6,2 Ustekinumab cada 12 semanas 14.681 17×2 (17) 15.719 1.037; 6,6 Infliximab cada 2 meses (4 viales, 80kg) 16.763 26×2 (26) 17.769 1.005; 5,7 Infliximab cada 8 semanas (4 viales, 80kg) 17.911 31×2 (31) 18.908 997; 5,3 - 2.
Cambio a ustekinumab cada 12 semanas: a partir de la 18.a semana.
- 3.
Cambio a infliximab: a partir de la 32.a semana si se administra cada 8 semanas, o la 27.a semana si se administra cada 2 meses.
Así pues, el cambio a adalimumab o a ustekinumab administrado cada 3 meses serían las alternativas más eficientes después de 12 semanas de intensificación, seguido de ustekinumab cada 12 semanas e infliximab.
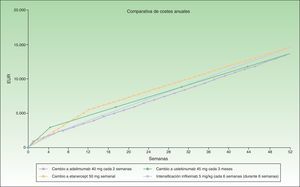
En la figura 2 se ha representado el coste correspondiente a intensificar etanercept durante 12 semanas en comparación con el coste del cambio a otro biológico, considerándose el coste de cambio a infliximab y ustekinumab con una posología mensual en mantenimiento. Se observa un menor coste anual de adalimumab (13.602€), seguido de ustekinumab (13.670€), etanercept (14.580€) e infliximab (16.763€).
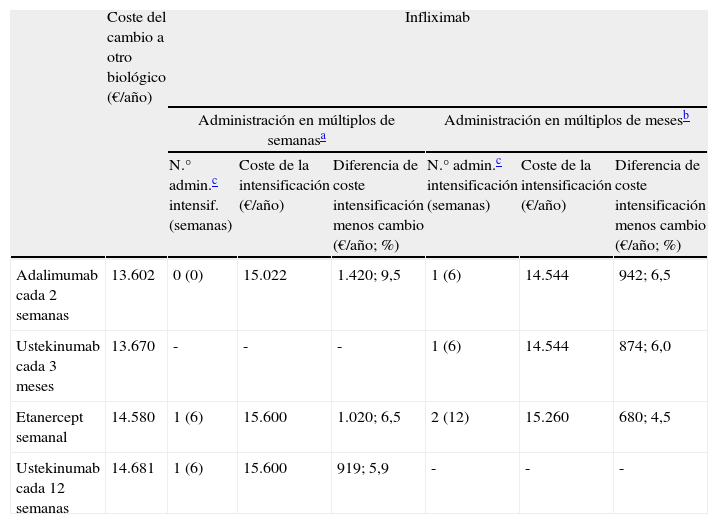
Intensificación de infliximab frente a cambio a otro biológico (tabla 3)Se presenta la intensificación de infliximab cada 6 semanas, incorporando la posibilidad de que la administración se realice en múltiplos de semanas o en múltiplos de meses durante el mantenimiento.
Intensificación de infliximab (cada 6 semanas) frente a cambio a otro biológico
| Coste del cambio a otro biológico (€/año) | Infliximab | ||||||
| Administración en múltiplos de semanasa | Administración en múltiplos de mesesb | ||||||
| N.° admin.c intensif. (semanas) | Coste de la intensificación (€/año) | Diferencia de coste intensificación menos cambio (€/año; %) | N.° admin.c intensificación (semanas) | Coste de la intensificación (€/año) | Diferencia de coste intensificación menos cambio (€/año; %) | ||
| Adalimumab cada 2 semanas | 13.602 | 0 (0) | 15.022 | 1.420; 9,5 | 1 (6) | 14.544 | 942; 6,5 |
| Ustekinumab cada 3 meses | 13.670 | - | - | - | 1 (6) | 14.544 | 874; 6,0 |
| Etanercept semanal | 14.580 | 1 (6) | 15.600 | 1.020; 6,5 | 2 (12) | 15.260 | 680; 4,5 |
| Ustekinumab cada 12 semanas | 14.681 | 1 (6) | 15.600 | 919; 5,9 | - | - | - |
Infliximab administrado cada 8 semanas en mantenimiento, antes y después de la intensificación; ustekinumab administrado cada 12 semanas en mantenimiento.
En caso de fracaso secundario durante el tratamiento con infliximab en mantenimiento cada 8 semanas (tabla 3 y fig. 3) las alternativas de cambio serían, por orden de eficiencia:
- 1.
Cambio a adalimumab cada 2 semanas: sería recomendable realizar el cambio antes de comenzar con la intensificación, puesto que desde el primer momento se alcanza la diferencia de coste propuesta de 1.000€/año.
- 2.
Cambio a etanercept semanal o a ustekinumab cada 12 semanas: a partir de la 2.a administración. En este caso la diferencia entre ambos sería mínima (101€/año) por lo que habría que considerar otros factores.
Si la administración se realiza en múltiplos de meses (infliximab administrado cada 2 meses y ustekinumab cada 3 meses en mantenimiento), este periodo de intensificación a infliximab cada 6 semanas sería de 6 semanas (una administración), y a partir de entonces las alternativas de cambio más eficientes serían, en este orden:
- 1.
Cambio a adalimumab cada 2 semanas o a ustekinumab cada 3 meses: a partir de la 2.a administración. En este caso la diferencia entre ambos sería mínima (68€/año), por lo que habría que considerar la conveniencia de la diferente frecuencia de administración, diferencias en el coste de mantenimiento, etc.
- 2.
Cambio a etanercept semanal: a partir de la 3.a administración.
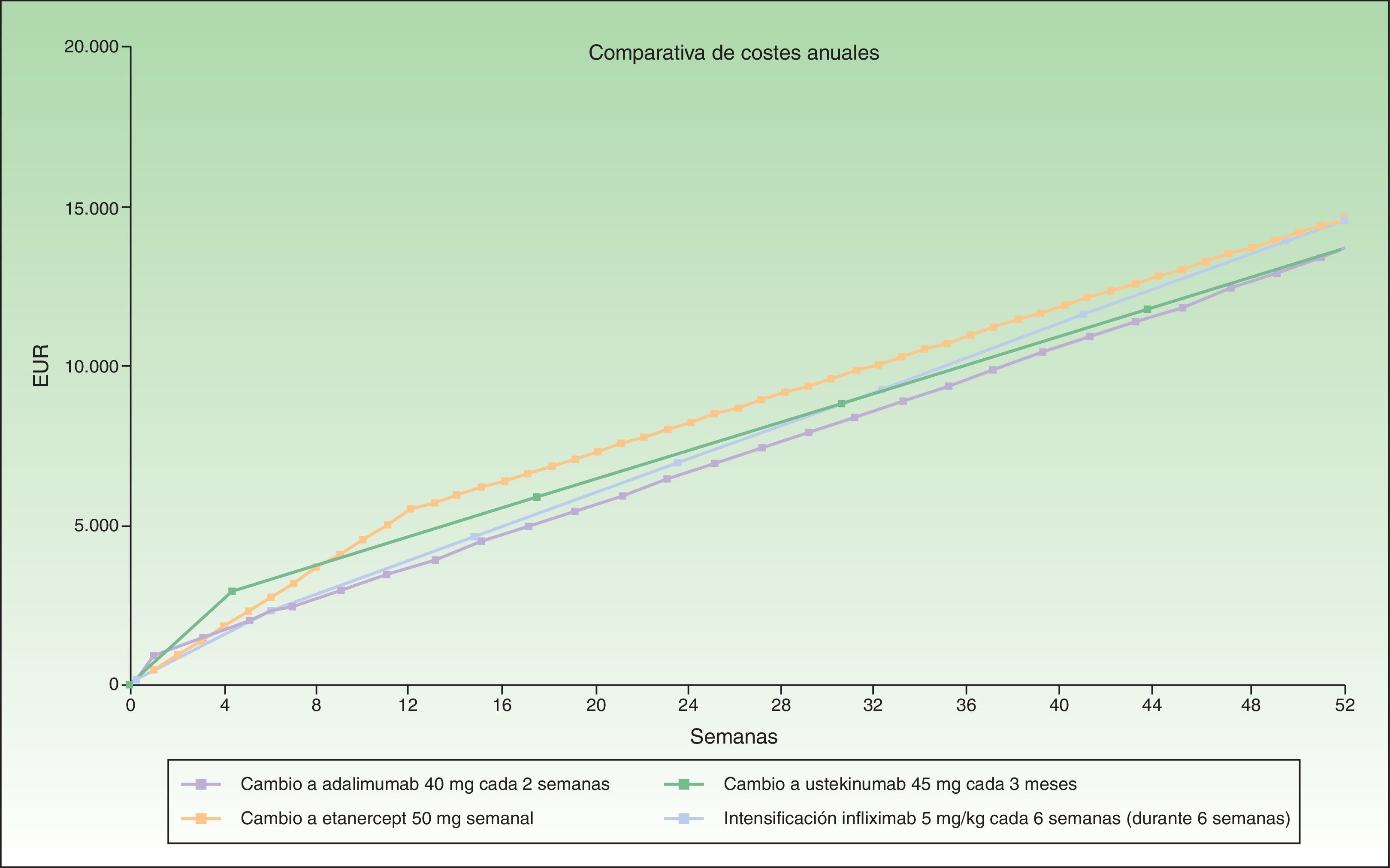
El cambio a adalimumab sería la alternativa más eficiente antes de iniciar la intensificación cada 6 semanas, seguido de ustekinumab y por último etanercept. En caso de administraciones en múltiplo de meses el cambio a adalimumab o ustekinumab cada 3 meses serían las alternativas más eficientes, aunque el sobrecoste anualizado de una administración de infliximab en intensificación cada 6 semanas no alcanza los 1.000€.
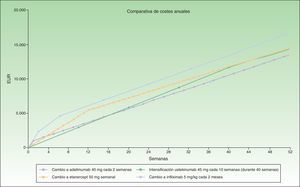
En la figura 3 se ha representado el coste correspondiente a intensificar infliximab durante 6 semanas en comparación con el coste del cambio a otro biológico, considerándose una posología en mantenimiento en múltiplos de meses para infliximab y ustekinumab. Se observa que el coste anualizado es menor para adalimumab (13.602€), seguido de ustekinumab (13.670€), infliximab (14.544€) y etanercept (14.580€).
Intensificación de ustekinumab frente a cambio a otro biológico (tablas 4 y 5)Se presentan 2 escenarios posibles de intensificación; ustekinumab cada 10 semanas y cada 8 semanas. A su vez, estos escenarios contemplan la administración en múltiplos de semanas (según ficha técnica) y la administración en múltiplos de meses, puesto que como se ha apuntado anteriormente en la práctica clínica habitual es cada vez más frecuente.
Intensificación de ustekinumab (cada 10 semanas) frente a cambio a otro biológico
| Coste del cambio a otro biológico (€/año) | Ustekinumab | ||||||
| Administración en múltiplos de semanasa | Administración en múltiplos de mesesb | ||||||
| N.° admin.c intensif. (semanas) | Coste de la intensificación (€/año) | Diferencia de coste intensificación menos cambio (€/año; %) | N.° admin.c intensif. (semanas) | Coste de la intensificación (€/año) | Diferencia de coste intensificación menos cambio (€/año; %) | ||
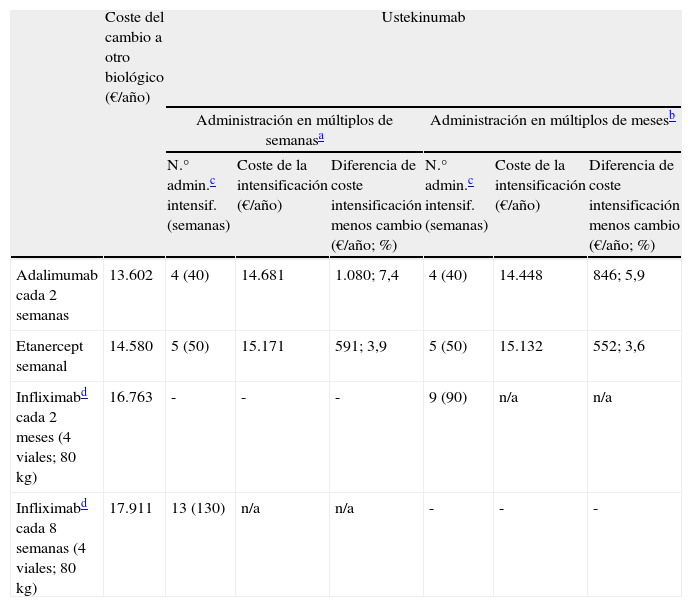
| Adalimumab cada 2 semanas | 13.602 | 4 (40) | 14.681 | 1.080; 7,4 | 4 (40) | 14.448 | 846; 5,9 |
| Etanercept semanal | 14.580 | 5 (50) | 15.171 | 591; 3,9 | 5 (50) | 15.132 | 552; 3,6 |
| Infliximabd cada 2 meses (4 viales; 80kg) | 16.763 | - | - | - | 9 (90) | n/a | n/a |
| Infliximabd cada 8 semanas (4 viales; 80kg) | 17.911 | 13 (130) | n/a | n/a | - | - | - |
Ustekinumab administrado cada 12 semanas en mantenimiento, antes y después de la intensificación; infliximab administrado cada 8 semanas en mantenimiento.
Ustekinumab administrado cada 3 meses en mantenimiento, antes y después de la intensificación; infliximab administrado cada 2 meses en mantenimiento.
Intensificación de ustekinumab (cada 8 semanas) frente a cambio a otro biológico
| Coste del cambio a otro biológico (€/año) | Ustekinumab | ||||||
| Administración en múltiplos de semanasa | Administración en múltiplos de mesesb | ||||||
| N.° admin.c intensif. (semanas) | Coste de la intensificación (€/año) | Dif. coste intensificación menos cambio (€/año; %) | N.° admin.c intensif. (semanas) | Coste de la intensif. (€/año) | Diferencia coste intensificación menos cambio (€/año; %) | ||
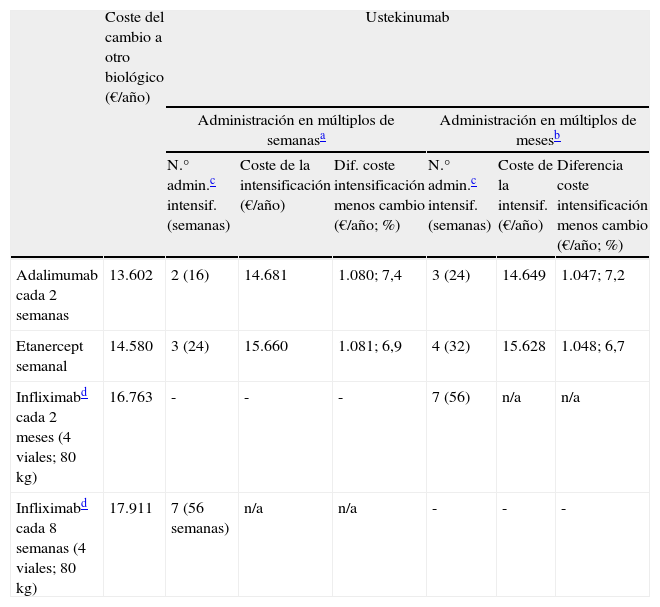
| Adalimumab cada 2 semanas | 13.602 | 2 (16) | 14.681 | 1.080; 7,4 | 3 (24) | 14.649 | 1.047; 7,2 |
| Etanercept semanal | 14.580 | 3 (24) | 15.660 | 1.081; 6,9 | 4 (32) | 15.628 | 1.048; 6,7 |
| Infliximabd cada 2 meses (4 viales; 80kg) | 16.763 | - | - | - | 7 (56) | n/a | n/a |
| Infliximabd cada 8 semanas (4 viales; 80kg) | 17.911 | 7 (56 semanas) | n/a | n/a | - | - | - |
Ustekinumab administrado cada 12 semanas en mantenimiento, antes y después de la intensificación; infliximab administrado cada 8 semanas en mantenimiento.
Ustekinumab administrado cada 3 meses en mantenimiento, antes y después de la intensificación; ustekinumab administrado cada 2 meses en intensificación; infliximab administrado cada 2 meses en mantenimiento.
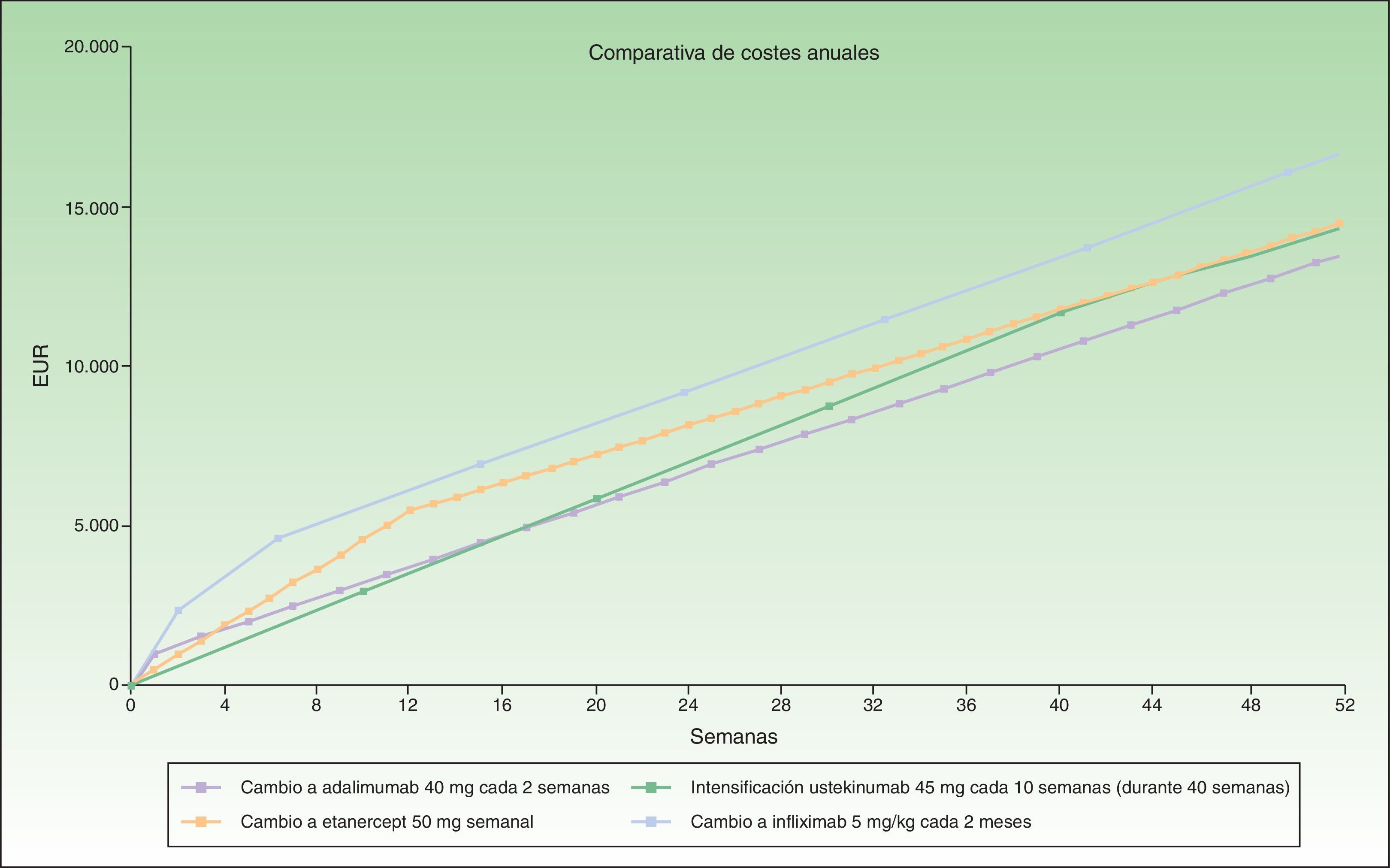
En caso de fracaso secundario durante el tratamiento con ustekinumab en mantenimiento, la intensificación a ustekinumab cada 10 semanas durante un periodo de 40 semanas (4 administraciones) sería una alternativa con un sobrecoste similar (una diferencia de unos 1.000€ al año) al cambio a otro biológico (tabla 4 y fig. 4). Las alternativas de cambio serían, por orden de eficiencia:
- 1.
Cambio a adalimumab cada 2 semanas: a partir de la 5.a administración.
- 2.
Cambio a etanercept semanal: a partir de la 6.a administración.
- 3.
Cambio a infliximab: la intensificación a ustekinumab cada 10 semanas podría prolongarse durante un periodo de más de un año, sin que la diferencia con respecto al cambio llegase a los 1.000€/año.
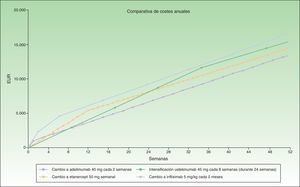
En la figura 4 se ha representado el coste correspondiente a intensificar ustekinumab durante 10 semanas en comparación con el coste del cambio a otro biológico, considerándose una posología en mantenimiento en múltiplos de meses para infliximab y ustekinumab. Se observa que el coste anualizado es menor para adalimumab (13.602€), seguido de ustekinumab (14.448€), etanercept (14.580€) e infliximab (16.763€).
Intensificación a ustekinumab cada 8 semanas (tabla 5)En caso de fracaso secundario durante el tratamiento con ustekinumab en mantenimiento cada 12 semanas la intensificación a ustekinumab cada 8 semanas durante un periodo de 16 semanas (2 administraciones) alcanzaría el umbral de sobrecoste de 1.000€ con respecto al cambio a otro biológico (tabla 4). Si la administración de ustekinumab en mantenimiento fuese cada 3 meses este periodo sería de 24 semanas (3 administraciones) (fig. 5). Las alternativas de cambio, por orden decreciente de eficiencia, serían:
- 1.
Cambio a adalimumab cada 2 semanas: a partir de la 3.a administración (a partir de la 4.a administración si la administración de ustekinumab en mantenimiento fuese cada 3 meses).
- 2.
Cambio a etanercept semanal: a partir de la 4.a administración (a partir de la 5.a administración si la administración de ustekinumab en mantenimiento fuese cada 3 meses).
- 3.
Cambio a infliximab: la intensificación a ustekinumab cada 8 semanas podría prolongarse durante un periodo de más de un año, sin que la diferencia llegase a los 1.000€/año.
En conclusión, en pacientes con fallo a ustekinumab el cambio a adalimumab después de 4 administraciones de intensificación cada 10 semanas sería la alternativa más próxima al umbral de sobrecoste de 1.000€/año. Si se intensifica cada 8 semanas o 2 meses,el cambio a adalimumab sería más eficiente tras 2 o 3 administraciones, según se administre en múltiplo de semanas o meses, seguido de etanercept y por último infliximab.
DiscusiónEl análisis que se presenta pretende dar una orientación sobre el momento en el que las diferentes pautas de intensificación alcanzarían el umbral de sobrecoste anualizado de 1.000€ con respecto al cambio a otro biológico para un paciente tipo de 80kg, teniendo en cuenta solo el coste de adquisición (e infusión en el caso de infliximab). Asimismo, permite disponer de información sobre un posible orden de eficiencia, asumiendo que la probabilidad de respuesta terapéutica tras el cambio de agente biológico fuera independiente de los fármacos implicados.
Es importante mencionar la limitación que supone asumir que todos los pacientes responden a la intensificación o al cambio a otro fármaco biológico tras fracaso secundario al tratamiento de inicio. Sin embargo, debido a la ausencia de información científica respecto a la eficacia de los tratamientos biológicos tras el cambio de tratamiento y/o la intensificación del mismo, se ha incorporado el análisis de eficiencia en este estudio asumiendo que todos los pacientes responden a ambas opciones.
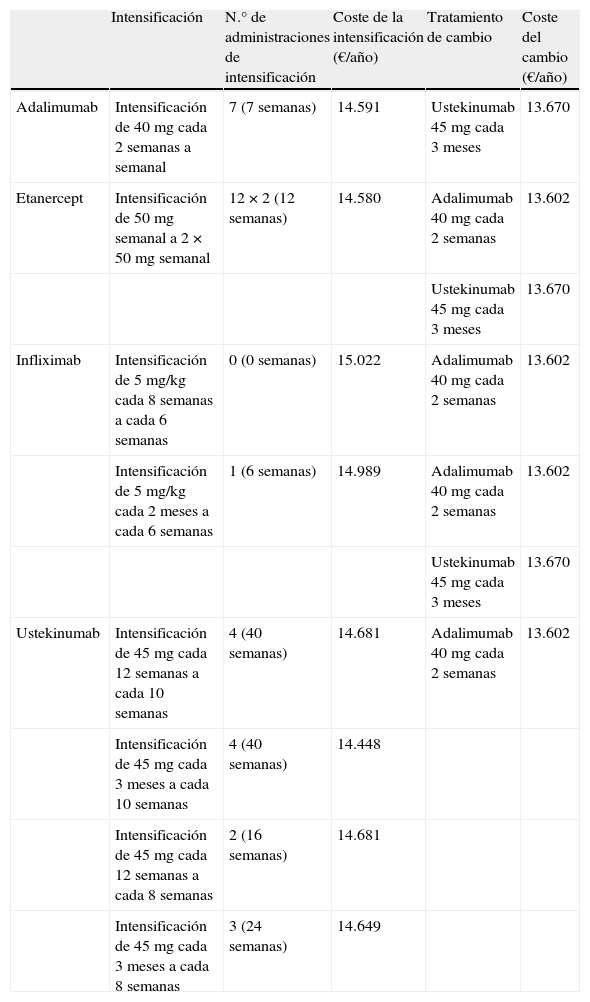
En la tabla 6 se recoge la información referente al número máximo de semanas durante las que podría ser eficiente la intensificación (hasta el momento en el que se alcanza el umbral de sobrecoste de unos 1.000€/año), así como la opción de cambio más eficiente.
Resumen de intensificación frente a cambio a otro biológico
| Intensificación | N.° de administraciones de intensificación | Coste de la intensificación (€/año) | Tratamiento de cambio | Coste del cambio (€/año) | |
| Adalimumab | Intensificación de 40mg cada 2 semanas a semanal | 7 (7 semanas) | 14.591 | Ustekinumab 45mg cada 3 meses | 13.670 |
| Etanercept | Intensificación de 50mg semanal a 2×50mg semanal | 12×2 (12 semanas) | 14.580 | Adalimumab 40mg cada 2 semanas | 13.602 |
| Ustekinumab 45mg cada 3 meses | 13.670 | ||||
| Infliximab | Intensificación de 5mg/kg cada 8 semanas a cada 6 semanas | 0 (0 semanas) | 15.022 | Adalimumab 40mg cada 2 semanas | 13.602 |
| Intensificación de 5mg/kg cada 2 meses a cada 6 semanas | 1 (6 semanas) | 14.989 | Adalimumab 40mg cada 2 semanas | 13.602 | |
| Ustekinumab 45mg cada 3 meses | 13.670 | ||||
| Ustekinumab | Intensificación de 45mg cada 12 semanas a cada 10 semanas | 4 (40 semanas) | 14.681 | Adalimumab 40mg cada 2 semanas | 13.602 |
| Intensificación de 45mg cada 3 meses a cada 10 semanas | 4 (40 semanas) | 14.448 | |||
| Intensificación de 45mg cada 12 semanas a cada 8 semanas | 2 (16 semanas) | 14.681 | |||
| Intensificación de 45mg cada 3 meses a cada 8 semanas | 3 (24 semanas) | 14.649 |
Debido a la diferente frecuencia de administración los fármacos biológicos presentan importantes diferencias en cuanto a las posibilidades de intensificación y al número de semanas que podrían intensificarse hasta alcanzar el umbral fijado para el cambio (sobrecoste de 1.000€/año), asumiendo que la respuesta a la intensificación fuera adecuada en todos los casos y similar a la del cambio. Ustekinumab podría intensificarse durante 40 semanas hasta alcanzar el umbral predefinido, etanercept 12, adalimumab 7, y finalmente infliximab es el fármaco menos susceptible de intensificación como consecuencia del sobrecoste, al alcanzarse el umbral de 1.000€/año entre las semanas 0 y 6.
En general, en caso de cambio a otro biológico las alternativas con menor sobrecoste anualizado serían adalimumab y/o ustekinumab (dependiendo del biológico sustituido).
Se requieren estudios adicionales que permitan evaluar la eficacia diferencial de los diferentes biológicos empleados como tratamiento de rescate en caso de fracaso primario o secundario de otro biológico. En este sentido, deberán tenerse en cuenta otras consideraciones, como el papel del desarrollo de anticuerpos antifármaco, que confieren cierta especificidad de fármaco al fracaso, o aspectos farmacocinéticos1. En este sentido cabe destacar que en el modelo empleado no se ha tenido en cuenta el sobrecoste relacionado con la dosificación basada en el peso de infliximab o ustekinumab, ni las diferencias de eficacia de algunos fármacos biológicos en relación con el peso del paciente20.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLluis Puig ha participado en ensayos clínicos patrocinados por Abbvie, Amgen, Lilly, Merck, Novartis, Pfizer España y VBL y ha recibido honorarios por ejercer como asesor y participar como ponente en actividades patrocinadas por Abbvie, Merck, Janssen, Merck, Novartis y Pzifer.