INTRODUCCION
El fenómeno de Raynaud fue descrito por primera vez en 1862 por Maurice Raynaud1, tras la observación de 25 pacientes que presentaban dolor y cambios en la coloración en las extremidades distales relacionados con el frío. El fenómeno de Raynaud se puede dar de forma aislada (fenómeno de Raynaud primario o enfermedad de Raynaud) o asociado a otras enfermedades (fenómeno de Raynaud secundario), sobre todo colagenosis. Una de las manifestaciones más incapacitantes del fenómeno de Raynaud es el dolor. Para su tratamiento, la primera opción es el uso de ropa de abrigo, evitar el frío y dejar de fumar. Si esto no es suficiente se pueden usar diferentes tratamientos farmacológicos como los antagonistas del calcio o los análogos de las prostaglandinas2. Sin embargo, hay pacientes que tampoco responden y en éstos se pueden probar otros tratamientos más agresivos como la simpatectomía o la electroestimulación medular (EEM).
El uso de la EEM se basa en la teoría de la doble puerta de control del dolor formulada por Melzack y Wall en 19653. Según esta teoría, los estímulos nerviosos dolorosos que se transmiten por fibras amielínicas modulan en parte su transmisión por la estimulación de fibras nerviosas mielínicas aferentes que transmiten estímulos propioceptivos. Basándose en esta teoría, Wall y Sweet4 y Shealy5 usaron la EEM para el tratamiento de pacientes con dolor crónico. En 1976, Cook et al6 emplearon la EEM en pacientes con dolor de tipo isquémico, pero hasta 1982 Augustinsson7 no planteó su utilidad en pacientes con vasospasmo. Desde ese momento se han publicado casos aislados8-10 y series de casos11-13 en las que se ha usado esta técnica para el tratamiento del fenómeno de Raynaud.
En el Hospital General Universitario de Valencia, desde el año 1993 está en marcha un protocolo para el tratamiento de enfermos con fenómeno de Raynaud resistente a tratamiento médico (nifedipino, ácido acetilsalicílico o pentoxifilina) y quirúrgico (simpatectomía) mediante EEM.
PACIENTES Y MÉTODOS
Durante un período de 8 años (1993-2001) se recogieron 6 pacientes con fenómeno de Raynaud asociado a diferentes enfermedades (cinco con enfermedades del tejido conjuntivo y uno con enfermedad de Buerger) refractario a tratamiento (tabla 1). Todos los pacientes recibían tratamiento médico de forma continua y tres de ellos se habían sometido a simpatectomías (tabla 1). A estos pacientes se les realizó una entrevista por un psicólogo clínico y tests psicométricos antes de someterse al implante. Se evaluaron sus perfiles psicopatológicos, sus estilos de afrontar el dolor, las expectativas y atribuciones que esperaban del implante, el perfil del cuidador primario (cuando el paciente no era capaz de manejar el implante) y la existencia de ganancias secundarias con el dolor. Si pasaban este examen psicológico se procedía a la realización del implante.
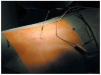
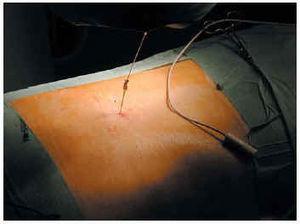
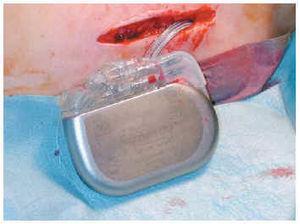
Se inyecta anestesia local lumbar, y mediante una punción epidural (fig. 1) se insertan electrodos Quad Plus® o Cervitrode®. Estos electrodos se colocaron a nivel epidural medial (en relación con los cordones posteriores de la médula), en los segmentos cervicales o lumbares según se quisiera estimular los miembros superiores o inferiores. El otro extremo se conectaba a generadores Itel II® o Itel III®, que quedaban alojados en un bolsillo subcutáneo situado en la pared torácica anterior (fig. 2).
Fig. 1.--Inserción de un electrodo mediante punción lumbar.
Fig. 2.--Preparación del bolsillo subcutáneo para la batería.
Se evaluó el dolor de los pacientes antes del implante con la escala analógica visual (puntuación de 1 a 10) y posteriormente en cada visita de revisión, considerando una respuesta favorable cuando había una mejoría del dolor del 50 % respecto a la puntuación inicial. El período de seguimiento de los pacientes varió entre 9 años (paciente 1) y un año (paciente 6), con revisiones cada 6 meses los primeros 3 años y después una revisión anual.
RESULTADOS
Cinco pacientes respondieron a los implantes (tabla 2), lo cual permitió que tres de ellos abandonaran la medicación y los otros dos disminuyeran la dosis necesaria para controlar sus síntomas, pasando de tomar el tratamiento farmacológico de forma casi continua, a tomarlo sólo en invierno y de forma ocasional cuando tenían síntomas. El único paciente que no respondió al tratamiento fue el paciente con enfermedad de Buerger, que sufrió la amputación de los dedos un año después de someterse al implante.
La única complicación (tabla 2) fue la recolocación del electrodo en el primero de los pacientes. No se registraron infecciones de la herida quirúrgica ni del electrodo.
DISCUSION
Los resultados obtenidos en nuestra serie concuerdan con los obtenidos en otras más amplias, como la de Raso12 y la de Francaviglia et al13. Raso presentó una serie de 40 pacientes y todos ellos respondieron al implante; la respuesta fue excelente en 18 de ellos, buena en seis y moderada en seis. Francaviglia presentó 15 pacientes en su serie y en todos ellos había una disminución de al menos el 50 % en su dolor respecto al nivel inicial.
La respuesta obtenida en nuestra serie puede calificarse como excelente en 3 pacientes, que dejaron la medicación y como buena en otros dos. El único paciente que no respondió al tratamiento fue un paciente con enfermedad de Buerger. Esta falta de respuesta puede ser debida a que en estos pacientes predominan los fenómenos de trombosis sobre el vasospasmo.
En la selección de los pacientes es muy importante la valoración de los factores psicológicos14. Monsalve y De Andrés15 han propuesto un algoritmo de selección de pacientes basándose en variables psicológicas, y obtienen un aumento en la respuesta frente al dolor y una disminución en los implantes retirados en la muestra en la que aplican el algoritmo de selección. Este algoritmo es el que usamos en nuestro hospital. Los principales factores y métodos que se usan en esta evaluación han quedado expuestos en el apartado «Material y métodos».
Tres de nuestros pacientes se habían sometido a simpatectomías antes de la EEM (tabla 2). La simpatectomía presenta una serie de desventajas respecto a la EEM: es técnicamente más difícil, se acompaña de complicaciones en un 5-15 % de los casos, ofrece pocos beneficios a los pacientes con arteriopatía subyacente y su efecto analgésico disminuye con el tiempo2. Las principales complicaciones en la EEM16 son la migración del electrodo (13 %), la rotura o el fallo del mismo (9,3 %) y la infección de la herida quirúrgica (7,8 %); todas ellas son reversibles y de poca importancia.
Las complicaciones registradas en nuestra serie han sido mínimas. La paciente 1 presentó con el tiempo una falta de respuesta debido a que la batería se agotó y el electrodo se había movido de su posición inicial. Este problema se solucionó con la recolocación del electrodo y el recambio de la batería. En la paciente 2 también se agotó la batería y cuando ésta se cambió, el implante volvió a funcionar sin problemas.
Según los datos que hemos obtenido de nuestra serie de pacientes y de otras series de la literatura médica12,13, la EEM resulta un tratamiento efectivo en pacientes con fenómeno de Raynaud refractario a otros tratamientos. Aunque en nuestra serie no se siguió la evolución de los trastornos tróficos, en otras13 se ha observado una mejoría de las úlceras y de los trastornos tróficos de las manos en pacientes con esclerodermia sistémica. Este tratamiento tiene la ventaja de resultar poco agresivo (se necesita sólo una punción a nivel lumbar y preparar un bolsillo subcutáneo para la batería), reversible (el implante se puede retirar si es necesario) y con pocas complicaciones. Además, los pacientes notan la mejoría desde el momento de realizar el implante y éste se puede mantener de forma indefinida. Estos aparatos no requieren un mantenimiento especial, sólo deben tener un seguimiento cada 6 meses los primeros 3 años y luego anual de forma indefinida, para comprobar la función del implante. Como posibles inconvenientes de la EEM destacan la necesidad de recambio de batería cada cierto tiempo (vida media de dos años) y la falta de estudios amplios comparándolo con otros tratamientos.