La crioterapia es el tratamiento más frecuentemente utilizado para las queratosis actínicas, ejerciendo su efecto únicamente sobre lesiones individuales. Existen fármacos tópicos que tratan además el campo de cancerización, actuando sobre queratosis actínicas no clínicamente evidentes, entre los que se encuentran el 5-fluorouracilo, el imiquimod, el diclofenaco o el ingenol mebutato.
Presentamos 17 pacientes con queratosis actínicas tratados con ingenol mebutato y describimos las observaciones en relación con la efectividad, el cumplimiento terapéutico y la tolerancia del fármaco. Las tasas de respuesta completa y parcial fueron del 35% y del 53%, respectivamente. El cumplimiento fue correcto en un 94% de los casos. En el 18% de los pacientes existieron reacciones locales intensas.
El ingenol mebutato es efectivo para el tratamiento de las queratosis actínicas. Aunque presenta similar tasa de reacciones locales a los restantes tratamientos disponibles para esta indicación, su pauta corta de administración favorece el cumplimiento.
Cryotherapy is the most common treatment for actinic keratosis, but its effect is limited to individual lesions. Several topical drugs, however, are available that, in addition to treating individual actinic keratoses, target field cancerization and thereby act on subclinical lesions. Examples are 5-fluorouracil, imiquimod, diclofenac, and ingenol mebutate. We report on 17 patients with actinic keratoses treated with ingenol mebutate and describe our findings on treatment effectiveness, adherence, and tolerance. Complete and partial response rates were 35% and 53%, respectively. Ninety-four percent of patients fully adhered to treatment and 18% developed severe local reactions. Ingenol mebutate is an effective treatment for actinic keratosis. Although it has a similar rate of local reactions to other treatments available for actinic keratosis, its short treatment regimen favors better adherence.
La queratosis actínica (QA) es considerada por la mayoría de los autores como una lesión premaligna con capacidad de evolucionar a un carcinoma epidermoide invasivo1. Entre sus opciones terapéuticas, además de los métodos dirigidos exclusivamente a la lesión, como la crioterapia, existen tratamientos tópicos que actúan tanto sobre la QA individual y clínicamente visible, como sobre el área circundante, con daño actínico crónico y QA subclínicas. Estos tratamientos incluyen el 5-fluorouracilo, el imiquimod (IMQ), el diclofenaco (DCF) o la terapia fotodinámica1,2.
El ingenol mebutato es un tratamiento de reciente comercialización indicado para las QA. Se ha demostrado efectivo para las lesiones individuales y para el campo de cancerización, en pautas de 3 días consecutivos para el área facial y el cuero cabelludo, y de 2 días para el tronco o las extremidades, consiguiendo curaciones completas de en torno al 40%1. La principal diferencia con respecto a los tratamientos de campo previos es su pauta de administración, más corta y de más fácil cumplimiento.
Casos clínicosSe presenta una serie de 17 pacientes que recibieron tratamiento con ingenol mebutato. Se evaluaron sus características demográficas, clínicas y datos relacionados con el tratamiento (efectividad, cumplimiento y tolerancia) (tabla 1). La efectividad se evaluó a los 2 meses2. Se denominó respuesta completa si en la zona tratada no existían alteraciones (piel normal); repuesta parcial si, habiendo disminuido las QA, persistió algún elemento, siendo necesaria la aplicación de un segundo tratamiento; y ausencia de respuesta si las lesiones no mostraban cambios. Se consideró que existió cumplimiento si el paciente aplicó las 3 o las 2 dosis según la localización fuese facial o corporal, respectivamente; y cumplimiento parcial en caso de no aplicación de alguna de las dosis. Para la graduación de la tolerancia, se preguntó a los pacientes acerca de la presencia de irritación en la zona de aplicación del fármaco, haciendo referencia a lo indicado en la ficha informativa del producto (mínima —tipo i—, leve —tipo ii—, moderada —tipo iii—, o intensa —tipo iv—).
Pacientes tratados con ingenol mebutato
| Edad | Sexo | AP ML | AP CCNM | TTO previo | T desde TTO (último TTO) | Localización | Cumplimientoa | Toleranciaa | Efectividada | Tiempo máximo seguimiento |
|---|---|---|---|---|---|---|---|---|---|---|
| 84 | M | Sí (LM) | Sí (CBC) | No | Facial | Correcto | Tipo III | Completa | 17 meses (no recidiva) | |
| 88 | M | No | No | No | Facial | Correcto | Tipo IV | Completa | 12 meses (no recidiva) | |
| 86 | M | No | Sí (CBC) | Sí (CT, IMQ, 5-FU) | 6 meses (CT) | Facial | Correcto | Tipo I/II | Parcial | |
| 82 | M | No | No | Sí (CT, DCF) | 6 meses (CT) | Facial | Correcto | Tipo III | Parcial | |
| 78 | M | No | No | Sí (CT) | 6 meses (CT) | Facial | Correcto | Tipo I/II | Parcial | |
| 64 | V | No | No | Sí (CT, ELC, IMQ) | 10 años (CT) | Cuero cabelludo | Correcto | Tipo III | Parcial | |
| 68 | V | No | No | Sí (CT, DCF) | 6 meses (DCF) | Facial | Correcto | Tipo I/II | Parcial | |
| 93 | M | No | No | Sí (CT, IMQ) | 6 meses (CT) | Cuero cabelludo | Correcto | Tipo I | No | |
| 86 | V | No | No | No | Cuero cabelludo | Correcto | Tipo I | No | ||
| 80 | M | No | No | Sí (CT, DCF) | 8 meses (DCF) | Facial | Correcto | Tipo III | Parcial | |
| 77 | V | No | No | Sí (CT, DCF, TFD) | Facial | Correcto | Tipo I/II | Parcial | ||
| 64 | V | No | No | Sí (CT, IMQ) | 7 meses (CT) | Facial | Correcto | Tipo III | Completa | 10 meses (no recidiva) |
| 74 | V | No | Sí (CBC, CE) | Sí (CT, IMQ) | 3 meses (CT) | Cuero cabelludo | Correcto | Tipo I/II | Completa | 5 meses (recidiva: 3 lesiones) |
| 81 | M | No | No | Sí (CT) | 8 meses (CT) | Facial | Correcto | Tipo III | Parcial | |
| 51 | M | No | No | No | Facial | Parcial | Tipo IV | Parcial | ||
| 53 | M | No | No | Sí (CT) | 5 años (CT) | Facial | Correcto | Tipo IV | Completa | 11 meses |
| 89 | M | No | No | Sí (CT, DCF) | 3 meses (DCF) | Facial | Correcto | Tipo III | Completa | 4 meses (recidiva: una lesión) |
AP: antecedentes personales; CBC: carcinoma basocelular; CE: carcinoma epidermoide; CCNM: cáncer cutáneo no melanoma; CT: crioterapia; DCF: diclofenaco; ELC: electrocoagulación; IMQ: imiquimod; LM: léntigo maligno; M: mujer; ML: melanoma; TFD: terapia fotodinámica; T: tiempo; TTO: tratamiento; V: varón.
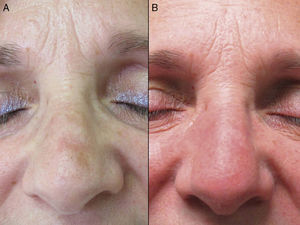
La media de edad de los pacientes fue de 76 años. Solo en un caso existió el antecedente de cáncer cutáneo melanoma y en 3 pacientes, de cáncer cutáneo no melanoma. En ningún caso el cáncer cutáneo previo se localizó en el área de aplicación de ingenol mebutato. En el 82% (14/17) de los casos se habían realizado tratamientos previos para las QA, mayoritariamente crioterapia (76%; 13/17) seguida de IMQ o DCF (ambos en un 29% [5/17] de los casos). La media de tiempo desde el último tratamiento hasta la aplicación de ingenol mebutato fue de 20 meses (mediana 6 meses). En el 100% de los pacientes el ingenol mebutato se había indicado para QA faciales (76%; 13/17) o en el cuero cabelludo (24%; 4/17). Se observó respuesta completa en el 35% (6/17) de los pacientes, repuesta parcial en el 53% (9/17) y ausencia de respuesta en el 12% (2/17). En la figura 1 se muestra uno de los casos de respuesta completa a ingenol mebutato. A partir de la evaluación a los 2 meses el seguimiento a largo plazo fue variable. En la tabla 1 se muestran los datos acerca del tiempo de seguimiento máximo y la situación clínica en ese momento de los pacientes que presentaron respuesta completa (media: 10 meses, mediana: 11 meses; remisión completa en el 67% de los casos). El cumplimiento fue correcto en el 94% (16/17) de los pacientes. El único caso en que existió cumplimiento parcial fue debido a una reacción local tipo iv tras la aplicación de la primera dosis, que por marcada sintomatología motivó la suspensión de las 2 siguientes administraciones (fig. 2). Solo en este caso y en 2 pacientes más (3/17; 18%) las reacciones locales fueron clasificadas como tipo iv. Las reacciones tipo iii y tipos i/ii se presentaron en porcentajes similares (41% en ambos grupos). No se observó relación entre la intensidad de la reacción y una mejor o peor respuesta (p=0,4; test de Fisher). No se comunicaron alteraciones cosméticas ni cicatrices en el área tratada en ninguno de los casos.
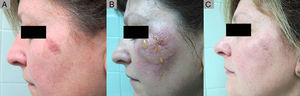
Respuesta parcial a ingenol mebutato tras tratamiento incompleto por reacción local tipo iv. A. Queratosis actínica no hiperqueratósica malar izquierda. B. Reacción local tipo iv tras administración de la primera monodosis de ingenol mebutato (suspensión de las 2 siguientes aplicaciones). C. Queratosis actínica residual. La paciente requirió una sesión de crioterapia adicional.
En esta serie de pacientes tratados con ingenol mebutato en la práctica clínica diaria hemos observado una tasa de respuesta del 88% (completa 35%, parcial 53%), gran adherencia al tratamiento (94% de cumplimiento) y frecuentes reacciones cutáneas locales (mínima-leve: 41%, moderada-intensa: 59%).
Nuestros porcentajes de respuesta fueron discretamente inferiores a los datos publicados (tabla 2)1. Se ha observado que el porcentaje de éxito puede incrementarse si el ingenol mebutato se combina con otras terapias (tabla 2)3.
Principales estudios que evalúan la efectividad, reacciones locales y cumplimiento de los tratamientos para queratosis actínicas
| Estudio | Características | Intervención | Efectividad |
|---|---|---|---|
| Lebwohl et al.1 | ECA fase iii-Efectividad en cara y cuero cabelludo: n=547 (277 IM, 270 placebo)-Efectividad en tronco y extremidades n=458 (226 IM, 232 placebo) | IM vs. placeboObjetivo: porcentaje de aclaramiento completo (evaluación a los 57 días) | Aclaramiento completo:QA de cara y cuero cabelludo: 42%QA de tronco y extremidades: 34%Respuesta parcial (aclaramiento igual o mayor del 75%):QA de cara y cuero cabelludo: 64%QA de tronco y extremidades: 49% |
| Berman et al.3 | ECA fase iiin=329 | IM+CT vs. CTObjetivos:-Porcentaje de aclaramiento completo en la semana 11-Efectividad en el mes 12 | Semana 11: aclaramiento completoCT e IM: 61%CT: 49%Mes 12: aclaramiento completoCT e IM: 55%CT: 40% |
| Vegter et al.7 | Metaanálisis25 estudios (ECA)n=5.562 | Tratamientos para QA de cara y cuero cabelludo.Objetivo: conseguir aclaramiento completo | TFD-ALA gel: 85,3%TFD–MAL: 65,9%TFD-ALA parche: 62%IMQ 5% 4 semanas: 57,2%5-FU 0,5%: 54,6%CT: 49,1%IMQ 5% 16 semanas: 45,1%IM: 43%DCF 3%: 35,4%IMQ 3,75% 2-3 semanas: 34,8%Placebo: 6,9% |
| Estudio | Características | Intervención | Efectividad |
|---|---|---|---|
| Gupta y Paquet6 (actualización de revisión Cochrane) | Metaanálisis36 estudios (ECA)n=6.473Recogida de datos: hasta abril de 2012 | Tratamientos QAObjetivo: conseguir aclaramiento completo | No se especifica porcentaje de aclaramiento. Se ordenan los tratamientos según efectividad |
| Todas las localizaciones | |||
| 5-FU 5%>5-FU 0,5%, TFD-ALA>IMQ 5%>IM>TFD-MAL>CT>DCF>placebo | |||
| Solo en cuero cabelludo | |||
| 5-FU 5%>5-FU 0,5%>IM>TFD-ALA>IMQ 5%>TFD-MAL>CT>placebo | |||
| Gradación global | |||
| 5-FU>TFD-ALA≈IMQ 5%≈IM≈TFD-MAL>CT>DCF |
| Estudio | Características e Intervención | Efectos adversos locales |
|---|---|---|
| Lebwohl et al.1 | Indicado previamente | Reacciones locales:-QA cara y cuero cabelludo:98%Reacciones moderadas-intensas en «una minoría»QA tronco y extremidades 96%70% moderadas-intensas |
| Estudio | Características | Intervención | Cumplimiento |
|---|---|---|---|
| Lebwohl et al.1 | Indicado previamente | Indicado previamente | >98% |
| Shergill et al.8 | Estudio transversaln=305DCF, 5-FU 5%, IMQ 5%, 5-FU 0,5% | Objetivo: identificar tasa de adherencia y los factores que la condicionan | Porcentaje de no adherencia o no persistenciaa88%Porcentajes de no adherencia según tiempo de tratamiento52% en tratamientos de 3-4 semanas de duración69% en tratamientos de 6-8 semanas de duración71% en tratamientos de 6-12 semanas de duración |
5-FU: 5-fluorouracilo; CT: crioterapia; DCF: diclofenaco; ECA: ensayos clínicos aleatorizados; IM: ingenol mebutato; IMQ: imiquimod; n: número de pacientes; QA: queratosis actínicas; TFD-ALA: terapia fotodinámica con ácido deltaminolevulínico, TFD-MAL: terapia fotodinámica con metilaminolevulinato; vs: versus.
La comparación entre las distintas opciones de tratamiento para las QA es difícil debido a la heterogeneidad de los trabajos que las evalúan4,5. En la tabla 2 se exponen los resultados de los estudios que con mayor evidencia científica analizan la efectividad de las diferentes intervenciones, incluyendo el ingenol mebutato. Los estudios coinciden en que el ingenol mebutato se sitúa entre la opción más efectiva (5-fluorouracilo) y las menos (CT y DCF), con resultados equiparables a aquellos fármacos con una efectividad intermedia (terapia fotodinámica e IMQ)6,7. Asimismo, se describe que solo en el caso del ingenol mebutato la efectividad relativa se influencia por la localización corporal a tratar, con porcentajes de aclaramiento más elevados en el polo cefálico, superando en esta localización al IMQ al 5%6.
Con respecto al cumplimiento terapéutico, el 94% de nuestros pacientes realizó el tratamiento completo, porcentaje similar a otros trabajos1. El ingenol mebutato presenta un grado de adherencia muy superior a los restantes fármacos tópicos de aplicación por el paciente (tabla 2)8. El alto grado de adherencia puede explicarse por su corta pauta de aplicación9.
Aunque las reacciones cutáneas locales en el área de aplicación de ingenol mebutato son frecuentes (>96%), suelen aparecer una vez finalizada la pauta de tratamiento, y no ser causa de abandono del mismo1. Estos fenómenos inflamatorios sobre la superficie cutánea tratada son también habituales durante la administración de los restantes tratamientos tópicos disponibles para las QA10.
El carácter retrospectivo de nuestro trabajo nos ha permitido describir las características del tratamiento con ingenol mebutato en una situación de práctica clínica real. Sin embargo, presenta también varias limitaciones. No se dispone de un análisis histológico de las lesiones del área de tratamiento, por lo que existe un componente subjetivo en la selección de las QA no hiperqueratósicas o «superficiales». Esto ha podido influir en pequeñas diferencias en la gravedad del área tratada y, secundariamente, afectar a nuestros resultados. También en la consideración de la respuesta parcial existe cierta subjetividad, ya que no se ha realizado un recuento exacto del número de lesiones. En cuanto al momento de la monitorización de la respuesta, la evaluación precoz a los 2 meses pudo haber influido de modo positivo nuestros resultados. Sin embargo, este momento lo consideramos el más idóneo por ser idéntico para todos los pacientes del estudio, pues los facultativos prescriptores se ajustaron a lo indicado en la ficha técnica del fármaco. Asimismo, el escaso número de pacientes nos dificulta realizar comparaciones con los estudios existentes.
Como conclusión, se destaca que el ingenol mebutato es de utilidad para el tratamiento de las QA y el campo de cancerización, y que su posología favorece el cumplimiento.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesAna Batalla y Ángeles Flórez han recibido honorarios en concepto de charlas relacionadas con la temática de queratosis actínicas por parte de Laboratorios Leo-Pharma.
El resto de autores declara que no tiene ningún conflicto de intereses.