INTRODUCCION
Iressa (gefitinib, ZD1839) es un agente anticancerígeno de reciente aparición que actúa inhibiendo de forma selectiva la tirosina quinasa del receptor de factor de crecimiento epidérmico (EGFR). Este receptor es una proteína transmembrana codificada por el proto-oncogén c-erb-B. Iressa inhibe la señal de este receptor al impedir la unión de la adenosina trifosfato a la región de la tirosina quinasa, bloqueando de esta forma la vía de traducción de su señal1.
El EGFR se expresa en muchos tumores sólidos, en los queratinocitos epidérmicos y en otras células presentes en la piel. Su activación contribuye al crecimiento tumoral, ya que induce la proliferación, la migración celular, y la angiogénesis. Iressa se está empleando en el tratamiento de tumores sólidos de varios tipos; el cáncer de pulmón no microcítico es una de las neoplasias en las que más se ha utilizado este fármaco. Su vía de administración es oral y, a diferencia de otros agentes antineoplásicos, no se utiliza a dosis máximas tolerables, sino a dosis biológicas óptimas (250-500 mg/día). Esto implica que disminuye el riesgo de efectos adversos sin disminuir su eficacia2.
Los efectos secundarios de Iressa no suelen ser muy intensos y consisten sobre todo en diarrea, molestias gastrointestinales y alteraciones dermatológicas. Las alteraciones dermatológicas se deben al mecanismo de acción del fármaco y aparecen en mayor o menor grado en casi todos los pacientes3.
DESCRIPCION DEL CASO
Un varón de 78 años, ex fumador importante, con antecedentes personales de cardiopatía isquémica y claudicación intermitente, fue diagnosticado de carcinoma epidermoide no microcítico de pulmón (estadio IIIB). Recibió tratamiento con quimioterapia (carboplatino y gemcitabina) con mala tolerancia hematológica; tras el segundo ciclo presentó un cuadro de diverticulitis aguda. El paciente rechazó un nuevo tratamiento quimioterápico. Tras varios meses se objetivó progresión pulmonar, por lo que se realizó tratamiento con radioterapia loco-regional. Dado que el paciente presentaba buen estado general, y la situación de su enfermedad tumoral (progresión sintomática), se solicitó tratamiento con Iressa como uso compasivo, habiéndose demostrado anteriormente su eficacia en casos similares.
Se inició el tratamiento con una dosis de 250 mg/día. Al cabo de 18 días, el paciente acudió a nuestro servicio por la presencia de lesiones cutáneas que habían comenzado a los pocos días de iniciarse el tratamiento. El paciente había sido tratado anteriormente por brotes de rosácea, refiriendo que estas lesiones eran semejantes a las de sus anteriores brotes.
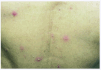
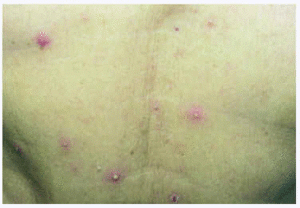
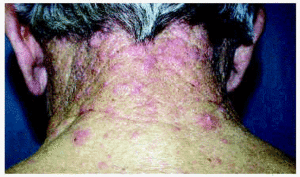
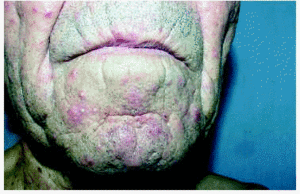
En la exploración física se apreciaban lesiones pustulosas, otras papulosas de color eritematoso localizadas en mentón, mejillas, nuca y parte anterior del tórax, dolorosas para el paciente (figs. 1, 2 y 3). Posteriormente aparecieron lesiones en ambas axilas de las mismas características.
Fig. 1.--Lesiones pustulosas en tórax.
Fig. 2.--Lesiones papulosas y pustulosas en nuca.
Fig. 3.--Lesiones pustulosas, con halo eritematoso localizadas en barbilla y mejillas.
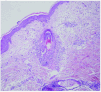
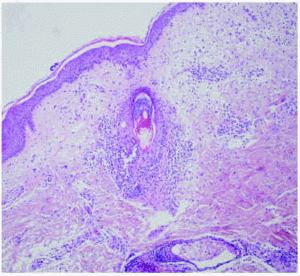
Se realizó una biopsia de una de las lesiones del tórax, donde se observaba un denso infiltrado neutrofílico, con células linfohistocitarias alrededor y en el seno de los folículos pilosos, con formación de pústulas en las zonas más superficiales de éstos (fig. 4). El diagnóstico histológico fue foliculitis aguda pustulosa. Asimismo, se tomó una muestra para cultivo bacteriano de una de las lesiones pustulosas, en la que creció Staphylococcus epidermidis.
Fig. 4.--Histología: infiltrado neutrofílico y linfohistiocitario alrededor del folículo piloso, con formación de pústula superficial. (Hematoxilina-eosina, x20.)
Dado el aspecto acneiforme de las lesiones se inició tratamiento tópico con peróxido de benzoilo. Las primeras semanas se apreció cierta mejoría. No obstante, se continuó el tratamiento con Iressa, presentando el paciente un brote intenso y extenso de lesiones pustulosas al mes de haberlo iniciado. En esta ocasión se instauró un ciclo de antibiótico oral (amoxicilina-ácido clavulánico) con buena respuesta sólo temporal, ya que, a la semana, volvieron a aparecer las lesiones. Dado que el paciente refería intenso malestar, el oncólogo decidió suspender provisionalmente el tratamiento con Iressa, con lo que remitieron en pocos días las lesiones cutáneas. Tras iniciar de nuevo el tratamiento no se han vuelto a repetir brotes tan extensos de lesiones, y ha podido continuarse la administración con Iressa, ya que se está obteniendo una buena respuesta oncológica.
DISCUSION
Los efectos secundarios dermatológicos relacionados con Iressa son semejantes a los encontrados al utilizar otros fármacos que actúan al mismo nivel (es decir, el bloqueo de la señal del EGFR); este es el caso del cetuximab (C225), un anticuerpo monoclonal frente a dicho receptor4,5. En los tratamientos con ambos fármacos se han descrito erupciones papulopustulosas de localización folicular, descamación difusa y alteraciones en el cuero cabelludo (pelo fino, curvado y quebradizo). Estas alteraciones no están mediadas por un mecanismo inmunológico, sino que son consecuencia directa de la inhibición de la señal transmitida por el EGFR en el epitelio epidérmico y folicular6.
En la piel, el EGFR se expresa en la epidermis, glándula sudorípara y epitelio del folículo piloso7,8. La activación de dicho receptor en la epidermis promueve la proliferación, pero reduce la capacidad de diferenciación terminal de los queratinocitos basales. Se han realizado estudios in vitro en los que se demuestra que la inhibición del EGFR detiene el crecimiento de los queratinocitos e induce la diferenciación terminal9. Por lo tanto, se crea un desequilibrio entre proliferación y diferenciación. En el folículo piloso la activación del EGFR estimula la transición de anagén a catagén10. Esto puede explicar los cambios en el pelo que presentan algunos de los pacientes tratados con Iressa.
Nuestro paciente comenzó con una erupción papulopustulosa muy poco tiempo después de haber iniciado el tratamiento con Iressa; el paciente describía las lesiones como semejantes a sus brotes de rosácea previos. La presencia de lesiones en zonas alejadas y no características de la rosácea, como el tórax, la nuca o las axilas hizo que las lesiones se atribuyeran al tratamiento con Iressa. La histología de una de las lesiones mostró una foliculitis pustulosa superficial, por lo tanto semejante al patrón encontrado en otros casos de la literatura médica, no sólo en pacientes tratados con Iressa sino también con otros antagonistas del EGFR como el cetuximab. El S. epidermidis es un componente de la flora habitual de la piel, y no está implicado normalmente en infecciones del folículo piloso. No obstante, nuestro paciente mejoró tras un ciclo de tratamiento con amoxicilina-ácido clavulánico. Aunque se considera que esta bacteria no es la causante de las lesiones del paciente, es posible que las alteraciones provocadas por Iressa favorezcan la patogenicidad de gérmenes habituales en la piel6. Aunque se conoce el efecto de la activación y de la inhibición del EGFR sobre los queratinocitos in vitro, se desconoce el mecanismo preciso por el cual la inhibición de la señal de dicho receptor induce una foliculitis pustulosa.
El tratamiento de las lesiones pustulosas se ha realizado en el resto de casos descritos en la literatura médica de forma empírica, con tratamientos empleados para el acné, como tetraciclinas orales, tretinoína tópica, y otros. No obstante, la mayoría de los pacientes toleran bastante bien los efectos adversos dermatológicos asociados al uso de Iressa. La intensidad de las alteraciones dermatológicas varía durante el tratamiento, pero suelen ir disminuyendo en intensidad tras varias semanas. No suele ser necesario suspender el tratamiento, sino a veces sólo interrumpirlo temporalmente.
Es interesante investigar en la etiopatogenia de reacciones cutáneas, casi siempre foliculitis pustulosa en fármacos como Iressa. Conocer la actividad del EGFR en la piel puede ayudar a explicar el mecanismo de producción de ciertas enfermedades cutáneas y disponer de fármacos antagonistas de dicho receptor puede ser utilizado como un arma terapéutica en el futuro en enfermedades en las que está aumentada su actividad, como las neoplasias cutáneas o la psoriasis.