INTRODUCCIÓN
La necrolisis epidérmica tóxica (NET) es una entidad grave consistente en una erupción eritematosa, generalizada y dolorosa, con formación de ampollas flácidas que afectan al menos al 30 % de la superficie cutánea y con signo de Nikolsky positivo; cursa con afectación de mucosas y, a veces, con un estado prodrómico de fiebre y malestar general1 . Suele estar relacionado con la ingesta previa de fármacos hasta en el 80 % de los casos2 , como antiinflamatorios no esteroideos, antibióticos, alopurinol y antiepilépticos. Su patogenia no está del todo clara, pero parece estar relacionada con alteraciones en el metabolismo de los fármacos al no poder destoxificarse los productos intermedios de los mismos, y actuar éstos como tóxicos directos3 , o al provocar una respuesta inmunitaria desencadenante del daño epidérmico4,5 ; se ha implicado un cierto componente hereditario y un respuesta inmunológica citotóxica6,7 .
DESCRIPCIÓN DEL CASO
Una mujer de 37 años de edad, con antecedente de migraña con aura prolongada, comenzó a recibir, por este motivo, tratamiento con lamotrigina (50 mg/día), asociada a nicardipino (20 mg/día), ácido acetilsalicílico (100 mg/día) y omeprazol (20 mg/día); la única medicación que no había recibido previamente era lamotrigina, mientras que el resto de fármacos se habían introducido al menos 6 meses antes. A los 3 días del inicio del tratamiento comenzó con odinofagia, artromialgias y malestar general y 48 h después se instauró fiebre de 39 °C y una erupción cutánea pruriginosa que comenzó en el cuello y se fue diseminando por toda la superficie corporal. Su médico de atención primaria pautó tratamiento con antihistamínicos y corticoides orales sin mejoría. Se decidió el ingreso hospitalario en el servicio de dermatología ante la progresión del cuadro 9 días después de haberse iniciado.
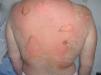
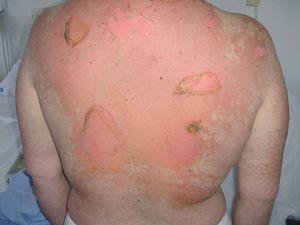
En la exploración dermatológica se observaba un exantema maculopapuloso generalizado de pequeños elementos, confluentes sobre todo en la raíz de los miembros, con intenso eritema y mínima vesiculación. Las lesiones respetaban palmas y plantas. Además, presentaba inyección conjuntival y faríngea y erosiones en la semimucosa labial superior, inferior y mucosa yugal. En la espalda y miembros superiores se observaban ampollas que fueron confluyendo en los 2 días siguientes, con signo de Nikolsky positivo (fig. 1).
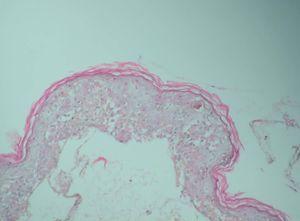
Se realizó una toma de biopsia de una de las lesiones ampollosas y el estudio anatomopatológico reveló un despegamiento dermoepidérmico con necrosis de la epidermis (fig. 2), y en la dermis un infiltrado mononuclear de predominio perivascular.
Se instauró tratamiento con medidas de soporte, y prednisona en dosis de 0,5 mg/kg/día, y se retiró la lamotrigina. La paciente evolucionó favorablemente y fue dada de alta 20 días después con buena reepitelización de las lesiones.
Fig. 1.—Áreas erosivas por rotura de ampollas y signo de Nikolsky positivo.
DISCUSIÓN
La lamotrigina es un fármaco antiepiléptico no sedante, perteneciente a la familia de las triacinas, que comenzó a utilizarse en Europa en 19904 y en España en 19938 . Está indicado en el tratamiento monoterápico de la epilepsia en adultos y como terapia añadida en niños y adultos4,8-10 , y es eficaz en las crisis parciales con o sin generalización secundaria, crisis tonicoclónicas generalizadas, crisis asociadas al síndrome de Lennox-Gastaut4 y crisis de ausencia8 . Se recomienda como tratamiento de primera línea en la epilepsia idiopática generalizada de la mujer en edad fértil (incluido en el embarazo y el período de lactancia), en pacientes mayores y en aquellos con deterioro intelectual11 . Actualmente está siendo investigado su uso en otros trastornos como el bipolar, la adicción a la cocaína, la neuralgia del trigémino, el dolor postoperatorio10 y la migraña12,13 . Se estima que, aproximadamente, del 5 a 10 % de los pacientes tratados con lamotrigina experimentan una erupción cutá-10,14-16 , siendo mayor el riesgo en los dos primeros meses de tratamiento2,17 y con la asociación de valproato sódico, al inhibir competitivamente la glucuro-5,8,10,14,15,18,19 y tener mayor afinidad por las proteínas, lo que duplica la vida media de la lamotrigina4 . Se ha descrito una mayor incidencia de toxicodermias en niños10,19 , al inicio de tratamiento con dosis altas y en el escalonamiento rápido de la dosis4,19 .
El tratamiento de la NET consistirá en la retirada del fármaco sospechoso y de aquellos con los que exista reactividad cruzada. El uso de corticoides sistémicos sigue siendo controvertido y su administración, si se realiza, debe ser precoz, habiéndose descrito buenos resultados con el uso de ciclosporina A18,20 e inmunoglobulinas intravenosas21,22 .
Fig. 2.—Ampolla subepidérmica con necrosis de los queratinocitos. (Hematoxilina-eosina, ×200.)
Correspondencia:
Isabel Rodríguez-Blanco. Departamento de Dermatología. Facultad de Medicina. San Francisco, s/n. 15782 Santiago de Compostela. España. mejaime@usc.es.
Recibido el 15 de noviembre de 2004. Aceptado el 13 de diciembre de 2004.