INTRODUCCIÓN
El captopril (3-mercapto-2-metil-propanoil-proli-na) es un antihipertensivo y vasodilatador que actúa como inhibidor de la enzima conversora de la angiotensina (IECA). Ampliamente utilizado en las últimas décadas, ha dejado tras de sí un gran número de efectos secundarios1-3 . La fotosensibilidad se incluye entre ellos, aunque no ha sido uno de los más frecuentemente informados4-6 . Se presenta en este trabajo el caso de una paciente con una erupción en áreas fotoexpuestas, que histológicamente mostró cambios compatibles con mucinosis folicular, en la que se obtuvo un fotoparche positivo al captopril y en la que las lesiones se resolvieron al suspender la administración del fármaco.
MATERIAL Y MÉTODOS
El fototest se realizó con un simulador solar de arco de xenón 150W (Solar Light Co), modelo 16S. El sistema está provisto de dos filtros internos, el WG320que elimina la radiación inferior a 250 nm (toda la UVB y la UVC más nociva) y el filtro Corning azul UG11, que elimina la radiación emitida superior a 400 nm (visible e infrarroja). Además, el aparato dispone de un filtro externo móvil que permite eliminar a voluntad la radiación UVB (por debajo de 320 nm), permitiendo únicamente el paso de la radiación UVA (entre 320 y 400 nm). El calibrado del simulador fue realizado por el Departamento de Termodinámica de la Facultad de Físicas de Valencia7 . Se utilizaron dosis crecientes de UVB hasta un máximo de 24,3 mJ/cm2 e igualmente dosis crecientes de UVA hasta un máximo de 5,6 J/cm2 .
El fotoparche se realizó con una lámpara de luz PUVA 500 (Herbert Waldmann, Germany) irradiando durante 30 min (9 J/cm2 ) la batería de alérgenos homologada por el Grupo Español de Fotobiología, que se aplicó por duplicado, retirando los parches a las 48 h e irradiando sólo la mitad de ellos. Además se parchearon por duplicado en vaselina al 1 %, el Eca-zide® , Captopril e hidroclorotiazida, estos dos últimos amablemente facilitados por el servicio de farmacia de nuestro hospital.
Se obtuvieron dos muestras cutáneas de las lesiones de la paciente, a través de sendos sacabocados (punchs) de 4 mm de diámetro. Una de ellas fue fijada con formol, incluida en parafina y teñida con hema-toxilina-eosina y hierro coloidal. La otra se congeló en nitrógeno líquido para realizar posteriormente inmunofluorescencia directa de piel afectada.
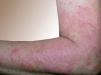
Fig. 1.—Placas eritematosas, infiltradas y de aspecto eczematoso localizada en tercio inferior del brazo izquierdo.
DESCRIPCIÓN DEL CASO
Una mujer de 50 años consultó en octubre de 2000 por una erupción muy pruriginosa de unos 2 meses de evolución. A la exploración se observaban placas eritematosas, confluentes, infiltradas, de aspecto eczematoso y de predominio en áreas fotoexpuestas: tercio inferior de los brazos, antebrazos, escote, parte superior de la espalda y piernas (fig. 1). La paciente había sido tratada de forma ambulatoria con corticoides orales a dosis bajas sin mejoría clínica. Como antecedentes personales destacaba una hipertensión arterial en tratamiento con Ecazide® (captopril + hidroclorotiazida) desde hacía 2 años e hipercolesterolemia en control dietético.
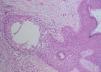
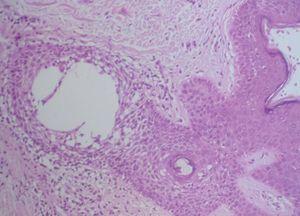
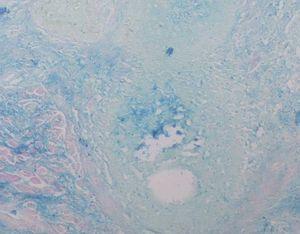
Se practicó una biopsia cutánea que mostró una epidermis normal sin alteraciones de la membrana basal. Destacaban infiltrados linfocitarios de predominio perifolicular y grandes espacios quísticos con pérdida de la conexión entre los queratinocitos foliculares (fig. 2). La tinción con hierro coloidal mostró depósitos de mucina en estos espacios quísticos (fig. 3). Se realizaron las siguientes exploraciones complementarias con resultados normales y/o negativos: inmunofluorescencia directa de piel afectada, recuento, fórmula y bioquímica sanguínea básicas, hormonas tiroideas, anticuerpos antinucleares, anti-ADN, anti-Ro y anti-La.
El fototest realizado 2 meses después de la retirada de Ecazide® resultó dentro de la normalidad para el fototipo de piel de la paciente. Se obtuvieron un parche y fotoparche positivos al Ecazide® pero también fueron positivos los controles realizados. Se optó por realizar parche y fotoparche del captopril y la hidroclorotiazida por separado, obteniéndose un fotoparche positivo al captopril (fig. 4). Los controles realizados en 20 pacientes fueron negativos, por lo que le dimos al fotoparche relevancia actual. El resto de los hallazgos de la exploración fotobiológica de la paciente se encuentran recogidos en la tabla 1.
Fig. 2.—Infiltrado linfocitario perifolicular con grandes espacios quísticos con pérdida de conexión entre los queratinocitos foliculares. (Hematoxilina-eosina, ×100.)
Tras retirar el fármaco las lesiones de la paciente se resolvieron con corticoides tópicos y, después de 3 años de seguimiento, no ha presentado recidivas.
COMENTARIO
La interacción de un fármaco y la luz solar puede provocar reacciones de fotosensibilidad en pacientes predispuestos. Existen en la actualidad unos 268 fármacos recogidos que han sido capaces de provocar reacciones de fotosensibilidad1,3 . Las sulfamidas, tetraciclinas y tranquilizantes derivados de las fenotiazinas fueron los fármacos fotosensibilizantes dominantes en las décadas de los cincuenta y sesenta1,8 . Actualmente existen tres grupos terapéuticos que producen reacciones de fotosensibilidad más frecuentemente: los antiinflamatorios no esteroideos (AINE), los diuréticos y los antibióticos derivados de las quinolonas1 .
El captopril ha sido un fármaco ampliamente usado a partir de 1977 como antihipertensivo y vasodilatador. A pesar de que un 10 % de los pacientes tratados ha presentado efectos secundarios cutáneos variados (tabla 2)3,4 , la fotosensibilidad ha sido escasamente recogida en la literatura especializada4-6 , demostrándose fotoparche positivo al captopril sólo en uno de los casos descritos4 .
Por otro lado, la mucinosis folicular tiene dos formas de presentación clínica distintas9 : la mucinosis folicular de Pinkus, también conocida como alopecia mucinosa, que se caracteriza por la aparición de pápulas induradas rasposas, de distribución folicular, que causan pérdida de pelo y la mucinosis folicular urticariforme, que suele afectar a varones de mediana edad y se presenta como una erupción cíclica, transitoria, de curso benigno, formada por pápulas urticariales localizadas en cabeza y cuello, sin tapones foliculares y sin alopecia. Histológicamente, sin embargo, ambas formas de mucinosis folicular presentan los mismos hallazgos característicos 10 . Se observan depósitos de mucina en el epitelio folicular y las glándulas sebáceas, lo cual provoca la desconexión entre los queratinocitos. En fases más avanzadas, esto se traduce en la aparición de espacios quísticos que contienen mucina, células inflamatorias y queratinocitos alterados. En ocasiones se observan infiltrados linfocitarios perivasculares o intersticiales, superficiales y profundos que pueden estar acompañados de eosinófilos y neutrófilos aislados. La mucinosis folicular se ha descrito como un epifenómeno histológico en una gran variedad de procesos dermatológicos, como linfomas sobre todo micosis fungoide, lupus eritematoso, liquen simple crónico, e incluso erupciones fotoinduci- 9,11 . En la mucinosis folicular secundaria los hallazgos principales son los característicos del proceso al que acompañan y, a diferencia de las formas primarias de mucinosis, donde pueden estar afectados todos los folículos de una sección, es característico que sólo se encuentra un folículo piloso afectado por los depósitos. En nuestra paciente los hallazgos histológicos fundamentales fueron los de la mucinosis folicular, sin que se observaran otros cambios dérmicos o epidérmicos que hicieran sospechar otro proceso.
Fig. 3.—La tinción de hierro coloidal pone de manifiesto la existencia de gran cantidad de mucina ×100.
TABLA 1. EXPLORACIÓN FOTOBIOLÓGICA
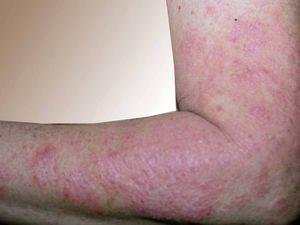
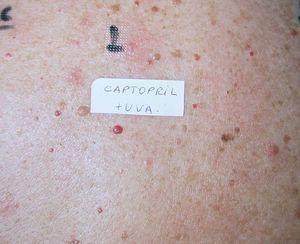
Fig. 4.—Fotoparche positivo al captopril.
TABLA 2. REACCIONES CUTÁNEAS Y CAPTOPRIL
No hemos encontrado referencias en la literatura médica que relacionen el captopril y la mucinosis folicular. Magro y Crowson12 recogen en la literatura médica 22 pacientes en tratamiento con diferentes fármacos, con infiltrados linfoides cutáneos atípicos tipo micosis fungoide, reacción vascular linfomatoide, linfocitoma cutis y mucinosis folicular. En 13 de los 22 pacientes el diagnóstico clínico fue de linfoma y en 17 pacientes las lesiones se resolvieron al retirar el fármaco sospechoso. Los fármacos en los que con más frecuencia se encontraron prescritos fueron los antagonistas del calcio, IECA, antidepresivos, antihistamínicos, bloqueantes , benzodiazepinas e hipocolesterolemiantes. Todos estos fármacos están reconocidos como perturbadores de la función linfocitaria o bien han estado implicados en casos de pseudolinfoma. No se especifica en dicho trabajo si aquellos pacientes en los que se observó mucinosis folicular eran los que estaban tomando un IECA. Posteriormente se han descrito 2 casos de hiperplasia linfoide atípica13 en relación con la ingesta de losartán, un inhibidor de la angiotensina II. En uno de los casos se pudo demostrar reordenamiento clonal de células T y en ambos pacientes la erupción se resolvió tras suspender el fármaco.
En nuestro caso, la erupción cutánea en áreas foto-expuestas, la exploración fotobiológica con un foto-parche positivo al captopril, la curación de las lesiones tras la retirada del fármaco, sin recidivas después de 3 años de seguimiento y la ausencia de otros hallazgos histológicos, nos hacen pensar en una mucinosis folicular secundaria a fotoalergia por captopril.
Correspondencia:
Teresa Martínez-Menchón. Consorcio Hospital General Universitario. Avda. Tres Cruces, s/n. 46014 Valencia. España. teresammenchon@aedv.es
Recibido el 1 de abril de 2004. Aceptado el 3 de febrero de 2005.