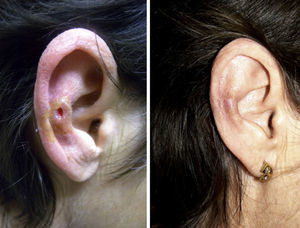
La condrodermatitis nodular del hélix (CNH) es un proceso idiopático, degenerativo y doloroso que afecta a la piel y al cartílago del hélix o del antéhelix.
Recientemente se ha descrito la utilidad de la nitroglicerina (NTG) tópica a 2% en el tratamiento de la CNH con buenos resultados, aunque con una tasa de efectos secundarios en el 17% de los casos. Es probable que a una concentración menor se pueda mantener el mismo efecto mejorando la tolerancia.
Nuestra finalidad fue evaluar la efectividad y seguridad de la NTG tópica al 0,2% para el tratamiento de la CNH.
Material y métodosSe llevó a cabo un estudio observacional retrospectivo entre los años 2012 y 2014 en 2 centros hospitalarios españoles. La efectividad se determinó a través de la evaluación clínica, realizada mediante seguimiento fotográfico, y de los síntomas de la lesión, medido mediante una escala numérica verbal.
ResultadosVeintinueve pacientes recibieron el tratamiento, de los cuales el 93% manifestaron una mejoría clínica con una duración media del tratamiento de 1,8 meses y un tiempo de seguimiento medio en los pacientes respondedores de 5,9 meses. La tolerancia fue buena en general en todos los casos.
ConclusiónLa NTG tópica al 0,2% se plantea como una opción conservadora, efectiva y bien tolerada para el tratamiento de la condrodermatitis nodular del hélix que mejora tanto la apariencia clínica como la sintomatología en la mayoría de los pacientes.
Chondrodermatitis nodularis helicis (CNH) is a painful idiopathic degenerative condition involving the skin and cartilage of the helix or antihelix of the ear. Topical nitroglycerin 2% is a relatively recent treatment option for CNH that has produced good results, although with adverse effects (17% of cases). The use of a lower concentration would probably achieve similar results with fewer adverse effects. The aim of this study was to evaluate the effectiveness and safety of topical nitroglycerin 0.2% in the treatment of CNH.
Material and methodsWe performed a retrospective observational study of patients treated in 2 Spanish hospitals between 2012 and 2014. The effectiveness of treatment was determined by clinical photography and assessment of symptoms using a verbal numerical rating scale.
ResultsOf the 29 patients treated, 93% showed clinical improvement. In the group of responders, mean treatment duration was 1.8 months and mean follow-up was 5.9 months. Overall tolerance was good in all cases.
ConclusionTopical nitroglycerin 0.2% is an effective and well-tolerated conservative treatment option that improves the appearance of lesions and provides symptomatic relief in the majority of patients with CNH.
La condrodermatitis nodular del hélix (CNH) fue descrita por Wrinkler en el año 1915 y consiste en una lesión inflamatoria que se localiza principalmente en el hélix o antehélix de la oreja. Los principales factores etiopatogénicos reconocidos son la exposición solar crónica y los traumatismos locales de repetición1,2.
Existen diversas modalidades de tratamiento, médicas o quirúrgicas, con resultados variables y a menudo insatisfactorios que conllevan en múltiples ocasiones a la recidiva. Hay pocos estudios controlados realizados que demuestren la superioridad de unas opciones terapéuticas frente a las otras.
La adopción de medidas generales posturales constituye un pilar fundamental del tratamiento, pero a menudo no es suficiente, o al menos no conlleva la rápida mejoría de los síntomas. En los últimos años han sido descritas algunas terapias novedosas no invasivas para el manejo de esta condición, como la terapia fotodinámica o la nitroglicerina (NTG) tópica al 2% con buenos resultados e índices de respuesta completa en torno al 60%, y con una tasa de efectos secundarios alrededor del 17%3–7. Sin embargo, es probable que la NTG tópica a una concentración menor pueda mantener la misma respuesta clínica mejorando la tolerancia.
ObjetivoEstablecer la seguridad y efectividad de la NTG al 0,2% por vía tópica como alternativa de tratamiento para la CNH.
Material y métodosSe llevó a cabo un estudio observacional retrospectivo entre los años 2012 y 2014 en 2 centros hospitalarios españoles: el Hospital Universitario 12 de Octubre de Madrid y el Hospital de Manises de Valencia.
Se instauró el tratamiento mediante la fórmula magistral de NTG tópica al 0,2% en vaselina filante.
Como procedimiento estándar se indicaba la aplicación inicial de la fórmula una vez al día durante los primeros 10 días, aplicada en capa fina abarcando la lesión y 0,5cm de margen de piel sana. En caso de buena tolerancia el paciente procedía a la aplicación del producto cada 12h hasta la resolución del cuadro clínico.
Adicionalmente, el paciente era instruido con medidas generales de carácter mecánico con el fin de aliviar la presión en el área lesional, como la adopción de medidas posturales y la utilización de almohadas anatómicas especiales.
La efectividad del tratamiento se determinó a través de un examen clínico, de la toma de imagen fotográfica y de un cuestionario de dolor mediante escala numérica verbal, todo ello realizado previamente al inicio de tratamiento, tras 1-2 meses de iniciado y cada 3 meses tras su finalización. Se consideró respuesta completa a la resolución de la sintomatología inicial con ausencia de dolor (medido por la escala numérica verbal como 0/10) y desaparición de la lesión o establecimiento de cicatriz. Se definió respuesta parcial a la disminución del dolor (mejoría en el numerador de la fracción de la escala numérica verbal respecto al valor basal) y mejoría del aspecto (disminución del tamaño y/o eritema) con respecto al inicio. Se definió respuesta ausente la falta de alivio del dolor (definido como la ausencia de variación de la gradación del dolor en la escala numérica verbal) y/o mejoría de la apariencia de la lesión inicial en la primera visita tras iniciado el tratamiento (1-2 meses después).
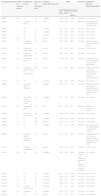
ResultadosVeintinueve pacientes fueron tratados con NTG tópica al 0,2%, 20 mujeres y 9 hombres, con una edad media de 67,8 años (rango de 29-85 años). Aproximadamente la mitad de los pacientes (48%) había realizado uno o varios tratamientos previos junto con medidas generales para reducir la presión sobre la lesión con falta de respuesta (fracaso primario) o recaída posterior (fracaso secundario). El resto de pacientes recibieron la fórmula como primer tratamiento. Los datos clínico-demográficos, así como los de eficacia se resumen en la tabla 1.
Datos demográficos y clínicos, respuesta al tratamiento, tolerancia y seguimiento
| Paciente/género/edad | Tiempo de evolución (meses) | Tratamientos previos | Duración del tratamiento (días) | Respuesta (nula/completa/parcial) | Dolor | Tolerancia | Seguimiento duración (meses)/comentarios | ||
|---|---|---|---|---|---|---|---|---|---|
| Antes del tto | Después del tto | Porcentaje de mejoría | |||||||
| 1/M/74 | NA | No | 30 | Completa | 10/10 | 0/10 | 100% | Excelente | 3/No recidiva |
| 2/M/79 | 12 | Corticoides tópicos | 30 | Nula | 10/10 | 10/10 | 0% | Excelente | 0/Extirpación de la lesión por falta de eficacia de NTG |
| 3/M/63 | 6 | No | 15 | Completa | 4/10 | 0/10 | 100% | Excelente | 3/No recidiva |
| 4/M/69 | 7 | No | 30 | Completa | 5/10 | 0/10 | 100% | Excelente | 3/No recidiva |
| 5/M/83 | 2 | No | 30 | Completa | 9/10 | 0/10 | 100% | Excelente | 3/No recidiva |
| 6/M/85 | NA | No | 30 | Parcial | 6/10 | 1/10 | 83% | Excelente | 6/No recidiva |
| 7/M/55 | 24 | Corticoides intralesionales | 30 | Parcial | 10/10 | 8/10 | 20% | Excelente | 6/Extirpación de la lesión por respuesta escasa |
| 8/V/56 | 36 | Corticoides intralesionales | 30 | Parcial | 10/10 | 2/10 | 80% | Excelente | 12/No recidiva |
| 9/V/29 | 120 | Corticoides intralesionales | 45 | Parcial | 10/10 | 2/10 | 80% | Excelente | 17/No recidiva |
| 10/M/53 | 142 | Corticoides tópicos | 45 | Parcial | 10/10 | 2/10 | 80% | Excelente | 18/Recidiva tras 18 meses coincidiendo con reinicio de quimioterapia |
| 11/M/74 | NA | Corticoides tópicos, cirugía (2 intervenciones) | 105 | Parcial | 8/10 | 0/10 | 100% | Excelente | 3/Mínima molestia al mes de la finalización que se resolvió en una semana con aplicación de NTG |
| 12/V/48 | 36 | No | 45 | Completa | 6/10 | 0/10 | 100% | Excelente | 3/No recidiva |
| 13/M/81 | NA | Corticoides tópicos, crioterapia | 10 | Completa | 10/10 | 0/10 | 100% | Excelente | 6/Mínima molestia a los 2 meses de finalización que se resolvió con 10 días de aplicación de NTG |
| 14/M/81 | 72 | Corticoides tópicos, crioterapia, cirugía | 67 | Completa | 7/10 | 0/10 | 100% | Excelente | 3/No recidiva |
| 15/V/41 | NA | Crioterapia, cirugía | 30 | Nula | 8/10 | 8/10 | 0% | Excelente | 0/Cirugía por ausencia de respuesta |
| 16/V/58 | 12 | Corticoides intralesionales | 150 | Completa | 10/10 | 0/10 | 100% | Excelente | 3/No recidiva |
| 17/M/86 | 3 | No | 90 | Completa | 10/10 | 0/10 | 100% | Excelente | 4/No recidiva |
| 18/M/83 | NA | No | 100 | Parcial | 10/10 | 1/10 | 90% | Excelente | 4//No recidiva |
| 19/M/72 | NA | No | 90 | Completa | 8/10 | 0/10 | 100% | Excelente | 6/A veces usa NTG por molestia mínima con muy buena respuesta |
| 20/M/62 | 48 | Corticoides tópicos, crioterapia, extirpación | 60 | Parcial | 10/10 | 2/10 | 80% | Excelente | 3/Mínima molestia a los 3 meses de finalización que se resolvió con 10 días de aplicación de NTG |
| 21/V/73 | 72 | Cirugía (2 intervenciones) | 60 | Parcial | 10/10 | 2/10 | 80% | Excelente | 12/No recidiva |
| 22/V/73 | NA | No | 90 | Completa | 7/10 | 0/10 | 100% | Excelente (cefalea post-aplicación por exceso de producto, se resolvió al reducir cantidad) | 7/No recidiva |
| 23/V/75 | 3 | No | 60 | Completa | 7/10 | 0/10 | 100% | Excelente | 15/No recidiva |
| 24/M/71 | 12 | No | 45 | Completa | 10/10 | 0/10 | 100% | Excelente | 4/No recidiva |
| 25/M/72 | NA | No | 45 | Completa | 10/10 | 0/10 | 100% | Excelente | 3/No recidiva |
| 26/V/56 | 12 | No | 37 | Completa | 10/10 | 4/10 | 60% | Excelente | 4/No recidiva |
| 27/M/80 | 240 | Cirugía (2 intervenciones) | 37 | Completa | 4/10 | 0/10 | 100% | Excelente | 3/No recidiva |
| 28/M/71 | 36 | Crioterapia | 45 | Completa | 10/10 | 0/10 | 100% | Excelente | 3/No recidiva |
| 29/M/62 | 4 | No | 90 | Parcial | 8/10 | 2/10 | 75% | Excelente | 3/No recidiva |
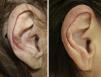
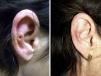
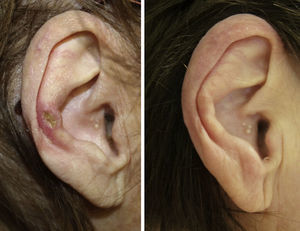
Veintisiete casos (93%) manifestaron una mejoría clínica evidente, 17 con respuesta completa (63%) y 10 con respuesta parcial (37%). La duración media del tratamiento en los pacientes respondedores fue de 1,8 meses (54,17 días) (figs. 1 y 2). Dos pacientes (6,9%) no respondieron (respuesta nula) tras 4 semanas de tratamiento y requirieron tratamientos adicionales.
Veintiocho de los casos (97%) mostraron una buena tolerancia. Un único caso aislado mostró cefalea como efecto adverso asociado al tratamiento.
El seguimiento postratamiento de los pacientes respondedores se realizó durante un periodo medio de 5,9 meses (rango temporal de 3 a 18 meses). El 48% de los pacientes (14 pacientes) fue seguido más de 4 meses tras finalizado el tratamiento. Solo una paciente presentó recidiva clínica tras 18 meses de seguimiento en coincidencia con el inicio de un tratamiento quimioterápico para el de cáncer de mama. Cuatro de los pacientes informaron de una molestia episódica, pero ligera, en el área previamente afecta por la CNH sin recidiva clínica aparente. Dicha molestia fue adecuadamente controlada mediante la aplicación ocasional de NTG 0,2% a demanda. Una paciente debido a respuesta insuficiente tras un mes de tratamiento (mejoría de 10/10 a 8/10) fue finalmente intervenida quirúrgicamente de su lesión.
DiscusiónEl presente estudio muestra la mejoría de la CNH en la mayoría de los pacientes que recibieron tratamiento con NTG tópica al 0,2% con una tasa de efectos secundarios casi nula.
Existen diversas opciones terapéuticas con variable eficacia, y hay pocos estudios controlados al respecto que incluyen tanto medidas médicas como quirúrgicas, como los corticoides tópicos8 o intralesionales9, la criocirugía2, el tratamiento con láser de CO210 y diversas técnicas quirúrgicas11,12 o incluso la terapia fotodinámica3. Recientemente se ha descrito la utilidad de la NTG tópica a 2% en el tratamiento de la CNH5–7.
Existen algunos mecanismos que podrían explicar la patogenia de la CNH y la respuesta al tratamiento con NTG, tales como una vasculopatía subyacente en la que el flujo arteriolar estaría comprometido por un estrechamiento de las arteriolas del pericondrio. Determinados factores físicos, como los traumatismos de repetición o las enfermedades del espectro cardiovascular o incluso afecciones autoinmunes pueden dañar la red vascular del pericondrio13. De cualquier modo, la afectación de la red vascular auricular, ya sea causa o consecuencia de la degeneración local del tejido conectivo, es la posible explicación a los resultados satisfactorios del tratamiento de la CNH con NTG tópica en función de su potente papel vasodilatador.
Flynn et al.5 describieron por primera vez la eficacia de la NTG tópica en la CNH. En su trabajo 13 pacientes fueron tratados con NTG tópica al 2% y 12 pacientes mejoraron clínicamente. El 61,5% de los pacientes mostró una respuesta completa y el 30,8% una respuesta parcial. Dos pacientes (17%) padecieron efectos secundarios asociados al tratamiento en forma de mareo y dolor de cabeza5. Posteriormente Yelamos et al.6 describieron un caso de una mujer de 83 años que respondió al tratamiento con NTG tópica al 2% sin evidencia de recidiva un mes más tarde de finalizado el tratamiento, con buena tolerancia6. Por último, Garrido-Colmenero et al.7 publicaron una serie de 11 pacientes tratados con parches de NTG (5mg) durante 12h cada día, 2 meses, de los cuales el 63,3% mostraron una respuesta completa. Dos pacientes (18,1%) padecieron cefalea moderada, por lo que suspendieron el tratamiento y uno requirió tratamiento quirúrgico por presentar una respuesta insuficiente7.
Hasta el momento se ha comunicado la eficacia del tratamiento con NTG tópica al 2% para esta condición, pero no al 0,2%, que es una de las concentraciones que se utiliza clásicamente para el manejo de otros trastornos como las fisuras anales14 y la que decidimos recomendar a nuestros pacientes. De hecho, inicialmente, y en función de los estudios publicados en la literatura, contactamos con un laboratorio especializado en formulación magistral en el que se nos indicó que no era posible la formulación de la NTG al 2%. El principio activo se presenta en polvo al 2% y se mezcla con un excipiente para constituir la fórmula magistral. En el momento que se hace la mezcla, la concentración disminuye hasta la deseada, pero siempre es menor al 2%. Una fórmula con concentración mayor o igual al 2% podría ser inestable y la manipulación sería muy delicada. Higuero15 publicó recientemente una revisión acerca del manejo actualizado de las fisuras anales. En el apartado de los nitratos tópicos describe los datos de eficacia con concentraciones de NTG tópica variables entre 0,05% y 0,4%, pero no menciona concentraciones mayores que podrían conllevar a una toxicidad aumentada sin un claro paralelo aumento de eficacia15.
La fórmula magistral se encuentra disponible en la mayor parte de laboratorios de formulación. Se trata de una medida conservadora, no agresiva y barata en comparación con otras terapias disponibles que suelen lograr buenos resultados pero son más agresivas, como la cirugía del cartílago preservando la piel suprayacente11.
La concentración al 0,2% parece ser eficaz y bien tolerada por todos los pacientes. En nuestra serie solo un caso de los 29 incluidos en el estudio informó de cefalea postaplicación por exceso de producto. Dicho efecto adverso se resolvió reduciendo la cantidad de aplicación del producto a la capa fina estandarizada.
Previamente se ha indicado que 2 pacientes no respondieron y otro presentó escasa mejoría (reducción del dolor desde 10/10 a 8/10) tras 4 semanas de tratamiento. Todos ellos coinciden en que habían recibido tratamiento quirúrgico previo con intención diagnóstica o terapéutica. Adicionalmente, aunque la mayoría de los pacientes solía responder al tratamiento desde las primeras semanas de aplicación, desconocemos si la prolongación de la administración de la fórmula en dichos pacientes más allá del mes pudiera haber conllevado un resultado favorable. Por otro lado, resulta interesante indicar que tan solo un 11,8% de los pacientes con respuesta completa había sido intervenido previamente de la lesión y, sin embargo, esta cifra ascendía a un 70% de los pacientes con respuesta parcial. De tales datos podríamos pensar que el antecedente de una intervención quirúrgica de cualquier tipo sobre la lesión podría condicionar una respuesta menor al tratamiento tópico NTG.
Nuestro trabajo presenta la limitación de tratarse de un estudio retrospectivo y descriptivo en el que no existe un grupo control que reciba un tratamiento a base del excipiente (vaselina filante) sin el principio activo (NTG tópica al 0,2%), o que reciba otro tratamiento considerado eficaz para comparar las respuestas.
En conclusión, la NTG tópica al 0,2% se presenta como una opción terapéutica conservadora, eficaz y segura para el tratamiento de la CNH, y permite evitar la realización de una exéresis quirúrgica, en ocasiones mutilante.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.