El metotrexato (MTX) es un fármaco anti-metabolito que inhibe la síntesis del ácido fólico. Es ampliamente utilizado en dermatología, reumatología y oncología1. Aunque presenta un buen perfil de seguridad, pueden observarse efectos adversos graves como neumonitis, fibrosis hepática y aplasia medular1–3. Estudios previos sugieren que la ulceración mucosa inducida por la intoxicación por MTX puede ser un marcador de daño medular2,3. Nuestro objetivo fue recoger las características clínicas, analíticas y epidemiológicas de los pacientes afectos por mucositis por MTX.
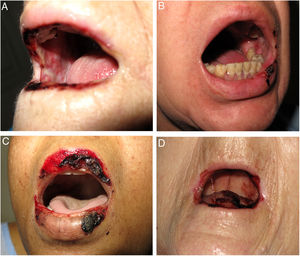
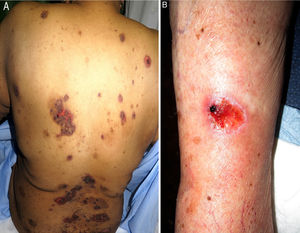
Se realizó un estudio retrospectivo de los pacientes diagnosticados de mucositis o úlceras orales por MTX valorados por el servicio de dermatología de nuestro hospital, desde enero del 2013 hasta julio del 2018. Se revisaron las historias clínicas, recogiéndose las características epidemiológicas, clínicas e iconografías. Se incluyeron 5 pacientes, un varón y 4 mujeres, con una mediana de edad de 72 años (rango: 50-90). La tabla 1 recoge sus características epidemiológicas y clínicas. La mediana de la dosis de MTX fue de 15mg/semana (rango: 10-35). La vía de administración fue subcutánea en 3/5 y oral en 2/5. En 2/5 el MTX se indicó por psoriasis y en 3/5 por artritis reumatoide. La presentación clínica fue de erosiones y costras necróticas en cavidad oral en todos los pacientes (figs. 1A-D). En 4/4 se detectó pancitopenia o bicitopenia, 2/5 presentaron fiebre y 2/5 úlceras cutáneas, uno en las placas de psoriasis y otro en un carcinoma basocelular de la pierna (figs. 2A y B). La mediana de leucocitos en sangre periférica fue de 2.475×106 (rango: 330-4.200), hemoglobina 73,5g/l (rango: 53-92), volumen corpuscular medio (VCM) 98,5fl (rango: 93-105), plaquetas 92.500×106 (rango: 37.000-128.000). La creatinina sérica estaba alterada en la mitad de los pacientes (mediana: 2,42mg/dl [rango: 0,44-5]). Solo un paciente presentó alteración del perfil hepático con elevación de GGT (156mg/dl, ref <40) y del tiempo de protrombina (INR: 1,4). Se realizó aspirado de médula ósea en 3/5, mostrando una marcada hipocelularidad, compatible con intoxicación por MTX. El desencadenante más frecuente fue el uso de antiinflamatorios no esteroideos (2/5), seguido por errores en la administración (1/5), infección (1/5) y falta de ingesta de ácido fólico (1/5). En 3/5 se midieron los niveles plasmáticos de MTX, todos estaban en niveles normales (<0,3mol/l). En cuanto al tratamiento, todos los pacientes suspendieron el MTX, en 4/5 se administró ácido folínico intravenoso y en 1/5 factor estimulador de colonias de granulocitos. Todos los pacientes (5/5) se recuperaron completamente y solo uno reinició el MTX.
Características epidemiológicas y clínicas de los pacientes con intoxicación por metotrexato y lesiones mucocutáneas
| Caso | Edad/sexo | Comorbilidades | Dosis MTX | Vía administración | Tiempo tratamiento MTX | Desencadenante | Presentación clínica | Insuficiencia renal asociada | Evolución clínica | Tratamiento | Reinicio de MTX |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 90/F | A. reumatoideHTACáncer de mama | 5mg/semana | Oral | 5 años | Error en administración(5mg/día) | Fiebre, mucositis, pancitopenia | No | RC | Suspensión MTXAc. folínico 15mg/día iv | No |
| 2 | 61/M | A. reumatoideDM2HTAIRC (crea 2) | 10mg/semana | subcutáneo | 9 años | Falta de administración de ac. fólico | Fiebre, mucositis,pancitopenia | SíClcr 25ml/min | RC | Suspensión MTXAc. folínico 15mg/día iv | Sí10mg/semana |
| 3 | 50/F | PsoriasisDM2-IDHTAIRC | 25mg/semana | subcutáneo | 25 años | Empeoramiento de la función renal por AINE | Mucositis, úlceras cutáneas, pancitopenia | SíClcr 9,8ml/min | RC | Suspensión MTXAc folínico 140mg iv y luego 50mg c/6h ivEstimulador de colonias de granulocitos | No |
| 4 | 72/F | PsoriasisDM2 | 15mg/semana | subcutáneo | Un mes | Uso de AINE | Mucositis | Desconocido | RC | Suspensión MTX | NoEtanercept |
| 5 | 81/F | A. reumatoideNeumopatía crónicaIRC | 10mg/semana | oral | Desconocido | Infección cutánea y AINE | Mucositis, úlceras cutáneas, bicitopenia | SíClcr 22ml/min | RC | Suspensión MTXAc. folínico iv (dosis no especificada) | Desconocido |
A. reumatoide: artritis reumatoide; Ac. folínico: ácido folínico; AINE: antiinflamatorios no esteroideos; Clcr: clearence de creatinina; DM2: diabetes mellitus tipo 2; DM2-IR: diabetes mellitus tipo 2 insulino-dependiente; F: femenino; HTA: hipertensión arterial; IRC: insuficiencia renal crónica; iv: intravenoso; M: masculino; MTX: metotrexato; RC: respuesta completa.
El efecto adverso grave más frecuente del MTX es la toxicidad medular, observada en el 2,5-10% de los pacientes y potencialmente letal4. La ulceración mucocutánea es un hallazgo característico en pacientes con toxicidad aguda3,5. El MTX inhibe las células con rápido recambio celular, como las células hematopoyéticas y cutáneas, más propensas a afectarse por su acción anti-proliferativa6. El MTX es eliminado del organismo principalmente por filtración glomerular, y una pequeña fracción es metabolizada en el hígado. Debido a esto, disminuciones en el filtrado glomerular secundarias a deshidratación, infecciones, fármacos como AINE u otros, pueden ocasionar acumulación del MTX y toxicidad3,7. En nuestro estudio la mayoría de los pacientes presentó disminución de la función renal (3/4), y en 3/5 se asoció a ingesta de AINE. Esto concuerda con los estudios previos, donde las causas más frecuentes de intoxicación por MTX fueron errores en la dosificación, insuficiencia renal, interacciones farmacológicas (AINE, antibióticos o salicilatos), reinicio o aumentos de dosis de MTX2,3,5,7.
Todos los individuos de nuestro estudio con analíticas disponibles (4/4) presentaron pancitopenia o bicitopenia, y 2 requirieron antibioticoterapia empírica por neutropenia febril. Estos hallazgos subrayan el complejo manejo requerido, las potenciales complicaciones y la necesidad de una alta sospecha clínica en pacientes con MTX que presenten úlceras mucocutáneas, especialmente si tienen factores de riesgo que puedan disminuir el filtrado glomerular2,3. Un signo precoz de afectación medular por déficit de folatos puede ser la elevación del VCM (presente en 2 de nuestros pacientes). En 3 de los pacientes con mucositis y pancitopenia en que se determinaron los niveles séricos de MTX, estos eran bajos. Esto se explica por la acumulación del MTX a nivel celular. Las concentraciones plasmáticas usualmente son 0,01M a las 24h después de suspender el fármaco, no existiendo una buena correlación entre los niveles séricos del MTX y su toxicidad7.
Las úlceras cutáneas por MTX han sido descritas mayoritariamente en pacientes con psoriasis o daño previo2,5, como fue el caso de 2 de nuestros pacientes (psoriasis y carcinoma basocelular), aunque también se han observado en piel sana.
La intoxicación por MTX puede cursar con una elevada morbimortalidad3. En pacientes en tratamiento con MTX la aparición de úlceras mucocutáneas debe alertar sobre la posible presencia de pancitopenia y de insuficiencia renal, aun cuando las dosis del fármaco sean bajas y los niveles séricos del fármaco normales. Estos individuos deben ser ingresados y tratados por un equipo multidisciplinario.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.