La leflunomida es un fármaco inmunosupresor aprobado por la Food and Drug Administration (FDA) para el tratamiento de la artritis reumatoide y la artritis psoriásica. Además, es un fármaco ampliamente utilizado en otras enfermedades fuera de ficha técnica, como la espondilitis anquilosante o el lupus eritematoso sistémico (LES). La leflunomida puede producir algunos efectos secundarios y los más frecuentes son los síntomas gastrointestinales, la hipertensión o la alopecia. A pesar de que la leflunomida se considera un fármaco eficaz y seguro para el tratamiento de los pacientes con LES, se han publicado casos en los que se ha asociado con erupciones cutáneas como el eritema multiforme1, la necrólisis epidérmica tóxica2, vasculitis3, o incluso ha actuado como un desencadenante de las lesiones cutáneas de un lupus eritematoso subagudo4.
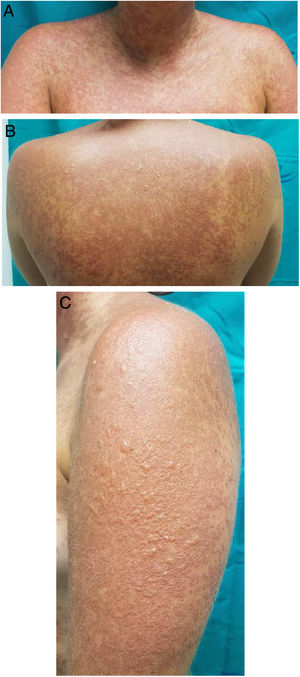
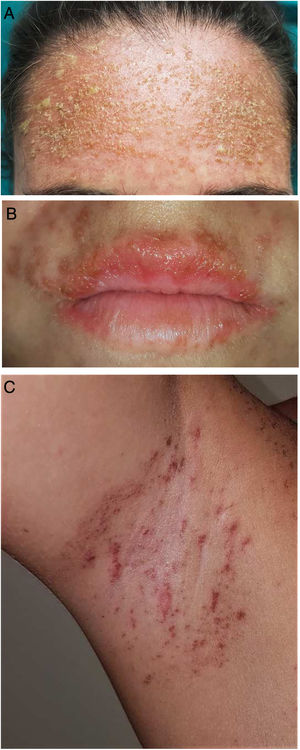
Una mujer de 25 años estaba en seguimiento por el Servicio de Reumatología tras el diagnóstico de un lupus eritematoso sistémico de cuatro años de evolución. Entre los criterios diagnósticos de la paciente no se registró la existencia de antecedentes de fotosensibilidad. El tratamiento inicial fue con rituximab (500 mg cada 15 días, dos sesiones), prednisona oral en dosis decrecientes y metotrexato subcutáneo (17,5 mg semanales). A los tres meses de iniciar el tratamiento con metotrexato, debido a los efectos secundarios gastrointestinales, fue sustituido por leflunomida (tres dosis diarias de 100 mg, seguidas de una dosis de mantenimiento de 20 mg al día). Dos meses después de iniciar el tratamiento con leflunomida, y tras una exposición solar intensa en la playa, la paciente acudió en las primeras 24 h por el desarrollo de una erupción máculo-papular generalizada muy pruriginosa (fig. 1A-B), que en 48 h evolucionó a lesiones vesículo-ampollosas, principalmente en los brazos (fig. 1C), asociada con pústulas en la región frontal (fig. 2A), vesículas en área labial (fig. 2B), y máculo-pápulas de aspecto equimótico en ambas axilas (fig. 2C). La exploración de la mucosa oral y genital fue normal. El estudio analítico mostró unos títulos elevados para ANA (1/640 U/mL), anti-SSA/Ro-60 (157), anti-SSA/Ro-52 (167) y factor reumatoide (80 U/mL). El resto de parámetros, incluido el complemento C3 y C4, mostraron niveles normales. El estudio serológico (VHS, CMV, VEB, VHH-6) fue negativo. El estudio histológico de una biopsia en sacabocados de una lesión ampollosa en tronco posterior mostró una epidermis atrofiada con focos de queratinocitos necróticos, espongiosis, con la formación ampollosa subepidérmica y la presencia de un infiltrado mononuclear perivascular inflamatorio moderado de linfocitos y eosinófilos localizado en la dermis, compatible con una erupción fototóxica. El estudio con inmunofluorescencia directa (IFD) fue negativo. Se indicó la interrupción del tratamiento con leflunomida, e inició el tratamiento sistémico con prednisona oral (1 mg/kg/día). A los 10 días la paciente mostró una resolución completa de las lesiones con una hiperpigmentación residual.
Los pacientes con LES asocian una especial sensibilidad a la exposición solar, considerándose un factor desencadenante o agravante de la enfermedad. En raras ocasiones, se realiza el diagnóstico de LES sin que entre los criterios se encuentre la fotosensibilidad. Entre los diferentes tratamientos utilizados en el LES, la leflunomida no es de primera línea, por lo que se usa en ciertos pacientes que sufren efectos secundarios relacionados con otros medicamentos, como el metotrexato. Hay en la literatura múltiples artículos que atribuyen a la leflunomida la inducción de lesiones de un lupus eritematoso subagudo cutáneo (LESC) de manera exclusiva5, LESC asociado con lesiones tipo eritema multiforme, o bien eritema multiforme major. A pesar de considerarse un tema controvertido, algunos autores defienden que la coexistencia de lupus eritematoso y eritema multiforme en un mismo paciente debería diagnosticarse como un síndrome de Rowell. De hecho, Zeitouni et al.6 en el año 2000 definió los nuevos criterios para realizar el diagnóstico del síndrome de Rowell. Aunque nuestra paciente cumplió con los criterios suficientes para poder ser diagnosticada de este síndrome, nuestra principal sospecha fue una erupción fototóxica por leflunomida. A los dos meses de resolverse el cuadro clínico, se le realizaron las pruebas epicutáneas con la serie europea de fotoparche (Chemotechnique Diagnostics, Vellinge, Sweden) y el preparado con leflunomida al 1, 5 y 10% en vaselina, con irradiación de UVA 10 J/cm2. La lectura a los 30 min, 48 y 96 h fue negativa.
Entendemos que las erupciones fotosensibles en pacientes con LES son frecuentes, y que están incluidas dentro de los criterios diagnósticos. Sin embargo, con este caso clínico pensamos que algunos de los fármacos utilizados en esta enfermedad podrían jugar un papel relevante a la hora de desencadenar una erupción fototóxica o fotoalérgica. Diferenciar clínicamente una erupción fototóxica de una erupción fotosensible por el propio LES puede resultar difícil. El estudio histopatológico podría diferenciar a los pacientes con un verdadero LES (donde observaremos en la IFD depósitos de IgM y C3 en la unión dermoepidérmica), hallazgos ausentes en la erupción fototóxica. La realización del fotoparche debe plantearse como prueba complementaria, con el objetivo de diferenciar las reacciones fototóxicas de las fotoalérgicas. Entre los hallazgos analíticos, la positividad a anticuerpos anti-SSA/Ro podría considerarse un factor de riesgo para desarrollar un LES inducido por fármacos7. Por otro lado, los anticuerpos antihistona aparecen en más del 95% de los casos de LES inducido por fármacos, sin embargo, también pueden observarse hasta en el 50-70% de los pacientes con LES no inducido por fármacos. En nuestra paciente, los anticuerpos antihistona fueron negativos, dato que nos orienta hacia la sospecha clínica inicial, una erupción fototóxica.
En conclusión, pensamos que ante pacientes con características similares al caso descrito, dentro del diagnóstico diferencial deberían incluirse las erupciones fotosensibles por fármacos, sobre todo tras el inicio de tratamientos, como en este caso, con leflunomida. La realización de pruebas complementarias es fundamental para alcanzar un diagnóstico adecuado, considerando las pruebas epicutáneas (y fotoparche) como una de ellas.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.