La eritrodermia es un síndrome inflamatorio de la piel caracterizado por descamación y eritema en más del 90% de la superficie corporal. Representa la etapa final de muchas enfermedades dermatológicas en el adulto. La causa más frecuente es la psoriasis, le siguen las enfermedades eccematosas, las reacciones medicamentosas, la pitiriasis rubra pilaris y los linfomas cutáneos de células T. El abordaje diagnóstico debe incluir una historia y examen físicos exhaustivos. Si se desconoce la etiología de la eritrodermia es posible que múltiples biopsias a lo largo del curso de la enfermedad aumenten las posibilidades de un diagnóstico correcto. El abordaje inicial de la eritrodermia debe incluir la evaluación de un experto en nutrición, la valoración del balance hidroelectrolítico, medidas para mantener la función de barrera de la piel, antihistamínicos con efecto sedante y la exclusión de infecciones bacterianas secundarias. Presentamos una revisión práctica de la etiología, diagnóstico y tratamiento de esta entidad.
Erythroderma is an inflammatory skin syndrome that involves desquamation and erythema of more than 90% of the body surface area. It represents a final clinical endpoint for many adult dermatological conditions. The most frequent cause of erythroderma is psoriasis followed by eczematous conditions, drug-induced reactions, pityriasis rubra pilaris and cutaneous T-cell lymphomas. Diagnostic approach must include a thorough history and clinical examination. If the etiology of erythroderma is uncertain multiple skin biopsies may enhance diagnostic accuracy. The initial management of erythroderma must include a nutrition expert evaluation, fluid imbalance assessment, maintaining skin barrier function, sedative antihistamines and exclusion of secondary bacterial infection. We present a practical review of the etiology, diagnosis, and treatment of this entity.
La eritrodermia es el hallazgo clínico de eritema generalizado y descamación de la piel. Es potencialmente mortal, en especial cuando es fulminante, y se ha asociado con una alta mortalidad en pacientes hospitalizados1,2. En 1868 Ferdinand von Hebra en su trabajo «Sobre las enfermedades de la piel», emplea por primera vez el término eritrodermia para describir el enrojecimiento y descamación generalizada de la piel3. Está causada por una amplia variedad de enfermedades y factores exógenos. Aunque es poco frecuente, mantiene su interés por la dificultad que supone a los dermatólogos su tratamiento. El objetivo de este artículo es revisar los principios generales, los aspectos clínicos y la patogenia de la eritrodermia en adultos, así como proporcionar una guía concisa para su abordaje diagnóstico y terapéutico.
DefiniciónLa eritrodermia, también conocida como dermatitis exfoliativa generalizada o eritrodermia exfoliativa, es un síndrome cutáneo inflamatorio grave caracterizado por eritema y descamación generalizada que afecta a una extensión ≥ 90% de la superficie cutánea4. El término de elección para referirnos a este síndrome es el de eritrodermia4,5. Anteriormente, algunos autores usaron el término «síndrome del hombre rojo» para referirse a la eritrodermia idiopática (que no debe confundirse con la reacción cutánea asociada a la administración intravenosa rápida de vancomicina)6.
EpidemiologíaSe trata de un cuadro poco frecuente. La mayoría de los estudios son retrospectivos y no abordan el tema de la incidencia global7,8. Un estudio retrospectivo realizado en China estableció que 13 de cada 100.000 pacientes dermatológicos presentan eritrodermia9. Recientemente, un estudio retrospectivo portugués comunicó una incidencia de 9,4 casos/año10. Si excluimos a los niños, la edad media de presentación se encuentra entre los 41 a los 61 años, aunque por lo general suele afectar a pacientes mayores de 45 años11,12. Los estudios se inclinan por un predominio en los varones con una proporción hombre-mujer de 2-4: 1.
PatogeniaLos mecanismos patogénicos implicados dependen de la causa subyacente. Sigue siendo objeto de debate cuáles son las vías fisiopatogénicas que comparten las distintas etiologías6. Se cree que este síndrome procede de una interacción compleja entre las citoquinas y las moléculas de adhesión celular. La IL-1, IL-2, IL-8, la molécula de adhesión intercelular-1 (ICAM-1), el factor de necrosis tumoral y el interferón gamma son moléculas que se han relacionado con la patogenia de la eritrodermia4,7,8. La interacción entre estas citoquinas se traduce en un aumento de la división de las células epidérmicas. Al aumentar la tasa mitótica, el tiempo de tránsito de las células a través de la epidermis se acorta y se produce la exfoliación. Las escamas contienen aminoácidos, proteínas y ácidos nucleicos que se pierden con la descamación13,14. Se ha calculado que este proceso de descamación puede aumentar la pérdida de proteínas entre un 25-30% en los casos de eritrodermia psoriásica, y entre un 10-15% en otras etiologías14.
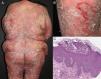
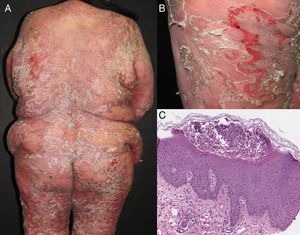
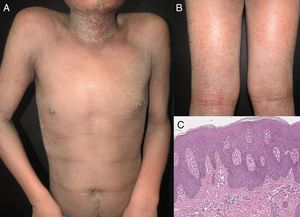
EtiologíaLa eritrodermia representa la etapa final de muchas enfermedades dermatológicas15. Como se ha visto en un estudio retrospectivo reciente, la incidencia relativa de etiologías distintas puede variar entre las poblaciones por diferencias genéticas, geográficas y sociales10. La mayoría de los estudios señalan que la eritrodermia suele asociarse a una exacerbación de una dermatosis preexistente; esta es la razón por la que el historial médico del paciente es crucial para alcanzar un diagnóstico correcto. La causa más frecuente de eritrodermia es la psoriasis, representando el 25-50% de los casos según algunos estudios (fig. 1)10,16,17. La mayoría de los pacientes tienen historia de enfermedad localizada previa a la instauración de la eritrodermia, que se desarrolla con mayor frecuencia en pacientes con psoriasis de larga evolución (de más de 10 años tras el diagnóstico)9,10,18,19. La eritrodermia psoriásica se ha relacionado con ciertos desencadenantes, incluyendo la supresión brusca de los corticosteroides tópicos o sistémicos y el metotrexato, la fototoxicidad o la infección sistémica20.
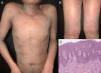
Se ha reportado que la dermatitis exfoliativa relacionada con la dermatitis atópica varía en frecuencia entre 4,76 y 23,9% (fig. 2)17,21. Se ha descrito un historial de eccema no atópico en un 5,12-25,3% de los pacientes con eritrodermia22–24. En series de casos, las reacciones medicamentosas representan la segunda causa más frecuente de eritrodermia, oscilando entre el 11,3 y el 21,6% de los casos9,10,18. La lista de fármacos causantes de eritrodermia es larga y crece de forma continua. Según algunos autores los medicamentos antiepilépticos y el alopurinol son los fármacos con mayor capacidad para desencadenar eritrodermia9,10,18,20. La carbamacepina es el fármaco antiepiléptico más comúnmente relacionado con este síndrome, y se han propuesto como posibles causas bien una susceptibilidad genética o bien su frecuente prescripción11. Los antituberculosos se han relacionado con la eritrodermia en pacientes VIH-seropositivos25,26, así como con el uso de hierbas tradicionales chinas como analgésicos9,27. Otros fármacos frecuentemente relacionados con esta enfermedad son: la fentoína, los betalactámicos, las sulfonamidas, el fenobarbital, la sulfasalacina, y los inhibidores de la bomba de protones10,28. También se ha descrito como inductores de la eritrodermia los materiales de contraste no iónico29. La dermatitis exfoliativa se ha relacionado con una forma grave de pitiriasis rubra pilaris en un 1,25-8,2% de los casos11,22.
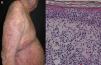
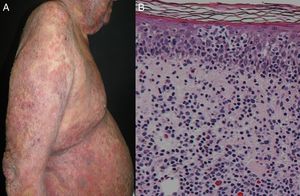
La etiología neoplásica o paraneoplásica representa en la mayoría de las series el 1% de los casos de eritrodermia8,21,30,31. Se le han implicado los cánceres de laringe, tiroides, mama, pulmón, esofágo, estómago, hígado, lengua, vesícula biliar, colon, trompas de Falopio y próstata4,9,32-40; aunque se ha relacionado más frecuentemente con neoplasias hematológicas y linfomas cutáneos de células T, que representan del 25 al 40% de los casos asociados a malignidad4. Dentro de este subgrupo, la micosis fungoides (fig. 3), y el síndrome de Sézary son los más frecuentes41,42. También se han involucrado la leucemia aguda y crónica, el sarcoma de células reticulares y las histiocitosis malignas10,43,44.
En un 6,51 a un 36% de los pacientes, no se logra identificar la etiología con precisión45. Algunos autores han descrito la progresión de la eritrodermia idiopática crónica al linfoma cutáneo de células T17. Como causas poco frecuentes de la dermatitis exfoliativa del adulto tenemos las ictiosis congénitas6, síndrome de piel escaldada por estafilococo6, enfermedades ampollosas autoinmunes46, patologías del tejido conjuntivo como la dermatomiositis47, dermatitis actínica crónica48, sarcoidosis49, sarna noruega50, histiocitosis de células de Langerhans51, radiodermitis, enfermedad de injerto contra huésped, papuloeritrodermia de Ofuji y síndrome de Omenn52-57.
Manifestaciones clínicasLa eritrodermia se presenta de manera gradual e insidiosa, excepto en los casos de origen medicamentoso22. Este trastorno comienza como placas de eritema que se extienden y se fusionan hasta que finalmente afectan a casi toda la superficie de la piel. Se asocia a un grado variable de descamación que aparece típicamente a los 2-6 días tras la aparición del eritema. La piel suele aparecer de color rojo brillante, seca, caliente e indurada. La mayoría de los pacientes se quejan de dolor o prurito. En las fases agudas, las escamas son grandes y de aspecto costroso, mientras que en los estadios crónicos tienden a ser de menor tamaño y más secas4,12. El tipo de escama puede orientar a la etiología subyacente: las escamas finas suelen encontrarse en enfermedades eccematosas, las escamas costrosas en enfermedades ampollosas, las escamas exfoliativas en reacciones medicamentosas y las escamas oleosas en la dermatitis seborreica6. En la eritrodermia crónica, los pacientes pueden desarrollar erosiones costrosas y liquenificación secundaria a rascado intenso. También puede aparecer hiper- o hipopigmentación. Las uñas pueden aparecer engrosadas, secas, frágiles, brillantes y con crestas4,12. El estudio clínico de Mahabaleshwar et al. reportó los siguientes cambios en las uñas de los pacientes con eritrodermia: decoloración (40%), crestas (36%), depresiones puntiformes (20%), onicólisis (18%), uñas brillantes (4%) y paroniquia (2%)18. Aproximadamente el 30% de los pacientes presentan queratodermia palmoplantar. La queratodermia palmoplantar se ha asociado clásicamente a la pitiriasis rubra pilaris, sin embargo, algunos estudios han encontrado que la queratodermia palmoplantar y los cambios en las uñas son signos clínicos predictivos de psoriasis6,9,10,20,23. Algunos síndromes hematológicos raros, como el síndrome hipererosinofílico idiopático, pueden mostrar manifestaciones clínicas similares a la eritrodermia psoriásica58.
La pitiriasis rubra pilaris muestra típicamente islas de piel respetada, queratodermia palmoplantar anaranjada y pápulas foliculares hiperqueratósicas en las superficies extensoras59. La aparición de pápulas violáceas y lesiones reticuladas de la mucosa oral pueden indicar un diagnóstico subyacente de liquen plano60. En los pacientes con sarna noruega se pueden desarrollar costras gruesas en las palmas y plantas, así como hiperqueratosis subungueal50,59. Las pápulas de Gottron, la erupción en heliotropo, la poiquilodermia, las telangiectasias periungueales y la debilidad muscular pueden orientar al diagnóstico de dermatomiositis eritrodérmica61,62. La aparición de lesiones húmedas y costrosas en la cara y tronco superior puede ser una manifestación temprana de pénfigo foliáceo. El 20% de los pacientes con eritrodermia crónica pueden presentar alopecia no cicatricial. En la eritrodermia crónica secundaria al síndrome de Sézary son especialmente importantes las complicaciones oftalmológicas como el ectropión bilateral y la conjuntivitis purulenta6. Algunos estudios han descrito el «signo de la nariz» caracterizado por piel respetada en la nariz y las áreas paranasales63.
Manifestaciones sistémicasLos pacientes con eritrodermia presentan temblores con frecuencia y se quejan de sensación de frío. Cesar et al. identificaron recientemente el prurito como el síntoma más común10. También puede haber una linfadenopatía periférica generalizada que hace necesario un análisis histológico y molecular para poder descartar neoplasias hematológicas. También se han descrito los siguientes síntomas: edema facial, podal o pretibial; hipotermia, caquexia, hepatomegalia, esplenomegalia6,10 y fiebre en aproximadamente la mitad de los pacientes10,27.
Las manifestaciones sistémicas deben ser vigiladas ya que podrían complicar la evolución de la enfermedad. La dermatitis exfoliativa puede dar lugar a complicaciones sistémicas como alteraciones del equilibrio electrolítico, insuficiencia cardiaca de alto gasto, síndrome de distrés respiratorio agudo e infecciones secundarias (la piel eritrodérmica suele ser colonizada por Staphylococcus aureus)6,64-67. La sepsis por estafilococo puede estar asociada a la inflamación y escoriación de la piel, en especial en pacientes VIH positivos o con una malignidad hematológica subyacente68,69.
HistopatologíaEn los pacientes con eritrodermia puede ser difícil establecer una correcta correlación clínico-patológica22. Patólogos experimentados pudieran dar un diagnóstico preciso10. Por lo general, las muestras de piel se obtienen a partir de biopsias en sacabocado de 4mm, y la toma de múltiples biopsias a lo largo del tiempo mejora la precisión diagnóstica64. Según algunos estudios, las biopsias resultan útiles en un 53-66% de los casos de eritrodermia10,70,71. Con frecuencia se encuentran los siguientes hallazgos histopatológicos: hiperqueratosis, acantosis, espongiosis e infiltrado inflamatorio perivascular72. En el estudio retrospectivo de Megna et al. llevado a cabo con 82 pacientes con eritrodermia el 23,2% de estos fueron diagnosticados con psoriasis, fuertemente apoyado por la presencia de acantosis, paraqueratosis difusa, hipogranulosis difusa y la presencia de neutrófilos en la epidermis y la dermis. Se identificó dermatitis espongiótica en el 20,7% de los pacientes, observándose exocitosis, infiltrado linfocítico superficial, espongiosis, acantosis irregular e infiltrado eosinofílico en la dermis. Se diagnosticó eritrodermia inducida por fármacos en un 8,5% de los individuos, cuyas biopsias mostraron linfocitos y cuerpos coloidales, además de vacuolización en la capa basal de la epidermis. En el caso del linfoma cutáneo de células T (LCCT)/micosis fungoide (8,5% en este estudio) las biopsias revelaron microabscesos de linfocitos, además de la presencia de linfocitos atípicos en la dermis y la epidermis. Es importante destacar que en un número amplio de casos (39,1%) el diagnóstico histopatológico no fue concluyente y no coincidió con el diagnóstico final73. Todos estos resultados sugieren que las biopsias cutáneas son un primer paso obligatorio en el estudio de estos pacientes.
En la mayoría de los estudios se señala la presencia de linfadenopatías dermopáticas en las biopsias de los ganglios linfáticos10,27,74. La biopsia ganglionar puede ser la clave para realizar el diagnóstico de linfomas o enfermedades poco comunes, como sucede con la enfermedad de Castleman multicéntrica75. La observación de linfocitos atípicos debe conducir a la realización de pruebas de inmunohistoquímica y de reordenamiento del gen del receptor de células T. El síndrome de Sézary está caracterizado por la presencia de células T que carecen de los antígenos de las células T maduras (CD3+, CD4+, CD7-) y en el reordenamiento clonal del gen receptor de células T76. Cuando los estudios histopatológicos sugieran enfermedad inmunobullosa, o enfermedad injerto contra huésped o patologías del tejido conjuntivo, se deberá considerar la conveniencia de realizar pruebas de inmunofluorescencia.
Laboratorio e imagenPor lo general, los hallazgos de laboratorio son inespecíficos. Las alteraciones que con más frecuencia se describen en estudios previos (ordenados según su frecuencia) incluyen: velocidad de sedimentación eritrocitaria elevada (96,1%), leucocitosis (48,5%), eosinofilia (39,8%) y anemia (30,1%)10. En el caso de enfermedades alérgicas los niveles séricos de IgE pueden estar aumentados. Ante la sospecha de eritrodermia inducida por fármacos, principalmente ante un síndrome DRESS, es necesario realizar un recuento de eosinófilos7,31,47,77,78. Un estudio reciente encontró la existencia de una correlación entre la presencia de eosinofilia y la eritrodermia relacionada con malignidad10. También podemos encontrar altos los niveles de ácido úrico y de creatinina, así como una reducción en los niveles de proteínas séricas17,22. Los electrólitos séricos se pueden utilizar para monitorizar la pérdida de líquidos. Las pruebas de funcionalidad hepática y renal pueden estar alteradas en eritrodermia asociada a reacciones medicamentosas graves. Para diagnosticar el síndrome de Sézary es necesario realizar pruebas específicas como el recuento de células de Sézary79. Entre las posibles pruebas para la detección de las enfermedades del tejido conjuntivo se encuentran los anticuerpos antinucleares, el antígeno nuclear extraíble, el factor reumatoide, los anticuerpos anti-ADN y los niveles de complemento. En pacientes con eritrodermia pertenecientes a poblaciones de alto riesgo puede ser obligatorio realizar las pruebas del virus HIV80.
Pudiera ser necesario realizar múltiples hemocultivos que permitan excluir una sepsis estafilocócica, ya que los hemocultivos se pueden contaminar con estafilococos cutáneos66. Ante la sospecha de superinfecciones puede resultar útil realizar cultivos frente a hongos, y pruebas de la PCR para la detección de los virus herpes simplex y varicela zóster. En el caso de la escabiasis se puede realizar un estudio microscópico de raspados de las zonas de piel afectada50. Los estudios de imagen como la radiografía de tórax, la tomografía axial computarizada y la resonancia magnética pueden ser útiles en el diagnóstico de la eritrodermia paraneoplásica.
DiagnósticoAl tratarse de una entidad sindrómica, el diagnóstico de la eritrodermia se realiza con facilidad mediante la identificación del eritema generalizado y de la descamación de una superficie corporal ≥ 90%4. Lo que supone un reto para los médicos es determinar la enfermedad subyacente, y debe incluir una correlación clínico-patológica minuciosa. Describimos los principales diagnósticos diferenciales en la tabla 1.
Características de las causas comunes de eritrodermia en adultos
| Etiología | Frecuencia reportada | Clínica | Claves para el diagnóstico | Dermatoscopia | Histopatología |
|---|---|---|---|---|---|
| Psoriasis | 25 - 50% | Placas psoriásicas previas, queratodermia palmoplantar, cambios en uñas, artritis, afectación cuero cabelludo, características similares a dermatitis seborreica | -Causa más común -Psoriasis de larga duración (más de 10 años desde el diagnóstico) -Suspensión de corticoesteroides sistémicos o tópicos (uso prolongado), metotrexato o ciclosporina | Escamas blanquecinas, vasos punteados, fondo rojizo homogéneo regularmente dispuesto | Hiperplasia epidérmica psoriasiforme con paraqueratosis confluente en capas con neutrófilos, hipogranulosis y vasos papilares dilatados y tortuosos, microabscesos de Munro, pústulas espongiformes de Kogoj |
| Dermatitis espongióticas | 5,12% - 25,3% | Escamas delgadas, liquenificación, picor intenso, piel exudativa, pápulas y placas eritematosas | Buscar historial de: - Dermatitis atópica (9%) - Dermatitis de contacto (6%) - Dermatitis seborreica (4%) | Dermatitis atópica: escamas amarillentas / costra serosa, Vasos con puntos distribuidos de forma irregular | Infiltrado dérmico perivascular superficial con eosinófilos, espongiosis suprayacente |
| Medicamentosa | 11,3 – 21,6% | Escama exfoliativa precedida por erupción morbiliforme, edema facial, prurito | -Buscar consumo de antiepilépticos, alopurinol, beta-lactámicos, sulfonamidas, hierbas Chinas, AINE -Se suele resolver 2-6 semanas tras la interrupción del fármaco responsable -Eosinofilia -Aumento enzimas hepáticas -Aumento creatinina | Infiltrado perivascular con eosinófilos, dermatitis de interfase con queratinocitos necróticos | |
| Pitiriasis rubra pilaris | 1,25% - 8,2% | Pápulas hiperqueratósicas foliculares, islas de piel respetada, queratodermia palmoplantar anaranjada | -Diseminación cefalocaudal -Aparición aguda -Sexta década de la vida -Ectropión | Escamas blanquecinas, manchas anaranjadas, vasos dispersos punteados, islas de piel respetada | Hiperplasia epidérmica con ortoqueratosis alternante horizontal y vertical y paraqueratosis, tapones foliculares con «paraqueratosis en hombros» |
| Linfoma de células T (sindrome de Sézary sindrome y micosis fungoides) | 1% | Queratodermia palmoplantar fisurada dolorosa, prurito intenso, hepatoesplenomegalia, uñas hipertróficas, ectropión | -Linfadenopatía -Alopecia -Facies leonina -Hepatoesplenomegalia -Sangre periférica: células de Sézary (núcleos cerebriformes), CD4:CD8 relación de 10 o más | Micosis fungoides: vasos serpiginosos con forma de espermatozoide, fondo blanquecino-rosado | Linfocitos con núcleos atípicos, conglomerado de células atípicas en la epidermis, población de células T clónicas, espongiosis mínima, pueden mostrar un infiltrado inflamatorio inespecífico |
| Otras etiologías | |
|---|---|
| Dermatofitosis | • Buscar uso crónico de corticosteroides tópicos. • Hifas en el estrato córneo |
| Sarna noruega | • Túneles, nódulos en genitales, escama en espacios interdigitales, placas costrosas generalizadas, uñas engrosadas, queratodermia |
| Liquen plano | • Buscar pápulas violáceas pruriginosas con predilección por por las extremidades |
| Enfermedades inmunobullosas | • Ampollas, erosiones y úlceras |
| Dermatomiositis | • Pápulas de Gottron, signo del heliotropo, poiquilodermia • Debilidad muscular |
| Paraneoplásica | • Pérdida de peso |
La eritrodermia es una urgencia dermatológica y los casos graves requieren ingreso hospitalario80,81. Tanto la aproximación diagnóstica inicial como los principios generales del tratamiento de la eritrodermia se describen detalladamente en la figura 4. El abordaje terapéutico debería incluir la interrupción de cualquier medicamento que resulte innecesario y un examen adecuado dirigido a excluir cualquier tipo de malignidad subyacente. El reposo en cama y la sedación deben usarse cuando sean necesarios. El tratamiento inicial de todos los tipos de eritrodermia es similar, aun cuando no se disponga del diagnóstico etiológico. Es preciso controlar la temperatura ambiental ya que estos pacientes muestran una pérdida de las funciones homeostáticas corporales termorreguladoras que previenen el enfriamiento o el sobrecalentamiento80. La función de barrera de la piel puede mejorarse mediante baños coloides y compresas húmedas sobre una superficie no mayor a una cuarta parte del cuerpo a la vez80, acompañado con cremas emolientes y corticosteroides tópicos de baja potencia82. No se recomiendan los corticosteroides tópicos de alta potencia o el tacrólimus tópico ya que la absorción sistémica se ve reforzada por una mayor permeabilidad de la piel83,84. El abordaje terapéutico inicial debe incluir también valoración nutricional e hidroelectrolítica tal y como se describe en la figura 4.
Abordaje diagnóstico inicial y principios generales de manejo de los pacientes con eritrodermia. ANAs: anticuerpos antinucleares; BID: bis in die (dos veces al día); ej.: por ejemplo; HC: hemograma completo; IFI: inmunofluorescencia indirecta; IMC: índice de masa corporal; PET-CT: tomografía por emisión de positrones-tomografía computarizada; PO: per os (vía oral); QID: quarter in die (4 veces al día); QD: quaque die (una vez al día); SCT: área de superficie corporal total; VIH: virus de la inmunodeficiencia humana. Fuentes y comentarios: 1.- Scarisbrick et al.91. 2.- NICE: Guía clínica para el soporte nutricional en adultos (actualización de 2017)92. 3.- Criterios de hipovolemia: presión sanguínea sistólica <100mmHg, frecuencia cardiaca> 90 lpm, tiempo de relleno capilar> 2 segundos, frecuencia respiratoria> 20 respiraciones por minuto, maniobra de elevación pasiva de las piernas que sugiera respuesta a volumen93. 4.- Para el manejo adicional de fluidos IV: NICE: guía clínica para la terapia intravenosa en adultos hospitalizados (2013)93. 5.- Martínez-Morán et al.81. 6.- Kanthraj et al.14. 7.- Eichenfield et al.94. 8.- Stevens et al.95.
Los antihistamínicos con efecto sedante intramusculares o intravenosos pueden disminuir el prurito previniendo de esta forma infecciones cutáneas secundarias al rascado y al mismo tiempo mitigando la ansiedad del paciente (p. ej. clorhidrato de hidroxicina, 25-50mg P.O. QID)82.
Son pocos los datos basados en evidencia que permitan establecer recomendaciones para el tratamiento de la eritrodermia psoriásica. Un panel de expertos sugiere que la ciclosporina (evidencia IIB) o el infliximab (evidencia IIB) podrían ser los agentes con efecto más rápido. Otros tratamientos de primera línea de elección son la acitretina (evidencia IB) o el metotrexato (evidencia III), si bien actúan de forma más lenta. Una segunda línea de tratamiento basada en series de casos es el etanercept (evidencia IIB). El uso de corticosteroides tópicos es controversial ya que su suspensión puede precipitar un brote de eritrodermia. La evidencia de estas recomendaciones se estableció teniendo en cuenta los niveles de evidencia de Shekelle et al.85.
Los tratamientos de primera línea en pacientes adultos con dermatitis atópica grave, especialmente después de fallar el tratamiento tópico, incluyen la fototerapia UVB de banda ancha (evidencia IIB) o la inmunosupresión sistémica. Se ha valorado el uso de la ciclosporina oral en ensayos aleatorizados y revisiones sistemáticas, representa un tratamiento a corto plazo adecuado (evidencia I-IIB). La evaluación de los niveles de evidencia de estas recomendaciones se hizo usando la escala Strenght of Recommendation Taxonomy (SORT)86. Recientemente diferentes ensayos clínicos aleatorizados han probado que el tratamiento con dupilumab, antagonista del receptor alfa de la interleucina 4 (IL-4), puede ser una alternativa terapéutica sistémica frente a dermatitis atópica grave de larga duración en adultos87.
Las recomendaciones para el tratamiento de la pitiriasis rubra pilaris se basan solamente en reportes de casos y en pequeñas series; aún no hay disponibles ensayos clínicos aleatorizados. Como terapia de primera línea tenemos los retinoides orales y el metotrexato. En terapias de segunda línea están los inhibidores del factor de necrosis tumoral alfa (anti-TNF-α), los esteroides sistémicos, la ciclosporina o la azatioprina88,89. En aquellos pacientes con eritrodermia idiopática en los que han fallado los tratamientos tópicos se pueden emplear regímenes terapéuticos empíricos tales como corticosteroides sistémicos u otros inmunosupresores como el metotrexato y la ciclosporina. Sin embargo, la evidencia de este tipo de abordaje terapéutico es escasa9,11,20,45.
En la tabla 2 se describen los regímenes terapéuticos específicos frente a las causas comunes de la eritrodermia.
Regímenes terapéuticos específicos para eritrodermia de etiología conocida
| Etiología | Tratamiento | Dosis | Contraindicaciones absolutas | Contraindicaciones relativas importantes |
|---|---|---|---|---|
| Psoriasis | Ciclosporina (primera línea) | Dosis media inicial 4 mg/kg/día, reducir gradualmente tras la remisión 0,5 mg/kg cada 2 semanas | Función renal reducida, hipertensión incotrolada, hipersensibilidad, malignidad activa | Hipertensión controlada, edad <18 años o> 64 años, infección activa, vacuna viva atenuada, inmunodeficiencia, embarazo (C), fármaco inmunosupresor concomitante |
| Infliximab (primera línea) | 5 mg/kg i.v. en las semanas 0, 2, 6, y posteriormente cada 8 semanas | Hipersensibilidad, infecciones activas, uso concomitante de anakinra | Insuficiencia cardíaca congestiva, antecedentes familiares de enfermedad desmielinizante, aumento del riesgo de malignidad | |
| Acitretina (primera línea, acción lenta) | 0,3–0,75 mg/kg | Embarazo (X), lactancia, incumplimiento de la anticoncepción | Leucopenia, disfunción hepática o renal, dislipidemia, hipotiroidismo | |
| Metotrexato (primera línea, acción lenta) | 7,5–15 mg/semana | Embarazo (X) y lactancia | Enfermedad hepática, función renal disminuida, inmunodeficiencia, anomalía hematológica grave, enfermedad infecciosa activa o posible reactivación de la tuberculosis | |
| Etanercept | 50mg subcutáneo dos veces a la semana, reducir a 50 mg/semana después de 3 meses | Hipersensibilidad, infecciones activas o crónicas, uso concurrente de anakinra | Insuficiencia cardíaca congestiva, antecedentes familiares de enfermedad desmielinizante, aumento del riesgo de malignidad | |
| Fototerapia | UVB-NB: dosis inicial según fototipo (130-400 mJ/cm2) o DEM (50% de la DEM). A continuación aumento de la dosis a 15-65 mJ/cm2 o ≤ 10% de la DEM inicial. Pauta 3-5 veces/semana | Pénfigo y penfigoide, lupus eritematoso con fotosensibilidad, xeroderma pigmentosa | Fotosensibilidad / medicación fotosensibilizadora, antecedentes de cáncer de piel, antecedentes personales o antecedentes familiares de melanoma, incapacidad física, antecedentes de ingesta de arsénico o radioterapia ionizante, mal apego (Menter et al.) | |
| Adalimumab | 80mg a la semana 0, 40mg a la semana 1, después 40mg cada 2 semanas | Hipersensibilidad, infecciones activas, uso concurrente de anakinra | Insuficiencia cardíaca congestiva, antecedentes familiares de enfermedad desmielinizante, aumento del riesgo de malignidad | |
| Ustekinumab | 45/90mg (según peso) en la semana 0,4 y después cada 12 semanas | Hipersensibilidad, infección grave activa | Mayor riesgo de malignidad, evitar el embarazo | |
| Corticoesteroides sistémicos | - | - | Evitar, ya que su retirada puede provocar un brote pustular o eritrodermia que puede poner en peligro la vida del paciente | |
| Dermatitis atópica | Ciclosporina (primera línea) | Dosis media inicial 5 mg/kg/día, reducir gradualmente tras la remisión 0,5 mg/kg cada 2 semanas | Función renal reducida, hipertensión incotrolada, hipersensibilidad, malignidad activa | Hipertensión controlada, edad <18 años o> 64 años, infección activa, vacuna viva atenuada, inmunodeficiencia, embarazo (C), fármaco inmunosupresor concomitante |
| Fototerapia (primera línea) | UVB-NB (311–313 nm) | Pénfigo y penfigoide, lupus eritematoso con fotosensibilidad, xeroderma pigmentosa | Fotosensibilidad / medicación fotosensibilizadora, antecedentes de cáncer de piel, antecedentes personales o antecedentes familiares de melanoma, incapacidad física, antecedentes de ingesta de arsénico o radioterapia ionizante, mal apego a tratamiento | |
| Metotrexato | 10–25 mg/semana, reducir lentamente tras la remisión | Embarazo (X) y lactancia | Enfermedad hepática, función renal disminuida, inmunodeficiencia, anomalía hematológica grave, enfermedad infecciosa activa o posible reactivación de la tuberculosis | |
| Micofenolato mofetil | 1–2 g/día, reducir lentamente tras la remisión | Embarazo (D), alergia al medicamento | Lactancia, úlcera péptica, enfermedad hepática/renal, uso concomitante de azatioprina | |
| Azatioprina | 100–200 mg/día, reducir lentamente tras la remisión | Embarazo (D), hipersensibilidad, infección activa, mielosupresión | Uso de alopurinol, uso previo de agentes alquilantes, enfermedad hepática | |
| Inmunoglobulinas intravenosas | 2 g/kg/mes durante 3–6 meses | Anafilaxia secundaria a infusiones previas | Insuficiencia cardíaca congestiva, insuficiencia renal, deficiencia de IgA, artritis reumatoide | |
| Corticosteroides sistémicos | Prednisona 1 mg/kg/24 h, reduciendo dosis gradualmente | Infecciones fúngicas sistémicas, herpes simplex, queratitis, hipersensibilidad | Hipertensión, ICC, psicosis previa, TB activa, prueba positiva de tuberculina, osteoporosis, cataratas, glaucoma, embarazo (C), diabetes mellitus, enfermedad gástrica | |
| Medicamentosa | Corticosteroides sistémicos | Prednisona 1 mg/kg/24 h, reduciendo dosis gradualmente | Infecciones fúngicas sistémicas, herpes simplex, queratitis, hipersensibilidad | Hipertensión, ICC, psicosis previa, TB activa, prueba positiva de tuberculina, osteoporosis, cataratas, glaucoma, embarazo (C), diabetes mellitus, enfermedad gástrica |
| Inmunoglobulinas intravenosas | Dosis alta (1 g/kg/día durante 3 días) | Anafilaxia secundaria a infusiones previas | Insuficiencia cardíaca congestiva, insuficiencia renal, deficiencia de IgA, artritis reumatoide | |
| Pitiriasis rubra pilaris | Acitretina (primera línea) | 0,3–0,75 mg/kg/día reducir lentamente tras la remisión | Embarazo (X), lactancia, incumplimiento de la anticoncepción | Leucopenia, disfunción hepática o renal, dislipidemia, hipotiroidismo |
| Metotrexato (primera línea) | 10–25 mg/semana reducir lentamente tras la remisión | Embarazo (X) y lactancia | Enfermedad hepática, enfermedad infecciosa activa o posible reactivación de TB | |
| Corticosteroides sistémicos | Prednisona 1 mg/kg/24 h, reduciendo dosis gradualmente | Infecciones fúngicas sistémicas, herpes simplex, queratitis hipersensibilidad | Hipertensión, ICC, psicosis previa, TB activa, prueba positiva de tuberculina, osteoporosis, cataratas, glaucoma, embarazo (C), diabetes mellitus, enfermedad gástrica |
La eritrodermia secundaria a reacciones farmacológicas mejora o se resuelve en 2-6 semanas tras la supresión del fármaco. La dermatitis exfoliativa asociada a la psoriasis y el eccema puede mejorar en varias semanas o meses, sin embargo, en el 15% de los pacientes las lesiones pueden recidivar tras el primer episodio. Cuando se asocia al LCCT u otra malignidad, la eritrodermia puede persistir y ser refractaria a los tratamientos. El 30% de los individuos aquejados de eritrodermia idiopática pueden mostrar una remisión completa o parcial del 50% de las lesiones64.
Los estudios sobre el pronóstico son escasos y los resultados son inconsistentes. En los primeros estudios que se realizaron se reportaba de una mortalidad significativa secundaria a complicaciones31,43. En cambio, en los estudios llevados a cabo en las últimas décadas la mortalidad registrada es baja, probablemente debido tanto a los avances producidos en los cuidados hospitalarios como a la disponibilidad de más opciones terapéuticas40,90. Sin embargo, un estudio retrospectivo reciente de cohortes de base poblacional en Dinamarca encontró que el 30,8% de los pacientes con eritrodermia psoriásica y el 39,6% con eritrodermia, murieron en los 3 primeros años tras el ingreso hospitalario2. Esta alta mortalidad es comparable con la reportada por estudios más antiguos.
ConclusiónLa eritrodermia es una entidad sindrómica y la determinación correcta de su etiología puede ser un reto para los dermatólogos. Las características clínicas son, con frecuencia, inespecíficas y el dermatólogo debe buscar pistas orientadas a la etiología subyacente. Se puede mejorar la precisión diagnóstica mediante la realización de múltiples biopsias a lo largo del transcurso de la enfermedad. El manejo inicial de la eritrodermia debe incluir una evaluación por parte de expertos en nutrición, la valoración del desequilibrio hidroelectrolítico, el mantenimiento de la función barrera de la piel, el uso de antihistamínicos con efecto sedante y la exclusión de infección bacteriana secundaria. Este proceso puede ser mortal y puede requerir hospitalización.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.