Sr. Director:
La crema anestésica EMLA® (Eutectic Mixture of Local Anesthetic) es un preparado tópico cuyos principios activos son la lidocaína (25 mg/ml) y la prilocaína (25 mg/ml), vehiculizados en un excipiente de polioxietileno y carboxipolimetileno que le confiere un pH de 9,4. EMLA® es un medicamento aprobado por la Food and Drug Administration (FDA) en pacientes mayores de 3 años de edad y para aplicar en piel intacta. En nuestro país se comercializa en forma de crema (tubos de 5 y 30 gramos) y parches autoadhesivos de 4 cm, y se emplea frecuentemente en las consultas de Dermatología y Pediatría como anestésico tópico.
Entre sus efectos secundarios destaca, por su incidencia, el blanqueamiento local y el eritema en la zona de aplicación; mucho más raras son urticarias de contacto, dermatitis irritativas, eczemas alérgicos de contacto y púrpura. Las complicaciones sistémicas son excepcionales, aunque se ha descrito metahemoglobinemia en niños, atribuida al metabolito de prilocaína, y que cursa con cefalea, visión borrosa, marcha inestable, cianosis y metahemoglobina en sangre.
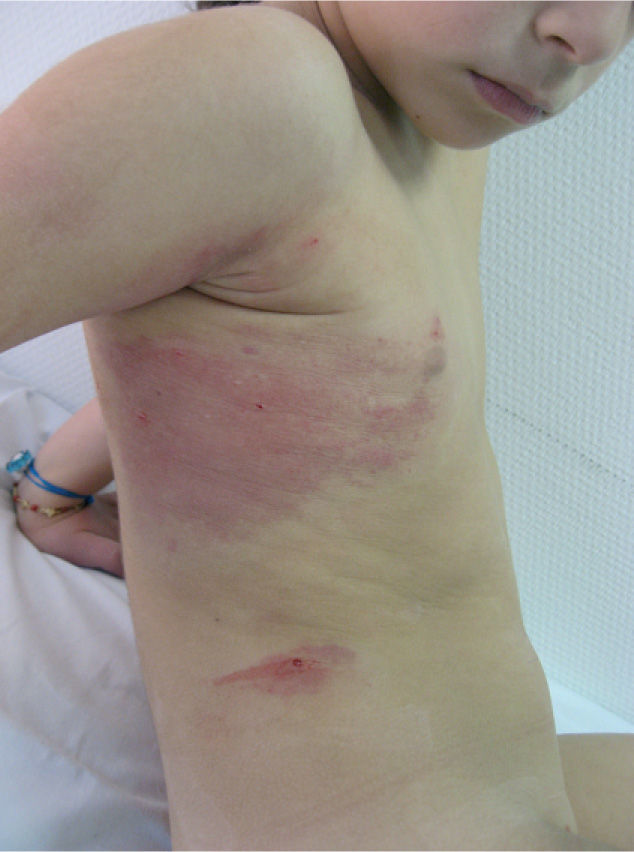
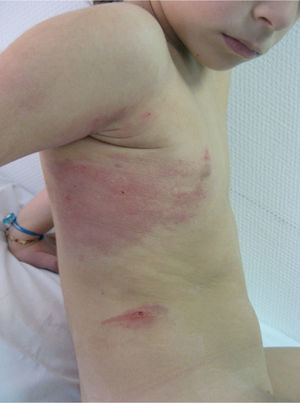
Presentamos dos episodios de púrpura por EMLA® en dos pacientes pediátricos y revisamos la literatura publicada al respecto, constatando que son pocos los casos descritos de esta patología. Se trata de dos niñas, de 9 y 1 año y medio de edad respectivamente, con antecedentes de dermatitis atópica y a las que se pautó EMLA® en cura oclusiva durante una hora y media previo al legrado de múltiples molluscum contagiosum. Al levantar el film plástico se observó, en la zona ocluida, una erupción petequial asintomática (fig. 1) que se resolvió sin tratamiento y sin secuelas en dos semanas. Debido al aspecto clínico característico de las lesiones no consideramos necesaria la realización de biopsia.
La reacción purpúrica por EMLA® es una complicación infrecuente de la que sólo hemos encontrado unos 25 casos publicados1-4. El mecanismo patogénico no se conoce con exactitud, pero parece tener una base tóxica y no alérgica3. Aunque en nuestras pacientes no se realizaron pruebas epicutáneas, otros autores que sí las han realizado han obtenido resultados negativos, tanto en lecturas inmediatas (30 minutos), como a las 48 y 72 horas3.
Es bien conocido que la crema EMLA® puede tener un efecto directo sobre los vasos, que induce el blanqueamiento y el eritema, y que podría llegar a producir alteraciones estructurales en la pared vascular que condicionarían la extravasación de hematíes y, por tanto, la púrpura. Probablemente la dermatitis atópica también se comporte como un factor de riesgo, ya que la alteración de la barrera cutánea favorece una mayor absorción del medicamento1. La fragilidad cutánea y vascular de los niños, demostrada en las erupciones purpúricas secundarias a esfuerzos como el vómito, la tos y el llanto, así como el efecto traumático que puede ejercer el plástico de la cura oclusiva también podrían influir en la aparición de este infrecuente efecto secundario1.