El complejo de esclerosis tuberosa (CET) es un trastorno autosómico dominante con expresividad variable, producido por mutación en los genes de supresión tumoral TSC1 y TSC2, que codifican las proteínas hamartina y tuberina, respectivamente1-3. Se manifiesta por la formación de hamartomas en múltiples órganos, fundamentalmente la piel, el sistema nervioso central, los riñones, los pulmones y el corazón1-3. Las anomalías vasculares asociadas a sobrecrecimiento/hipertrofia o gigantismo en CET son infrecuentes2. Presentamos una paciente con CET que presenta hipertrofia congénita y malformaciones vasculares combinadas del miembro superior izquierdo.
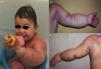
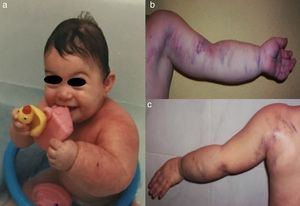
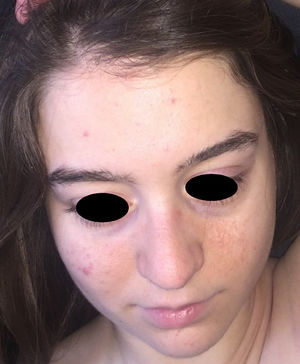
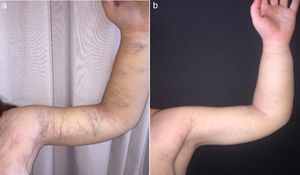
Una mujer de 17 años de edad, diagnosticada a los 9 años de CET, estaba en seguimiento desde el nacimiento por hipertrofia y malformaciones vasculares combinadas en el miembro superior izquierdo. El diagnóstico de CET se confirmó tras identificar la mutación c.235G>T en TSC2 en heterocigosis sin presentar ningún rasgo clínico de la enfermedad. La madre de la paciente presentaba signos de CET y la misma mutación. La exploración física, realizada durante los primeros meses de vida, había puesto de manifiesto un aumento de diámetro del miembro superior izquierdo, con presencia en su superficie de lesiones vasculares telangiectáticas y purpúricas (fig. 1a), con apariencia clínica de vasos capilares y venosos múltiples (fig. 1b y c). No se observaron lesiones cutáneas sospechosas de CET. La ecografía Doppler realizada a los 20 días de vida no mostró alteración del sistema arterial ni venoso profundo. A los 4 meses de vida se realizó una biopsia cutánea profunda, incluyendo músculo, que evidenció aumento de vasos sanguíneos en la dermis y en el tejido celular subcutáneo, sugestivo de malformaciones capilares y venosas, además de una ectasia de vasos linfáticos con positividad para D2-40 y negatividad de GLUT-1 y WT-1. El tejido muscular no mostraba alteraciones. No se observaron atipias, ni figuras de mitosis. A partir de los 8 años fue haciéndose cada vez más evidente la presencia de máculas hipopigmentadas en los muslos, angiofibromas faciales (fig. 2), fibromas periunguales en manos y pies, así como placas de chagrín en el tronco compatibles con CET, que se confirmó mediante estudio genético. La exploración física general y las técnicas de imagen, incluyendo radiología convencional, ecografía abdominopélvica, RM cerebral y ecografía cardiaca no detectaron alteraciones sistémicas. Con el diagnóstico de malformación vascular combinada de predominio linfático asociada a CET por mutación en TSC2, se inició tratamiento a los 11 años con rapamicina por vía oral a dosis de 0,8mg/m2 cada 12h durante 6 meses. Dado que no se objetivó disminución de la circunferencia de la extremidad superior afectada y que la paciente no presentaba sintomatología sistémica, el fármaco se suspendió. Las malformaciones capilares superficiales se han ido tratando desde los 14 años mediante láser de colorante pulsado ([LCP] 10mm, 10ms, 6J/cm2), y las malformaciones venosas superficiales con láser N-YAG múltiplex (LCP pulsado 10mm, 10ms, 6J/cm2 seguido tras un retraso de 1s de láser de Nd:YAG 10mm, 15ms, 70J/cm2), con resultados satisfactorios en ambas (fig. 3a y b).
La vía PI3K/AKT/PTEN/mTOR está involucrada en la patogénesis de síndromes hamartomatosos como el CET, anomalías vasculares, sobrecrecimiento y tumores malignos2,4-6. La molécula diana de la rapamicina, en mamíferos (mTOR), conformada por dos complejos multiproteicos (mTORC 1 y 2), es una cinasa perteneciente a la familia de fosfatidil-3-inositol, que está involucrada en la regulación de diferentes procesos relacionados con el crecimiento, la diferenciación celular, la angiogénesis y la modulación de la respuesta inflamatoria7. La actividad angiogénica, que desempeña mTOR, la realiza fundamentalmente a través de la traslación y la activación de HIF-1 (factor 1 inducible por hipoxia), molécula relacionada con la expresión de VEGF en situaciones de hipoxia celular y que mantiene a mTORC1 inactivo7. Una de las enfermedades más claramente asociadas con la desregulación de la ruta mTOR es el CET, por lo que es evidente el potencial desarrollo de varios tipos de malformaciones vasculares en esta enfermedad, aunque son poco reportadas2. Entre los tipos de anomalías vasculares descritas en CET se incluyen: angiomiolipomas, malformaciones linfáticas, y menos comunes, anomalías arteriales (oclusión, estenosis, aneurismas), estos últimos probablemente relacionados con alteración de los vaso-vasorum por los hamartomas2. El linfedema en el CET8 puede deberse a una malformación linfática, y se ha sugerido que el linfedema congénito y el adquirido son más frecuentes en el CET2.
La afectación de un segmento entero corporal, como en nuestro caso, puede ser debido a la pérdida de heterocigosidad en el desarrollo fetal temprano2, añadido a la mutación germinal. Cuando se producen mutaciones en mosaico poscigóticas, que afectan las vías de señalización celular, que regulan el crecimiento celular, la apoptosis o la migración, se producen alteraciones regionales, y pueden ocurrir a veces con sobrecrecimiento, que puede comprometer la piel, el tejido celular subcutáneo, el músculo, el hueso y/o los nervios. El sobrecrecimiento puede ser de gravedad variable, estable o progresivo9. Del mismo modo, las alteraciones en estas vías conllevan una mayor susceptibilidad a desarrollar diversos tumores malignos2,4, a tener en cuenta en la vigilancia de los pacientes.
En cuanto al tratamiento, se han utilizado inhibidores del mTOR, como la rapamicina (sirolimus) en el CET, con buenos resultados de la sintomatología neurológica, aunque sin clara respuesta en el sobrecrecimiento y/o las malformaciones vasculares2. En otro tipo de pacientes, con malformaciones vasculares, presentaron buenos resultados10. Probablemente se necesitan mejor control de dosis y periodos de tiempo más prolongados para evidenciar su verdadera eficacia, por lo que se requiere desarrollar más estudios, teniendo en cuenta que el bloqueo de la vía del mTOR podría tener un papel fundamental en lesiones vasculares de los pacientes con CET.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.