La cera para huesos es un material inerte y maleable que se utiliza como hemostático en los defectos óseos. La curación por segunda intención es una opción terapéutica en determinados casos después de la cirugía dermatológica. En las heridas quirúrgicas profundas, con exposición de distintos tejidos como hueso o cartílago, ciertos apósitos pueden adherirse al tejido de granulación. Esto dificulta y hace muy dolorosa la curación posterior. En estos casos la aplicación de un molde con cera para huesos proporciona un microambiente oclusivo hemostático ideal que favorece la cicatrización por segunda intención.
Bone wax is an inert, malleable material used as a hemostatic agent in treating surgical defects. Healing by secondary intention is an appropriate approach for certain situations in dermatologic surgery. When surgical wounds are deep enough for such tissues as bone or cartilage to be exposed, dressings may adhere to granulation tissue, making removal and subsequent wound care difficult and painful. In such cases bone wax can be molded around deep tissues to create an ideal occlusive, hemostatic microenvironment that facilitates second-intention wound healing.
En la cirugía dermatológica la cicatrización por segunda intención es una alternativa a la reconstrucción quirúrgica mediante cierre directo, colgajo o injerto. Aunque supone un mayor tiempo en la curación de la herida, tiene la ventaja oncológica de que no implica movimiento de planos cutáneos adyacentes, y por tanto no esconde posibles focos tumorales en profundidad. Sin embargo, si la herida quirúrgica se deja que cierre totalmente por segunda intención se puede complicar con sangrado, dolor y sobre todo, con la contracción/retracción de la herida, lo cual conlleva finalmente a una cicatriz no estética.
La cicatrización por segunda intención de cualquier herida quirúrgica consta de 4 fases1. Una primera fase que se inicia inmediatamente posterior al corte quirúrgico con la exposición de plaquetas que activan la cascada de coagulación. Pocas horas después de la fase hemostática aparece la fase inflamatoria, con el reclutamiento inicial de neutrófilos en la herida y 3-4 días después de macrófagos, ambos con la intención de limpiar los materiales extraños, residuos necróticos y bacterias. En condiciones normales los neutrófilos solo permanecen pocos días, pero su acción puede alargarse más tiempo en casos de contaminación. En esta fase inflamatoria, que acontece normalmente 2-4 días después, se pueden observar por lo tanto abundantes neutrófilos y vasos ocluidos por trombos ricos en fibrina.
Los macrófagos activados secretan factores de crecimiento que estimulan la formación del tejido de granulación, pasando a la tercera fase proliferativa. Los fibroblastos migran hacia la herida y producen una matriz provisional de fibrina, fibronectina y ácido hialurónico, que gradualmente va sustituyéndose por una matriz de colágeno. La fase final de remodelación tiene lugar durante los 6-18 meses posteriores, cuando aparecen miofibroblastos con capacidad contráctil y se fabrica colágeno tipo i que confiere fuerza tensora a la cicatriz. La contracción de la herida es el resultado de los miofibroblastos ricos en actina y fibronectina, y es proporcional a la profundidad de la herida.
La contracción también depende de la localización, de manera que las heridas localizadas periorificialmente tienden a retraer a partir del tejido orificial móvil, y por tanto se debería contraindicar el cierre por segunda intención en estos casos.
Por norma general, la segunda intención es mejor en las zonas cóncavas que en las zonas convexas. En la concavidad del canto interno del ojo, la concha auricular, los pliegues nasogenianos y las zonas pre y retroauricular, la cicatrización por segunda intención puede finalizar con resultados estéticos más satisfactorios.
En cuanto a la profundidad del defecto debe tenerse en cuenta que, si el tejido está bien vascularizado, con curas apropiadas es posible la total regeneración tisular. La exposición del cartílago o hueso retrasa o imposibilita la formación del tejido de granulación, por lo que es necesario realizar varias incisiones a partir de las cuales es posible la regeneración del tejido.
Cuando se decide el cierre por segunda intención deben aplicarse unas curas tópicas que garanticen un clima húmedo a la herida para propiciar la formación del tejido de granulación2.
Las gasas con vaselina, con o sin antibiótico, que se colocan en toda la extensión de la herida quirúrgica pueden adherirse cuando las heridas son profundas, o con exposición de otros tejidos como el hueso o el cartílago. Esto dificulta y hace muy doloroso el proceso de retirada. En estos casos se recurre a los apósitos de silicona o espumas de poliuretano que evitarían estas complicaciones.
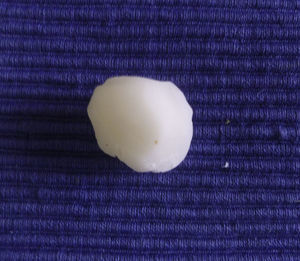
En nuestros pacientes hemos empleado la cera para huesos. Se trata de una mezcla compuesta por cera de abejas, palmitato de isopropilo y un agente estabilizador. Su uso original fue para la hemostasia debido al efecto de taponamiento puramente mecánico que ejerce en los canales abiertos sangrantes. Es un material biológicamente inerte que no ocasiona alergia cutánea ni dermatitis irritativa. No se absorbe y permanece en la herida sin adherirse a ella. Esta pobre adhesión hace que la retirada sea fácil e indolora. Además, tiene la gran ventaja de que es un material maleable. Su formato original es una lámina rectangular fina (fig. 1), pero con el calor de las manos se moldea para que cubra perfectamente las curvaturas del defecto quirúrgico (fig. 2). Esta cualidad es especialmente ventajosa en localizaciones como la oreja, nariz o el canto interno del ojo, donde otros apósitos podrían no presionar en profundidad y/o levantarse a modo de «tienda de campaña».
Pero además de estas cualidades, la cera para huesos posee otras ventajas añadidas como apósito en la segunda intención de la cirugía dermatológica; ya sea por las propiedades reparadoras y emolientes que posee la cera de abejas, o por el microambiente húmedo y oclusivo que se crea, se aprecia un buen tejido de granulación cuando se retira el apósito al cabo se una semana.
A continuación, a modo de ejemplo, se presentan 2 pacientes en los que se utilizó la cera para huesos con muy buenos resultados:
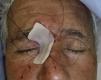
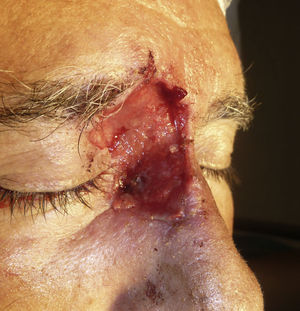
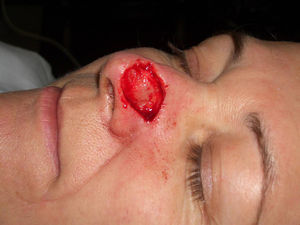
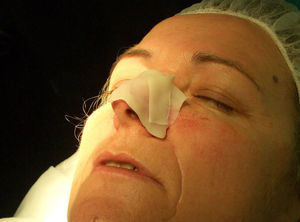
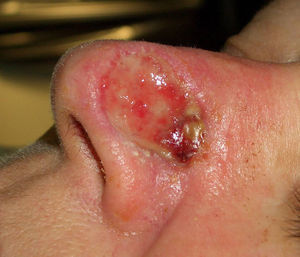
Paciente 1: varón de 73 años con un carcinoma basocelular infiltrante recurrente en el canto interno del ojo derecho en el que, una vez eliminado, se prefirió realizar la reconstrucción en un segundo tiempo mediante un injerto. En la figura 3 se muestra un profundo defecto quirúrgico tras 3 etapas de cirugía de Mohs. Se aplicó la cera para huesos para la cura por segunda intención (fig. 4), y al cabo de una semana se retiró y se demostró cómo había regenerado la herida, siendo menos profunda y con un apropiado tejido de granulación (fig. 5).
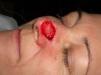
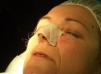
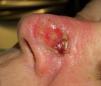
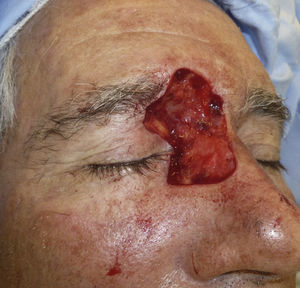
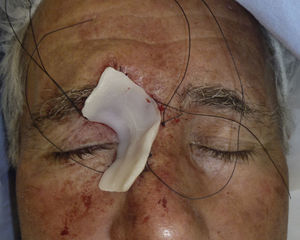
Paciente 2: mujer de 64 años con un carcinoma basocelular infiltrante en la cara lateral izquierda de la nariz, a quien se realizó una cirugía de Mohs que resultó en un profundo defecto quirúrgico, con exposición del cartílago (fig. 6). Se aplicó cera para huesos que cubría perfectamente toda la profundidad del defecto (fig. 7), y al cabo de una semana se retiró observándose una excelente regeneración de la herida (fig. 8).
La segunda intención es una alternativa terapéutica considerable en la cirugía dermatológica. Se puede plantear como opción reconstructiva única o para reducir el defecto quirúrgico y plantear en un segundo tiempo la reconstrucción quirúrgica. Tiene la desventaja de la contracción, que es más importante en localizaciones periorificiales y, por tanto, está desaconsejada en la zona orbicular inferior, por el ectropión resultante, y cerca de los labios. En las zonas pilosas la segunda intención da lugar a cicatrices alopécicas.
Es importante evaluar las condiciones generales del paciente, ya que las situaciones de inmunodepresión, la presencia de patologías como diabetes mellitus, coagulopatías, tabaquismo o alcoholismo no favorecen la cicatrización por segunda intención y aumenta el riesgo de infección o necrosis3.
El origen de la cera para huesos se remonta al año 1892. A pesar de que su uso en cirugía craneal fue descrito inicialmente por Henri Ferdinand Dolbeauen4 1842, fue Victor Horsley quien popularizó su uso en la neurocirugía en 1892. Horsley utilizó un preparado que denominó «cera de hueso», compuesta por cera de abejas, ácido salicílico y aceite de almendras. La utilizaba para controlar el sangrado masivo de los cráneos de los perros en sus experimentos.
Posteriormente se ha extendido su uso en neurocirugía, en cirugía cardíaca para la hemostasia de las esternotomías y en cirugía ortopédica. Su indicación es exclusivamente hemostática por el efecto mecánico, no químico, que ejerce al taponar los vasos sangrantes5.
Sin embargo, en este tipo de cirugías la cera para huesos permanece en el hueso sangrante indefinidamente, por lo que se han descrito casos de granuloma a cuerpo extraño con inflamación y dolor local6,7.
Algunos autores han sugerido que la cera para huesos inhibiría la osteogénesis en experimentos animales8. Sin embargo, la reducción de la mortalidad asociada al menor sangrado en la cirugía craneofacial justificaría su uso ante su posible acción negativa en la formación ósea9.
En ortodoncia la cera para huesos se utiliza como prevención de las heridas mucosas que los aparatos dentales ocasionan10.
En cirugía plástica la cera para huesos se ha utilizado únicamente como molde tridimensional para defectos nasales en los que se precisa un injerto condrocutáneo de la oreja. El molde serviría para ajustar en forma y tamaño para escoger la mejor localización de la zona dadora11.
En la cirugía dermatológica la cera para huesos proporciona unas cualidades idóneas como apósito no adherible, deformable y ajustable en el defecto quirúrgico. Actúa como una excelente barrera cutánea hemostática y, aunque no se conoce el mecanismo exacto, favorece la regeneración de las heridas. Serían precisos estudios comparativos con otros apósitos convencionales para reafirmar dicha propiedad.
Su utilización como apósito no permanente evita las complicaciones granulomatosas descritas en el hueso, donde permanece indefinidamente.
Otra de las ventajas que presenta la cera para huesos en comparación con otros apósitos es su bajo precio (aproximadamente 2 euros la unidad).
En conclusión, la cera para huesos puede ser una alternativa terapéutica muy útil como apósito de las heridas quirúrgicas extensas y profundas.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de la correspondencia.
Conflicto de interesesEl autor declara no tener ningún conflicto de interés.