INTRODUCCION
El tratamiento del herpes zóster (HZ) debe tener presente los siguientes objetivos: delimitar la aparición de lesiones a zonas anatómicas concretas, evitando su generalización; aliviar el dolor que suele acompañar a la infección cutánea; prevenir o disminuir la intensidad del dolor que se asocia con la neuralgia postherpética (NPH), y evitar las complicaciones agudas o crónicas que puedan surgir durante el transcurso de la infección 1. Los fármacos antivirales conseguirán estos efectos mediante un acortamiento del tiempo de replicación del virus 2.
Es importante tener presente cada uno de estos objetivos en el tratamiento del HZ, ya que solamente así podremos realizar un enfoque terapéutico adecuado en cada uno de los pacientes. Además, estos objetivos deben adaptarse a las situaciones clínicas de cada sujeto, ya que dependiendo del estado inmunológico, edad del paciente, y de si existen factores clínicos o enfermedades asociadas agravantes, puede condicionar una actuación médica diferente. A continuación analizaremos cada uno de estos puntos.
Además, todas las indicaciones terapéuticas que se realicen en cualquier enfermedad, deben establecerse según unos niveles de evidencia científica para cada unos de los fármacos. Esta información permitirá a los médicos poder actuar con unos niveles de certeza clínica diferentes en cada caso. Son muchas las clasificaciones creadas con este fin. Proponemos la aconsejada por algunos autores 3. Pueden establecerse las siguientes categorías según niveles de evidencia (NE):
1. NE 1. Evidencia consistente, a través de al menos un estudio clínico controlado, realizado a doble ciego y aleatorizado.
2. NE 2. Evidencia clínica basada en al menos un ensayo clínico sin aleatorización, realizado como estudio de cohorte o como estudio clínico-analítico controlado (preferiblemente en más de un centro), o también como estudios llevados a cabo por la comunicación de resultados en varios pacientes pero sin ser experimentos controlados.
3. NE 3. Evidencia basada en la opinión de autores con experiencia clínica en esa enfermedad o con ese fármaco, en la descripción de casos aislados, o en las recomendaciones de Comités de expertos en esa área.
4. NE 4. Se requiere más investigación o algunos hallazgos de investigación orientan hacia su utilización en esa enfermedad.
TRATAMIENTO LOCAL EN EL HERPES ZOSTER
Es aceptado en la comunidad dermatológica que la aplicación de antivirales tópicos en las lesiones de HZ no es eficaz (NE 1). Mediante esta forma terapéutica no se consiguen los objetivos más importantes del tratamiento: impedir la replicación del virus varicela-zóster (VVZ) y disminuir el riesgo de diseminación posterior 4. Por eso, fármacos como la idoxuridina hoy en día están descartados en el tratamiento del HZ 5.
De forma complementaria al tratamiento sistémico, pueden utilizarse medidas locales, con el fin de acelerar el proceso de curación y cicatrización de las lesiones. Durante la fase aguda, son eficaces las compresas frías, o lociones de calamina que alivian el dolor neural. En esta fase son útiles también soluciones antisépticas y secantes como el permanganato potásico a una concentración de 1/10.000. Deben evitarse las curas oclusivas, y no deben utilizarse cremas de corticoides. Una vez pasada la fase aguda, las lesiones costrosas pueden ser eliminadas. No es frecuente la sobreinfección bacteriana de las lesiones ulcerosas con aparición de celulitis secundaria.
INDICACIONES PARA EL TRATAMIENTO SISTÉMICO ANTIVIRAL DEL HERPES ZOSTER
Varios estudios han demostrado que la administración de fármacos antivirales sistémicos en el HZ reduce la inflamación, mejora el proceso de curación, y reduce las posibles complicaciones, en especial la aparición de NPH 6. Estos hallazgos han sido confirmados en varios trabajos, donde se aprecia que en personas más mayores el grado de inflamación y el riesgo de NPH son mayores 7-10. Además, la presencia de dolor como parte de los pródromos del cuadro clínico antes de la aparición de las lesiones en la piel 11, puede predisponer a un dolor neural persistente a los 6 meses de curarse las lesiones cutáneas hasta en el 50-75 % de los casos 12.
En condiciones normales, el HZ suele tener una evolución clínica favorable sin tratamiento en personas inmunocompetentes por debajo de 50 años. En estos casos el riesgo de NPH es menor. No obstante, a pesar de estas consideraciones algunos autores incluyen a este grupo de pacientes jóvenes dentro de las indicaciones relativas en el tratamiento sistémico del HZ (tabla 1) 13.
El tratamiento del HZ deberá realizarse con fármacos antivirales sistémicos en las siguientes situaciones, consideradas como indicaciones urgentes:
1. Cuando el HZ aparezca en pacientes mayores de 50 años o que presenten alguna forma de inmunodeficiencia (pacientes con procesos linforreticulares, trasplantados, tratamiento con inmunosupresores, enfermedades asociadas a inmunosupresión, etc.).
2. En aquellos pacientes en los que las lesiones cutáneas asientan en algún nervio craneal, en especial en la primera rama del trigémino (HZ oftálmico) o en pabellón auricular (HZ ótico o asociado a síndrome de Ramsay-Hunt).
3. En aquellos casos asociados a dermatitis atópica graves o a lesiones eczematosas extensas (tabla 1) 13.
A estas indicaciones incluidas en la tabla 1, el Grupo de Investigación para el HZ de la Sociedad Alemana de Dermatología, después de establecer qué pacientes con HZ presentan unas manifestaciones clínicas más desfavorables, y de evaluar su curso clínico mediante un sistema de puntuación, concluyen que deberían ser tratados los siguientes pacientes con HZ con el fin de evitar la aparición de NPH 13:
1. Mujeres por encima de los 50 años 14.
2. Dolor neurítico antes de aparecer las lesiones cutáneas.
3. Cuando están afectados más de un segmento de la superficie cutánea.
4. En aquellos casos en los que las lesiones sean hemorrágicas.
5. Si existe afectación de mucosas.
6. Presencia de más de 50 lesiones cutáneas.
7. Lesiones localizadas en polo cefálico o en región sacra.
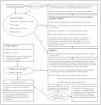
Hoy en día están disponible en internet varias Guidelines de HZ que condensan las indicaciones terapéuticas que se ofrecen en esta revisión, tanto en Estados Unidos como en Europa 13,15-20 (fig. 1). Aunque básicamente las recomendaciones de cada una de ellas son las mismas, parece muy útil el esquema propuesto por la International Herpes Management Forum (IHMF), ya que da una serie de pautas según un cuadro de algoritmos. Este mismo esquema ha sido aceptado por diferentes escuelas europeas 21. Por ello, será el esquema propuesto en esta revisión (fig. 1).
Fig. 1.--Esquema terapéutico del herpes zóster. (Algoritmos en el manejo del herpes zóster en pacientes inmunocompetentes, basado en las recomendaciones de la International Herpes Management Forum 15, la Sociedad Alemana de Dermatología 12 y del Current Management of Herpes Zoster-The European View 20. NPH: neuralgia postherpética.)
¿CUANDO DEBEMOS COMENZAR EL TRATAMIENTO ANTIVIRIAL SISTÉMICO?
La acción terapéutica de los antivirales depende del momento en el que se inicie la administración del fármaco. Los antivirales disponibles en el mercado tienen una eficacia mayor si se administran dentro de las 72 h desde que comienzan los síntomas cutáneos, principalmente el dolor. No obstante, existen situaciones en las que incluso después de 72 h puede ser aconsejable también administrar este tratamiento, ya que los pacientes presentarán todavía un beneficio clínico 13,16:
1. En pacientes con HZ cutáneo diseminado.
2. En aquellos casos con HZ en los que existe afectación de órganos internos.
3. También en pacientes con afectación de pares craneales, principalmente del trigémino y cuando existe HZ ótico 19.
¿DE QUÉ FARMACOS DISPONEMOS PARA TRATAR LOS CASOS DE HERPES ZOSTER?
Fármacos sistémicos como interferón o vidarabina hoy en día están descartados en el tratamiento del HZ, ya que son de limitado valor en esta infección, en especial a la hora de prevenir la NPH 20. En nuestro país, al igual en la mayoría de los países de Europa, disponemos de 4 moléculas para el tratamiento del HZ, en condiciones normales: aciclovir (NE 1), valaciclovir (NE 1), famciclovir (NE 1) y brivudina (NE 1)16,21-38 (fig. 1). Recientemente, una revisión del tratamiento del HZ en Europa, llevada a cabo por varios expertos, incluye estos cuatro fármacos para el tratamiento del HZ 21. En cambio, si revisamos otras Guías terapéuticas en el mundo anglosajón, observaremos que no incluyen la brivudina, debido a que este fármaco no está en muchos de esos países, incluido Estados Unidos 15-17.
Existen algunas ventajas de unos antivirales frente a otros que deberemos conocer a la hora de indicar un fármaco u otro:
1. Todos ellos pueden administrase por vía oral, pero solamente el aciclovir puede hacerlo por vía parenteral.
2. El valaciclovir y el famciclovir presentan una mejor biodisponibilidad y farmacocinética, comparados con el aciclovir.
3. De todos ellos, la brivudina tiene como ventaja frente a aciclovir y valaciclovir, y en común con famciclovir, la posología más cómoda para el paciente, ya que se administra en una única dosis diaria.
4. Todos ellos han demostrado prevenir la aparición de NPH 15,27-34 (NE 1) aunque con la brivudina este papel preventivo es incluso ligeramente superior al demostrado por el aciclovir (NE 1) 32,33.
5. Recientemente se ha observado que la brivudina puede ser ligeramente superior a aciclovir en el cese de formación de nuevas ampollas (NE 1) 31, y un efecto clínico similar al famciclovir (NE 1) 34.
6. A pesar de lo dicho, la brivudina tiene algunas limitaciones. Este fármaco no puede ser administrado en las siguientes situaciones 13:
a)Pacientes inmunodeprimidos.
b)Pacientes en edad pediátrica.
c)Cuando el paciente está recibiendo 5-fluorouracilo, 5-fluoropirimidinas o derivados, siendo necesario respetar un intervalo mínimo de 4 semanas antes de iniciar un tratamiento con fármacos 5-fluoropirimidínicos.
7. La dosis de los antivirales deberá adaptarse a la función renal que presenta el paciente. Únicamente la dosis de brivudina no está influenciada por el aclaramiento de creatinina, lo que lo hace un fármaco ideal en paciente con una función renal deteriorada 13.
¿QUÉ DOSIS DE ANTIVIRALES
DEBEREMOS UTILIZAR?
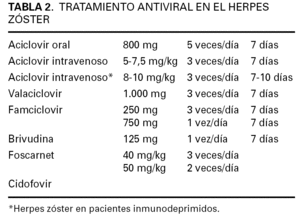
En la tabla 2 se detallan las dosis y la duración de cada uno de los antivirales. Existen numerosos estudios que demuestran la eficacia del aciclovir en el tratamiento del HZ en adultos inmunocompetentes (fig. 1) 35,36. Hoy está establecido que en pacientes mayores de 50 años, cuando se administra una dosis de 800 mg cinco veces al día dentro de las primeras 48 h de la aparición del eritema y las vesículas, y durante 7-10 días, se consigue una mejoría significativa de las manifestaciones clínicas (NE 1). Igualmente, la administración de valaciclovir 1.000 mg tres veces al día, y famciclovir 250 mg tres veces al día o 750 mg/día en una dosis, durante una semana presenta un efecto similar o incluso superior al aciclovir a dosis elevadas, sin efectos secundarios importantes (NE 1) 36,37. La dosis diaria de 125 mg de brivudina ha demostrado ser igual de eficaz que dosis elevadas de aciclovir por vía oral (NE 1).
TRATAMIENTO DEL HERPES ZOSTER EN DIFERENTES SITUACIONES CLINICAS
Tratamiento analgésico
No está claro si la administración de analgésicos de forma precoz puede disminuir la incidencia de NPH. No obstante, este tipo de tratamiento al menos alivia la sintomatología del paciente de forma importante.
Existe una gradación internacional del dolor, que puede ayudar a calibrar la situación del paciente en cada momento, y ayudarnos a utilizar un tratamiento analgésico u otro (fig. 2) 39.
Fig. 2.--Medición de la intensidad del dolor en el herpes zóster.
En términos generales, la administración de fármacos antivirales deberá ser un tratamiento que se instaure pronto a los pacientes con el fin de eliminar la infección herpética, y también minimizar al máximo el riesgo de daño neural, y de esta manera disminuir la aparición de NPH. Dependiendo de cómo se presente el dolor neural, y también de cómo sea su evolución en cada caso, deberemos abordarlo de una forma u otra. En unos casos será únicamente un tratamiento que acompañe al tratamiento antiviral, ya que en pocas semanas cederá la sintomatología. En otros casos, puede quedar un dolor neurítico residual, como consecuencia del daño en la fibra nerviosa, y que es propiamente lo que se conoce como NPH. Cada una de estas dos circunstancias deberá ser abordada de forma diferente.
Algunos estudios han recomendado la administración precoz de prednisona a una dosis de 40-80 mg/día, los primeros días. Este tratamiento puede aliviar el dolor de los primeros días, pero no parece prevenir la aparición de NPH (NE 1) 40,41. Son necesarios más estudios para conocer no solamente si la utilización de corticoides en el HZ previene el daño neural, sino también en qué grupo de pacientes y en qué localización anatómica podrían ser más eficaces. El Forum Australiano para el manejo del Herpes Zoster, recomienda la administración de corticoides durante los primeros días de la infección, junto a fármacos antivirales, únicamente en pacientes mayores de 50 años, ya que en estos es en los que el riesgo de NPH es mayor 15.
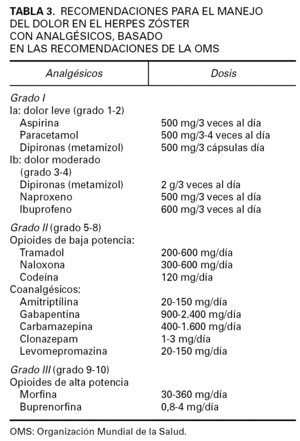
Pueden establecerse 3 pasos en el tratamiento analgésico del HZ, basados en las recomendaciones de la Organización Mundial de la Salud (OMS) para el tratamiento del dolor oncológico, según se observa en la tabla 3 2,39. La pauta analgésica está basada en la intensidad del dolor que el paciente refiere en cada caso, según la escala indicada en la figura 2.
TABLA 3. RECOMENDACIONES PARA EL MANEJO DEL DOLOR EN EL HERPES ZÓSTER CON ANALGÉSICOS, BASADO EN LAS RECOMENDACIONES DE LA OMS
Cuando el dolor es poco intenso, únicamente se administrarán analgésicos convencionales (dipironas, paracetamol), o fármacos antiinflamatorios. Pueden combinarse con los fármacos incluidos en el grado II, o con aquéllos incluidos en el grado III (tabla 3).
Un grupo especial lo constituyen los pacientes mayores, ya que por una parte son los que con más frecuencia presentan NPH, pero por otra pueden tener más efectos secundarios con algunos fármacos. En estos pacientes, el uso precoz de antidepresivos tricíclicos (amitriptilina) en las fases iniciales del HZ está considerado de gran eficacia al reducir o incluso prevenir la NPH 16 (NE 2). A su efecto antidepresivo se añaden propiedades analgésicas importantes. En pacientes mayores de 60 años, la administración de 25 mg al día se puede aumentar hasta 150 mg/día de amitriptilina junto a aciclovir a la dosis estándar, y dentro de las 48 h del inicio de los síntomas, reduce de forma significativa la aparición de NPH 42,43.
A su vez, al ser pacientes polimedicados, deberemos evitar interacciones medicamentosas, como por ejemplo las que pueden ocurrir cuando utilizamos carbamazepina.
Algunos estudios han recomendado la administración de gabapentina en la NPH (NE 3) 16. En pacientes jóvenes puede aumentarse la dosis rápidamente (300 mg/día el día 1, 600 mg/día el día 2, 900 mg/día el día 3), hasta alcanzar una dosis máxima de 3.600 mg/día. Una vez alcanzada la dosis eficaz, puede mantenerse una dosis de mantenimiento hasta 2 meses. En personas mayores este incremento debe realizarse más lentamente. Además, deberá evaluarse la función renal antes de iniciar este tratamiento, ya que el fármaco activo se excreta por el riñón.
Recientemente se ha propuesto que la administración de pregabalina, con una acción farmacológica similar a la gabapentina, es de gran eficacia en el tratamiento de la NPH. En una dosis máxima diaria de 600 mg/día, reduce de forma significativa el dolor neurítico frente a placebo (NE 4) 44. No obstante, se necesitan más estudios para confirmar su eficacia de forma rutinaria en el HZ.
Cuando las lesiones se han resuelto y queda en el paciente una NPH, que no se controla con la medicación anteriormente indicada, pueden existir otras formas de tratamiento del dolor, que podríamos incluir dentro de miscelánea. Aunque en muchos de esos tratamientos se necesita más experiencia para confirmar su eficacia en la NPH, podemos destacar los siguientes (tabla 4):
1. Antagonistas del receptor de N-metil-D-aspartato, como la ketamina o el dextrometorfano (NE 4) 45-47.
2. Bloqueo de fibras nerviosas (NE 3) 16,48,49.
3. Administración intratecal de corticoides (NE 4) 50,51.
4. Antagonistas del ácido g -aminobutírico, como el baclofeno (NE 4) 52.
5. Aplicación de electrodos para realizar estimulación espinal (NE 4) 53-55.
6. Extirpación quirúrgica del dermatoma afectado 56.
7. Colocación de catéteres epidurales para la administración periódica de analgésicos 57.
Por último, hay varias referencias en la literatura médica que han estudiado la eficacia de analgésicos tópicos en el dolor neural del HZ. Podemos destacar los siguientes (tabla 5):
1. Capsaicina 58-60. Se ha postulado que su acción es debida a una inhibición de la sustancia P, y también a una acción atrofiante de las fibras nerviosas localizadas en la epidermis 61. Los resultados con esta medicación han sido variables, observándose mejoría o incluso empeoramiento tras su aplicación (NE 3) 60,62.
2. Aspirina/dietil-éter o benzidamina. Su aplicación tópica ha demostrado ser eficaz en el control del dolor neurítico, acelerando además la curación de las lesiones cutáneas por el HZ 63-67. No obstante, en otros casos no se ha observado beneficio clínico (NE 4) 68.
3. Lidocaína. Es un anestésico con un amplio uso en cirugía dermatológica. Actúa mediante bloqueo de los canales de sodio de la membrana celular. Inicialmente, su uso en forma de geles al 5 % demostró analgesia a los 30 min que duraba hasta 24 h desde su aplicación 69. Posteriormente, se ha empleado este mismo medicamento en parches al 5 % (700 mg por parche) 70-73, con importante analgesia, sin observarse niveles tóxicos en sangre tras la administración de 4 parches al día, durante 3 días consecutivos. Su uso dependerá de las necesidades del paciente, aunque se han llegado a utilizar hasta 8 años seguidos, sin observarse efectos secundarios (NE 3) 71.
4. Clonidina. Su aplicación tópica ha demostrado ser útil en pacientes con NPH. A la concentración de 150 mg/g de crema, produjo un alivio importante en los pacientes que comenzó a los pocos minutos de su aplicación (NE 4) 74.
Tratamiento del herpes zóster en pacientes inmunocompetentes menores de 50 años
No existe unanimidad en la conducta que se debe seguir en este grupo de pacientes, siempre y cuando no existan factores añadidos como dermatitis atópica, o en aquellos con HZ muy extenso e inflamatorio. Hasta que dispongamos de estudios a doble ciego en este grupo de población, la experiencia del médico le llevará a actuar de una u otra forma. Algunos autores incluyen a este grupo de pacientes, tal y como comentábamos anteriormente, dentro de las indicaciones relativas para el empleo de antivirales sistémicos 13 (tabla 1).
Tratamiento del herpes zóster en pares craneales
Con el fin de evitar complicaciones oculares, todos los pacientes que presenten HZ oftálmico de menos de una semana de evolución deberían tratarse con fármacos antivirales (NE 2) 16. Cuando está afectado el V par craneal, en especial la rama oftálmica y la rama nasociliar, los pacientes deberían ser evaluados por un oftalmólogo. En estos casos, la gravedad se centra en la afectación ocular por el HZ, llegando hasta del 50 % de los casos 75. Con tratamiento antiviral este porcentaje se reduce hasta el 20-30 % 76,77. Colin et al 78 demostraron que a la dosis estándar (tabla 2), aciclovir y famciclovir tenían la misma eficacia en prevenir las complicaciones oculares, aunque proponen que el tratamiento debe ser superior a 7 días, ya que de esta manera pueden minimizarse las complicaciones clínicas secundarias (queratitis, dolor ocular, conjuntivitis). Sin embargo, otros estudios no han demostrado una eficacia mayor cuando se administran los fármacos durante 14 días 37,79. El valaciclovir ha demostrado la misma eficacia que los otros dos antivirales (NE 2) 16,77.
Si se demuestra la presencia de uveítis, se recomienda la utilización de fármacos midriáticos para prevenir la aparición de sinequias; si existe dolor pueden administrarse fármacos antiinflamatorios 80; en caso de queratitis epitelial pueden administrarse agentes virostáticos en gotas. Además, será necesaria la medición de la presión intraocular, y de demostrarse un incremento, deben usarse fármacos antihipertensivos 81. Solamente se administrarán corticoides sistémicos junto a agentes antivirales cuando exista endotelitis y trabeculitis oftálmica, y siempre bajo la supervisión de un oftalmólogo (NE 3) 16. No obstante, en estos casos deberá valorarse el beneficio antiinflamatorio y el daño en el sistema inmunológico 82.
El HZ ótico puede tener complicaciones en el VII o en el VIII par craneal. Estos pacientes deberán ser evaluados por un otorrinolaringólogo. La complicación más relevante en el HZ del VII par craneal es la parálisis facial (parálisis de Bell), y del VIII par craneal el síndrome de Ramsay-Hunt. Ambas son reversibles en la mayoría de los casos. Aunque existe poca experiencia, algunas Guías de manejo del HZ en estas localizaciones recomiendan administrar corticoides y antivirales sistémicos a la dosis estándar (tabla 2) dentro de los 7 días desde el inicio de las lesiones, y preferiblemente por vía intavenosa 35.
Además del tratamiento indicado, en el HZ ótico será de gran utilidad la utilización de agentes hemorreológicos que favorezcan la circulación sanguínea local. Deberá completarse este tratamiento con analgésicos y fármacos antivértigo.
Tratamiento del herpes zóster cuando se asocian otras complicaciones neurológicas
No existen unos NE definidos en el tratamiento y manejo de las complicaciones neurológicas del HZ, debido al pequeño número de pacientes en este grupo. Complicaciones como son meningitis, encefalitis o mielitis, deberán ser evaluadas por un neurólogo. Se recomienda la administración de aciclovir intravenoso a una dosis de 10 mg/kg/8 h, durante 7-10 días 83. En el caso de hemiparesia contralateral por HZ, además de antivirales a dosis elevadas se recomienda la utilización de corticoides sistémicos, aunque a pesar de este tratamiento la mortalidad es alta (hasta en el 25 % de los casos) y las secuelas importantes 83,84.
Tratamiento del herpes zóster en niños y adolescentes
La aparición de HZ en la infancia no es por lo general una indicación de tratamiento antiviral sistémico 85, excepto en aquellos casos en los que está afectado un par craneal 12,86,87.
También deberían ser tratados con fármacos sistémicos aquellos niños con inmunodeficiencias asociadas, o cuando presentan formas de dermatitis atópica severas 13. No obstante, mientras no existan estudios en edad infantil con niños con inmunodeficiencias asociadas a HZ, únicamente podemos especular que el tratamiento sistémico del HZ en estos casos podría prevenir la diseminación, y reducir la severidad 13. Es también especulativo que la destrucción local de tejido, las infecciones bacterianas secundarias y la aparición de cicatrices podrían reducirse en estos niños con la administración precoz de antivirales. El tratamiento recomendado es aciclovir intravenoso durante 7-10 días.
Pacientes inmunodeprimidos
Los pacientes inmunodeprimidos son una población de riesgo a la hora de presentar HZ. La disfunción inmunológica les puede producir una extensión mayor de la infección por el VVZ, con un número mayor de complicaciones, y con presentaciones clínicas atípicas en ocasiones. En concreto, en este grupo de pacientes deberemos estar más atentos a complicaciones graves como la presencia de HZ generalizado, HZ abdominal antes de manifestarse en la superficie cutánea, y encefalitis crónica después de unos días de presentar HZ cutáneo 16.
Las manifestaciones clínicas del HZ en pacientes con infección por el virus de la inmunodeficiencia humana (VIH) son similares a aquéllas observadas en la población general, excepto en que en aquéllos no son infrecuentes las recurrencias, la aparición ocasional de lesiones atípicas, y la mayor duración de las lesiones 88. En los pacientes con infección por VIH y terapia HAART (tratamiento antirretroviral de alta potencia) la aparición de HZ suele considerarse como una consecuencia inmunopatológica de la mejoría inmunológica del paciente 89. Hay suficiente experiencia clínica para afirmar que en estos pacientes es eficaz la administración de aciclovir por vía intravenosa (NE 1) 16. Cuando los episodios de HZ son recurrentes o progresivos, puede recomendarse, además, tratamiento profiláctico con aciclovir por vía oral durante tiempos prolongados 90. Sin embargo, el tratamiento antirretroviral puede ayudar a restablecer el sistema inmunológico del paciente, de manera que el tratamiento profiláctico para diferentes enfermedades infecciosas, incluida el HZ, puede no ser necesaria. Sólo casos aislados han sido tratados con valaciclovir, y famciclovir, demostrándose también su beneficio clínico (NE 3) 16,91-93.
Aunque no es frecuente, se han descrito casos de resistencia al VVZ en este grupo de pacientes, principalmente en casos de síndrome de inmunodeficiencia adquirida (SIDA). En esos pacientes deberá utilizarse foscarnet (NE 2) 16,94,95 (120-200 mg/kg/día, divido en 2 o 3 dosis, evaluando siempre la función renal del paciente). La incidencia y las características de la NPH en pacientes con infección por VIH o SIDA no difiere de lo observado en la población inmunocompetente 88,91.
La dosis y régimen de tratamiento con aciclovir en estos pacientes estará en función de la gravedad de la inmunodeficiencia, y en concreto de los valores de CD4. Si permanecen todavía en límites dentro de la normalidad (> 400 cél./μl), el HZ dermatómico puede tratarse a la dosis estándar de 5-7,5 mg/kg/8 h de aciclovir, durante 7 días (tabla 2). En aquellos casos con inmunodeficiencia grave, con lesiones cutáneas extensas, y en especial cuando se acompañe de síntomas neurológicos, la dosis de aciclovir por vía intravenosa será 10 mg/kg/8 h (tabla 2) 13.
Cuando se administra aciclovir intravenoso hay que valorar estrechamente la función renal, y mantener una fluidoterapia adecuada para evitar la formación de cristales del fármaco en los túbulos renales. Si la función renal está alterada hay que ajustar la dosis del fármaco dependiendo del aclaramiento de creatinina, distanciando las dosis de 8 a cada 12 h, o incluso a una única dosis al día.
Dentro de los pacientes inmunodeprimidos, un grupo importante es el de los receptores de trasplantes de órganos, u otros sujetos sometidos a fármacos inmunosupresores 93,96. En primer lugar, deberemos conocer si existen pautas terapéuticas que disminuyan el riesgo de HZ en estos pacientes. Se ha demostrado que la administración de vacunas de VVZ es eficaz en los pacientes con trasplante de médula ósea. Cuando se administra en los primeros días del periodo postrasplante (administrado en 3 dosis en el primero, segundo y tercer meses), aumenta la inmunidad celular frente al VVZ y disminuye la gravedad del HZ (NE 3) 97. En otros casos, se ha realizado tratamiento profiláctico con aciclovir intravenoso (250 mg/m 2 tres veces al día), comenzando 5 días antes de trasplante de médula ósea, y prolongándolo durante 5 semanas, para posteriormente disminuir la dosis a 400 mg tres veces al día por vía oral, hasta un periodo de 6 meses. De esta manera, se redujo la aparición de HZ frente a placebo 98. En algunos pacientes inmunodeprimidos el tratamiento del HZ se ha realizado por vía oral, con aciclovir, famciclovir o con valaciclovir, según la pauta estándar, encontrándose unos resultados similares entre ellos (tabla 2) 99.
El HZ en pacientes oncológicos aparece con más frecuencia en aquellos con leucemia, linfomas, y en los sometidos a trasplantes autólogos o alogénicos 100,101. En estos pacientes el tratamiento de elección será la administración de aciclovir intravenoso (10 mg/kg/8 h, 7-10 días) (NE 1) 16,102,103. En aquellos casos con formas localizadas y asociadas a inmunosupresión moderada o leve, puede administrarse aciclovir por vía oral, así como valaciclovir o famciclovir (tabla 2) con resultados terapéuticos similares 16.
Cuando existe daño renal (p. ej., por los propios inmunosupresores, o por rechazo renal en casos de trasplante) utilizaremos fármacos virostáticos pero que no sean nefrotóxicos. De todos los antivirales, sólo la brivudina no está influenciada por los niveles de creatinina 13.
Tratamiento del herpes zóster durante el embarazo
Todos los fármacos antivirales sistémicos están incluidos en la categoría C según la Food and Drug Administration (FDA), por lo que en condiciones normales su uso no está aconsejado en mujeres embarazadas (consultar: http:pfarmals.portalfarma.com: 8080/farma/scripts/bot.dll?accion = 0). Así pues, ante una mujer embarazada, inmunocompetente, y con HZ localizado, debe tratarse sólo con medidas locales, evitando la administración de antivirales sistémicos.
No obstante, en aquellos casos en los que existan otros factores de riesgo añadido, como inmunosupresión (p. ej., pacientes trasplantadas), deberemos optar por terapia sistémica siempre y cuando el riesgo de complicaciones secundarias graves por el propio HZ pueda poner en peligro la vida de la madre o del feto. Por otra parte, a diferencia de lo que ocurre con la varicela, la aparición de HZ en las pacientes embarazadas no constituye un riesgo para el feto, ya que la viremia suele ser pequeña al existir una inmunidad previa de la madre.
Tratamiento del herpes zóster en pacientes con resistencia a los antivirales convencionales
Pueden encontrarse casos de resistencia del VVZ a antivirales como aciclovir, valaciclovir, famciclovir y brivudina, probablemente por mutaciones en el gen que regula la timidincinasa, o por mutaciones en el gen polimerasa. Se han aislado cepas de estos virus principalmente en pacientes con infección por VIH 12,86. En estos casos la infección no se resuelve aunque incrementemos la dosis del fármaco. Debe sospecharse una resistencia al antiviral empleado cuando la mejoría clínica no se produce o es solamente parcial 13. Algunos autores prefieren esperar 21 días de tratamiento para confirmar el diagnóstico de resistencia al aciclovir 104. Suele indicarse entonces foscarnet, a una dosis de 40 mg/kg tres veces al día, o 50 mg/kg dos veces al día, durante 2-3 semanas 96. A veces pueden encontrarse también resistencias al foscarnet, por mutaciones en el gen polimerasa. En estos casos la única alternativa que tenemos hoy en día es la administración de cidofovir 105,106.
¿PUEDE SER EL HERPES ZOSTER PREVENIDO? ¿EN QUÉ PACIENTES DEBERIAN TOMARSE MEDIDAS TERAPÉUTICAS ESPECIALES PARA EVITAR LA APARICION DE HERPES ZOSTER?
En los últimos años varios estudios están dirigidos a evaluar si la administración de la vacuna de la varicela en niños puede disminuir de forma significativa la aparición de HZ en la edad adulta, y por tanto de sus complicaciones, principalmente la NPH 107. No obstante, la observación de que la inmunidad frente al VVZ declina con la edad 108, plantea el interrogante de si a las personas mayores no se les expondría a un riesgo mayor de padecer un HZ más agresivo al no haber estado en contacto con el virus en la infancia 109,110.
La vacuna de la varicela incrementa la respuesta citotóxica linfocitaria específica frente al VVZ en personas mayores seropositivas previamente frente a este virus 111. Por este motivo, aunque faltan más estudios que lo confirmen, quizá la administración de vacunas del VVZ a personas mayores podrá reducir de forma significativa la aparición de HZ y por tanto de NPH 112.
Por último, y como fue comentado anteriormente, se ha propuesto administrar aciclovir intravenoso en pacientes trasplantados con una inmunodepresión importante, a una dosis de 500 mg/m 2, tres veces al día, durante un mes, seguido por aciclovir por vía oral, a una dosis de 800 mg cuatro veces al día durante 6 meses (NE 2) 16. Esta pauta se ha indicado principalmente en pacientes con trasplante de médula ósea, en quienes la aparición de enfermedad de injerto contra el huésped, requiere una inmunosupresión importante añadida.
Este documento ha sido consensuado y avalado por la Academia Española de Dermatología y Venereología
Declaración de conflicto de intereses
Declaramos no tener ningún conflicto de intereses.
Correspondencia:
Pedro Redondo. Departamento de Dermatología.
Clínica Universitaria de Navarra.
Avda. Pío XII, s/n. 31080 Pamplona. España.
predondo@unav.es
Recibido el 12 de diciembre de 2005.
Aceptado el 7 de febrero de 2006.