La hiperhidrosis primaria (HP) consiste en un exceso de sudación de una zona concreta del cuerpo que es clínicamente perceptible. La HP no debe considerarse un simple problema cosmético, pues supone una dificultad muy importante de relación social y laboral para las personas que lo experimentan. Los objetivos de este estudio han sido definir el perfil clínico de los pacientes con HP y evaluar en la práctica clínica los resultados que consigue el tratamiento con Toxina Botulínica A (TB-A).
Material y métodosLa muestra acota un total de 52 pacientes, 39 mujeres y 13 hombres, con diagnóstico de HP tratada por primera vez con TB-A. Todos cumplimentaron una encuesta donde se registraron: edad, sexo, profesión, inicio, antecedentes familiares, localización, signos/síntomas acompañantes y tratamientos previos; inicio del efecto de la TB-A; efectos secundarios locales y/o sistémicos y el grado de severidad de su hiperhidrosis antes del tratamiento y después del mismo.
Resultados y conclusionesLa HP se inicia en la pubertad en el 61,5% de los casos; el 75% son mujeres con una edad media de 29,9 años. El 36,5% de los pacientes tienen familiares de primer grado con HP. La localización de la hipersudación es palmar en el 61,5% casos, plantar en el 53,8% y axilar en el 59,6 %, siendo menor en otras localizaciones. La clínica acompañante más frecuente es: eritema facial (32,7%), palpitaciones (30,7%), tensión muscular (28,8%), temblor (23%) y cefalea (17,3%). El tratamiento con TB-A es bien tolerado y respecto a la escala de severidad de la hiperhidrosis, se produce una mejoría muy significativa (p<1,0×10−32; potencia estadística=1) a los dos meses del tratamiento.
Primary hyperhidrosis is characterized by excessive sweating in a defined region of the body. It should not be considered a purely cosmetic problem as it has a significant impact on the social and professional relationships of affected individuals. The aim of this study was to determine the clinical profile of patients with primary hyperhidrosis and assess the results obtained with the use of botulinum toxin type A (BTX-A) in clinical practice.
Material and methodsThe study included 52 patients (39 women and 13 men) with a diagnosis of primary hyperhidrosis treated for the first time with BTX-A. All patients completed a questionnaire that included the following information: age; sex; profession; age at onset, family history, and site of hyperhidrosis; accompanying signs and symptoms, and previous treatment; time to effect of BTX-A; local or systemic side effects; and severity of hyperhidrosis before and after BTX-A treatment.
Results and conclusionsPrimary hyperhidrosis began during puberty in 61.5% of the patients included in the study, 75% were women, and the mean age was 29.9 years. In 36.5% of patients, first-degree relatives also had primary hyperhidrosis. Hyperhidrosis was classified as palmar in 61.5% of cases, plantar in 53.8%, and axillary in 59.6%. Other sites were affected less frequently. The most common accompanying symptoms were facial erythema (32.7%), palpitations (30.7%), muscle tension (28.8%), shivering (23%), and headache (17.3%). Treatment with BTX-A was well tolerated and there was a highly significant reduction in the severity of hyperhidrosis 2 months after performing the treatment (P<0.001).
La hiperhidrosis primaria o idiopática es una afección benigna de etiología desconocida, aunque la mayoría de los autores coinciden en su relación con una disfunción del mecanismo de control vegetativo autónomo mediado por fibras colinérgicas postgangliónicas1. Consiste en un exceso de sudación de una zona concreta del cuerpo (focal) que es clínicamente perceptible1,2.
Puede afectar a todas las glándulas ecrinas del cuerpo, las cuales reciben el impulso nervioso a partir de la acetilcolina, aunque en especial afecta a las situadas en las palmas, plantas, axilas y, en ocasiones, a las de la cara y cuero cabelludo. Es una alteración frecuente que puede afectar a un 1% de la población3–6.
La hiperhidrosis focal idiopática no debe considerarse un simple problema cosmético, pues supone una dificultad muy importante de relación social y laboral para las personas que lo experimentan. Los métodos terapéuticos utilizados hasta fechas recientes eran poco útiles, como la aplicación tópica de sales de aluminio o de glutaraldehído; engorrosos de aplicar, como en el caso de la iontoforesis de agua; o muy traumáticos, como la extirpación de las glándulas sudoríparas axilares7,8. Además se utilizan fármacos sistémicos, no exentos de efectos secundarios; psicoterapia, toxina botulínica y la simpatectomía torácica.
La toxina botulínica es una neurotoxina muy potente producida por Clostridium botulinum (bacteria anaerobia grampositiva), responsable del botulismo. Su mecanismo de acción consiste en bloquear la liberación de acetilcolina en las sinapsis colinérgicas periféricas. Cuando la sinapsis se bloquea, se estimula la neurogénesis y brotan nuevas terminaciones en la porción terminal del axón, con lo que la neurotransmisión se recupera en semanas o meses9–14. Existen 7 serotipos de toxina botulínica (A, B, C1, D, E, F y G). Los 7 serotipos tienen diferencias de biosíntesis, tamaño y mecanismo de acción. En el tratamiento de la hiperhidrosis primaria se utiliza la toxina botulínica A (TB-A).
Los objetivos de este estudio han sido definir el perfil clínico de los pacientes con hiperhidrosis primaria palmar y/o axilar estudiados en el servicio de Dermatología del Hospital Clínico Universitario de Valencia para la valoración de tratamiento con toxina botulínica A (TB-A) y evaluar en la práctica clínica los resultados, tolerancia y tiempo de remisión que consigue el tratamiento con TB-A en la hiperhidrosis primaria axilar y/o palmar.
Material y métodosRealizamos un estudio descriptivo, prospectivo y observacional de los pacientes tratados por primera vez con TB-A por hiperhidrosis primaria axilar y/o palmar entre septiembre del 2006 y abril del 2008 en el servicio de dermatología del Hospital Clínico Universitario de Valencia.
PacientesLa muestra acota un total de 52 pacientes, 39 mujeres y 13 hombres, con diagnóstico de hiperhidrosis primaria tratada por primera vez con TB-A. Los criterios de inclusión fueron la entrega de una encuesta, realizada por nosotros, cumplimentada a los 2 meses y el haber sido revisados y entrevistados un período mínimo de 12 meses posteriormente al tratamiento.
El tratamiento con TB-A se realizó en 20 pacientes por hiperhidrosis axilar, en 22 por hiperhidrosis palmar y en 10 pacientes por hiperhidrosis palmar y axilar. En total se trataron 60 axilas y 64 palmas.
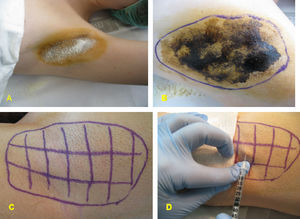
MétodosA todos los pacientes se les realizó una evaluación pretratamiento (descartar hiperhidrosis secundaria y contraindicaciones para el uso de TB), identificación objetiva del área de hiperhidrosis (test de Minor) y fotodocumentación de la misma. Todos los pacientes firmaron el consentimiento informado y uso compasivo (si la localización a tratar era palmar) para el tratamiento de la hiperhidrosis primaria con TB-A.
Además se les entregó una encuesta que entregaron cumplimentada a los 2 meses y en siguientes revisiones se recogieron una serie de datos de interés de cada paciente.
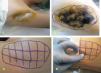
Para el tratamiento de la hiperhidrosis axilar se diluyó el vial de TB-A (Botox®; Allergan, Irvine, CA, EE.UU.), que contiene 100MU, en 4ml de suero salino, obteniéndose una concentración de 25MU/ml. Se marcaron 20 puntos en el área previamente identificada en cada axila y se inyectaron 0,1 ml en cada punto; colocando un total de 50MU en cada axila (fig. 1). No se requirió anestesia ya que la inyección en la axila es usualmente bien tolerada.
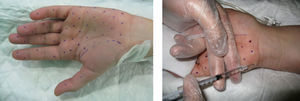
Para el tratamiento de la hiperhidrosis palmar se diluyó el vial de TB-A en 5ml de suero salino, obteniéndose una concentración de 20MU/ml. Se marcaron 30 puntos en cada palma, evitando la eminencia tenar, y 20 en cara palmar de los dedos (1 en cada falange proximal y media y 2 en falanges distales) y se inyectaron 0,1ml en cada punto, colocando un total de 100MU en cada palma (fig. 2). En todos los casos de hiperhidrosis palmar, se realizó previamente anestesia loco-regional.
La encuesta constaba de una primera parte de preguntas acerca de datos epidemiológicos y clínicos de interés: edad, sexo, profesión, edad de inicio de la hiperhidrosis, antecedentes familiares con el mismo problema, afectación de más áreas de hiperhidrosis además de la tratada, signos/síntomas acompañantes y tratamientos previos; una segunda parte en la que preguntamos a los pacientes el inicio del efecto de la TB-A; efectos secundarios locales y/o sistémicos y una tercera parte en la que preguntamos sobre el grado de severidad de su hiperhidrosis antes del tratamiento y 2 meses después del mismo, utilizando «La escala de severidad de la hiperhidrosis»:
- 1.
• Puntuación 1: mi sudoración no es notable y no interfiere con mi actividad diaria.
- 2.
• Puntuación 2: mi sudoración es tolerable pero a veces interfiere con mi actividad diaria.
- 3.
• Puntuación 3: mi sudoración es poco tolerable y frecuentemente interfiere con mi actividad diaria.
- 4.
• Puntuación 4: mi sudoración es intolerable y siempre interfiere en mi vida diaria.
La escala de severidad de la hiperhidrosis es rápida y fácil de entender. Ofrece una medida cualitativa del grado de afectación del paciente basado en cómo afecta la hiperhidrosis a su vida diaria. Una puntuación de 3 o 4 indica hiperhidrosis severa. Una puntuación de 1 o 2 indica hiperhidrosis leve o moderada.
Además, la escala de severidad de la hiperhidrosis, sirve postratamiento, como un instrumento de medida de la eficacia del tratamiento y de la satisfacción del paciente.
Una mejoría de 1 punto ha sido asociada con una reducción del 50% de la producción de sudor y una mejoría de 2 puntos con una reducción del 80%15,16.
Posteriormente se recogieron los siguientes datos de cada paciente: tiempo en el que se reinicia la sudación y presencia de efectos secundarios locales y sistémicos a largo plazo.
Análisis estadístico e interpretación de la informaciónLa base de datos y su procesamiento y análisis se realizaron con el paquete estadístico para las ciencias sociales SPSS (versión 15). Para evaluar la efectividad del tratamiento, se compararon los resultados de la escala de severidad antes y después de dos meses de iniciar el tratamiento mediante ANOVA de muestras repetidas. Para evaluar el efecto de variables confusoras, analizamos los datos de la eficacia del tratamiento usando edad del paciente en el momento del tratamiento, sexo (hombre o mujer), localización del tratamiento (axila y palma), y edad de inicio de la hiperhidrosis como covariables en modelos multifactoriales de ANOVA de muestras repetidas. Cuando detectamos alguna interacción significativa con alguna covariable, realizamos estudios seleccionando tipo de sexo (hombre o mujer) o tipo de localización (axila y palma) para esclarecer la causa de la interacción. Por último, definimos una nueva variable (Respuesta) como la diferencia en la escala pre- y postratamiento. En este caso analizamos los resultados mediante ANOVA simple usando como variable independiente el sexo o la localización del tratamiento y como variable dependiente la variable Respuesta. Todos los análisis fueron bivariados y los valores que se muestran en el texto o en las tablas son media±desviación estándar. La significación se definió como p<0,05.
ResultadosLa edad media de los pacientes es 29,8±9,5 años (media±DS); con una mediana de 29 (rango 15–53). De ellos, el 75% (n=52) son mujeres con una edad media de 29,9 años, y el 25% son hombres con una edad media de 31,9 años.
En cuanto a la profesión u ocupación laboral de los pacientes, el 26,9 % trabaja en la administración, el 21,1% son estudiantes, el 13,5% se dedica a la construcción, la industria o el transporte, el 11,5% son profesionales liberales, el 9,6% trabaja en un comercio, el 7,6% en la sanidad, el 3,8% en la hostelería y el 5,8% no tiene trabajo.
Por lo que se refiere a los antecedentes patológicos, 2 habían sido diagnosticados de hipotiroidismo y 1 de hipertensión arterial; estos pacientes siguen tratamiento específico.
En relación con la historia familiar de hiperhidrosis, 19 (36,5%) tienen un familiar de primer grado afectado de hiperhidrosis primaria con una localización y gravedad variables.
En cuanto a la clínica, la edad media de inicio de hiperhidrosis fue 11,38±4,6 años (media±DS), con una mediana de 10 (rango 5–30). El inicio fue en la edad puberal en un 61,5% (n=32), en la infancia en un 35% y su aparición fue tardía en el 6,25% restante.
La localización de la hiperhidrosis es palmar en 22 pacientes (42,3%), axilar en 20 pacientes (38,5%), palmar y axilar en 10 pacientes (19,2%). En cuanto a la pregunta relativa a la sudación en otras regiones corporales, se observa que los pacientes que consultan por sudación en una región exclusiva refieren igual sudación en otras zonas del cuerpo, en la siguiente proporción: en las manos el 61,5 % (n=32), seguido de pies (53,8%), axilas (59,6%), región inguinal (15,4%), región facial (11,5%), espalda (9,6%), pecho (7,7%) y abdomen (5,8%) (tabla 1).
En cuanto a la presencia de síntomas y signos asociados, el 71,8% de los pacientes con hiperhidrosis palmar presenta frialdad en las manos y el 81,2% eritema. El 34,3% de estos, refiere lesiones cutáneas acompañantes a la hiperhidrosis en forma de onicopatía, prurito y descamación (tabla 2).
Respecto a la sintomatología acompañante, en el 32,7% de los casos la hiperhidrosis primaria coexiste con eritema facial, con palpitaciones en el 30,7%, con tensión muscular en el 28,8%, con temblor en el 23%, con cefalea en el 17,3%, con vacío gástrico o epigastralgia inespecífica en el 15,4% y sequedad de boca en el 13,5% (tabla 3).
Clínica acompañante de la hiperhidrosis
| Clínica | N.o pacientes | Porcentaje |
|---|---|---|
| Cefalea | 9 | 17,3 |
| Eritema facial | 17 | 32,7 |
| Sequedad boca | 7 | 13,5 |
| Epigastralgia/vacío gástrico | 8 | 15,4 |
| Tensión muscular | 15 | 28,8 |
| Temblor | 12 | 23 |
| Palpitaciones | 16 | 30,7 |
Todos los casos habían recibido tratamiento médico previo sin buenos resultados. Los 52 pacientes (100%) habían recibido tratamientos tópicos, 3 pacientes (5,77%) tratamientos farmacológicos sistémicos y solamente 1 paciente (1,9%) había realizado tratamiento con iontoforesis.
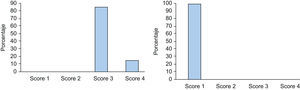
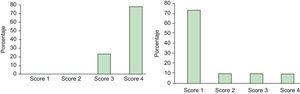
La puntuación según la «Escala de Severidad de la Hiperhidrosis» previa al tratamiento para los pacientes tratados solamente por hiperhidrosis axilar fue de 3 en 17 pacientes (85%) y de 4 en 3 pacientes (15%). Dos meses después del tratamiento los 20 pacientes (100%) alcanzaron una puntuación de 1 (fig. 3).
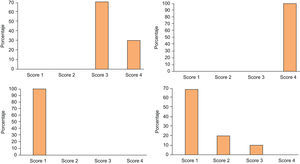
De los pacientes tratados solamente por hiperhidrosis palmar, 5 pacientes se consideraron en una puntuación de 3 (22,72%) y 17 en una puntuación de 4 (77,27%) previamente al tratamiento con TB-A. Dos meses después del tratamiento, 16 pacientes alcanzaron una puntuación de 1 (72,72%); 2 pacientes pasaron de una puntuación de 4 a una puntuación de 2 (9,09%); 2 pacientes marcaron una puntuación de 3 (9,09%) posteriormente al tratamiento (uno de ellos pasó de 4 a 3 por la persistencia de la sudación a nivel de pulpejos y caras laterales de los dedos y el otro paciente no experimentó mejoría en la escala de severidad de la hiperhidrosis, manteniéndose en una puntuación de 3, dado que el efecto del tratamiento con TB-A solamente persistió un mes). Por último, 2 pacientes no mejoraron su puntuación inicial de 4 (9,09%); en uno de ellos el tratamiento no fue efectivo y en otro la duración del efecto fue de tan solo 1,5 meses (fig. 4).
De los diez pacientes que fueron tratados por hiperhidrosis palmar y axilar, 7 pacientes consideraron para su hiperhidrosis axilar una puntuación de 3 (70%) y 3 pacientes una puntuación de 4 (30%) antes de iniciar el tratamiento; mientras que los diez pacientes marcaron una puntuación de 4 (100%) para su hiperhidrosis palmar.
Dos meses después, el 100% de los pacientes alcanzaron una puntuación de 1 para su hiperhidrosis axilar y respecto a la hiperhidrosis palmar: 7 pacientes marcaron una puntuación de 1 (70%), 1 paciente pasó de 4 a 3 (10%) por mantener la hipersudación a nivel de los pulpejos y eminencia tenar y 2 pacientes pasaron de 4 a 2 (20%).
El inicio del efecto de la inyección de TB-A en los 30 pacientes tratados por hiperhidrosis axilar fue de 3,8±3,5 días (media±DS); la mediana fue de 2 días (rango 1–14).
La inyección de TB-A por hiperhidrosis palmar se realizó en un total de 32 pacientes pero en uno de ellos no fue efectiva; para los 31 pacientes en que sí se objetivó efecto, el inicio del mismo se observó en 3,6±3,4 días (media±DS); con una mediana de 2 días en un rango de 1–15 días.
Los 30 pacientes (100%) tratados por hiperhidrosis axilar presentaron reinicio de sudación en una media de 6,6±2,3 meses (media±DS), con una mediana de 6 meses en un rango de 1–12 meses.
De los 32 pacientes tratados por hiperhidrosis palmar, en los 31 pacientes (96,9%) en los que sí fue efectivo el tratamiento, la duración del efecto del mismo fue de 4,9±1,9 meses (media±DS), siendo la mediana de 5 meses en un rango de 1–9 meses.
Respecto a los efectos secundarios locales a corto plazo, solamente 5 pacientes de los 30 tratados por hiperhidrosis axilar (16,6%), refirieron irritación local de menos de 24 horas de duración y 2 pacientes de los 32 tratados por hiperhidrosis palmar (6,25%) presentaron hematomas postratamiento. Por otro lado, en 16 pacientes de los 32 tratados por hiperhidrosis palmar (50%), se produjo debilidad transitoria en las manos, afectando a la pinza entre el pulgar y el índice con una duración de 2±0,8 semanas (media±DS).
No se observó ningún efecto local a largo plazo (período mínimo de seguimiento de 12 meses tras la primera sesión de tratamiento) ni ningún efecto sistémico en los 52 pacientes.
Respecto a la escala de severidad de la hiperhidrosis, se produce una mejoría muy significativa (p<1,0×10−32; potencia estadística=1) a los dos meses del tratamiento cuando analizamos los datos conjuntos sin tener en cuenta localización ni sexo. Además, el tratamiento es efectivo independientemente de la edad del paciente, ya que cuando pusimos la edad del paciente como covariable, la interacción entre la edad y el tratamiento no fue significativa. Lo mismo se observó con la edad de inicio de la hiperhidrosis y con el área de aplicación del tratamiento. Sin embargo, el tratamiento sí depende del sexo porque la interacción entre tratamiento y sexo fue significativa (p=0,019). Por tanto, dado que existía una interacción de la efectividad del tratamiento con el sexo, decidimos estudiar el efecto del sexo en las dos localizaciones por separado (ver más abajo).
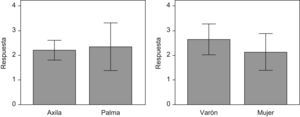
De este modo, se observa que la respuesta al tratamiento (diferencia de la escala de severidad dos meses después del tratamiento y antes del tratamiento) no presenta diferencias significativas entre las dos localizaciones del tratamiento pero sí entre los dos sexos (fig. 5).
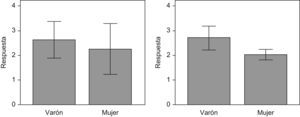
Por último, al comparar la respuesta obtenida por localizaciones, se observa que en la palma no hay diferencias significativas de respuesta entre hombres y mujeres; sin embargo, sí hay diferencias significativas de respuesta entre hombres y mujeres a nivel axilar (figs. 6 y 7).
La hiperhidrosis primaria es un trastorno caracterizado por una hiperactividad simpática, aunque no está claro si de forma generalizada o localizada en los ganglios simpáticos encargados de la inervación sudomotora de la extremidad superior, en la mayoría de los casos17,18.
Esta entidad clínica ha sido durante años motivo de estudio con el objetivo de eliminar dicha sudación no por los problemas clínicos que la acompañan, sino más bien por los problemas que comporta en la vida diaria o como síntoma de otras enfermedades19. Los resultados obtenidos en nuestra serie nos permiten delimitar las características clínicas habituales del paciente hiperhidrótico en nuestra área de influencia.
En nuestro estudio el inicio del proceso es fundamentalmente en la edad puberal, edad clásica de debut1,20; sin embargo, para otros autores19 se produce en la infancia (en nuestra serie presentan esta circunstancia 18 pacientes). Son pacientes con escasas enfermedades asociadas, debido posiblemente a su baja media de edad.
En nuestra serie, hemos registrado un 36,5% de pacientes con familiares de primer grado afectados de hiperhidrosis. Este hallazgo ha sido notificado por otros autores, los cuales han considerado empíricamente que la etiología es debida a un trastorno hereditario autosómico dominante21, o a un trastorno hereditario con penetrancia incompleta no relacionado con el sexo22. Sin embargo, no se puede hablar de la hiperhidrosis primaria como una enfermedad hereditaria, ya que no se han de excluir otras causas.
En cuanto a la hipersudación, se observa que no se localiza exclusivamente en un área, sino que se extiende a otras regiones corporales, lo que indica que la hiperhidrosis focal podría ser el signo más predominante de una hiperfunción simpática, más o menos generalizada, que en algunos casos se manifiesta en diferente intensidad, aunque solo es una hipótesis que no podemos confirmar en este estudio.
Respecto a la sintomatología acompañante, muchos pacientes refieren una clínica que no podemos esclarecer si es causa o consecuencia de la hiperhidrosis. Existen estudios que mencionan la hiperhidrosis primaria como síntoma de trastornos psiquiátricos, como es la fobia social23, o la relacionan con un alto grado de ansiedad6. La posible psicopatología de los pacientes hiperhidróticos ha sido estudiada por algunos autores, que observan que la clínica de ansiedad y depresión que refieren es reactiva a la hiperhidrosis, sin ser su causa24.
En cuanto a la profesión, los pacientes coinciden en referir incomodidad y un elevado grado de ansiedad ante situaciones que requieren el contacto manual e incluso el contacto social con un grupo de personas.
Por otro lado, hemos observado una mejoría estadísticamente significativa en la escala de severidad de la hiperhidrosis, siendo esta mayor a nivel axilar en los hombres respecto a las mujeres. No obstante, se requieren más estudios para confirmar este hallazgo, que no es el objetivo de este estudio.
Se han descrito duraciones más prolongadas de la anhidrosis axilar utilizando altas dosis (200 MU de Botox por axila)25,26; no obstante, el uso de altas dosis podría incrementar el riesgo de formación de anticuerpos neutralizantes y/o los efectos secundarios.
En conclusión, nuestro estudio indica que la hiperhidrosis focal es un trastorno con una clínica que se inicia sobre todo en la edad puberal; los pacientes tienen pocas enfermedades asociadas y una repercusión dermatológica local acompañante de baja intensidad. Este proceso puede que tenga una base genética, por el grado de coincidencia en miembros familiares, la clínica se caracteriza por hipersudación no solo en una región corporal sino en varias y además puede presentar sintomatología acompañante.
Dado que la hiperhidrosis primaria es un proceso frecuente y con repercusiones importantes en la vida cotidiana de los pacientes; cuando los síntomas no se controlan con tratamientos tópicos, la infiltración con toxina botulínica es una opción terapéutica razonable antes que los tratamientos quirúrgicos.
Se trata de un tratamiento de fácil aplicación, con mínimos efectos secundarios, y con buena tolerabilidad en el proceso de aplicación. Las limitaciones a su uso derivan de su coste y de la duración transitoria de los efectos terapéuticos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.