Paradójicamente se han descrito casos de inducción o empeoramiento de una psoriasis durante el tratamiento con todos los agentes anti-factor de necrosis tumoral α (anti-TNFα) (infliximab, etanercept, adalimumab y certolizumab). Se ha postulado que la alteración del equilibrio entre el TNFα y el interferón α estaría implicada en su etiopatogenia. Clínicamente se distinguen varios patrones de reacciones psoriasiformes paradójicas: la psoriasis de novo en pacientes que no han presentado anteriormente esta enfermedad y que reciben este tratamiento por otra enfermedad inflamatoria, que es la más frecuente y la mejor descrita, y la exacerbación de una psoriasis preexistente durante la terapia anti-TNFα, que puede presentarse con o sin un cambio de morfología. En este trabajo realizamos una revisión de la literatura en relación con las características clínicas e histológicas de este tipo de reacciones, así como de su evolución y tratamiento, y planteamos un esquema de manejo en la práctica clínica.
There have been reports of paradoxical induction or worsening of psoriasis during treatment with tumor necrosis factor (TNF) α agents (infliximab, etanercept, adalimumab, and certolizumab). It has been hypothesized that an imbalance between TNF-α and interferon α might have a role in the etiology and pathogenesis of these reactions. Paradoxical psoriasiform reactions can be divided clinically into de novo psoriasis and exacerbation of preexisting psoriasis. The first, which is more common and more extensively described in the literature, occurs in patients without a history of psoriasis who are receiving TNF-α therapy for another inflammatory disorder. The second can occur with or without changes in the morphology of the lesions. In this article, we review the literature on the clinical and histologic features of paradoxical psoriasiform reactions, analyze their clinical course and treatment, and propose a clinical management model for use in routine practice.
La psoriasis es una enfermedad inflamatoria crónica de etiología desconocida, que afecta aproximadamente al 2-3% de la población mundial1. Se postula que es debida al resultado de la combinación de factores genéticos y ambientales. Existe una predisposición genética, sin que se haya podido describir un patrón hereditario mendeliano clásico1.
Se han descrito múltiples factores que actúan como desencadenantes o agravantes de la psoriasis o de nuevos brotes, como las infecciones, el estrés o fármacos (bloqueadores beta, litio…)1,2.
Se han propuesto distintas hipótesis y modelos para intentar explicar la patogénesis de la psoriasis, de la que actualmente se conoce que no hemos de detenernos en la piel, sino que presenta múltiples comorbilidades como la artritis psoriásica o la enfermedad cardiovascular3,4. Una hipótesis unificadora es el modelo de la red de citocinas, que defiende que tanto un estímulo exógeno, como por ejemplo el estrés, como uno endógeno, como los virus, los neuropéptidos o la ingesta de fármacos, pueden actuar como desencadenantes para iniciar una cascada de citocinas. Entre ellas se encontrarían el factor de necrosis tumoral α (TNFα) derivado de las células dendríticas presentadoras de antígeno y los queratinocitos y el interferón (IFN)-γ producido por linfocitos Th1 activados1.
Alrededor del 90% de los individuos con psoriasis presenta el tipo más frecuente, la denominada psoriasis en placas o psoriasis vulgar. En la mayoría de los casos se trata de formas leves que se controlan con tratamientos tópicos. No obstante, hasta un tercio de los pacientes desarrolla una psoriasis moderada-severa y requiere modalidades terapéuticas sistémicas, como la fototerapia, la acitretina, el metotrexato o la ciclosporina5. Debido a la falta de respuesta o a la toxicidad de estos fármacos en muchos casos, en los últimos 15 años se han desarrollado las denominadas terapias biológicas que actúan a distintos niveles de la cascada inflamatoria que da lugar a las placas de psoriasis.
El uso de la terapia biológica en general está aumentando en el tratamiento no solo de la psoriasis, sino de otras enfermedades inflamatorias crónicas inmunomediadas como la artritis reumatoide, la espondilitis anquilosante o la enfermedad inflamatoria intestinal. En la actualidad, los más utilizados son aquellos fármacos que bloquean el TNFα (infliximab, etanercept y adalimumab). No obstante, se han publicado algunos efectos adversos durante su uso, como infecciones, reactivación de la tuberculosis latente, enfermedades desmielinizantes o insuficiencia cardíaca congestiva6–8.
En cuanto a los efectos secundarios cutáneos derivados del uso de terapia anti-TNFα se ha puesto de manifiesto que son más prevalentes de lo estimado9. Entre ellos se han descrito reacciones en el punto de infusión o inyección, infecciones cutáneas, eccema e, incluso, psoriasis o reacciones psoriasiformes, entre otras10. Aunque resulte paradójico, puesto que estos fármacos han demostrado su eficacia en el tratamiento de la psoriasis11–17, se han publicado casos individuales y algunas series de pacientes que desarrollan un empeoramiento de la misma o, incluso, la aparición de novo de distintos subtipos de psoriasis durante el uso de la terapia anti-TNFα9,10,18–73. Los artículos y revisiones más destacadas se resumen en las tablas 1 y 2.
Revisión de la literatura: artículos con al menos 8 pacientes que desarrollaron reacciones paradójicas psoriasiformes durante el tratamiento con fármacos anti-TNF
| Referencia | Tipo de reacción | Enfermedad basal | Número total de pacientes | N.° de pacientes con cada agente anti-TNF |
| Kary et al. (2006)36 | De novo | AR | 5 | Infliximab 2 Etanercept 3 Adalimumab 4 |
| Exacerbación sin cambio morfológico | 4 | Infliximab 2 Etanercept 3 Adalimumab 1 | ||
| Goiriz et al. (2006)31 | De novo | Reumatológica | 2 | Infliximab 1 Adalimumab 1 |
| Cambio morfológico | Psoriasis | 6 | Etanercept 6 | |
| De Gannes et al. (2007)52 | De novo | Reumatológica | 15 | Infliximab 5 Etanercept 6 Adalimumab 4 |
| Lee et al. (2007)69 | De novo | Reumatológica | 6 | Infliximab 3 Etanercept 2 Adalimumab 1 |
| Exacerbación sin cambio morfológico | 2 | Etanercept 1 Adalimumab 1 | ||
| Seneschal et al. (2007)48 | De novo | Reumatológica | 13 | Infliximab 7 Etanercept 3 Adalimumab 3 |
| Harrison et al. (2009)54 | De novo | AR | 25 | Infliximab 6 Etanercept 6 Adalimumab 13 |
| Cullen et al. (2011)27 | De novo | EII | 30 | Infliximab 21 Adalimumab 7 Certolizumab 2 |
| Guerra et al. (2012)33 | De novo | EII | 21 | Infliximab 14 Adalimumab 7 |
AR: artritis reumatoide; EII: enfermedad inflamatoria intestinal;TNF: factor de necrosis tumoral.
Revisiones más relevantes publicadas en la literatura
| Referencia | Tipo de reacción | Enfermedad basal | Número total de pacientes | Porcentaje de casos con los distintos agentes anti-TNF |
| Collamer et al. (2008)26 | Psoriasis de novo y exacerbaciones con/sin cambios de morfología | Reumatológica, digestiva y psoriasis | 104 | Infliximab 53 Etanercept 29 Adalimumab 18 |
| Wollina et al. (2008)9 | Psoriasis de novo y exacerbaciones con/sin cambios de morfología | Reumatológica, digestiva y psoriasis | 120 | Infliximab 52,5 Etanercept 30,8 Adalimumab 21,7 |
| Ko et al. (2009)37 | Psoriasis de novo y exacerbaciones con/sin cambios de morfología | Reumatológica, digestiva y psoriasis | 127 | Infliximab 55,1 Etanercept 27,6 Adalimumab 17,3 |
| Collamer et al. (2010)25 | Psoriasis de novo y exacerbaciones con/sin cambios de morfología | Reumatológica, digestiva y psoriasis | 207 | Infliximab 59 Etanercept 19 Adalimumab 22 |
| Cullen et al. (2011)27 | Psoriasis de novo | Digestiva | 120 | Infliximab 79 Adalimumab 17 Certolizumab 4 |
| Denadai et al. (2012)28 | Psoriasis de novo | Digestiva | 222 | Infliximab 69,4 Adalimumab 22,5 Certolizumab 2,7Sin especificar 5,4 |
TNF: factor de necrosis tumoral.
Moustou et al. publicaron una revisión de la literatura en la que establecieron la fuerza de asociación entre los efectos adversos publicados y el uso de uno o varios agentes anti-TNFα, dividiéndola en pobre, moderada, fuerte o definitivamente asociada. Los criterios de inclusión utilizados fueron: el tipo de estudios (metaanálisis, ensayos aleatorizados, estudios retrospectivos o prospectivos, series de casos o casos clínicos) publicados que describían dicho efecto adverso, el número de agentes anti-TNFα implicados, el número de las distintas enfermedades inflamatorias en las que había aparecido la reacción adversa durante el tratamiento con fármacos anti-TNFα y la evolución tras la retirada y la reintroducción del fármaco. Los autores no describieron solo la clínica de estas reacciones cutáneas, sino que establecieron que existía una relación fuerte entre la terapia anti-TNFα y la aparición de psoriasis de novo o reacciones psoriasiformes10.
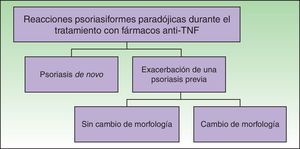
ClasificaciónClínicamente se distinguen varios patrones de reacciones psoriasiformes paradójicas durante el tratamiento con fármacos que bloquean el TNFα (fig. 1):
- -
Inducción de psoriasis de novo, es decir, aparición de lesiones de psoriasis en los pacientes que no han presentado anteriormente esta enfermedad y que reciben este tratamiento por otra enfermedad inflamatoria.
- -
Exacerbación de una psoriasis preexistente durante la terapia anti-TNFα, que puede presentarse con o sin un cambio de morfología.
La fisiopatología de la inducción o empeoramiento de una psoriasis durante el tratamiento con bloqueadores del TNFα es actualmente desconocida. Se han postulado varias teorías, como la alteración del equilibrio entre el TNFα y el IFNα, la activación de los linfocitos T autorreactivos, el diagnóstico erróneo, el curso natural de la enfermedad primaria o infecciones que desencadenarían dichas reacciones9,10,25,37. Collamer et al. explicaron en su artículo que en la patogénesis de las reacciones psoriasiformes estaría implicado un disbalance de citocinas que conduciría a un aumento de la producción de INF-α por las células dendríticas en personas genéticamente predispuestas, y que los polimorfismos genéticos podrían desempeñar un papel en esta reacción paradójica secundaria al bloqueo del TNFα25.
En su artículo de 2007 de Gannes et al. demostraron que los pacientes en tratamiento con agentes anti-TNFα que desarrollaron psoriasis de novo presentan una expresión aumentada de proteína anti–myxovirus-resistance protein A (MxA), una adenosina trifosfatasa que se induce selectivamente en respuesta al INF tipo 1, que puede utilizarse como un marcador subrogado de la actividad lesional del INF tipo 1. En este trabajo la tinción para MxA en las biopsias de los pacientes en tratamiento con anti-TNFα era más intensa que en aquellos con psoriasis vulgar no asociada a terapia anti-TNFα. Este incremento promovería la formación de lesiones de psoriasis en individuos predispuestos52. Posteriormente, Seneschal et al. describieron 13 pacientes que desarrollaron distintos subtipos de psoriasis, en cuyas biopsias se detectaba aumento de la producción de la proteína MxA comparadas con las biopsias de piel sana y psoriasis no inducida. Para estos autores esto denota que el incremento de IFNα junto con un disbalance de citocinas, ambos secundarios a la inhibición del TNFα, ejercería un papel importante en el desarrollo de este tipo de reacciones, considerándolas una forma de reacción medicamentosa que diferiría de verdaderas psoriasis48.
No obstante, en otro trabajo no hallaron diferencias entre psoriasis inducida y no-inducida en el análisis inmunohistoquímico con tinciones frente al ARNm de IFN y TNFα y el factor de crecimiento del endotelio vascular53.
Algunos autores han supuesto que debe existir una predisposición genética, puesto que la mayoría de los pacientes tratados con terapia anti-TNFα debido a muy diferentes enfermedades no desarrollan psoriasis. Algún factor ambiental podría actuar también dado que la latencia entre el inicio del tratamiento y la aparición de la psoriasis es muy variable (de días a años)25,27,37.
Debido a esta elevada variabilidad resulta difícil establecer una relación causal en algunos casos. Por ello, es importante descartar cualquier otro factor que podría desencadenar su aparición, tales como una infección, traumatismos, situaciones de estrés o nuevos fármacos44.
Según algunos autores las reacciones psoriasiformes paradójicas son consecuencia de un efecto de clase, puesto que existen casos descritos con los 3 fármacos anti-TNFα clásicos (infliximab, etanercept y adalimumab), proporcionalmente a su prevalencia de uso37. Más recientemente se ha descrito este fenómeno en pacientes que recibían tratamiento con certolizumab, un anti-TNFα de más reciente utilización. En relación con este fármaco hemos hallado en la literatura 6 casos en una revisión de pacientes con enfermedad inflamatoria intestinal, además de otro caso en nuestra experiencia clínica27. La recaída tras la administración de fármacos anti-TNFα distintos apoya la teoría del efecto de clase25,27,33,36,37,55.
No obstante, en la literatura médica se han publicado casos de inicio o empeoramiento de una psoriasis durante el tratamiento con otros fármacos anti-psoriásicos distintos a los anti-TNFα como efalizumab, ciclosporina, suspensión de glucocorticoides, antralina o fototerapia55. Otros tratamientos biológicos se han visto implicados, como el abatacept en un paciente que tuvo un brote de psoriasis guttata durante el tratamiento con etanercept y 2 años más tarde un nuevo brote con la misma morfología mientras recibía tratamiento con abatacept70. Esto supone para Rallis et al. una brecha en el conocimiento de la fisiopatología de la psoriasis y del mecanismo exacto por el que actúan algunos de estos fármacos44.
Psoriasis de novoLa gran mayoría de los casos publicados corresponden a este subtipo, especialmente pacientes con enfermedades reumatológicas que desarrollaron una psoriasis de novo. Basados en los estudios publicados se describe que la prevalencia de psoriasis durante la terapia anti-TNFα supone entre un 0,6 a 5,3%, dependiendo de las variaciones de las distintas poblaciones estudiadas y tratadas27,54. En una reciente publicación de casos de psoriasis inducida durante el tratamiento con agentes anti-TNFα en pacientes con enfermedad inflamatoria intestinal describen una prevalencia del 1,62%33.
Los datos proporcionados por las series de mayor tamaño publicadas y de las revisiones de la literatura no son del todo homogéneos. Ello, unido a que no todos los casos existentes habrán sido publicados, puede conducir a unas conclusiones parcialmente sesgadas. En una revisión reciente, en la que se describen 207 casos, se excluyen aquellos pacientes con algún factor desencadenante conocido. De ellos el 85% eran pacientes que habían experimentado la aparición de un brote de psoriasis de novo25.
Existe un predominio femenino (2 mujeres:1 hombre), a expensas de los casos con artritis reumatoide y enfermedad inflamatoria intestinal25,37. Las series en artritis reumatoide muestran mayor variación, hasta de 5,3 mujeres:1 hombre54. Incluyendo todos los casos la edad media de aparición es de 44,9 años (13-78 años)25; sin embargo, los pacientes con enfermedad digestiva presentan una edad media menor (30 años)27.
Tomando todos los casos revisados en su totalidad el fármaco más frecuentemente implicado es infliximab, lo que supone un 55,1-59%25,37. En su revisión de la literatura Ko et al. identificaron 127 casos publicados hasta septiembre de 2007, señalando que el segundo fármaco más frecuente era etanercept (27,6%) y por último adalimumab (17,3%)37. Sin embargo, en la serie más reciente de Collamer et al. el 22% del total de los casos estaba en tratamiento con adalimumab y el 17% con etanercept25.
Cullen et al. aportaron 30 casos realizando una revisión exclusivamente de los casos de enfermedad inflamatoria intestinal, en la que incluyeron 120 pacientes. Teniendo en cuenta que el uso de etanercept no está aprobado en estas enfermedades, sus resultados indicaron que el 79% recibía infliximab, el 17%, adalimumab y el 4% de los casos el nuevo fármaco, certolizumab27.
Estos porcentajes serían proporcionales a la utilización de cada uno de los fármacos. Contrariamente a estos datos, en una serie de pacientes del Registro de la Sociedad Británica para los Biológicos en Reumatología en la que describieron 25 casos de psoriasis de novo en una cohorte de 9.826 pacientes con AR, 13 de ellos estaban en tratamiento con adalimumab. En este trabajo comparan este grupo con otro constituido por pacientes en tratamiento con fármacos modificadores de la enfermedad (DMARD) en el que ningún paciente desarrolló psoriasis tras un seguimiento de 2,81 años54.
La latencia es altamente variable, desde días a 80 meses, con una media de 10,5 meses. En la revisión de Ko et al. los pacientes tratados con etanercept presentan una latencia menor, aunque el 42,9% se trata de casos en los que se desarrolló una exacerbación de una psoriasis previa, en lugar de una psoriasis de novo37. No obstante, otros autores como Chen et al., que realizaron una revisión de casos acontecidos con etanercept, también apoya que la latencia con este fármaco es menor. En los 25 pacientes que incluye la media es de 3,5 meses desde el inicio del tratamiento24.
Más de la mitad de los casos publicados ocurren en pacientes con enfermedad reumatológica, especialmente artritis reumatoide, que según distintas revisiones varía entre un 42,5-50,4%25,37.
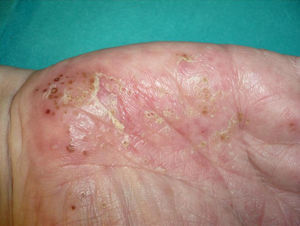
Se han descrito casos de cualquier tipo y localización de psoriasis: vulgar, guttata, invertida, pustulosa generalizada o palmoplantar (fig. 2), siendo esta última la más prevalente en las series y revisiones de mayor tamaño9,25,37. Se ha descrito que adalimumab es el fármaco que con mayor frecuencia desarrolla pustulosis palmoplantar. Más de la mitad de las reacciones paradójicas descritas con este fármaco muestran este subtipo. Sin embargo, en el artículo de Ko et al. los casos en tratamiento con etanercept presentaron con más frecuencia psoriasis en placas. No obstante, este hecho probablemente no pueda ser valorable puesto que, como ya hemos comentado, casi en la mitad de los casos se trataba de exacerbaciones37.
El hecho de que la incidencia de pustulosis palmoplantar en los casos de psoriasis inducida por anti-TNFα constituya el doble de la incidencia en la población general con psoriasis, podría sugerir que pueda existir un predominio del TNFα en las glándulas ecrinas en individuos predispuestos67.
En una revisión que incluía solamente casos publicados en pacientes con enfermedad inflamatoria intestinal los autores describieron que, en este tipo de pacientes, la afectación palmoplantar y del cuero cabelludo son las más frecuentes, suponiendo el 43 y 42% respectivamente27. No obstante, en una serie reciente española que incluye 21 casos de pacientes con enfermedad inflamatoria intestinal la afectación más frecuente era en forma de psoriasis en placas en las extremidades (62%), seguida del tronco y del cuero cabelludo33.
Entre el 36 y el 100% de los pacientes, según las series, recibían de manera concomitante otros tratamientos antipsoriásicos como el metotrexato o la azatioprina, por lo que no han demostrado ser capaces de prevenir este tipo de reacciones25,27,33.
En cuanto a la modalidad terapéutica, en la revisión de Ko et al. el tratamiento tópico con corticoides es el más utilizado, en casi el 40% de los casos, sin acompañarse de otros cambios en el tratamiento. En un cuarto de estos pacientes se describe la resolución de la psoriasis. Otro 50% utilizó tratamiento tópico junto con la retirada del agente anti-TNFα implicado. El uso de terapias anti-psoriásicas sistémicas con o sin suspensión del agente implicado fue más eficaz que los tratamientos tópicos (44% obtuvieron la resolución de las lesiones). Solamente el 15% de los individuos a los que se cambió a otro agente anti-TNFα obtuvieron una respuesta satisfactoria, mientras que el 64% de los que recibieron tratamientos con distinto mecanismo de acción la consiguieron. Por ello, estos autores consideran que lo esencial de la terapia es suspender el agente anti-TNFα. En los casos leve-moderados iniciarían tratamiento tópico o con fototerapia en monoterapia o junto con acitretina, según la respuesta, y en los casos agudos o graves ciclosporina o metotrexato podrían ser beneficiosos. En los casos en los que las lesiones cutáneas no se resolvieron no se han encontrado diferencias en cuanto a la gravedad del cuadro, el tipo o la distribución de la psoriasis37.
Sin embargo, en la revisión de Cullen et al. de pacientes con enfermedad inflamatoria intestinal aproximadamente el 50% respondieron a tratamiento tópico27, al igual que en el trabajo de Collamer et al. en el que la mayoría de los pacientes respondieron al tratamiento conservador, sin retirar el fármaco asociado25. En algunos casos, tanto de psoriasis de novo como de exacerbación, la suspensión o la disminución de la dosis del fármaco mejoró o hizo desaparecer las lesiones cutáneas en pacientes con artritis reumatoide36.
La más reciente incorporación de otros fármacos con distintos mecanismos de acción como ustekinumab, un agente anti-p40, abre el abanico de posibles tratamientos para este tipo de reacciones. Autores españoles presentaron una paciente con enfermedad de Crohn que desarrolló una psoriasis con 2 fármacos anti-TNFα (infliximab y adalimumab). Ustekinumab, a una dosis de 90mg cada 8 semanas, obtuvo la remisión de las lesiones cutáneas, manteniendo el control de la enfermedad digestiva con azatioprina y mesalazina47. Contradictoriamente, también se ha publicado algún caso en que, a pesar de este tratamiento, la pustulosis palmoplantar no se resuelve o incluso sufre una exacerbación46. Más recientemente Puig et al. presentaron su experiencia en otra paciente con artritis psoriásica y realizaron una revisión de casos tratados con ustekinumab. Estos autores concluyen que puede ser una buena opción terapéutica en los pacientes que desarrollen reacciones paradójicas con anti-TNFα43.
Exacerbación de una psoriasis previaA pesar de que en nuestra práctica clínica habitual es más frecuente el desarrollo de un agravamiento de una psoriasis previa con o sin cambio de morfología, en la literatura solamente supone el 15% de los casos incluidos en una revisión de 207 pacientes. Por consiguiente, es difícil establecer las características de este tipo de reacción. En el análisis de estos pacientes, a diferencia de los casos de psoriasis de novo, no existe una diferencia significativa por sexos y el agente más frecuentemente implicado es etanercept (62%), seguido de los anticuerpos monoclonales, infliximab y adalimumab, en el 23 y 15% de los casos respectivamente. Son necesarios más estudios que aclaren si esta diferencia es significativa o se debe a que etanercept es el agente más empleado en Dermatología. Estos autores defienden que los pacientes con psoriasis y artritis psoriásica tienden a desarrollar lesiones de un tipo diferente a su psoriasis previa, el más frecuente la psoriasis en gotas. En el 38% de estos pacientes se resolvieron las lesiones tras suspender el agente implicado y en un 53% se alcanzó una remisión total o parcial manteniéndolo y añadiendo otros tratamientos antipsoriásicos25. Los datos sobre recidivas con otros fármacos anti-TNFα son poco valorables de manera conjunta debido a la heterogenicidad de los pacientes y al corto seguimiento en algunos de ellos, por lo que se mencionarán en cada subtipo.
Exacerbación de una psoriasis previa sin cambio de morfologíaMourao et al. realizaron una revisión publicada en 2010 en la que describieron 5 casos ya publicados y aportaron otros 3 en los que se describía la exacerbación de una psoriasis previa durante el tratamiento con un agente anti-TNFα. En una de las pacientes etanercept perdió eficacia tras 41 meses y posteriormente la enfermedad cutánea empeoró durante el uso de adalimumab e infliximab. El período de latencia de este agravamiento es muy variable, habiéndose descrito desde 2 semanas hasta 32meses tras el inicio de la exposición. No existían factores desencadenantes claros55.
Se ha descrito también la posibilidad de reaparición de las lesiones cutáneas en pacientes con una psoriasis latente durante el tratamiento con terapia anti-TNFα para el control de la artritis reumatoide. Kary et al. aportaron 3 casos, 2 presentaron un brote de psoriasis pustulosa y otro de psoriasis en placas. Para estos autores la mejoría tras la suspensión o disminución de la dosis del fármaco implicado refuerza la relación con el fármaco36.
En algunos casos con artritis psoriásica las lesiones cutáneas empeoraron, mientras que la artritis respondía de manera adecuada al tratamiento55.
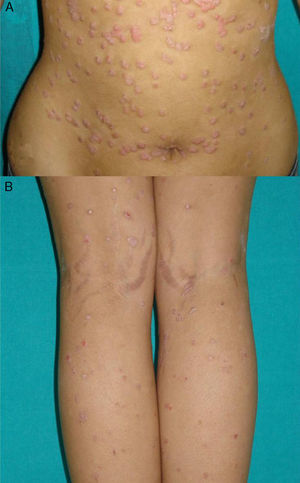
Cambio de morfología de una psoriasis previaLos datos de la literatura en relación con la exacerbación en forma de un cambio de morfología de la psoriasis durante el tratamiento con agentes biológicos son muy escasos. Nuestra experiencia clínica sugiere que este tipo de reacción ocurre con más frecuencia de lo que se ha publicado hasta el momento. En 2007 nuestro servicio describió 8 casos de aparición o agravamiento de la psoriasis. Seis de ellos desarrollaron una psoriasis guttata desde 15 días a 18 meses tras el inicio del tratamiento con etanercept para una psoriasis en placas grave. Ninguno de ellos presentó otro factor desencadenante. La retirada del agente biológico y su sustitución por ciclosporina fueron necesarias para controlar la psoriasis en uno de ellos, debido a la falta de mejoría con corticoides tópicos31. Este tipo de reacciones paradójicas se caracteriza por la aparición súbita de pequeñas lesiones en gotas de forma predominante en áreas no previamente afectadas por la psoriasis, mientras que las placas originales se mantienen en remisión (fig. 3). No conviene confundir estos brotes con un «rebrote» o agravamiento de la psoriasis de diferente origen, no inducido por el agente biológico, en el cual las nuevas lesiones son similares y aparecen en el seno de las placas previas. Tampoco deben confundirse con un «rebote» de la psoriasis que generalmente se define como el empeoramiento de la psoriasis en más de un 125% de la situación basal o un cambio de morfología inducido por el biológico, pero una vez suspendido el mismo. Los cambios de morfología a los que nos referimos en este apartado tienen lugar sin la suspensión del fármaco.
Mössner et al. publicaron una serie de 5 pacientes (3 varones y 2 mujeres) que desarrollaron pustulosis palmoplantar durante o después del tratamiento con infliximab para una psoriasis en placas. En uno de los casos las lesiones se acompañaban de lesiones pustulosas de manera generalizada. En 3 de los casos las lesiones en placas empeoraron concomitantemente. Ninguno de ellos había presentado previamente psoriasis pustulosa generalizada o palmoplantar. El periodo de latencia varió de 3 a 40 semanas. En cuanto a los factores de riesgo uno de los pacientes sufrió una infección previa, y en otro de los casos se había suspendido de manera súbita el infliximab. Solamente en uno de los 5 casos el control de las lesiones se obtuvo mediante la adición de corticodes tópicos sin la retirada de infliximab39.
Autores españoles han comunicado un caso con psoriasis en placas en tratamiento con etanercept que sufrió un brote de psoriasis pustulosa a las 24h después de la realización de la prueba de la tuberculina, lo que podía haber actuado como desencadenante73.
En ocasiones se ha descrito, y hemos experimentado también en nuestra práctica clínica, el desarrollo de una forma eritrodérmica de psoriasis tras el inicio del fármaco, con un periodo de latencia menor que en otros tipos de reacciones psoriasiformes. Santos-Juanes et al. publicaron los casos de 2 pacientes con psoriasis en placas que habían realizado previamente múltiples terapias antipsoriásicas con respuesta subóptima, que desarrollaron una eritrodermia durante el uso de etanercept, manteniéndose estables posteriormente durante el tratamiento con infliximab y adalimumab. Sin embargo, ambos obtuvieron una mejoría de más del 80% del PASI tras 4 semanas de tratamiento con ustekinumab57.
Características histopatológicasEn la literatura solo disponen de confirmación histológica el 39,4% de los 127 casos revisados por Ko et al.37. Algunos autores sugieren que estas reacciones presentan una histología compatible con psoriasis o pustulosis palmoplantar, indistinguible de los casos sin relación con terapia anti-TNFα36.
Sin embargo, en el artículo de Seneschal et al., tras realizar una descripción exhaustiva de las biopsias de sus pacientes con reacciones psoriasiformes durante la terapia anti-TNFα, encontraron algunas diferencias. En 11 de sus 13 casos se había realizado una biopsia cutánea. Clínicamente presentaron lesiones típicas de psoriasis en pequeñas placas junto con pustulosis o queratodermia palmoplantar en 3 de ellos. En 5 se observó un patrón psoriasiforme con paraqueratosis, hiperqueratosis y acantosis. Tres de estos 5 casos presentaban, además, un infiltrado liquenoide. Otras 3 biopsias mostraban también un patrón liquenoide focal. Queratinocitos necróticos se observaban en 3 pacientes. Siete de las muestras mostraron espongiosis con edema epidérmico y en otro de los casos una pústula unilocular subcórnea48.
Recientemente Laga et al. evaluaron el espectro histológico de pacientes con reacciones psoriasiformes asociadas con terapia anti-TNFα en 16 biopsias de 9 pacientes. Describieron diferentes patrones histológicos, incluyendo dermatitis de tipo liquen plano, foliculitis pustulosa estéril o un patrón similar a la psoriasis. Concluyeron que la correlación clínica es crucial para hacer el diagnóstico en este tipo de reacción68. En nuestra opinión, aquellas reacciones que clínica o histológicamente no se corresponden con psoriasis o pustulosis palmo-plantar no deberían incluirse en el grupo de reacciones psoriasiformes inducidas o asociadas a fármacos anti-TNFα.
A favor de esta opinión otros autores defienden que los hallazgos histológicos de las reacciones psoriasiformes son idénticas o muy similares a la psoriasis previa a la terapia anti-TNFα y distintas de reacciones medicamentosas pustulosas, incluyendo hiperplasia epidérmica, paraqueratosis, infiltrados linfocíticos epidérmicos, capilares dilatados y pustulosis intraepidérmica53.
Manejo práctico inicialAnte cualquier paciente que desarrolle una reacción psoriasiforme paradójica durante el tratamiento con algún agente anti-TNFα se deberán seguir los siguientes pasos (tablas 3 y 4):
- •
Anamnesis detallada que incluya:
- ∘
Características sociodemográficas.
- ∘
Historia personal y familiar de psoriasis.
- ∘
Antecedentes personales médicos y quirúrgicos, así como tratamientos habituales, con especial hincapié en la duración de los mismos.
- ∘
En relación con la enfermedad basal que precisa la terapia biológica se deberán recoger los datos sobre el tiempo de evolución y terapias concomitantes o previas.
- ∘
A propósito del tratamiento biológico actual se deben tomar los datos de duración y la dosis en el momento de la aparición de la reacción.
- ∘
En relación con el brote de las lesiones de psoriasis es necesaria su evolución, tipo o tipos de lesiones y la existencia o no de erupciones similares previamente.
- ∘
A través de una historia pormenorizada se deben descartar posibles factores desencadenantes como una infección, situaciones de estrés o ingesta de nuevos fármacos.
- ∘
Abordaje inicial de los pacientes con psoriasis de novo durante el tratamiento con terapia anti-factor de necrosis tumoral
| Antecedentes personales | Antecedentes de la enfermedad basal | Psoriasis | Pruebas complementarias |
| Enfermedades médico-quirúrgicasMedicación habitual | EvoluciónTratamientos previos | Tiempo de evoluciónFormas clínicasAntecedentes personales/familiaresDescartar factores desencadenantes | Analítica básicaBiopsia cutánea confirmatoria |
Abordaje inicial de los pacientes con empeoramiento de una psoriasis previa durante el tratamiento con terapia anti-factor de necrosis tumoral
| Antecedentes personales | Psoriasis basal | Brote psoriasis durante tratamiento anti-TNF | Pruebas complementarias |
| Enfermedades médico-quirúrgicasMedicación habitual | EvoluciónFormas clínicasTratamientos previos | Tiempo de evoluciónFormas clínicasDescartar desencadenantes | Analítica básica, ASLO y exudado faríngeoBiopsia cutánea confirmatoria |
TNF: factor de necrosis tumoral.
El manejo de estos pacientes no ha sido bien establecido. Basándonos en nuestra experiencia y en las revisiones publicadas se recomienda:
- ∘
Analítica de sangre con hemograma, perfil hepático y renal, título de anti-estreptolisina-O y exudado faríngeo en el inicio del brote.
- ∘
Excepto en casos clínicamente característicos una o varias biopsias de las lesiones cutáneas. Es conveniente para la confirmación diagnóstica ya que, como algunos autores han puesto de manifiesto, no todas las reacciones calificadas como psoriasiformes son verdaderas psoriasis.
En la tabla 5 se resume el tratamiento de las reacciones psoriasiformes paradójicas en general. No obstante, en función de nuestra experiencia y de la revisión de la literatura merece la pena especificar el tratamiento de cada uno de los subtipos:
- •
En pacientes con psoriasis de novo durante el tratamiento con fármacos bloqueadores del TNFα se recomienda el uso inicial de terapia tópica con corticoides de elevada potencia, análogos de la vitamina D o combinaciones de ambos. Si no se consigue controlar la situación se pueden dar 2 circunstancias. Si es necesario mantener el fármaco anti-TNFα responsable de inducir la psoriasis porque controla adecuadamente su enfermedad no dermatológica de base sin efectos adversos serios se puede aceptar el control parcial de las lesiones cutáneas con tópicos, o añadir otra terapia (fototerapia o terapia sistémica). Si no es imprescindible mantener el agente anti-TNFα lo mejor es sustituir el fármaco implicado. Debido al posible efecto de clase en los fármacos anti-TNFα recomendamos que la nueva terapia actúe mediante una vía distinta al bloqueo del TNFα para evitar empeoramiento o rebrotes de la enfermedad cutánea.
- •
En los casos de eritrodermia psoriásica el primer paso debería ser en todos los pacientes la sustitución del fármaco por otro con rápida respuesta, como ciclosporina o ustekinumab para mejoría del cuadro.
- •
En pacientes con un cambio de morfología de la psoriasis, como en la mayoría de los casos no es grave, la opción inicial más utilizada es mantener el mismo fármaco con la misma dosis y prescribir un tratamiento tópico. Si esto no fuera suficiente para controlar el brote recomendamos la sustitución del primer agente por otro fármaco, preferiblemente con un mecanismo de acción diferente, al igual que en los casos de psoriasis de novo. La opción de añadir otro fármaco sistémico, aunque es posible, en nuestra experiencia clínica es menos eficaz. Consigue retrasar la sustitución, que en la gran mayoría de los pacientes será necesaria finalmente. No obstante, modalidades terapéuticas como la fototerapia en monoterapia o en combinación con acitretina en los casos leve-moderados, o fármacos como la ciclosporina o el metotrexato en casos más graves han demostrado ser útiles en algunos pacientes, como se ha mencionado previamente en el texto.
Tratamiento general ante una reacción psoriasiforme paradójica
| Secuencia de tratamientos |
| 1. Añadir tratamiento tópico (corticoides de alta potencia, análogos de la vitamina D o combinaciones de ambos) |
| 2. Sustituir el fármaco implicado (preferiblemente por otro con distinto mecanismo de acción) |
| 3. Terapia combinada con otro tratamiento sistémico: |
| En casos leve-moderados: fototerapia y/o acitretina |
| En casos graves: ciclosporina o metotrexato |
Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesEl Dr. E. Daudén realiza o ha realizado las actividades siguientes: miembro de Advisory Board, consultor, recepción de becas, apoyo a la investigación, participación en ensayos clínicos y honorarios por impartir ponencias con las compañías farmacéuticas siguientes: Abbott, Astellas, Biogen, Centocor Ortho Biotech Inc, Galderma, Glaxo, Janssen-Cilag, Leo Pharma, MSD, Pfizer, Novartis, Stiefel, Wyeth Pharmaceuticals, 3M y Celgene.
La Dra. R. Navarro declara que no tiene conflicto de intereses.