En la era de los tratamientos biológicos, la reducción de un 75% en el PASI (PASI75) respecto el valor basal es el objetivo primario utilizado en la mayoría de ensayos clínicos1–4. Recientemente, el PASI90 y 100 han adquirido mayor relevancia con la elevada eficacia de los nuevos inhibidores de la interleuquina-173,4. Sin embargo, en la práctica clínica habitual el uso del PASI absoluto suele ser mucho más frecuente como herramienta de efectividad.
El objetivo principal de nuestro estudio fue comparar el PASI absoluto con la reducción relativa del PASI en pacientes tratados con etanercept (ETN), adalimumab (ADA) y ustekinumab (UST). Secundariamente, analizar la efectividad entre los distintos tratamientos biológicos en la práctica clínica a largo plazo. Se trata de un estudio observacional, retrospectivo y unicéntrico de pacientes adultos con psoriasis en placa moderada-grave, con al menos un año de tratamiento biológico (desde junio de 2005 hasta mayo del 2017). Aunque en el momento del diseño del estudio no existieron criterios de exclusión, no se incluyeron los pacientes tratados con infliximab por su bajo número (N=4). Se recogieron las características demográficas y la información clínica al inicio del último tratamiento biológico (tabla 1), así como el motivo de discontinuación del mismo en los casos que aplicaba.
Características demográficas y clínicas en todos los pacientes y según tratamiento
| Todos (N=157) | Etanercept (N=23) | Adalimumab (N=38) | Ustekinumab (N=96) | Valor de pa | |
|---|---|---|---|---|---|
| Características demográficas | |||||
| Edad (años), media (DE) | 49,9 (16,2) | 53,4 (17,5) | 46,0 (17,1) | 50,6 (15,3) | 0,178 |
| Sexo (varón), n (%) | 90 (57,3) | 16 (69,6) | 24 (63,2) | 50 (52,1) | 0,221 |
| IMC (kg/m2), media (DE) | 27,2 (5,0) | 27,3 (4,4) | 26,3 (4,4) | 27,6 (5,4) | 0,435 |
| Estatus de peso corporal, n (%) | 0,420 | ||||
| Infrapeso | 2 (1,3) | 1 (4,3) | 1 (2,6) | 0 (0,0) | |
| Normopeso | 59 (37,6) | 7 (30,4) | 14 (36,8) | 38 (39,6) | |
| Sobrepeso | 60 (38,2) | 11 (47,8) | 16 (42,1) | 33 (34,4) | |
| Obesidad | 36 (22,9) | 4 (17,4) | 7 (18,4) | 25 (26,0) | |
| Características clínicas | |||||
| Pacientes naïve, n (%) | 78 (49,7) | 12 (52,2) | 19 (50,0) | 47 (49,0) | 0,961 |
| PASI basal, media (DE) | 16,9 (8,0) | 14,3 (5,6) | 16,1 (6,7) | 17,8 (8,9) | — |
| Presencia de artritis, n (%) | 37 (23,6) | 6 (26,1) | 9 (23,7) | 22 (22,9) | 0,949 |
| Afectación ungueal, n (%) | 58 (36,9) | 11 (47,8) | 12 (31,6) | 35 (36,5) | 0,439 |
DE: desviación estándar; IMC: índice de masa corporal; PASI: Psoriasis Area Severity Index.
Infrapeso: <18,5kg/m2; Normopeso: 18,5-24,9kg/m2; Sobrepeso: 25-29,9kg/m2; Obesidad: ≥30kg/m2.
El análisis estadístico se realizó a través del programa SPSS® (versión 21 para Windows) y se estableció un nivel de significación estadística de 0,05. No se emplearon métodos de sustitución para los datos ausentes (as observed).
Se incluyeron 157 pacientes, de los cuales el 14,6% (N=23) fue tratado con ETN, el 24,2% (N=38) con ADA y el 61,1% (N=96) con UST. La tabla 1 muestra las características basales de la población, sin diferencias significativas entre los diferentes grupos de tratamientos.
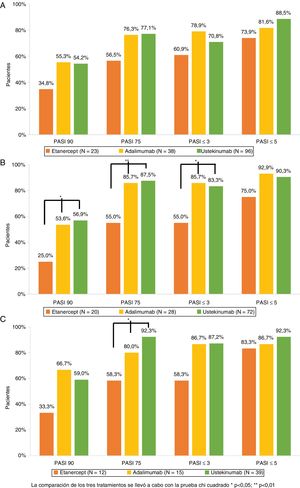
Los porcentajes de pacientes con PASI75, 90, ≤5 y ≤3 al año, 3 y 5 años de tratamiento se muestran en la figura 1. En los 3 períodos estudiados, un porcentaje no despreciable de los pacientes que no alcanzaron el PASI90 sí consiguieron un PASI≤5 o ≤3, tanto para el total de pacientes como en cada tratamiento (tabla 2). Al año de tratamiento, un 68,4% de los pacientes que no alcanzaron un PASI90, alcanzaron un PASI≤5 y un 40,8% un PASI≤3. Dichos porcentajes fueron mayores a los 3 y 5 años, no obstante, el tamaño muestral en estos períodos fue más pequeño (tabla 3).
Pacientes que no consiguieron PASI90 pero sí PASI≤3 y ≤5
| N (%) [IC 95%] | Pacientes que no consiguieron PASI 90 | Pacientes que no consiguieron PASI90 pero sí PASI≤3 | Pacientes que no consiguieron PASI90 pero sí PASI≤5 |
|---|---|---|---|
| Tras un año de tratamiento | |||
| Etanercept, N=23 (%) | 15 (65,2) | 6 (40,0) (19,8-64,3) | 9 (60,0) (35,8-80,2) |
| Adalimumab, N=38 (%) | 17 (44,7) | 9 (52,9) (31,0-73,8) | 10 (58,8) (36,0-78,4) |
| Ustekinumab, N=96 (%) | 44 (45,8) | 16 (36,4) (23,8-51,1) | 33 (75,0) (60,6-85,4) |
| Total, N=157 (%) | 76 (48,4) | 31 (40,8) (30,4-52,0) | 52 (68,4) (57,3-77,8) |
| Tras 3 años de tratamiento | |||
| Etanercept, N=20 (%) | 15 (75,0) | 6 (40,0) (19,8-64,3) | 10 (66,7) (41,7-84,8) |
| Adalimumab, N=28 (%) | 13 (46,4) | 9 (69,2) (42,4-87,3) | 11 (84,6) (57,7-95,7) |
| Ustekinumab, N=72 (%) | 31 (43,1) | 19 (61,3) (43,8-76,3) | 24 (77,4) (60,2-88,6) |
| Total, N=120 (%) | 59 (49,2) | 34 (57,6) (44,9-69,4) | 45 (76,2) (64,0-85,3) |
| Tras 5 años de tratamiento | |||
| Etanercept, N=12 (%) | 8 (66,7) | 3 (37,5) (13,7-69,4) | 6 (75,0) (40,9-92,9) |
| Adalimumab, N=15 (%) | 5 (33,3) | 3 (60,0) (23,1-88,2) | 4 (80,0) (37,6-96,4) |
| Ustekinumab, N=39 (%) | 16 (41,0) | 11 (68,8) (44,4-85,8) | 13 (81,3) (57,0-93,4) |
| Total, N=66 (%) | 29 (43,9) | 17 (58,6) (40,7-74,5) | 23 (79,3) (61,6-90,2) |
IC 95%: intervalo de confianza del 95%.
Disposición de pacientes en el tiempo
| Tratados >1 y <3 años | Tratados >3 y <5 años | Discontinuación de tratamiento | FT secundario | AA | Pérdida de seguimiento | Éxito terapéuticoa | |
|---|---|---|---|---|---|---|---|
| Etanercept, N=23 (%) | 2 (8,7) | 0 (0) | 9 (39,1) | 8 (34,7) | 0 (0) | 1 (4,3) | 0 (0) |
| Adalimumab, N=38 (%) | 4 (10,5) | 9 (23,7) | 10 (26,3) | 6 (15,8) | 2 (5,3) | 2 (5,3) | 0 (0) |
| Ustekinumab, N=96 (%) | 14 (14,6) | 16 (16,6) | 27 (28,1) | 12 (12,5) | 1 (1,0) | 12b (12,5) | 2 (2,1) |
| Total, N=157 (%) | 20 (12,7) | 25 (15,9) | 46 (29,2) | 26 (16,5) | 3 (1,9) | 15 (9,5) | 2 (1,3) |
AA: acontecimiento adverso; FT: fallo terapéutico.
En cuanto a la efectividad, la diferencia estadística no se observó de igual manera a través del tiempo (fig. 1). En el primer año no se observaron diferencias estadísticamente significativas entre los 3 tratamientos. A los 3 años, el porcentaje de pacientes que alcanzaron PASI90, 75 y ≤3 fue mayor para UST versus ETN (p=0,011, p=0,001 y p=0,08, respectivamente) así como para ADA versus ETN (p=0,048, p=0,018 y p=0,018, respectivamente). A los 5 años solo se observaron diferencias en el PASI75 entre UST versus ETN (p=0,005).
El principal motivo de discontinuación fue el fallo terapéutico secundario (16,5%) seguido de la pérdida de seguimiento (9,5%). Tres pacientes reportaron acontecimientos adversos que llevaron a la suspensión del fármaco: 2 con ADA (alopecia areata e hipertensión arterial) y uno con UST (taquicardia y cefalea).
En la práctica clínica diaria el PASI absoluto suele ser el método más utilizado para evaluar el éxito o el fracaso terapéutico. Existe un consenso cada vez mayor de que los valores absolutos de PASI inferiores a 3 o 5 podrían proporcionar una mejor referencia del éxito terapéutico5. Recientemente, en el consenso español de evaluación y tratamiento de la psoriasis moderada-grave, se incluye el PASI<5 como una respuesta apropiada al tratamiento6. Sin embargo, el PASI absoluto no se considera como objetivo de éxito terapéutico en el consenso europeo7. Además, es escasa la literatura acerca de la comparación de PASI absoluto y relativo. En el registro BioCAPTURE se observó que a la semana 24 un número considerable de series de tratamiento que no consiguieron respuesta PASI90 o 100, sí que alcanzaron valores de PASI≤5 (51,9 y 57,6%, respectivamente)8.
Por otro lado, en nuestra serie UST y ADA son los tratamientos que alcanzan mejores resultados respecto a ETN, siendo significativos a los 3 y 5 años. Un estudio con ADA a los 3 años, mostró tasas de respuesta del 76% en PASI75 y del 50% en PASI909. Con UST hay datos hasta 5 años, alcanzando el PASI75 un 63% de pacientes y el PASI90 un 40%10. Nuestros resultados son superiores posiblemente porque en el análisis utilizado no se utilizaron métodos de sustitución de datos (as observed), mientras que en los estudios sí (last observation carried forward)10.
Este estudio tiene como limitaciones el diseño retrospectivo, la participación de un solo centro y la diferencia en el número de pacientes en los 3 grupos. Sin embargo, una fortaleza es la evaluación de la efectividad en un período de 5 años en condiciones de práctica clínica habitual.
Como conclusión, destacamos que un porcentaje no despreciable de pacientes que no alcanzaron el PASI90 sí consiguieron un PASI≤5 y ≤3 con los 3 tratamientos, lo que demuestra que el PASI absoluto puede ser una mejor medida de éxito terapéutico en la práctica clínica que la reducción relativa del PASI.
Conflicto de interesesLos autores han participado en ensayos clínicos, han efectuado asesorías y/o han recibido honorarios por conferencias o financiación para asistir a actividades de formación con el patrocinio de Janssen, Abbvie, Novartis (Elena del Alcázar Viladomiu); Janssen, Abbvie, Novartis, Pfizer (Nuria Lamas Doménech) y Janssen, Abbvie, Novartis, Pfizer (Montserrat Salleras Redonnet).