El interferón beta fue aprobado en España en 1995 para el tratamiento de la esclerosis múltiple progresiva. Existen 2 tipos principales, el interferón beta-1a y el 1b, así como diversas presentaciones de cada uno de ellos en el mercado que implican, a su vez, respuestas diferentes ante una misma molécula. Las reacciones cutáneas locales constituyen un efecto secundario frecuente, que suele ser autolimitado. Por el contrario, son muy raras la paniculitis y la lipoatrofia, y pueden requerir la suspensión del tratamiento.
Presentamos el caso de una mujer de 43 años de edad, diagnosticada de esclerosis múltiple en 2005, por la que había recibido diversos tratamientos modificadores de la enfermedad. Desde octubre de 2009 recibía tratamiento con interferón beta-1a (Rebif 44®), 3 veces a la semana de forma subcutánea, administrado por la propia paciente, con una respuesta adecuada al mismo. Tras 18 meses de tratamiento comenzó a presentar induración en las zonas de punción, la cara anterior de los muslos y externa de los brazos. Unas semanas después aparecieron unas lesiones ulceradas en la cara anterior de los muslos, que habían aumentado de tamaño progresivamente. La paciente refería intenso dolor en las placas que le limitaba incluso la movilidad y la deambulación. No refería fiebre ni afectación sistémica y su estado neurológico no había empeorado.
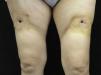
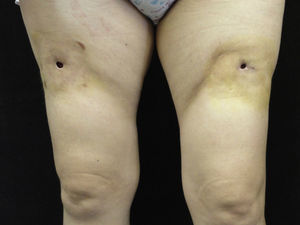
A la exploración se observaban en la cara anterior de los muslos 2 úlceras de bordes cicatriciales, de 1cm de diámetro, debajo de las cuales existía una cavidad de unos 4cm de diámetro. Asimismo, se palpaba una placa indurada e infiltrada alrededor de la úlcera de unos 15cm de diámetro, de superficie ligeramente eritematosa e intensamente dolorosa a la palpación (fig. 1). En la cara externa de ambos brazos también existían estas placas induradas, aunque no se apreciaba ninguna úlcera.
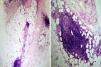
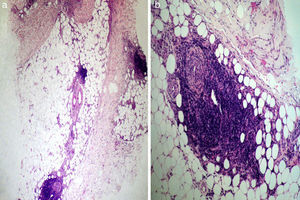
Realizamos un cultivo de las úlceras que fue negativo, así como una biopsia incisional de una de las placas del muslo. En el estudio anatomopatológico se observaba una epidermis conservada, esclerosis de la dermis media y profunda, y afectación del tejido celular subcutáneo. A mayor aumento se observaba un infiltrado que afectaba principalmente al lobulillo, aunque también se apreciaba un engrosamiento de los septos (fig. 2a); este infiltrado estaba compuesto principalmente por neutrófilos y linfocitos (fig. 2b). No se observaba vasculitis ni necrosis. Con estos datos se realizó el diagnóstico de paniculitis mixta secundaria al uso de interferón beta-1a. De acuerdo con su neurólogo, debido principalmente a la impotencia funcional, se decidió suspender el tratamiento con dicho fármaco.
El interferón beta-1a fue aprobado para el tratamiento de la esclerosis múltiple progresiva en 1995 en España. Se ha demostrado que su administración disminuye la frecuencia de los brotes en un 30% y reduce la aparición de nuevas lesiones en la resonancia magnética en un 66%. Las manifestaciones cutáneas locales, como eritema y dolor, están claramente descritas como un efecto secundario frecuente, apareciendo en el 63-85% de los pacientes1, si bien suelen ser autolimitadas y no requieren la suspensión del tratamiento. Existen, sin embargo, otras reacciones más graves como son las ulceraciones, necrosis2, esclerosis e induración de la zona de la inyección, que sí pueden condicionarlo. Asimismo, existen otras lesiones como granulomas sarcoideos, lipoatrofia3, lesiones lupus-like4 y paniculitis septal o lobulillar5, que se consideran efectos secundarios muy raros. En la tabla 1 se recogen los casos de paniculitis secundaria a interferón descritos hasta la fecha. Algunos autores han propuesto que esta paniculitis puede ser causada por la toxicidad vascular del interferón beta.
Pacientes descritos en la literatura que han desarrollado paniculitis tras la administración de interferón
| Edad y sexo | Localización | Inicio de los síntomas | Clínica | Hallazgos patológicos | |
| Ziegler et al. (1998)6 | 41, mujer | Piernas | 8 semanas | Eritema, induración y dolor | Infiltrado perivascular y paniculitis lobulillar con infiltrado linfocitario |
| Heinzerling et al. (2002)7 | 44, mujer | Brazos, piernas y abdomen | 4 años | Induración dolorosa | Paniculitis septal con predominio linfocitario |
| O'Sullivan et al. (2006)8 | 37, hombre | Pierna izquierda | 2 años y 3 meses | Eritema y dolor | Paniculitis septal con infiltrado inflamatorio |
| Nakamura et al. (2008)5 | 43, mujer | Glúteos | 5 años | Eritema, induración y dolor | Dermatitis perivascular y paniculitis lobulillar y septal con infiltrado linfocitario |
| Ball et al. (2009)9 | 46, mujer | No recogida | 1 año y 10 meses | Dolor e induración | Paniculitis lobulillar con infiltrado neutrofílico |
| Ball et al. (2009)9 | 45, mujer | No recogida | 6 años y 1 mes | Celulitis | Paniculitis lipomembranosa |
| Poulin et al. (2009)10 | 43, mujer | Abdomen | 9 años | Eritema, dolor y fiebre | Paniculitis septal de predominio linfocitario |
| Caso actual | 43, mujer | Piernas | 19 meses | Dolor, eritema, induración e impotencia funcional | Paniculitis lobulillar y septal con infiltrado inflamatorio mixto (linfocitos y neutrófilos) |
Ball et al.9 describieron en 2009 que, en algunas ocasiones, la paniculitis por interferón beta puede simular una paniculitis pancreática, por lo que puede ser conveniente en caso de sospecha solicitar pruebas analíticas como lipasa y amilasa para realizar el diagnóstico diferencial.
En cuanto a su fisiopatología se han propuesto 2 teorías. La primera establece un claro papel desencadenante al factor traumático propio de la autoinyección. La segunda teoría concede más importancia al factor inmunológico del propio interferón beta. Según esta teoría, la presencia de estas reacciones indicaría una activación del sistema inmunitario y podría ser un signo de efectividad del tratamiento9.
Respecto al manejo de estos pacientes cabe decir que es poco satisfactorio. Es imprescindible educar al paciente acerca de la correcta forma de autoinyección, que debe ser subcutánea, nunca intradérmica, así como de la rotación diaria de las zonas de autoinyección. Con estas medidas, la mayoría de las lesiones suelen mejorar5, si bien existen casos en que es necesaria la suspensión del tratamiento con interferón beta, decisión que debe ser tomada en colaboración con los demás especialistas que traten al paciente.