Vemurafenib, un inhibidor de la enzima BRAF, es un fármaco desarrollado para el tratamiento del melanoma metastásico en pacientes portadores de la mutación V600E BRAF que está presente aproximadamente en el 40 al 60% de los pacientes con melanoma avanzado. Este fármaco actúa inhibiendo la vía BRAF/MEK/ERK, vía de las MAP quinasas, en el paso BRAF/MEK. En estudios recientes se ha informado de una reducción en el riesgo de muerte de hasta el 63%1,2. Los efectos secundarios incluyen artralgias, fotosensibilidad cutánea, alopecia, astenia, hiperqueratosis, xerosis, exantemas inespecíficos, queratoacantomas y carcinomas epidermoides3–5. Presentamos un paciente con melanoma en estadio iv que desarrolló un nevus melanocítico atípico clínicamente amelanótico 2 meses después de comenzar el tratamiento con vemurafenib.
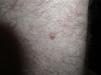
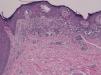
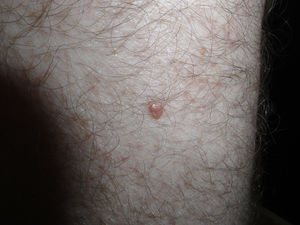
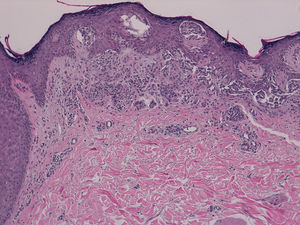
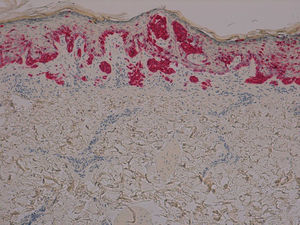
Presentamos el caso de un paciente caucásico de 42 años de edad, con un melanoma estadio iv, diagnosticado hacía 6 años de melanoma en el brazo derecho con ganglio centinela positivo, al que se le realizó linfadenectomía axilar derecha y tratamiento posterior con interferón. En controles posteriores, 6 años después, se objetivaron 2 nódulos pulmonares y lesiones óseas metastásicas en C5, D11 y ambas palas ilíacas y sacro, por lo que al detectarse la mutación BRAF V600E se inició tratamiento con vemurafenib 960mg cada 12h. Dos meses después de iniciar el tratamiento se objetivó una lesión papular en el muslo izquierdo, que no estaba presente en la revisión anterior un mes antes, de 10×8mm, cupuliforme, del color de la piel, asintomática, que había ido creciendo (fig. 1). Se le realizó una biopsia-extirpación de la lesión con el diagnóstico de sospecha de queratosis actínica hipertrófica, siendo la lesión extirpada en su totalidad. La evaluación histológica mostró una proliferación de melanocitos en la epidermis y en la dermis papilar, con discreta atipia arquitectural (fig. 2). Los melanocitos se agrupaban formando nidos en la epidermis y en la dermis papilar, con discreto pleomorfismo nuclear. Se solicitó estudio inmunohistoquímico con Melan-A y HMB-45 que mostró una proliferación de melanocitos en la capa basal de la epidermis con focos de melanocitos en capas más altas de la epidermis (fig. 3). Todos estos hallazgos son compatibles con un nevus atípico.
La activación paradójica de vemurafenib sobre las células BRAF salvajes conduce a un aumento de la fosforilación de ERK, con la consiguiente hiperactivación de la vía MAPK que promueve la proliferación y supervivencia celular, efecto responsable de la producción de efectos secundarios como queratoacantomas, carcinomas epidermoides y queratosis actínicas. El efecto estimulador paradójico de vemurafenib puede actuar como iniciador de la progresión de una lesión melanocítica benigna a melanoma6. Se han descrito proliferaciones melanocíticas atípicas y aparición de nuevos melanomas en pacientes en tratamiento con vemurafenib, y se ha documentado dermatoscópicamente los cambios sufridos por nevus preexistentes inducidos por vemurafenib7.
En resumen, presentamos un caso de un paciente en tratamiento con vemurafenib por un melanoma metastásico que desarrolló un nevus melanocítico atípico amelanótico, lo que debe mantenernos alerta en la vigilancia de estas lesiones y biopsiarlas en caso de duda para detectar de forma temprana lesiones neoplásicas malignas incipientes.