La modificación de dosis de biológicos en pacientes con psoriasis en remisión adecuadamente seleccionados podría reducir el riesgo de exposición al fármaco y su carga económica.
Material y métodosEstudio observacional, descriptivo y transversal en 112 pacientes con psoriasis moderada-grave tratados con biológicos durante ≥6 meses en enero de 2014. El objetivo consistió en alcanzar y mantener una respuesta PASI 75. Los pacientes iniciaron el tratamiento con la pauta estándar; en aquellos que cumplieron el objetivo se redujo la dosis, y cuando no alcanzaron la respuesta con la pauta estándar esta se intensificó.
ResultadosUn 42,9% siguió la pauta estándar, un 50% la reducida y un 7,1% la intensificada. El fármaco con el que más se redujo la dosis fue adalimumab (57,7%) y los que más se intensificaron fueron ustekinumab e infliximab (17,9% y 12,5%). Los pacientes que recibieron dosis reducidas presentaron una psoriasis de más evolución (p=0,049) y llevaban más tiempo en tratamiento con el mismo biológico (p=0,009) (diferencias significativas). Hubo una proporción significativamente superior de pacientes con artritis psoriásica entre los no aptos a reducir dosis (p=0,023). El ahorro del gasto fue del 21,5% con adalimumab, 13,8% con etanercept, 0,9% con ustekinumab y 0,55% con infliximab.
ConclusionesPresentaron una probabilidad de reducción de dosis significativamente mayor aquellos pacientes con más tiempo de evolución y más tiempo bajo el mismo tratamiento biológico. Entre los pacientes sin reducción de dosis hubo mayor proporción con artritis psoriásica. El ahorro global con este algoritmo de modificación de dosis fue del 13%. Se requieren estudios controlados que ayuden a definir el perfil de paciente más adecuado para reducir la dosis sin pérdida de eficacia del tratamiento.
In biologic therapy, dose modification in carefully selected patients when psoriasis is in remission could reduce treatment costs and the risks associated with drug exposure.
Material and methodsObservational, descriptive, crosssectional study, performed in January 2014, of 112 patients with moderate to severe psoriasis who had been on biologic therapy for at least 6 months. The therapeutic objective in all cases was to achieve and maintain a 75% reduction in Psoriasis Area and Severity Index (PASI 75). All the patients had started treatment with the standard regimen. During treatment, the dose had been reduced in patients who achieved the therapeutic objective and escalated in those who failed to respond adequately to standard doses.
ResultsAt the time of the study, 42.9% of the patients were receiving the standard dose, 50% were on a reduced dose, and 7.1% were on an escalated regimen. The agent with which the dose was most often reduced was adalimumab (57.7%), and the agents with which therapy was most often escalated were ustekinumab (17.9%) and infliximab (12.5%). Patients who received reduced doses had significantly longer-standing disease (P=.049) and longer treatment duration with the same biologic agent (P=.009). In the group that did not fulfill the criteria for dose reduction, the proportion of patients with psoriatic arthritis was significantly higher (P=.023). Cost savings were as follows: 21.5% with adalimumab, 13.8% with etanercept, .9% with ustekinumab, and .55% with infliximab.
ConclusionsPatients with longer-standing disease and longer treatment duration with the same biologic agent were significantly more likely to be candidates for dose reduction. The proportion of patients with psoriatic arthritis was greater in the group of patients who did not fulfill the conditions for dose reduction. The overall cost saving achieved using the dose modification algorithm described in this study was 13%. Controlled studies are needed to define the profile of the patients best suited for dose reduction strategies without loss of treatment efficacy.
La psoriasis es una enfermedad cutánea crónica y recidivante que afecta a un 2,3% de la población española1 y a un 2-3% de la población mundial2. Aproximadamente un tercio de estos pacientes sufren psoriasis moderada-severa, la cual requiere tratamiento a largo plazo con agentes sistémicos, que por lo general presentan toxicidad acumulativa, intolerancia y en ocasiones baja tasa de respuesta3.
Los fármacos mejor adaptados a una pauta de tratamiento continuo son los agentes biológicos. En la práctica, y de forma aplicable a la mayoría de los pacientes, con los agentes biológicos disponibles un objetivo terapéutico razonable sería alcanzar una respuesta PASI 75 (mejoría ≥75% del PASI basal) durante la fase de inducción, que puede extenderse hasta la semana 24, momento en el que todos los biológicos alcanzan la meseta de eficacia4.
Distintos autores han señalado que, en aquellos pacientes con psoriasis en remisión, el uso de dosis estándar de fármacos biológicos podría resultar en un sobretratamiento, por lo que en determinados casos podría ser razonable individualizar la pauta posológica5,6. Así, varios estudios han analizado la modificación de dosis del tratamiento con biológicos en pacientes con artritis reumatoide en remisión, mostrando que en el caso de los anti-TNF la eficacia se preserva en la mayoría de los pacientes7. La modificación de dosis de biológicos en pacientes en remisión adecuadamente seleccionados podría reducir el riesgo de exposición al fármaco y reducir la carga económica para los sistemas de salud8, algo que ya se propone en otras enfermedades crónicas, como la artritis reumatoide, como un intento de personalización de tratamiento utilizando la mínima dosis eficaz9–12.
Resulta de especial interés analizar los beneficios y los riesgos de modificar la pauta estándar de los distintos biológicos en el tratamiento de la psoriasis. Es importante identificar las características clínicas asociadas al éxito o al fracaso de dichas pautas modificadas, incluidos el riesgo de recaída y la aparición de anticuerpos específicos13. La decisión de modificar la pauta de biológico debe basarse en una selección adecuada de los pacientes, teniendo en cuenta que los posibles riesgos y beneficios irán en función de la gravedad de la enfermedad, la calidad de vida del paciente y la existencia de comorbilidades13.
Las publicaciones sobre modificación de la pauta posológica de biológicos en el tratamiento de la psoriasis son limitadas13–15 y no existen guías al respecto13. Estos estudios son valiosos, dado que incluyen pacientes con enfermedad recidivante y distintas comorbilidades que probablemente quedarían excluidos de los ensayos clínicos14. En una revisión sistemática Brezinski et al.13 sintetizaron los datos de 23 ensayos que analizaron pautas de modificación de dosis con etanercept, adalimumab, infliximab, ustekinumab y alefacept en psoriasis moderada-severa. El tratamiento continuo con fármacos anti-TNF y anti IL12/23 fue más eficaz que el tratamiento intermitente a la hora de mantener el control de la enfermedad y, para la mayoría de los biológicos, con el retratamiento no se alcanzaron las tasas de respuesta iniciales13. Además, se constató que, en pacientes no respondedores, el escalado de dosis con etanercept, adalimumab y uktekinumab presentó por lo general una mayor eficacia16–20.
Por otro lado, en un estudio llevado a cabo por Fotiadou et al.14 se incrementó el intervalo de dosis de adalimumab de 2 a 3 semanas en aquellos pacientes con psoriasis moderada-grave que alcanzaron una respuesta PASI 100 sostenida tras un año de tratamiento (n=14). Ninguno de ellos experimentó recaída, y un 71% habían completado 2,5 años de tratamiento. Cantini et al.8 demostraron, en pacientes con artritis psoriásica, que un 88,6% de los pacientes que recibieron una pauta reducida de adalimumab (40mg cada 4 semanas; n=53) se mantuvieron en remisión tras un periodo de seguimiento medio de 28,9±8,4 meses.
A la luz de estos datos el presente estudio tiene como objetivo analizar los patrones de modificación de dosis de fármacos biológicos en una cohorte de pacientes con psoriasis moderada-grave en condiciones de práctica clínica, así como sus consecuencias sobre el control de la enfermedad y el coste de tratamiento.
Pacientes y métodosEstudio observacional, descriptivo y transversal que incluyó a todos los pacientes con psoriasis moderada-grave, en tratamiento con biológicos durante al menos 6 meses, en fase de mantenimiento en enero de 2014. En aquellos pacientes que no alcanzaron al menos una respuesta PASI 50 tras la fase de inducción se consideró que el tratamiento había fracasado y no se incluyeron en el estudio. Los pacientes fueron seguidos por un solo investigador en la consulta monográfica de psoriasis del hospital.
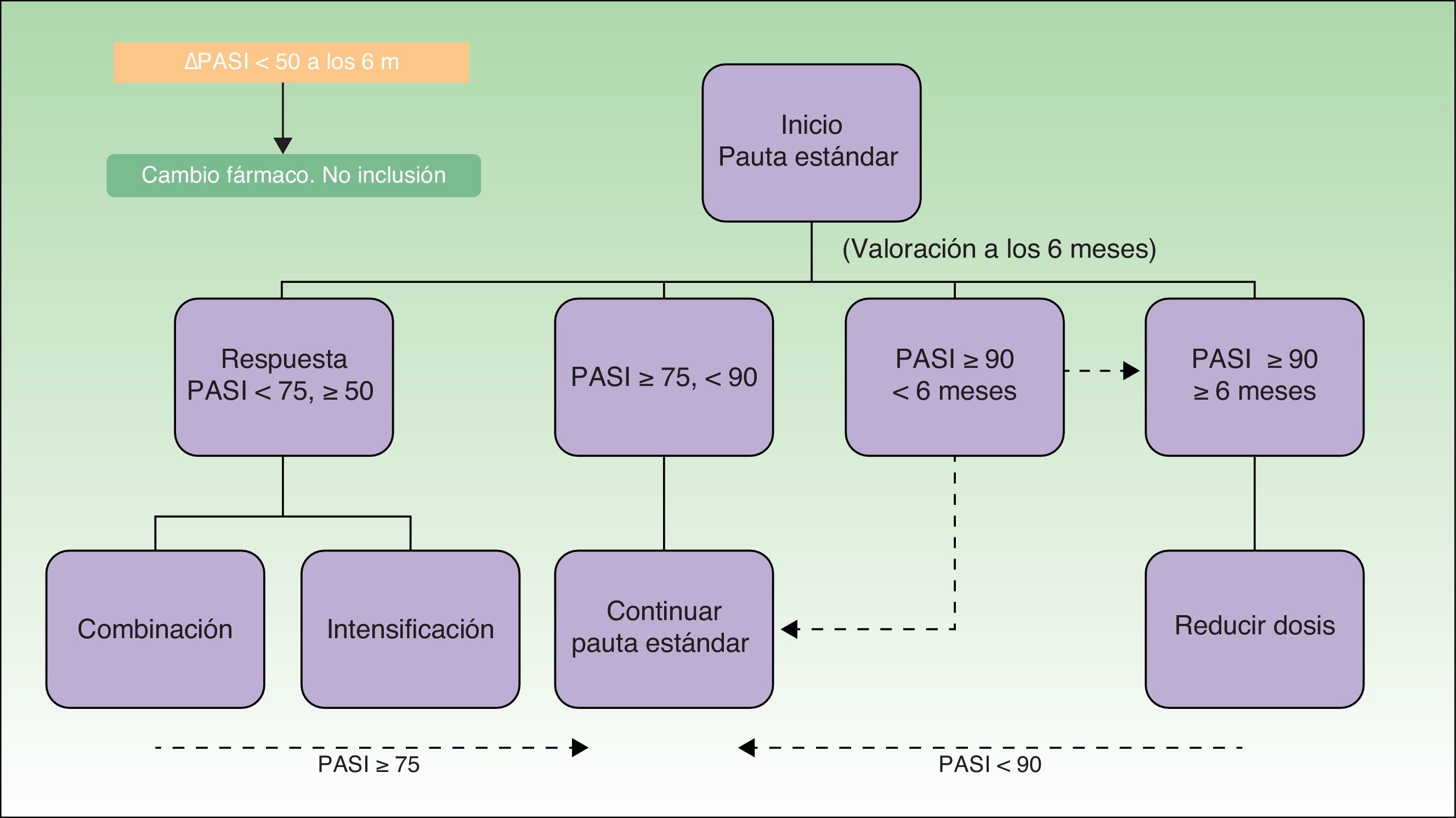
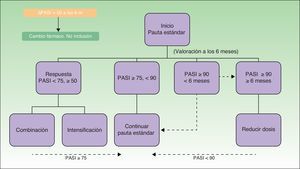
En la figura 1 se muestra el algoritmo de tratamiento seguido durante el estudio. El objetivo clínico consistió en alcanzar una respuesta PASI 75 y mantenerla durante el curso del tratamiento con el biológico. Todos los pacientes iniciaron el tratamiento con la pauta indicada en ficha técnica (pauta estándar). En aquellos que alcanzaron remisión de la enfermedad (respuesta PASI 90-100) y la mantuvieron durante al menos 6 meses, la dosis del biológico se redujo aumentando el intervalo entre dosis o disminuyendo la dosis (reducción de dosis) según un consenso establecido previamente entre el Servicio de Dermatología y el Servicio de Farmacia 2 años antes. Cuando, por el contrario, el paciente no alcanzó la respuesta PASI 75 con la pauta estándar, se decidió intensificar la pauta reduciendo el intervalo entre dosis o combinando con otro tratamiento sistémico clásico. La estrategia de reducción de dosis se mantuvo mientras el paciente continuara en remisión. La pérdida de respuesta PASI 90-100 fue criterio de reinstauración de la pauta estándar. La estrategia de intensificación se mantuvo hasta alcanzar el objetivo terapéutico (al menos una respuesta PASI 75).
Se recogieron variables relativas a la historia de psoriasis (tiempo de evolución, PASI basal, presencia de artritis psoriásica, tratamientos previos recibidos sistémicos y/o biológicos), características demográficas (edad, sexo, peso) e información del tratamiento biológico actual (tiempo en tratamiento, PASI en el momento de iniciar la pauta modificada, tiempo con la pauta modificada y PASI en la última visita).
Por otra parte, con el fin de identificar posibles características o perfiles de paciente que lo hicieran más susceptible de recibir una dosis reducida de biológico, se realizó un análisis que comparó a los pacientes sin reducción de dosis (pauta estándar+pauta intensificada) frente a aquellos que siguieron una pauta con dosis reducidas. Dicho análisis se hizo tanto para las variables continuas como para las variables categóricas.
CostesLos análisis de costes se aplicaron al total de la cohorte analizada y a cada grupo de análisis (pauta estándar, pauta con reducción de dosis y pauta intensificada). Para cada tipo de pauta y cada tratamiento se calculó el coste/paciente/año. Los costes unitarios de los biológicos empleados se calcularon a partir de su precio de venta de laboratorio (PVL) en España en 2014, al que se sumó el impuesto sobre el valor añadido (IVA) y se restó el descuento obligatorio del 7,5%. Dichos costes unitarios fueron 496,61€ para adalimumab (jeringa 40mg)21, 113,90€ para etanercept (jeringa 25mg), 227,8€ para etanercept (jeringa de 50mg), 515,90€ para infliximab (vial 100mg/20m) y 2.936,27€ para ustekinumab (jeringa 45mg).
Análisis estadísticoSe realizó un análisis descriptivo de la distribución de la población estudiada según las variables disponibles. Para describir las variables categóricas se utilizó la proporción. Para las continuas, en caso de distribución normal se utilizó la media como estadístico de centralización y la desviación estándar como estadístico de dispersión; cuando la distribución no era normal se emplearon la mediana y los percentiles.
La asociación entre el tipo de pauta y las variables clínicas se exploró mediante análisis bivariantes. Se utilizó la comparación de medias para las variables continuas y el análisis de contingencia para las variables categóricas. Para evaluar si las asociaciones eran o no estadísticamente significativas, se emplearon las pruebas estadísticas apropiadas de acuerdo a las características de las variables analizadas. Se consideraron significativos los valores de p<0,05. Los análisis estadísticos fueron realizados con SPSS para Windows versión 20.
ResultadosPoblación estudiadaEl estudio incluyó un total de 112 pacientes, cuyas características basales se muestran en la tabla 1. La edad media de la población estudiada fue de 49 años, con un tiempo medio de evolución de la psoriasis de 23,86 años. Un 69,6% fueron hombres y un 30,4% mujeres. Un 11,6% de la población estaba recibiendo tratamiento concomitante, fundamentalmente metotrexato (5,4%) y acitretino (2,7%).
Características demográficas y clínicas de los pacientes. Evolución de la psoriasis y tratamientos previos
| Número total de pacientes | 112 |
| Edad (años) media (rango) | 49,13 (23-87) |
| Sexo, n (%): hombres/mujeres | 78 (69,6)/34 (30,4) |
| Peso (kg) media (DE) | 81,35 (17,01) |
| Artritis psoriásica, n (%) | 33 (29,5) |
| PASI basal, media (rango) | 14,44 (7,20-29-30) |
| Tiempo de evolución de la psoriasis (años), media (rango) | 23,86 (3-62) |
| Tratamientos sistémicos previos, media (rango) | 2,79 (0-5) |
| Número de tratamientos, n (%): | |
| 0 | 3 (2,7) |
| 1 | 11(9,8) |
| 2 | 31 (27,7) |
| 3 | 36 (32,1) |
| 4 | 23 (20,5) |
| 5 | 8 (7,1) |
| Tratamientos biológicos previos, media (rango) | 0,99 (0-4) |
| Número de tratamientos, n (%) | |
| 0 | 46 (41,1) |
| 1 | 32 (28,6) |
| 2 | 26 (23,2) |
| 3 | 5 (4,5) |
| 4 | 3 (2,7) |
| Tratamiento biológico actual, n (%) | |
| Adalimumab | 52 (46,4) |
| Etanercept | 24 (21,4) |
| Infliximab | 8 (7,1) |
| Ustekinumab | 28 (25) |
| Tratamiento concomitante, n (%) | |
| No | 99 (88,4) |
| Tópicos | 1 (0,9) |
| Acitretino | 2 (1,8) |
| Acitretino+UVB | 1 (0,9) |
| Metrotexato | 6 (5,4) |
| Sulfasalazina | 1 (0,9) |
| UVB | 1 (0,9) |
El valor PASI medio en el momento del inicio del tratamiento biológico fue de 14,44 (rango 7,20-29,30), con una media de 2,79 tratamientos sistémicos previos y 0,99 biológicos previos; el tiempo medio total con el biológico actual fue de 38,11 meses. Del total de 112 pacientes, 52 recibían adalimumab (46,4%), 28 ustekinumab (25,0%), 24 etanercept (21,4%) y 8 infliximab (7,1%).
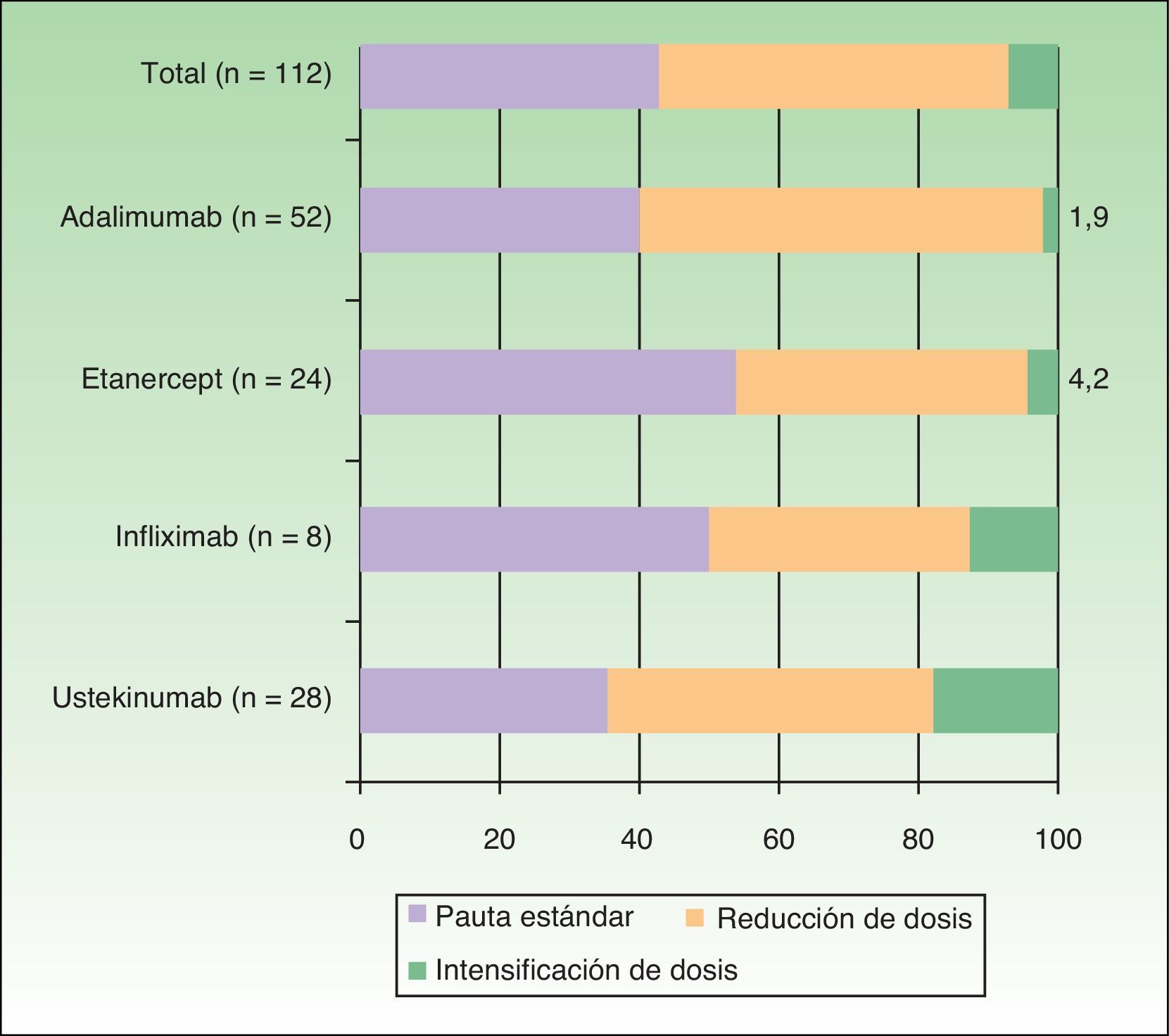
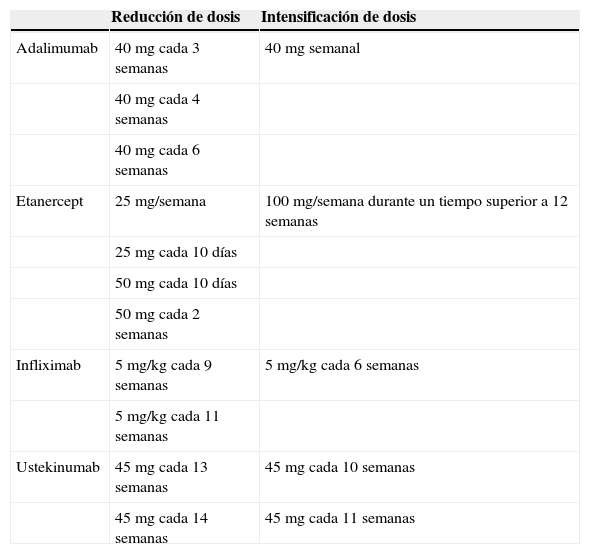
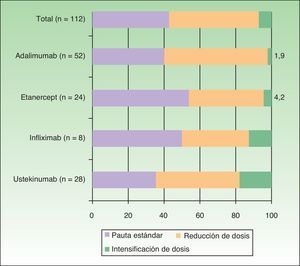
Pautas posológicasEn la tabla 2 se describen las pautas utilizadas para cada estrategia de modificación de dosis con los distintos biológicos. Asimismo, en la figura 2 se muestra la proporción de cada tipo de pauta seguida (estándar, reducida o intensificada) en función del tratamiento biológico administrado. En total, un 42,9% de la población siguió la pauta estándar, un 50% la pauta reducida y un 7,1% la pauta intensificada. El fármaco con el que más se redujo la dosis fue adalimumab (57,7%), y los que se intensificaron en mayor proporción fueron ustekinumab e infliximab (17,9% y 12,5% de los pacientes, respectivamente).
Pautas utilizadas para cada estrategia de modificación de dosis con los distintos biológicos empleados en el estudio
| Reducción de dosis | Intensificación de dosis | |
|---|---|---|
| Adalimumab | 40mg cada 3 semanas | 40mg semanal |
| 40mg cada 4 semanas | ||
| 40mg cada 6 semanas | ||
| Etanercept | 25mg/semana | 100mg/semana durante un tiempo superior a 12 semanas |
| 25mg cada 10 días | ||
| 50mg cada 10 días | ||
| 50mg cada 2 semanas | ||
| Infliximab | 5mg/kg cada 9 semanas | 5mg/kg cada 6 semanas |
| 5mg/kg cada 11 semanas | ||
| Ustekinumab | 45mg cada 13 semanas | 45mg cada 10 semanas |
| 45mg cada 14 semanas | 45mg cada 11 semanas |
En cuanto a la distribución porcentual de las distintas pautas de reducción de dosis, adalimumab se administró cada 3 (36,5%), 4 (17,3%) o 6 (3,8%) semanas y etanercept se administró en dosis de 25mg/10 días (8,3%), 25mg/semana (4,2%), 50mg/10 días (20,8%) o 50mg/2 semanas (8,3%). Infliximab se administró cada 9 (25%) u 11 semanas (12,5%) y ustekinumab cada 13 (39,3%) ó 14 semanas (7,1%). Esta estrategia de modificación de dosis (incluyendo a los pacientes con pauta estándar, intensificada y desintensificada) implica una reducción media de dosis/paciente/año de un 21% con adalimumab; un 13,8% con etanercept; un 0,9% con ustekinumab y 0,55% con infliximab en la cohorte estudiada.
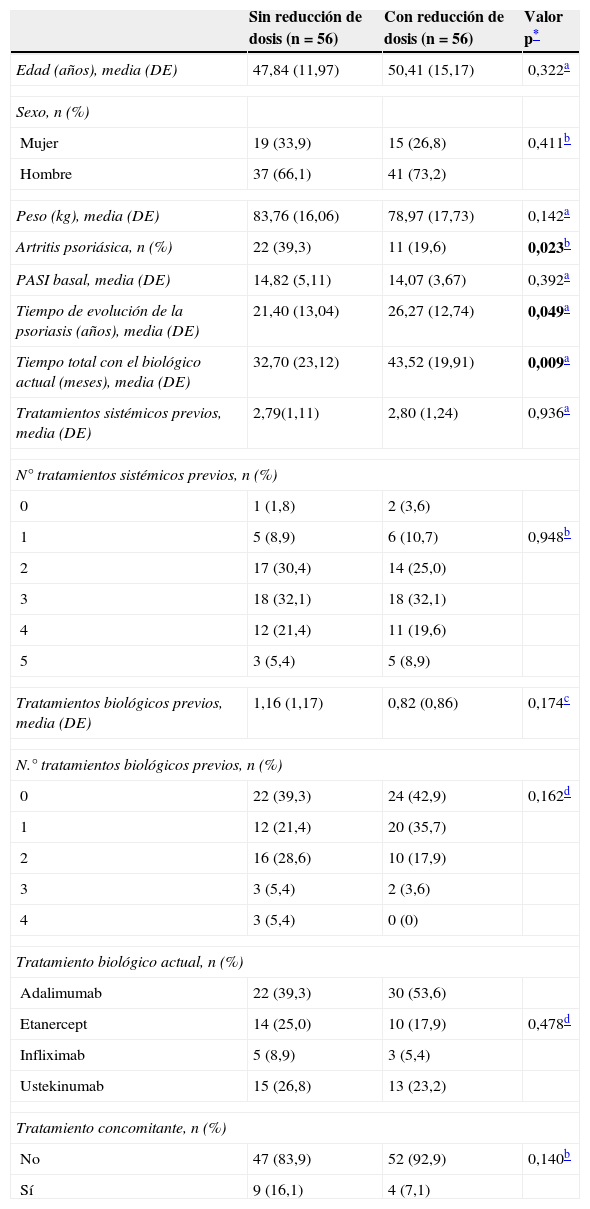
Perfiles de pacientes con reducción de dosisEl análisis comparativo entre los pacientes que pudieron recibir dosis reducidas frente al resto de pacientes, incluyendo los de dosis estándar e intensificados, reveló, respecto a las variables continuas diferencias significativas en que los primeros presentaban una psoriasis con más tiempo de evolución (p=0,049) y que llevaban más tiempo en tratamiento total con el mismo biológico (p=0,009) (tabla 3). En cuanto a las variables categóricas no se observaron diferencias significativas en cuanto al sexo, tipo de fármaco, necesidad y tipo de tratamiento concomitante o número de tratamientos previos (tanto sistémicos como biológicos) entre los pacientes con reducción de dosis y los que no fueron candidatos a reducirla (tabla 3). En cambio, hubo una mayor proporción de pacientes con artritis psoriásica entre los pacientes no aptos para reducir dosis frente a aquellos que la redujeron, siendo esta diferencia significativa (p=0,023) (tabla 3).
Análisis comparativo de las poblaciones/cohortes sin reducción de dosis (pauta estándar+pauta intensificada) frente a los que recibieron dosis reducidas
| Sin reducción de dosis (n=56) | Con reducción de dosis (n=56) | Valor p* | |
|---|---|---|---|
| Edad (años), media (DE) | 47,84 (11,97) | 50,41 (15,17) | 0,322a |
| Sexo, n (%) | |||
| Mujer | 19 (33,9) | 15 (26,8) | 0,411b |
| Hombre | 37 (66,1) | 41 (73,2) | |
| Peso (kg), media (DE) | 83,76 (16,06) | 78,97 (17,73) | 0,142a |
| Artritis psoriásica, n (%) | 22 (39,3) | 11 (19,6) | 0,023b |
| PASI basal, media (DE) | 14,82 (5,11) | 14,07 (3,67) | 0,392a |
| Tiempo de evolución de la psoriasis (años), media (DE) | 21,40 (13,04) | 26,27 (12,74) | 0,049a |
| Tiempo total con el biológico actual (meses), media (DE) | 32,70 (23,12) | 43,52 (19,91) | 0,009a |
| Tratamientos sistémicos previos, media (DE) | 2,79(1,11) | 2,80 (1,24) | 0,936a |
| N° tratamientos sistémicos previos, n (%) | |||
| 0 | 1 (1,8) | 2 (3,6) | |
| 1 | 5 (8,9) | 6 (10,7) | 0,948b |
| 2 | 17 (30,4) | 14 (25,0) | |
| 3 | 18 (32,1) | 18 (32,1) | |
| 4 | 12 (21,4) | 11 (19,6) | |
| 5 | 3 (5,4) | 5 (8,9) | |
| Tratamientos biológicos previos, media (DE) | 1,16 (1,17) | 0,82 (0,86) | 0,174c |
| N.° tratamientos biológicos previos, n (%) | |||
| 0 | 22 (39,3) | 24 (42,9) | 0,162d |
| 1 | 12 (21,4) | 20 (35,7) | |
| 2 | 16 (28,6) | 10 (17,9) | |
| 3 | 3 (5,4) | 2 (3,6) | |
| 4 | 3 (5,4) | 0 (0) | |
| Tratamiento biológico actual, n (%) | |||
| Adalimumab | 22 (39,3) | 30 (53,6) | |
| Etanercept | 14 (25,0) | 10 (17,9) | 0,478d |
| Infliximab | 5 (8,9) | 3 (5,4) | |
| Ustekinumab | 15 (26,8) | 13 (23,2) | |
| Tratamiento concomitante, n (%) | |||
| No | 47 (83,9) | 52 (92,9) | 0,140b |
| Sí | 9 (16,1) | 4 (7,1) | |
Se señalan en negrita los valores significativos.
DE: desviación estándar.
Merece la pena destacar que el peso no resultó una variable estadísticamente significativa entre el grupo de dosis reducida y el resto de los pacientes. Del total de pacientes incluidos en este estudio 14 pesaron más de 100kg (7 con pauta estándar, 2 intensificados y 5 en pauta reducida) y todos aquellos con pauta reducida fueron tratados con adalimumab. A los 2 pacientes con más de 100kg en tratamiento con ustekinumab se les mantuvo la dosis de 45mg/12 semanas cumpliendo con los objetivos terapéuticos.
En cuanto a los pacientes intensificados (n=8), en el análisis comparativo con el resto de pacientes, se encontraron diferencias estadísticamente significativas en el número previo de tratamientos biológicos que habían recibido (2,13 vs 0,9 respectivamente; p<0,05) y en la proporción de pacientes con tratamiento concomitante (50% vs 8,7% respectivamente; p<0,01).
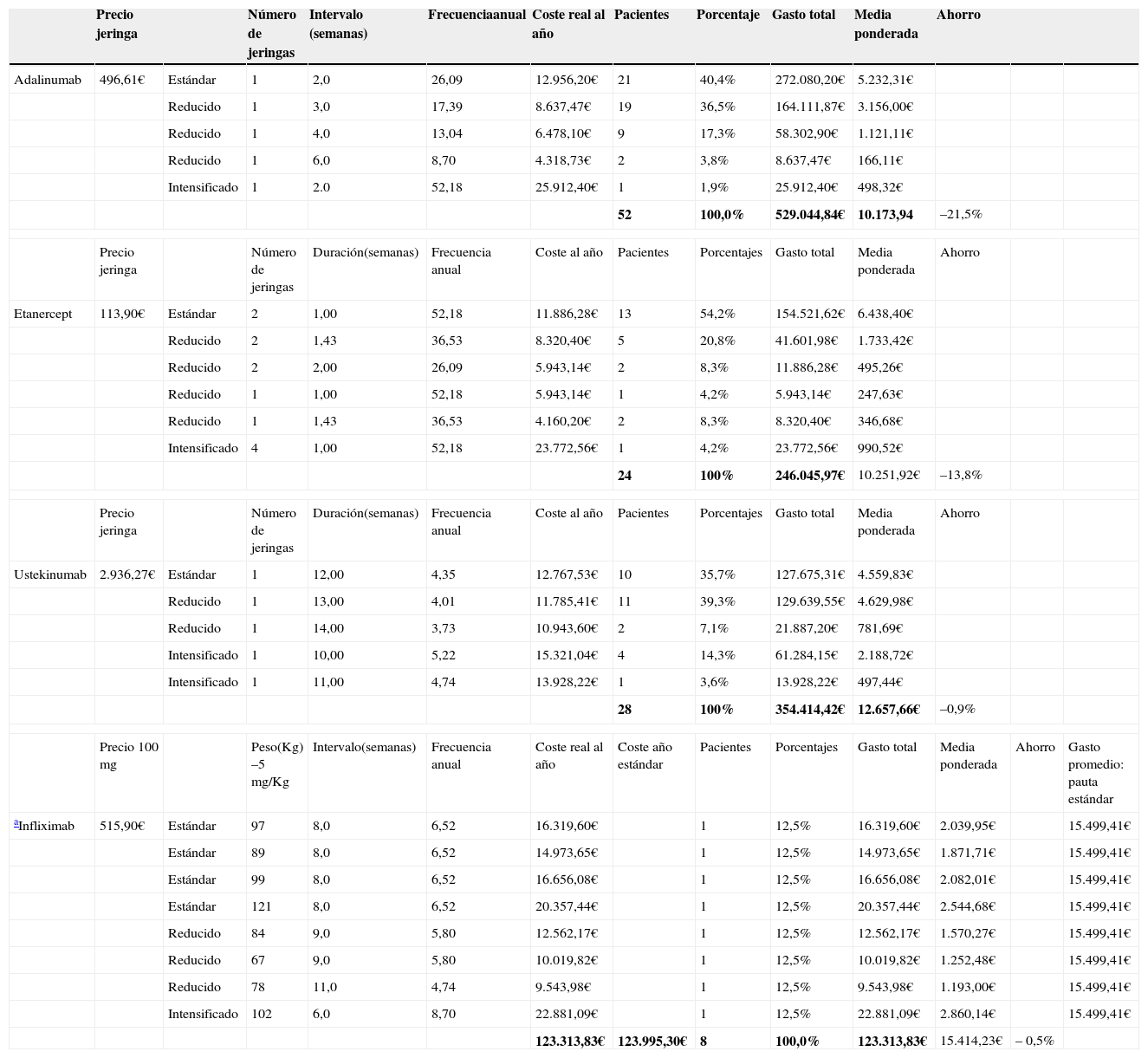
CostesSi examinamos los resultados en términos de costes por paciente/año del tratamiento, comparando los costes reales con los teóricos para la cohorte de pacientes estudiada (tabla 4), puede calcularse el porcentaje de ahorro derivado de esta intervención clínica. Los resultados para el total de la población analizada indican que la implementación de este algoritmo de modificación de dosis en la práctica clínica ha proporcionado, en esta población, un ahorro global del 13% del gasto farmacéutico (coste del tratamiento biológico).
Costes por paciente/año del tratamiento comparando los costes reales con los teóricos para la cohorte de pacientes estudiada. Porcentaje de ahorro derivado de esta intervención clínica para cada uno de los fármacos biológicos
| Precio jeringa | Número de jeringas | Intervalo (semanas) | Frecuenciaanual | Coste real al año | Pacientes | Porcentaje | Gasto total | Media ponderada | Ahorro | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Adalinumab | 496,61€ | Estándar | 1 | 2,0 | 26,09 | 12.956,20€ | 21 | 40,4% | 272.080,20€ | 5.232,31€ | |||
| Reducido | 1 | 3,0 | 17,39 | 8.637,47€ | 19 | 36,5% | 164.111,87€ | 3.156,00€ | |||||
| Reducido | 1 | 4,0 | 13,04 | 6.478,10€ | 9 | 17,3% | 58.302,90€ | 1.121,11€ | |||||
| Reducido | 1 | 6,0 | 8,70 | 4.318,73€ | 2 | 3,8% | 8.637,47€ | 166,11€ | |||||
| Intensificado | 1 | 2.0 | 52,18 | 25.912,40€ | 1 | 1,9% | 25.912,40€ | 498,32€ | |||||
| 52 | 100,0% | 529.044,84€ | 10.173,94 | –21,5% | |||||||||
| Precio jeringa | Número de jeringas | Duración(semanas) | Frecuencia anual | Coste al año | Pacientes | Porcentajes | Gasto total | Media ponderada | Ahorro | ||||
| Etanercept | 113,90€ | Estándar | 2 | 1,00 | 52,18 | 11.886,28€ | 13 | 54,2% | 154.521,62€ | 6.438,40€ | |||
| Reducido | 2 | 1,43 | 36,53 | 8.320,40€ | 5 | 20,8% | 41.601,98€ | 1.733,42€ | |||||
| Reducido | 2 | 2,00 | 26,09 | 5.943,14€ | 2 | 8,3% | 11.886,28€ | 495,26€ | |||||
| Reducido | 1 | 1,00 | 52,18 | 5.943,14€ | 1 | 4,2% | 5.943,14€ | 247,63€ | |||||
| Reducido | 1 | 1,43 | 36,53 | 4.160,20€ | 2 | 8,3% | 8.320,40€ | 346,68€ | |||||
| Intensificado | 4 | 1,00 | 52,18 | 23.772,56€ | 1 | 4,2% | 23.772,56€ | 990,52€ | |||||
| 24 | 100% | 246.045,97€ | 10.251,92€ | –13,8% | |||||||||
| Precio jeringa | Número de jeringas | Duración(semanas) | Frecuencia anual | Coste al año | Pacientes | Porcentajes | Gasto total | Media ponderada | Ahorro | ||||
| Ustekinumab | 2.936,27€ | Estándar | 1 | 12,00 | 4,35 | 12.767,53€ | 10 | 35,7% | 127.675,31€ | 4.559,83€ | |||
| Reducido | 1 | 13,00 | 4,01 | 11.785,41€ | 11 | 39,3% | 129.639,55€ | 4.629,98€ | |||||
| Reducido | 1 | 14,00 | 3,73 | 10.943,60€ | 2 | 7,1% | 21.887,20€ | 781,69€ | |||||
| Intensificado | 1 | 10,00 | 5,22 | 15.321,04€ | 4 | 14,3% | 61.284,15€ | 2.188,72€ | |||||
| Intensificado | 1 | 11,00 | 4,74 | 13.928,22€ | 1 | 3,6% | 13.928,22€ | 497,44€ | |||||
| 28 | 100% | 354.414,42€ | 12.657,66€ | –0,9% | |||||||||
| Precio 100 mg | Peso(Kg) –5 mg/Kg | Intervalo(semanas) | Frecuencia anual | Coste real al año | Coste año estándar | Pacientes | Porcentajes | Gasto total | Media ponderada | Ahorro | Gasto promedio: pauta estándar | ||
| aInfliximab | 515,90€ | Estándar | 97 | 8,0 | 6,52 | 16.319,60€ | 1 | 12,5% | 16.319,60€ | 2.039,95€ | 15.499,41€ | ||
| Estándar | 89 | 8,0 | 6,52 | 14.973,65€ | 1 | 12,5% | 14.973,65€ | 1.871,71€ | 15.499,41€ | ||||
| Estándar | 99 | 8,0 | 6,52 | 16.656,08€ | 1 | 12,5% | 16.656,08€ | 2.082,01€ | 15.499,41€ | ||||
| Estándar | 121 | 8,0 | 6,52 | 20.357,44€ | 1 | 12,5% | 20.357,44€ | 2.544,68€ | 15.499,41€ | ||||
| Reducido | 84 | 9,0 | 5,80 | 12.562,17€ | 1 | 12,5% | 12.562,17€ | 1.570,27€ | 15.499,41€ | ||||
| Reducido | 67 | 9,0 | 5,80 | 10.019,82€ | 1 | 12,5% | 10.019,82€ | 1.252,48€ | 15.499,41€ | ||||
| Reducido | 78 | 11,0 | 4,74 | 9.543,98€ | 1 | 12,5% | 9.543,98€ | 1.193,00€ | 15.499,41€ | ||||
| Intensificado | 102 | 6,0 | 8,70 | 22.881,09€ | 1 | 12,5% | 22.881,09€ | 2.860,14€ | 15.499,41€ | ||||
| 123.313,83€ | 123.995,30€ | 8 | 100,0% | 123.313,83€ | 15.414,23€ | – 0,5% | |||||||
Cuando este mismo análisis se realizó para cada uno de los fármacos biológicos, el porcentaje de ahorro oscila entre 21,5% con adalimumab, el 13,8% con etanercept, el 0,9% con ustekinumab y el 0,55% con infliximab.
El tratamiento que reveló ser la opción más cara según los costes reales de la cohorte estudiada fue infliximab (15.414€/paciente/año) derivado del alto peso medio de los pacientes (peso medio 92kg).
DiscusiónEste estudio ha analizado, en condiciones de práctica clínica, los patrones de modificación de dosis de fármacos biológicos en una cohorte de 112 pacientes con psoriasis moderada-grave, así como sus consecuencias sobre el control de la enfermedad y el coste de tratamiento.
Respecto a la distribución de los fármacos biológicos en la población estudiada, del total de 112 pacientes un 46,4% recibieron adalimumab, un 25% ustekinumab, un 21,4% etanercept y un 7,1% infliximab (tabla 1). Al tratarse de un estudio transversal estas diferencias en la distribución de los distintos fármacos biológicos estudiados podría ser reflejo del tiempo que estos llevan en el mercado.
Todos los pacientes se sometieron a una estrecha monitorización que permitió valorar la consecución o no de los objetivos terapéuticos marcados para aplicar una estrategia de modificación de dosis (fig. 1). Esta estrategia de modificación de dosis implicó una reducción media de dosis/paciente/año de un 21% con adalimumab; un 13,8% con etanercept; un 0,9% con ustekinumab y de un 0,55% con infliximab en la cohorte estudiada.
Son pocos los estudios disponibles que avalen el empleo de pautas modificadas, práctica habitual en distintos servicios de dermatología13,21–23. Teniendo en cuenta que la optimización de recursos económicos debe ir siempre ligada a la consecución de objetivos terapéuticos, es necesario profundizar en el conocimiento de estrategias de reducción de dosis, más frecuentes en un entorno de control estricto del gasto sanitario.
Los datos de seguridad de las pautas de biológicos modificadas son limitados. Su utilización debe por tanto individualizarse a cada paciente, en función de la gravedad de la psoriasis, su calidad de vida y la existencia de comorbilidades13. La detección de niveles de fármaco podría también facilitar esta decisión clínica, al poder identificar aquellos pacientes en remisión que presentan niveles excesivamente altos de fármaco, pero no se realiza de forma rutinaria en la mayoría de servicios de dermatología. Aunque se ha postulado que la ampliación del intervalo posológico con adalimumab aumenta el riesgo de formación de anticuerpos anti-adalimumab15, actualmente no existen datos que confirmen esta posibilidad22. Con infliximab, otro fármaco anti-TNF, se ha correlacionado el empleo de dosis menores o intervalos posológicos más largos con un riesgo mayor de aparición de anticuerpos antiinfliximab, fenómeno que produce una pérdida de eficacia del tratamiento24.
En nuestro estudio el análisis comparativo entre los pacientes que recibieron dosis reducidas frente al resto de pacientes reveló diferencias significativas en términos de que los primeros presentaban una psoriasis con más tiempo de evolución (p=0,049) y que llevaban más tiempo en tratamiento con biológico (p=0,009) (tabla 3). Estas diferencias podrían explicarse teniendo en cuenta que los pacientes que llevan más años bajo tratamiento en remisión, con buen control de esta enfermedad inflamatoria, podrían presentar un mayor umbral a sufrir nuevos brotes de actividad y, por tanto, podrían mantener el control de su psoriasis con menos dosis de tratamiento. Por otro lado, las diferencias encontradas en el PASI entre los grupos se justifican por el protocolo seguido en nuestra práctica clínica, que solo contempla esta estrategia cuando el paciente se encuentra en remisión. En cambio, entre los pacientes no aptos para reducir dosis hubo una mayor proporción de pacientes con artritis psoriásica (p<0,05) (tabla 3). Puede concluirse por tanto que la presencia de artritis psoriásica concomitante, al ser un factor de gravedad de la psoriasis, podría ser un factor limitante de la reducción de dosis.
Las publicaciones sobre la influencia de determinados factores predictivos en la eficacia de pautas modificadas de biológicos son escasas. En un estudio de práctica clínica realizado en 119 pacientes españoles con psoriasis moderada-severa tratados con adalimumab21, se estableció en análisis multivariante que las únicas variables independientes para el mantenimiento del biológico fueron la respuesta PASI 75 a un año y la habilidad de alargar los intervalos de inyección en los pacientes con mejor respuesta. Esta probabilidad pareció ser mayor en pacientes naïve a los biológicos y que presentaron las mejores respuestas en diferentes puntos temporales, lo que permitió alargar el intervalo posológico21. En nuestra cohorte, el porcentaje de pacientes naïve con cada uno de los tratamientos biológicos fue variable; osciló entre un 77% con etanercept, un 36,3% con adalimumab, un 25% con infliximab y un 17,85% con ustekinumab, diferencias que pudieron influir en la posibilidad de modificar la pauta con cada uno de los biológicos.
El presente estudio tiene una serie de limitaciones que deben mencionarse. En primer lugar, es un estudio observacional de práctica clínica, sin ningún protocolo preestablecido, por lo que la decisión y el momento de proceder a la reducción de dosis fue a criterio del investigador. La pauta de reducción de dosis fue empírica y se hizo de forma progresiva, aunque siempre teniendo en cuenta el objetivo clínico y, en caso de recidiva, volviendo a la dosis estándar. Además, dada la naturaleza retrospectiva del estudio, no todos los pacientes fueron tratados durante el mismo periodo de tiempo. Por otra parte, se incluyeron únicamente los pacientes en los que se alcanzó el objetivo terapéutico, por lo que no es posible obtener datos de efectividad clínica.
En resumen, presentamos una cohorte de 112 pacientes en práctica clínica habitual, con una pauta de reducción de dosis en el 50% de ellos, en el que el grupo de pacientes con dosis reducida mantiene una respuesta PASI 90. Presentaron mayor probabilidad de reducción de dosis, estadísticamente significativa, aquellos pacientes que presentaban mayor tiempo de evolución y más tiempo bajo tratamiento biológico. Al contrario, entre los pacientes sin reducción de dosis hubo mayor proporción de pacientes con artritis psoriásica. La implementación de este algoritmo de modificación de dosis en la práctica clínica ha proporcionado, en esta población, un ahorro global del 13% del gasto farmacéutico; para cada uno de los fármacos biológicos el porcentaje de ahorro paciente/año varía entre el 21,5% con adalimumab, el 13,8% con etanercept, el 0,9% con ustekinumab y 0,55% con infliximab.
Se requieren en un futuro estudios prospectivos controlados que ayuden a definir el perfil de paciente más adecuado para reducir la dosis, el porcentaje de pacientes que requerirán volver a la pauta habitual y si esto conlleva a largo plazo una pérdida de eficacia del tratamiento.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLa Dra. Baniandrés declara como conflicto de intereses haber recibido honorarios por su participación en ensayos clínicos, ponencias y asesoría para Abbvie, Pfizer, Janssen y MSD. El resto de autores declara no presentar conflicto de intereses.
A Antonio Javier Blasco y Pablo Lázaro de Mercado (TAISS) por la realización del análisis estadístico.