La leishmaniasis es endémica en España, siendo la leishmaniasis cutánea la forma más habitual de presentación. El objetivo del estudio fue valorar las características epidemiológicas y clínicas de la leishmaniasis cutánea en las últimas 2 décadas, haciendo hincapié en las diferencias clínicas según el estado inmunitario del paciente y el origen de la infección.
Materiales y métodosSe revisaron retrospectivamente 67 historias clínicas de pacientes diagnosticados de leishmaniasis entre 1992 y 2012, de ellas 54 eran cutáneas, y con datos de seguimiento.
ResultadosSe incluyeron 54 pacientes: 26 diagnosticados entre 1992-2002 y 28 entre 2003-2012.
La edad media fue de 49 años, con un predominio en varones y un tiempo medio de evolución previo a la consulta de 3 meses. Las manifestaciones clínicas más frecuentes fueron placas y úlceras. La mayoría de pacientes inmunodeprimidos y con leishmaniasis importada presentaron lesiones ulceradas y/o múltiples. El diagnóstico se basó en los hallazgos clínico-patológicos en la primera década, asociándose el diagnóstico por métodos moleculares en la segunda. El tratamiento de elección fue los antimoniales pentavalentes, con buenos resultados y escasos efectos adversos.
ConclusiónEl número de casos y de pacientes inmunodeprimidos fueron similares en ambas décadas, diagnosticándose un mayor número de leishmaniasis importada en la segunda. En los pacientes con lesiones múltiples y/o ulceradas deberían descartarse la inmunosupresión del huésped y la infección por cepas importadas. El tratamiento con antimoniato de meglumina fue eficaz y seguro, tanto por vía sistémica como intralesional.
Cutaneous leishmaniasis is the most common form of leishmaniasis, which is endemic in Spain. The aim of this study was to evaluate the epidemiological and clinical characteristics of cutaneous leishmaniasis seen in our hospital over a period of 20 years, with a particular focus on clinical differences according to immune status and origin of infection
Materials and methodsWe performed a chart review of 67 cases of cutaneous leishmaniasis diagnosed between 1992 and 2012. Follow-up data were available for 54 patients.
ResultsFifty-four patients with cutaneous leishmaniasis were included in the study. Of these, 26 had been diagnosed between 1992 and 2002 and 28 between 2003 and 2012.
The mean age at diagnosis was 49 years, there was a predominance of male patients, and the mean time from onset of symptoms to consultation was 3 months. The most common clinical manifestations were plaques and ulcers. Most of the immunodepressed patients and patients with imported leishmaniasis had skin ulcers and/or multiple lesions. During the first decade of the study, diagnosis was based on clinical and histologic findings. These were supported by molecular techniques in the second decade. Pentavalent antimonials were the treatment of choice, producing good results and very few adverse effects
ConclusionThe number of patients with cutaneous leishmaniasis and with compromised immune status was similar in the periods 1992-2002 and 2003-2013, but more cases of imported leishmaniasis were diagnosed in the second period. Patients with ulcers and/or multiple lesions should be evaluated to rule out immunosuppression or infection by Leishmania species from other parts of the world. Both systemic and intralesional meglumine antimonate was effective and safe
La leishmaniasis es una enfermedad infecciosa parasitaria ampliamente distribuida. Es endémica en más de 70 países, aunque su notificación es obligatoria solo en 32 de estos, por lo que se considera que su verdadera incidencia está subestimada1,2.
La prevalencia general de leishmaniasis es de 12 millones, con un número estimado de 1,5 millones de nuevos casos al año (0,5 millones de casos de leishmaniasis visceral y 1,5 millones de casos de leishmaniasis cutánea)3. Aproximadamente 350 millones de personas, que a menudo son pobres, están en riesgo de contraer la enfermedad. Los países más afectados son Afganistán, Brasil, Irán, Perú, Arabia Saudita y Libia. Además, en el viejo mundo la prevalencia es elevada en la zona mediterránea4,5, y en España se considera endémica en las comunidades de Andalucía, Aragón, Baleares, Cantabria, Castilla y León, Cataluña, Comunidad Valenciana, Extremadura, Madrid, Murcia, Navarra y La Rioja3.
Según el registro realizado por la Red Nacional de Vigilancia Epidemiológica desde 1996 hasta 2011, se han notificado en España 1.755 casos de leishmaniasis4, con una incidencia de media anual de 0,45 casos/100.000 hab. Esta cifra infraestima la incidencia de la enfermedad en el país, ya que solo es de declaración obligatoria en las comunidades donde se considera endémica.
De acuerdo al conjunto mínimo básico de datos en el periodo 2010-2011 hubo 2.739 hospitalizaciones en las que la leishmaniasis estaba codificada en el diagnóstico principal, de estos pacientes 98 (3,6%) tenían formas cutáneas.
Entre 2005 y 2010 se declararon una media de 115 casos anuales de leishmaniasis, elevándose el número de casos a 271 en 2011 (tasa 0,59 casos por 100.000 habitantes), debido a un brote surgido en la Comunidad de Madrid (tasa 2,83 casos por 100.000 habitantes)5,6.
En el área mediterránea las especies endémicas son la Leishmania infantum y la Leishmania tropica7. En España es endémica solo la Leishmania infantum. La forma clínica más frecuente es la afectación cutánea8,9 y las manifestaciones clínicas habituales son las pápulas y los nódulos autolimitados10.
Se ha descrito un aumento de la incidencia de leishmaniasis importadas y en pacientes inmunodeprimidos en los últimos años11 relacionado con la presencia de reservorios animales, la movilidad geográfica y el cambio climático, entre otros2.
Se ha dado un cambio en el tipo de inmunosupresión que padecen los pacientes con leishmaniasis, pues si bien con la terapia antirretroviral ha disminuido el número de casos de coinfección VIH-leishmania, han aumentado los pacientes con algún tipo de inmunosupresión farmacológica, particularmente los pacientes trasplantados, con enfermedades reumatológicas, oncológicas y/o hematológicas11.
El objetivo de este trabajo fue valorar las características epidemiológicas y clínicas de los pacientes diagnosticados de leishmaniasis cutánea en nuestro centro en las últimas 2 décadas, haciendo hincapié en las diferencias en su presentación clínica en pacientes inmunodeprimidos o en pacientes con infecciones importadas.
Materiales y métodosSe trata de un estudio retrospectivo, en el que revisaron los datos epidemiológicos, clínicos, microbiológicos e histopatológicos de 67 pacientes diagnosticados de leishmaniasis cutánea atendidos en el servicio de dermatología de un hospital terciario, en el período comprendido entre septiembre de 1992 y diciembre de 2012. De ellos 5 tenían leishmaniasis visceral. Se incluyeron finalmente 54 pacientes de los que se disponía de datos relevantes para el estudio. Se hizo un análisis comparativo de los resultados obtenidos entre 2 décadas consecutivas (1992 hasta 2002 y 2003 hasta 2012) para comprobar si se producía un aumento en el número de casos y/o se observaban cambios en las formas de presentación, ya que la introducción de los fármacos inmunosupresores o modificadores de la inmunidad, tales como los tratamientos biológicos, han sido introducidos mayoritariamente en la última década.
ResultadosSe incluyeron 54 pacientes. El número de casos registrados fue similar en ambas décadas, aunque el número fue ligeramente mayor en la segunda década (28 pacientes versus 26 pacientes).
La mediana de edad fue de 43 años (rango de 13 a 78 años) con un predominio del sexo masculino (proporción hombres/mujeres: 2,3/1). El tiempo medio de evolución desde la aparición de los síntomas hasta la consulta fue de 3 meses (un mes-4 años).
En la tabla 1 se exponen los datos epidemiológicos y clínicos de los pacientes.
Datos clínicos y epidemiológicos de 54 pacientes con diagnóstico de leishmaniasis cutánea
| Datos clínicos e inmunológicos | Pacientes | |||
|---|---|---|---|---|
| Total | 1.ª década | 2.ª década | ||
| 54 | 26 | 28 | ||
| Estado inmunitario | Inmunocompetentes | 36 | 18 | 18 |
| Inmunodeprimidos | 16 | 8 | 8 | |
| Origen de la infección | Autóctona | 32 | 17 | 15 |
| Importada | 19 | 8 | 11 | |
| Presentación clínica | Mácula/pápula/nódulo | 33 | 22 | 11 |
| Placa | 21 | 6 | 15 | |
| Úlcera | 27 | 10 | 17 | |
| Mucosa | 4 | 2 | 2 | |
| Número | Única | 21 | 13 | 8 |
| Múltiple | 33 | 14 | 18 | |
Dieciséis de los 54 pacientes (29,62%) eran inmunodeprimidos, siendo el número de pacientes inmunodeprimidos similar en ambas décadas. Las causas de inmunosupresión fueron enfermedades linfoproliferativas (3), enfermedades autoinmunes (4) e infección por VIH (7), tratamientos inmunosupresores (9) y tratamientos con fármacos biológicos (2).
De los 7 pacientes con VIH, 4 a la primera década de estudio y 3 a la segunda, en esta última década encontramos pacientes más inmunodeprimidos como consecuencia de tratamientos biológicos, antitumorales y aquellos tratados por enfermedades autoinmunes.
Diecinueve pacientes (35%) fueron diagnosticados de leishmaniasis cutánea importada. Los países de origen eran: Jordania, Ecuador, Perú, Guatemala, Túnez, Bolivia, Mauritania, Venezuela, Irán, Israel, India y Marruecos. La incidencia de leishmaniasis importada fue superior en la segunda década del estudio (11/19) que en la primera (8/19) (tabla 1).
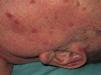
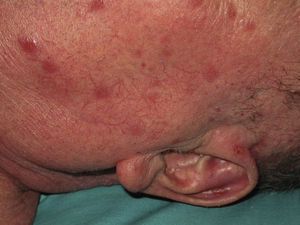
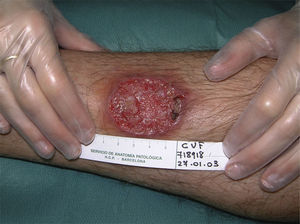
Se valoraron un total de 81 lesiones. Las formas en placas (26%) y las ulceradas (33%) fueron más predominantes, siendo ambas más frecuentes en la segunda década. El resto de las lesiones (41%) fueron máculas, pápulas y nódulos. Treinta y dos pacientes (59%) presentaron más de 2 lesiones, lo que se consideró como leishmaniasis múltiple (fig. 1).
Cuatro pacientes (2 en la primera década y 2 en la segunda) desarrollaron afectación mucosa oral y/o nasal por contigüidad de lesiones cutáneas faciales.
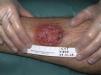
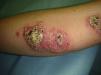
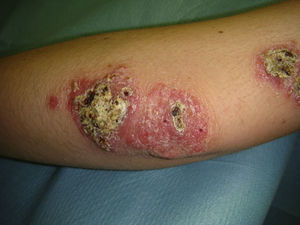
Todos los casos fueron observados en pacientes que no referían haber realizado viajes fuera del país, y en un caso se pudo confirmar por reacción en cadena de la polimerasa (PCR) la causalidad por L. infantum. Por ello se consideró que habían sido debidos a L. infantum, siendo diagnosticados de leishmaniasis cutánea con afectación mucosa. Dos casos se presentaron en pacientes inmunocompetentes y 2 en inmunodeprimidos. En la tabla 2 se describen las características de los pacientes según el origen en inmunidad de los mismos. De los 16 pacientes inmunodeprimidos un 62,5% tenía lesiones múltiples y la misma proporción de pacientes presentaba lesiones ulceradas. De los 19 pacientes con leishmaniasis importadas el 63% tenía lesiones múltiples y el 78% lesiones ulceradas (figs. 2 y 3).
Clasificación de los 54 casos de leishmaniasis cutánea según origen e inmunidad de los pacientes
| Lesiones múltiples, n (%) | Lesiones ulceradas, n (%) | Lesiones múltiples y ulceradas, n (%) | |
|---|---|---|---|
| Pacientes inmunocompetentes (n: 36) | 12 (33) | 4 (11) | 3 (8,3) |
| Pacientes inmunodeprimidos (n: 16) | 10 (62,5) | 10 (62,5) | 6 (37,3) |
| Leishmaniasis autóctonas (n: 32) | 6 (46,2) | 2 (15,4) | 2 (15,4) |
| Leishmaniasis importadas (n: 19) | 12 (63) | 2 (66,6) | 2 (66,6) |
| Pacientes inmunodeprimidos con leishmaniasis autóctonas (n: 13) | 6 (46,2) | 2 (15,4) | 2 (15,4) |
| Pacientes inmunodeprimidos con leishmaniasis importadas (n: 3) | 3 (100) | 2 (66,66) | 2 (66,66) |
De los 36 pacientes inmunocompetentes un 33% tenía lesiones múltiples y un 11% lesiones ulceradas, mientras que de los 32 pacientes con leishmaniasis autóctona un 31% tenía lesiones múltiples y un 6,25% lesiones ulceradas.
El diagnóstico durante la primera década se basó en los hallazgos clínico-patológicos en todos los casos. Se realizó estudio anatomopatológico en 41 pacientes, con tinción de hematoxilina-eosina, solo realizándose tinción de Giemsa en 3 de los casos.
En la segunda década, además del estudio clínico-patológico se realizaron técnicas de biología molecular que confirmaron el diagnóstico en 11 pacientes. Mediante la PCR se identificó la especie de Leishmania en 6 casos: L. infantum (5) y L. tropica (1), esta última adquirida en Jordania.
Se realizó tratamiento con antimonial pentavalente, antimoniato de meglumina, intralesional en 32 casos e intramuscular (20mg/kg/día por 21 días) en 16.
Se decidió tratar con antimoniato de meglumina intralesional a los pacientes con lesiones únicas de menos de 3cm y/o con menos de 5 lesiones. El tratamiento sistémico se empleó en las lesiones de mayor tamaño o múltiples (5 o más lesiones).
Solo un paciente tratado con antimoniato de meglumina intramuscular desarrolló efectos adversos graves: arritmia supraventricular, aumento de enzimas hepáticas y pancreáticas e insuficiencia renal aguda. Por este motivo el tratamiento fue suspendido a las 2 semanas, a pesar de lo cual las lesiones se resolvieron. No se pudo confirmar la curación, ya que el paciente falleció por progresión de su enfermedad de base. El resto de los pacientes tratados con antimoniato de meglumina finalizaron el tratamiento sin complicaciones.
En la segunda década 7 pacientes recibieron tratamiento con anfotericina B liposomal endovenosa (3-4mg/kg/día en días 1 al 5, 14 y 21, dependiendo de la inmunidad del paciente)12. Tres de ellos resolvieron las lesiones y 4 no respondieron al tratamiento. En los 4 pacientes no respondedores a anfotericina B liposomal se administró posteriormente antimoniato de meglumina intramuscular a la dosis habitual. Tres de estos pacientes tuvieron respuesta completa y uno con inmunosupresión grave asociada a VIH mejoró, aunque falleció por causas ajenas a la leishmaniasis o a su tratamiento.
Se hizo seguimiento clínico de un mínimo de 14 meses en 39 pacientes (74%), confirmándose la curación en 35 de ellos (65%) en los pacientes asintomáticos al año de seguimiento. En 14 pacientes no se realizó control tras el tratamiento; todos ellos presentaban una única lesión de leishmaniasis cutánea.
DiscusiónLa leishmaniasis es una parasitosis endémica del área mediterránea. Se prevé un incremento en el número de casos de leishmaniasis en los próximos años debido al aumento del reservorio (perros domésticos infectados)3, de huéspedes inmunodeprimidos, a los movimientos migratorios y al calentamiento global11.
Se estima que un 75% de los nuevos casos diagnosticados de leishmaniasis corresponden a formas cutáneas13.
En nuestro estudio, en el que se realizó una comparación entre las décadas 1992-2001 y 2002-2012, se comprobó una incidencia levemente mayor de leishmaniasis cutánea en la segunda década (26 versus 28).
Se observó un predominio en varones, tal como ha sido ya previamente descrito13. Aunque la leishmaniasis se considera una enfermedad de predominio infantil, en nuestra serie todos los pacientes incluidos fueron adultos, ya que nuestro centro no dispone de atención pediátrica.
En nuestro trabajo la incidencia de leishmaniasis en inmunodeprimidos fue similar en ambas décadas estudiadas, en contraposición a lo referido por otros autores, que prevén un aumento progresivo de la incidencia de leishmaniasis en este grupo de pacientes11. La introducción de la medicación antirretrovírica en los hospitales de España, incluido el nuestro, fue a finales de 1996, siendo aplicada completamente en 1997. Por lo que posiblemente el número de pacientes con inmunosupresión grave por infección por VIH se estabilizó en la segunda década, con disminución del número de casos de leishmaniasis con afectación cutánea en estos pacientes. El bajo número de pacientes incluidos podría ser también un factor para no hallar diferencias. El 60% de los casos de leishmaniasis importada provenían del viejo mundo, a diferencia de lo reportado por muchos autores, donde en España las leishmaniasis son más frecuentemente importadas desde el nuevo mundo14.
Las manifestaciones clínicas cutáneas habituales de la infección producida por L. infantum en pacientes inmunocompetentes son pápulas, placas o nódulos únicos o múltiples, autolimitados, que pueden ulcerarse10. En nuestro estudio las manifestaciones cutáneas fueron las ya descritas, pero cabe destacar que los pacientes inmunocompetentes y/o con leishmaniasis autóctonas presentaron más frecuentemente lesiones únicas y no ulceradas, mientras que la mayoría de los pacientes inmunodeprimidos y/o con leishmaniasis importadas presentaron lesiones múltiples y/o ulceradas. Por ello consideramos que sería aconsejable en pacientes con leishmaniasis cutánea con lesiones ulceradas y/o múltiples descartar inmunosupresión o infección por cepas importadas.
El retraso en el diagnóstico está frecuentemente descrito6. En nuestro caso, la media desde el inicio del proceso hasta el diagnóstico fue de 3 meses. El diagnóstico diferencial es amplio e incluye dermatosis tales como las picaduras de insectos, las infecciones bacterianas o por micobacterias, e incluso, procesos granulomatosos. El diagnóstico de la leishmaniasis incluye la histología, cultivo y técnicas de diagnóstico molecular. En el estudio anatomopatológico se pueden observar los amastigotes de Leishmania dentro de los macrófagos en la dermis superior, asociados a un infiltrado inflamatorio linfoplasmocitario. Se puede realizar el diagnóstico con la tinción de hematoxilina-eosina, siendo también muy útil la tinción de Giemsa. El cultivo se ha realizado típicamente en medio Novy, MacNeal, Nicolle (NNN). Sin embargo, este método es poco utilizado en nuestro centro por su escaso rendimiento y su lentitud en el crecimiento de la Leishmania. Finalmente, las técnicas diagnósticas moleculares, especialmente la PCR es una de las técnicas más sensibles para el diagnóstico de la leishmaniasis cutánea15.
Durante la primera década del estudio se confirmó el diagnóstico por histología, y a partir de 2003 la introducción de las técnicas de biología molecular permitió confirmar el diagnóstico en el 20% de los casos e identificar la especie en el 54% de ellos. La identificación de la especie es de especial importancia en las leishmaniasis importadas para decidir el tratamiento y predecir la evolución. Las leishmaniasis centroamericanas requieren tratamiento sistémico para evitar el desarrollo de la afectación mucosa y la diseminación linfática (tabla 3). Sin embargo, cuando el estudio molecular no es posible, una correcta anamnesis y el estudio histológico siguen siendo las bases del diagnóstico16.
Datos de diagnóstico, tratamiento y evolución de los 54 casos de leishmaniasis cutánea
| Pacientes | ||||
|---|---|---|---|---|
| Datos recolectados/total de casos revisados | Total | 1.ª década | 2.ª década | |
| Pacientes | 54 | 28 | 26 | |
| Diagnóstico | Clínico | 39 | 18 | 21 |
| Histopatológico | 41 | 23 | 18 | |
| Molecular | 11 | 0 | 11 | |
| Tratamiento | Glucantime IL | 32 | 19 | 13 |
| Glucantime IM | 16 | 5 | 11 | |
| Amfotericina B liposomal | 7 | 0 | 7 | |
| Evolución | Muerte | 4 | 2 | 2 |
| Curación | 35 | 15 | 20 | |
| Pérdida de seguimiento | 14 | 9 | 5 | |
IL: intralesional; IM: intramuscular.
El tratamiento con antimoniato de meglumina fue efectivo en la mayoría de los casos. Se han descrito múltiples efectos adversos a antimoniato de meglumina cuando se utiliza de forma sistémica17, entre los que se destacan mialgias, artralgias, elevación de enzimas pancreáticas, exantema, náuseas, dolor abdominal, fatiga, cefalea, elevación de transaminasas, leucopenia y elevación inespecífica del segmento ST del electrocardiograma18. En nuestra serie este fármaco resultó seguro y eficaz, siendo necesario suprimirlo solo en un paciente al que se le administró por vía sistémica, debido a efectos adversos graves.
El tratamiento de elección para la leishmaniasis cutánea, tanto en su forma localizada como diseminada, independientemente del estado inmunitario del paciente, continúan siendo los antimoniales pentavalentes10,19,20.
La anfotericina B liposomal es especialmente efectiva en la leishmaniasis visceral, y en nuestro caso fue parcialmente efectiva en la leishmaniasis cutánea.
Cuatro de 7 pacientes en los que se decidió tratamiento con anfotericina B liposomal no mostraron mejoría, aunque sí respondieron posteriormente a la administración de antimoniato de meglumina intramuscular.
Desde la década de los 90 se sabe que un alto porcentaje de casos de leishmaniasis cutáneas del viejo mundo curan espontáneamente, y además se han observado buenos resultados en los diferentes estudios publicados acerca de las terapias locales: crioterapia, pomada de paromomicina, antimoniales intralesionales. El antimonio de meglumina intralesional a una dosis de 0,5-3ml administrado una a 3 veces por semana durante 4-5 semanas se considera en la actualidad el tratamiento de primera línea en la mayoría de los casos, y tiene una eficacia demostrada para el tratamiento de L. infantum en el área mediterránea (nivel BII)21. Los efectos adversos descritos incluyen reacciones alérgicas locales, dolor, edema, prurito y eritema transitorio. La terapia intralesional no se recomienda para localizaciones especiales como dedos, pabellón auricular, labios y nariz22.
Las terapias locales sumadas al tratamiento sistémico han mostrado resultados superiores a cualquiera de estos tratamientos de forma aislada. Las diferentes terapias orales: azoles y miltefosina disminuyen los costes derivados de la hospitalización. La respuesta a estos fármacos es limitada, ya que el conocimiento actual se limita a series de casos basadas fundamentalmente en pacientes en los que otros tratamientos habían fracasado previamente23.
Para la leishmaniasis cutánea del nuevo mundo, si bien el tratamiento local puede considerarse en situaciones específicas, la vía sistémica es la de elección. La eficacia de cada fármaco depende de la especie de Leishmania implicada y de la zona geográfica. Los antimoniales pentavalentes son los fármacos más utilizados, pero con muchos efectos secundarios, además necesitan una administración prolongada. Para el tratamiento de la leishmaniasis cutaneomucosa del nuevo mundo se recomienda antimoniato de meglumina durante 30 días asociado con pentoxifilina15,21,23.
Se perdió el seguimiento de un 25% de pacientes, la mayoría de los cuales presentaba una única lesión y habían sido tratados con antimoniato de meglumina intralesional y/o crioterapia, por lo que presumimos que la mayoría de estos casos evolucionaron a la curación postratamiento. Ninguna de las 4 muertes ocurridas durante el estudio tuvo relación con la infección ni con el tratamiento.
En conclusión, no hemos detectado un aumento en el número de diagnósticos de leishmaniasis cutánea ni un incremento de pacientes inmunodeprimidos afectos en las 2 últimas décadas. Consideramos que ante un paciente con leishmaniasis cutánea con lesiones múltiples y/o lesiones ulceradas es recomendable valorar su estado inmunológico, así como descartar la posibilidad de infección por cepas importadas.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran que no tienen ningún conflicto de intereses.