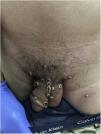
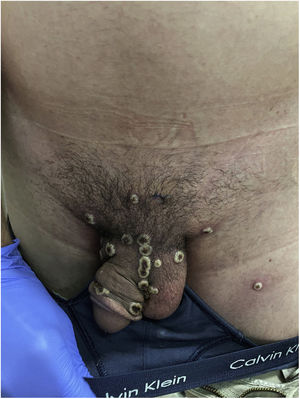
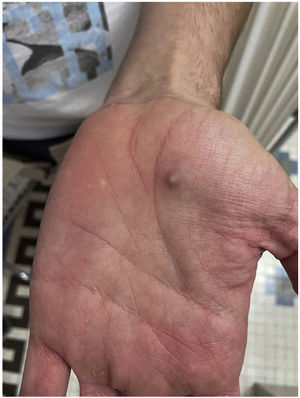
Un hombre de 32 años acudió al Centro Sanitario Sandoval (Comunidad Autónoma de Madrid) por la aparición de unas lesiones diseminadas que aparecieron ocho días antes (fig. 1). Refería mantener relaciones sexuales con hombres (HSH) y, como antecedentes personales, destacaban la infección por VIH controlada con TARGA, con una carga viral indetectable y episodios pasados de uretritis gonocócica y por Chlamydia trachomatis.
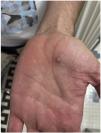
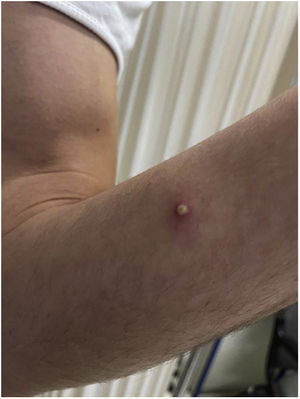
El paciente explicó que, tras aparecer las lesiones en los genitales, los brazos y las palmas acudió a un centro sanitario donde, de forma empírica y sin diagnóstico, se le pautó tratamiento con doxiciclina y prednisona, sin poder precisar la dosis, que recibió durante aproximadamente una semana. De manera simultánea, se aplicó crema de imiquimod al 5% durante cuatro a cinco días, a instancias de un conocido por sospechar una infección por molusco contagioso (fig. 2).
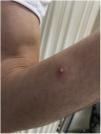
A la exploración presentaba múltiples pústulas umbilicadas con el centro oscuro en los genitales y el pubis, en ambas extremidades superiores y en las palmas de las manos con una inflamación peripustular. Además, presentaba adenopatías inguinales bilaterales dolorosas (fig. 3).
Ante la sospecha clínica de una infección por la viruela del mono, se volvió a interrogar al paciente, que refirió haber estado en una sauna, manteniendo relaciones sexuales con hombres, diez días antes de la aparición de fiebre y malestar general, seguida, dos días después, del brote de lesiones pustulosas.
Para confirmar la infección por el virus de la viruela del mono y descartar otras infecciones de transmisión sexual, se extrajeron muestras de exudado rectal, muestras de orina y sangre, así como de las lesiones para realizar la prueba de reacción en cadena de la polimerasa (PCR) para ortopoxvirus en el Centro Nacional de Microbiología de Majadahonda.
El paciente, de acuerdo con las recomendaciones de Salud Pública, permaneció en aislamiento domiciliario durante aproximadamente 10 días, durante los cuales recibió tratamiento de soporte oral con antiinflamatorios y antitérmicos, así como una solución de agua sulfatada para las lesiones cutáneas.
El resultado de la PCR fue positivo para virus de la viruela del mono y el paciente evolucionó satisfactoriamente con una lenta resolución de las lesiones, que fue completa a las dos semanas del inicio del aislamiento.
El caso descrito es uno de los primeros casos confirmados del brote de viruela del mono que comenzó en Madrid durante el mes de mayo del 20221. El virus de la viruela del mono o el virus Monkeypox (MPX) se transmite a los humanos a través del contacto con animales o humanos infectados o bien a través de material contaminado con el virus. El virus penetra en el organismo a través de soluciones de continuidad en la piel, el tracto respiratorio o las membranas mucosas. El periodo de incubación es de seis a 16 días, aunque puede variar entre cinco y 21 días. Existe evidencia de infecciones de MPX asintomáticas en individuos vacunados contra la viruela y en pacientes no vacunados2.
Se asume que el principal factor para la infección en humanos de MPX es la transmisión del virus a través del contacto directo o indirecto con animales vivos o muertos. Esto puede ocurrir por mordedura, contacto directo con fluidos o lesiones de un animal infectado o material contaminado. También puede ser una fuente de contagio comer carne inadecuadamente cocinada de un animal infectado.
La transmisión humano-humano es rara, pero se han descrito brotes causados por este medio. Además, el virus MPX puede ser transmitido por contacto directo con fluidos corporales de una persona infectada o por objetos contaminados como la ropa o la ropa de cama, entre otros.
La capacidad de detección por PCR del ADN del virus MPX de lesiones cutáneas sospechosas está bien establecida.
Dada la limitada duración de la viremia es preferible obtener muestras de exudados, costras y aspirado del fluido de las lesiones en lugar de muestras sanguíneas. La PCR en tiempo real puede discriminar no solo el virus MPX de otros Orthopoxvirus, sino también cepas distintas del propio virus MPX3.
La serología tiene un valor limitado dada la reacción cruzada inmunológica entre Orthopoxvirus patógenos en los humanos. Sin embargo, puede ser útil para excluir una infección reciente por Orthopoxvirus, para la investigación de los contactos y el estudio serológico poblacional. La inmunohistoquímica puede usarse para identificar antígenos en biopsias y para excluir o identificar otros agentes sospechosos4.
No hay vacuna o tratamiento específico disponible para el virus MPX. El tratamiento es sintomático y de soporte, incluyendo la prevención y el tratamiento de sobreinfecciones bacterianas. Actualmente, no hay vacuna específica contra el virus MPX. Las vacunas de primera y segunda generación contra la viruela administradas durante los programas de erradicación de la viruela a todos aquellos nacidos antes de marzo de 1978 confieren una protección efectiva contra el virus MPX.
Estas vacunas, debido a los efectos adversos, generalmente no se han usado para el control del virus MPX. Sin embargo, en EE. UU. en 2003, 30 personas recibieron la vacuna para la viruela durante ese brote. Existe una tercera generación de vacunas (MVA-BN/Imvanex) contra esta enfermedad desarrollada para individuos en los que las versiones previas de la vacuna de la viruela están contraindicadas. Dicha vacuna deriva de un virus que ha perdido la habilidad para replicarse en células de primates.
Esta vacuna tiene un perfil de seguridad mucho más favorable que previas generaciones de vacunas para la viruela. Está aprobada en Europa para inmunización contra la viruela en adultos y fue empleada en el Reino Unido en 2018 después de la identificación de casos de virus MPX.
Las medidas de control de salud pública tienen como objetivo reducir la transmisión de humano a humano a través del reconocimiento temprano de los casos, con base en la sospecha clínica y pruebas de laboratorio, el aislamiento de los pacientes infectados, la implementación de apropiada prevención de la infección y medidas de control en centros sanitarios (estándar, de contacto y aerosoles), así como la detección temprana de posibles nuevos casos por medio del rastreo de contactos y de los lugares de origen de los brotes.
La vacuna de la viruela se puede ofrecer a los contactos, incluyendo a los trabajadores sanitarios en contacto con pacientes, individuos con exposición al virus MPX en los lugares de los brotes y a los convivientes e individuos con un contacto estrecho.
El efecto protector de la vacuna de la viruela humana se ha demostrado en estudios en los años 80 que mostraban más de un 85% de efectividad5.
La Organización Mundial de la Salud (OMS) sugiere que las autoridades nacionales de salud deberían ofrecer la vacuna de la viruela a aquellos que traten pacientes o hayan estado expuestos a estos o a sus muestras.
Según los centros para el control y la prevención de enfermedades de EE. UU. la vacunación temprana post exposición con la vacuna de la viruela dentro de los primeros 14 días después de una exposición es una opción que considerar para reducir los síntomas del virus MPX.
Desde la erradicación mundial de la viruela, la vacuna de esta enfermedad no está disponible al público general pero varios países y la OMS mantienen stock de esta. Las vacunas de la viruela fabricadas con tecnologías antiguas no deberían ser administradas a personas inmunocomprometidas6.