Las fotodermatosis son enfermedades de la piel inducidas o exacerbadas por la radiación electromagnética (que incluye la radiación ultravioleta, la luz visible y la radiación infrarroja) emitida por el sol o por fuentes artificiales. En la primera parte de esta revisión expondremos los conocimientos actuales sobre la fisiopatología de estos procesos y su clasificación. Además, realizaremos una serie de consideraciones técnicas acerca de las bases físicas de los estudios fotobiológicos y, finalmente, se detallarán los equipos necesarios para su realización (fuentes de luz, instrumentos de medición y sistemas de calibración).
Photodermatoses are skin conditions that are induced or exacerbated by electromagnetic radiation (including visible light, UV light, and infrared radiation) from the sun or artificial light sources. In Part 1 of this series we review current understanding of the pathophysiology of these processes and their classification. We also discuss technical aspects and the basic physics of photobiology and describe the equipment required for photobiologic testing and calibration (light sources and measurement instruments).
Las fotodermatosis son enfermedades de la piel inducidas o exacerbadas por la radiación electromagnética (que incluye la radiación ultravioleta, la luz visible y la radiación infrarroja) emitida por el sol o por fuentes artificiales1 (tabla 1). Se definen como fotodermatosis idiopáticas o inflamatorias aquellas en las que el mecanismo etiopatogénico se desconoce, si bien se presume una disfunción inmunológica que ocasiona una reactividad alterada a ciertos alérgenos endógenos. Se excluyen aquellas dermatosis desencadenadas o agravadas por la luz que son secundarias a alteraciones genéticas o metabólicas, y también las dermatosis fotoagravadas. Las fotodermatosis exógenas son aquellas inducidas por la acción sobre la piel de agentes químicos (industriales, cosméticos o terapéuticos), tópicos o sistémicos, activados por la radiación solar.
Clasificación de las fotodermatosis
| Idiopáticas (o inmunológicamente mediadas) |
| Erupción polimorfa lumínica |
| Hidroa vacciniforme |
| Urticaria solar |
| Dermatitis crónica actínica |
| Prurigo actínico |
| Fotodermatosis inducida por agentes químicos |
| Exógenas |
| Fototoxicidad |
| Fotoalergia |
| Endógenas |
| Porfirias cutáneas |
| Defectos en la reparación del DNA |
| Xeroderma pigmentoso |
| Síndrome de Cokayne |
| Síndrome de Bloom |
| Síndrome de Rothmund-Thompson |
| Síndrome de Kindler |
| Tricotiodistrofia |
| Dermatosis fotoagravadas |
| Lupus eritematoso |
| Dermatomiositis |
| Rosácea |
| Psoriasis |
| Dermatitis seborreica |
| Dermatitis atópica |
| Penfigoide ampolloso |
| Pénfigo foliáceo |
| Enfermedad de Darier |
| Otras |
Se sabe que existen diferencias geográficas importantes en la incidencia de la mayoría de estas enfermedades y es necesario entender que el cuerpo central del conocimiento actual lo constituyen casi en exclusividad los trabajos en población caucásica y japonesa. Las más que posibles diferencias entre poblaciones con fototipos diferentes que habitan en distintas zonas geográficas invitan a contemplar un futuro de conocimiento fotobiológico más globalizado y a desarrollar un sistema de clasificación universalmente aceptado2. Un reciente estudio retrospectivo mostró que, en EE.UU., la erupción polimorfa lumínica es más prevalente en la población afroamericana que en la caucásica (un 67 frente a un 41%, con significación estadística)3. Esta prevalencia es mucho mayor que la observada en un estudio epidemiológico realizado en 6 países europeos desde el Mediterráneo hasta Escandinavia, un 18%, en el que las diferentes resultados pueden interpretarse como resultado de las distintas dosis de UV en relación con la localización geográfica, más que del fototipo cutáneo o la raza4. Más y mejores estudios epidemiológicos permitirán conocer con mayor detalle la influencia que las características pigmentarias poblacionales tienen en la incidencia y gravedad de estos procesos, así como, probablemente, reclasificar algunos de ellos, bien unificándolos bajo la misma terminología, bien caracterizando algunas enfermedades nuevas2. Sería deseable la implantación de registros de los posibles cambios geográficos en la incidencia y la prevalencia de las fotodermatosis, a modo de observatorio mundial.
El diagnóstico de las distintas fotodermatosis idiopáticas es fundamentalmente clínico. Cada enfermedad representa una respuesta patológica peculiar a la exposición lumínica. No existen pruebas diagnósticas específicas. Aunque los estudios histológicos y de laboratorio ayudan a descartar otros procesos fotoinducidos o fotoagravados, generalmente tienen escaso valor diagnóstico y pronóstico.
Los estudios fotobiológicos (que incluyen el fototest, la fotoprovocación y las pruebas de fotoparche) pueden ayudar a caracterizar cada uno de estos procesos mediante la determinación de: a) el espectro de acción de la radiación responsable, lo que es útil para determinar el pronóstico y para seleccionar un tratamiento desensibilizador con fototerapia; b) el umbral de sensibilidad a la luz (la fotosensibilidad), mediante la determinación de la dosis eritematosa mínima (DEM), la dosis fototóxica mínima (DFM), previa a la fototerapia tipo PUVA, y la dosis urticariana mínima (DUM), y c) los posibles agentes exógenos teóricamente responsables del inicio y el mantenimiento de la enfermedad, mediante la lectura e interpretación de las pruebas del fotoparche.
Para la realización de los estudios fotobiológicos se precisan equipos de fuentes de luz específicos con diferentes espectros lumínicos, con dosimetrías conocidas y adecuadamente calibradas5. No existe un consenso ni hay protocolos diagnósticos universalmente aceptados. Los parámetros mensurables (como la pigmentación, el eritema o los distintos «grados» de habón) y, a menudo, la interpretación de los resultados obedece a criterios subjetivos y a la experiencia de cada dermatólogo. Para interpretar cada prueba es necesario definir previamente los parámetros de lectura de los resultados, y los medios para realizarlas (visuales o artificiales).
Es muy difícil controlar todas las variables durante estas pruebas, dado el papel tan relevante de ciertas características idiosincrásicas como el tipo y el estado de pigmentación de cada paciente. Además, la utilidad clínica de estas pruebas a menudo está supeditada a las características climatológicas y estacionales que disfruta cada paciente, así como a sus hábitos de exposición solar (ocupacional o recreativa) o al uso de medidas de fotoprotección.
Fisiopatología de las fotodermatosis idiopáticasErupción polimorfa lumínicaEs un cuadro caracterizado por un polimorfismo clínico (pápulas, vesículas, lesiones eccematosas, erosiones y costras) y por la aparición retardada de los síntomas tras la exposición solar6. Esta última característica ha hecho que fuera considerado durante mucho tiempo un tipo de hipersensibilidad retardada a un autoantígeno fotoinducido.
Algunos estudios han mostrado que la inducción de la sensibilización y la respuesta efectora al dinitroclorobenceno son menos suprimidas por UV en estos pacientes que en los controles7,8. Posteriores investigaciones, sin embargo, no han podido confirmar diferencias significativas en la fase de respuesta tras la estimulación solar entre pacientes con EPL y personas sanas6.
Aunque se desconoce por completo el autoalérgeno responsable del EPL, cada vez se conocen mejor los mecanismos patogénicos de esta enfermedad, que incluyen respuestas anormales a la luz UV de las células de Langerhans (CL), los neutrófilos y los macrófagos. A lo largo de los últimos años, varios estudios in vivo en humanos han probado que la radiación UV induce una reducción del número de CL dérmicas y epidérmicas, en gran medida debida a una mayor migración linfática de estas células9–12. Sin embargo, en los pacientes con EPL, las CL persisten de forma anormal en la epidermis tras la exposición a UV. Además, hay una reducción significativa del número de células CD11b+ (macrófagos y neutrófilos), principales secretoras de la citocina inmunosupresora IL-109, y del número de linfocitos TH210,11. El flujo de neutrófilos es, en los pacientes con EPL, mucho menor que el esperable en personas sanas tras la exposición a UV11. La inducción de fototolerancia con UVB en estos pacientes revierte significativamente estas respuestas anormales en el número, la migración y la funcionalidad de estas células inflamatorias12.
Estos hallazgos apoyan la teoría actual que explica la EPL como el resultado de un fallo en la inmunosupresión normal inducida por la radiación UV. Un desequilibrio entre los efectos inmunosupresores y estimuladores de la radiación UV a favor de estos últimos permitiría reacciones de hipersensibilidad retardadas inducidas por neoalérgenos endógenos fotoinducidos. El menor efecto inmunosupresor que las radiaciones UV ocasionan en estos pacientes podría explicar también el menor riesgo de cáncer de piel que aparentemente presentan estos pacientes, una vez que estos resultados se ajustan al fototipo y a la cantidad de radiación solar recibida13.
Queda por caracterizar el cromóforo y el antígeno endógeno responsable de la EPL, aunque posiblemente se trata de una diversidad de ellos. Se ha sugerido la posibilidad de que se trate de proteínas del tipo heat-shock14.
Hidroa vacciniformeSe desconocen tanto los cromóforos como la patogenia de la hidroa vacciniforme (HV)6. Algunos casos se han asociado a infección latente por el virus de Epstein-Barr y pueden evolucionar a un linfoma. Es obligado un estudio de porfirinas eritrocitarias para descartar una protoporfiria eritropoyética (PPE).
Dadas las similitudes histológicas con la EPL, algunos autores consideran que se trata de una variante cicatricial de aparición más temprana y que mejora e incluso se resuelve durante la adolescencia. Por tanto, un tipo singular de reacción de hipersensibilidad retardada a algún autoalérgeno fotoinducido.
Urticaria solarLa urticaria solar (US) es un tipo de urticaria física muy infrecuente desencadenada por la luz del sol, de curso crónico y a menudo de difícil control15. La aparición del habón suele ser inmediata después de la exposición al sol, en piel generalmente no fotoexpuesta (cuello, escote y dorso de pies). La cara y el dorso de las manos desarrollan fototoadaptación o tolerancia solar (skin hardening).
Aunque la mayor parte de los casos son idiopáticos, pueden asociarse a otros procesos de origen inmunológico como la dermatitis atópica, la EPL (hasta en el 23% casos) o la dermatitis crónica actínica (DCA) (en el 3%)16. Se han descrito casos inducidos por medicaciones tópicas (como las breas) o sistémicas (benoxaprofeno, clorpromacina, progesterona)17. Ocasionalmente coexiste con otros tipos de urticaria, física o crónica17.
Según la hipótesis más aceptada, la luz absorbida por uno o más cromóforos de la piel o el suero de estos pacientes daría lugar a un fotoproducto con capacidad de fijación a la IgE y a la membrana del mastocito, con la consiguiente degranulación, lo que ocasionaría una respuesta inflamatoria de tipo habonoso. La posible transferencia de dicha respuesta mediante la inyección de suero irradiado de pacientes con US a personas sanas confirma el mecanismo patogénico inmunológico-alérgico de tipo i18. Los cromóforos son en la actualidad desconocidos, y pueden ser diferentes en cada paciente17. La presencia de un fotoproducto circulante puede evaluarse mediante la inyección subcutánea de suero autólogo previamente radiado con el espectro de acción a una dosis igual o superior a la de la fotoprovocación19, y podría tener valor a la hora de seleccionar ciertos tratamientos (como la plasmaféresis, la fotoféresis o las inmunoglobulinas intravenosas policlonales).
Desde el punto de vista fisiopatogénico existen 2 tipos de US20. El tipo 1 está producido por una IgE normal contra un fotoalérgeno específico anormal producido exclusivamente en pacientes con US, y puede o no transferirse pasivamente desde un paciente enfermo hasta uno sano. El tipo 2 es una hipersensibilidad mediada por una IgE anormal contra un fotoalérgeno no específico de pacientes con US y en el que la transferencia pasiva es siempre positiva. Esta clasificación fisiopatogénica tiene, sin embargo, escaso valor práctico, pues la prueba diagnóstica diferencial, la prueba de transferencia pasiva, se ha abandonado por los riesgos de infección que conlleva.
Dermatitis crónica actínicaLa DCA es una fotodermatosis infrecuente que incluye diversas entidades previamente descritas como reticuloide actínico, eccema fotosensible, dermatitis fotosensible o reacción persistente a la luz21. Se trata de una forma adquirida de eccema inducido por la radiación UV (muy raramente por la luz visible), propio de pacientes de edad avanzada con una historia de exposición solar importante. Tiene tendencia a persistir y progresar a lo largo de la vida del paciente. Muchos de ellos tienen una historia desde la juventud de eccema crónico, atópico, seborreico, de contacto o aerotransportado.
Los 3 criterios diagnósticos principales son: 1) una erupción eccematosa persistente inicialmente en áreas fotoexpuestas que luego puede extenderse a zonas cubiertas; 2) hallazgos histológicos de eccema con o sin cambios linfomatoides, y 3) una reducción del umbral de sensibilidad a la radiación UV (DEM disminuida o reacciones anómalas a la UVA)21.
Los hallazgos histológicos más característicos son la dermatitis espongiótica eccematosa y el infiltrado linfocitario perivascular superficial con tendencia al epidermotropismo, compuesto inicialmente por linfocitos T CD4+ y CD8+. En las fases más avanzadas hay un claro predominio de CD8+ dérmicos. Tras irradiar la piel de estos pacientes con UV, y a diferencia de lo que ocurre tras irradiar la piel de sujetos normales, se observa una activación de los queratinocitos (que expresan complejo mayor de histocompatibilidad [HLA-II]), de las CL y de los linfocitos T. Estos además presentan una tendencia al epidermotropismo como consecuencia del patrón específico de las moléculas de adhesión (expresión prolongada de E-selectina, ICAM-1 y VCAM-1)22. Todos estos hallazgos, que no suelen encontrarse tras radiar con UV la piel sana, llevan a pensar que se trata de un tipo de hipersensibilidad retardada similar a la dermatitis alérgica de contacto.
A pesar de que algunos pacientes presentan sensibilización a varios alérgenos demostrados en las pruebas epicutáneas (antibacterianos tópicos, fragancias, agentes blanqueadores, etc.), varios autores piensan hoy que la DCA es el resultado de una reacción primera contra un fotoalérgeno endógeno más que contra un agente externo21,23. La acción directa de la UV ocasionaría un cambio estructural en el cromóforo (presumiblemente el ADN o sus fragmentos) que iniciaría la fase efectora del eccema, o bien produciría cambios oxidativos en algunas proteínas normales de la piel que actuarían entonces como alérgenos endógenos21. Esto último se ha demostrado in vitro mediante la fotooxidación del componente de histidina de la albúmina23.
El daño solar crónico de la piel del anciano puede conllevar una reducción de la inmunosupresión inducida por UV (de forma similar a lo que pasa en la EPL) y una disminución en la capacidad para la eliminación antigénica de la piel, lo cual podría explicar la predisposición de estos pacientes a desarrollar procesos eccematosos crónicos. La perpetuación de estos eventos llevaría a su vez a predisponer a estos pacientes al desarrollo de una dermatitis de contacto autoalérgica.
Prurigo actínicoEl prurigo actínico (PA) es una fotodermatosis especialmente prevalente entre la población mestiza latinoamericana y algunas tribus amerindias de Norteamérica (Inuits, Navajos y otras tribus) y Mesoamérica (México, Centroamérica y el norte de Sudamérica)24.
Inicialmente se la consideró como una variante de la EPL. Sin embargo, la aparición en los primeros años de la vida y algunos datos clínicos permiten sospechar que se trata de 2 procesos diferentes24,25. Predomina la afectación facial, sobre todo labial, y es muy frecuente la coexistencia de una característica conjuntivitis crónica. Las lesiones son de morfología característicamente liquenoide, y por lo general faltan las vesículas. Los datos histológicos más relevantes son el denso infiltrado en la dermis superficial y la presencia de folículos linfoides. Además, las lesiones son más persistentes y no siempre desaparecen en invierno25. La excelente respuesta a la talidomida, que además puede modificar la respuesta inmunitaria en estos pacientes, es otro dato diferencial con la EPL.
Es recomendable realizar un estudio de autoinmunidad en estos pacientes para descartar un lupus eritematoso.
Estudios de proliferación in vitro han mostrado una reactividad autoinmunitaria26. En el infiltrado linfoide hay un predominio de linfocitos CD4 con secreción de IL2. Los queratinocitos muestran signos de inmunoactivación y producción de TNF-α. Existe una clara relación entre la prevalencia de la enfermedad y determinados antígenos del HLA en cada una de las zonas geográficas27. Incluso se ha señalado que algunos de los péptidos que conforman el HLA podrían intervenir en la patogenia del PA.
Todos estos hallazgos conducen a pensar que se trata de un proceso inflamatorio desencadenado por la radiación UV, que ocasionaría la producción queratinocítica de TNF-α y la consiguiente respuesta inflamatoria en individuos genéticamente predispuestos.
Fotodermatosis exógenasSon más frecuentes en pacientes de edad avanzada y en polimedicados28. Existen 2 patrones clínicos que responden a mecanismos patogénicos diferentes: la fototoxicidad y la fotoalergia (tabla 2).
Diagnóstico diferencial entre la fototoxicidad y la fotoalergia
| Fototoxicidad | Fotoalergia | |
| Prevalencia | Alta, más en ancianos | Baja |
| Primera exposición | Reacción | No reacción |
| Latencia | Minutos, horas | 24-48 h |
| Dosis requerida | Grande | Pequeña |
| Espectro de acción | Estrecho, UVA 1 | Amplio, incluyendo UVA |
| Clínica | Eritema solar | Lesiones eccematosas |
| Síntomas | Ardor, dolor | Picor |
| Tendencia a extenderse | No | Sí |
| Patogenia | Daño celular directo | Hipersensibilidad retardada |
| Reacciones cruzadas | No | Frecuentemente |
| Histología | Queratinocitos necróticos | Dermatitis espongiótica |
La fototoxicidad es la forma más frecuente y no precisa un período de sensibilización, por lo que puede aparecer en cualquier persona ante la primera exposición, dependiendo de la dosis del agente exógeno y la dosis de radiación UV. Clínicamente son lesiones muy similares a la quemadura solar, muy intensas, ante exposiciones al sol generalmente insuficientes para producirlas. Es el resultado del daño celular de la piel por la inducción de agentes tóxicos fotoactivados, algunos de los cuales actúan mediante un mecanismo fotodinámico generando especies reactivas de oxígeno (como las breas, los AINE, la furosemida o la clorpromacina). Otros posibles mecanismos de daño celular son la generación de fotoproductos estables (como en el caso de las tetraciclinas o las quinolonas), la formación de fotoaductos (como sucede con los psoralenos en la PUVA) o la producción o liberación directa de mediadores de la inflamación (como se ha mostrado con la demeclociclina o la clorpromacina).
La fotoalergia es mucho más rara y se produce casi exclusivamente por la exposición tópica a medicamentos o cosméticos. Clínicamente se caracteriza por una reacción eccematosa aguda, muy pruriginosa, en las zonas expuestas a una cantidad generalmente pequeña de luz tras la aplicación del agente responsable. El mecanismo es el mismo que el del eccema de contacto, solo que en este caso el alérgeno es un fotoproducto. Precisa un período de sensibilización de 7-10 días tras la primera exposición.
Consideraciones técnicas de los estudios fotobiológicosLos estudios fotobiológicos agrupan al conjunto de pruebas realizadas en la piel del paciente con la finalidad de determinar tanto el grado de sensibilidad a la luz como las bandas del espectro electromagnético responsables de la aparición o la inhibición de las diferentes respuestas cutáneas anómalas.
Espectro electromagnético. Medición de la luzPara poder entender las unidades en las que se mide la radiación electromagnética hay que tener en cuenta diversas premisas. En primer lugar, hay que diferenciar el ámbito puramente físico, el cual es independiente de la percepción humana, del dependiente de dicha percepción, ya que el objeto receptor es el sentido de la vista y es aquí donde aparecen los aspectos de brillo y color.
Basándonos en el aspecto puramente físico de la medición de la radiación, se diferencian 2 niveles: 1) el nivel de unidades energéticas asociadas a fotones, y 2) las unidades cuánticas, o de número de fotones que interaccionan con el receptor. La cantidad de radiación se puede medir por métodos físicos mediante el uso de radiómetros que miden la cantidad de energía, o la cantidad de fotones en cuestión y en un tiempo determinado.
El control de los equipos de iluminación pasa por conocer la distribución de la radiación sobre el espectro electromagnético de cada una de estas fuentes. La radiación UV corresponde a la parte no ionizante del espectro electromagnético con límites entre 100 y 400nm.
La clasificación de las bandas espectrales tanto en el campo de la medicina como el de la biología, ha establecido clásicamente los límites entre la radiación UVB y UVA en 320nm, adaptándose dichos límites al límite entre las longitudes de ondas que producen eritema (por debajo de 320nm). Más recientemente se han propuesto los límites para distinguir el UVA-1 (> 340-400nm) y el UVA-2 (320-340nm). No obstante, La Comisión Internacional de la Iluminación (CIE, Commission Internationale de l’Eclairage) ha normalizado los límites para cada una de las bandas espectrales de la radiación UV, visible e infrarroja (CIE, 1987) (tabla 3).
Regiones espectrales desde el ultravioleta al infrarrojo según la CIE
| Nombre | Ámbito de longitud de onda |
| UVC | 100 a 280 nm |
| UVB | 280 a 315 nm |
| UVA | 315 a 400 nm |
| VIS | Aprox. 360-400 a 760-800 nm |
| IRA (cercano) | 780 a 1.400 nm |
| IRB | 1,4 a 3 μm |
| IRC (lejano) | 3 μm a 1 mm |
Nota: Como se puede observar, el ámbito espectral de la radiación visible no tiene límites precisos ya que estos límites varían de persona a persona.
- -
Se denomina radiancia a la potencia o flujo radiante como la cantidad de energía electromagnética que emite un radiador por unidad de tiempo. Se mide en vatios (W = J · s-).
- -
En el caso de la energía incidente sobre una superficie receptora (como por ejemplo la piel), se denomina irradiancia o densidad de radiación a la potencia incidente por unidad de superficie. Se expresa en este caso como W · m-2, o más comúnmente utilizado en dermatología, mW · cm-2 o mJ · s-1 · cm-2.
- -
El término dosis de radiación es el factor acumulativo de la irradiancia a lo largo de un periodo de tiempo. Nos permite manejar la exposición del paciente a la fuente de iluminación y la determinación del umbral mínimo de energía incidente que produce la lesión. Se expresa en términos de J · cm-2.
Dosis = irradiancia (mJ/s · cm) × tiempo de exposición (s) = mJ/cm2
- -
Cuando se maneja el nivel cuántico en la medición de la radiación electromagnética, la cantidad de luz se mide como el número de cuantos (fotones) por unidad de superficie (m-2) y unidad de tiempo (s-1). El término se denomina tasa o densidad de flujo electrónico o fotónico.
Además de los conceptos puramente físicos que definen la medida de la luz, en fotobiología cutánea hay que manejar términos de radiación dentro del ámbito biológico, debido a que la piel es el órgano receptor de la energía electromagnética incidente. No todas las radiaciones van a tener la misma propiedad de penetración en la piel. Por tanto, solo es eficaz la radiación que es absorbida en el tejido.
La cantidad de radiación absorbida en la piel por cada longitud de onda incidente que es eficaz para producir un efecto biológico (a través de una reacción fotoquímica) es el denominado espectro de acción.
Las especies moleculares presentes en la piel capaces de absorber el espectro de acción y dar lugar a las reacciones fotoquímicas que constituyen el efecto biológico de la luz son los denominados cromóforos. Uno de los objetivos básicos de la fotobiología cutánea es la identificación del cromóforo responsable de cualquier reacción biológica en la piel. No obstante, la mayoría de los cromóforos responsables de las fotodermatosis idiopáticas son hoy desconocidos, dada la complejidad tisular, el solapamiento de cromóforos y el cambio en las características fisicoquímicas de estos por la interacción con otras moléculas.
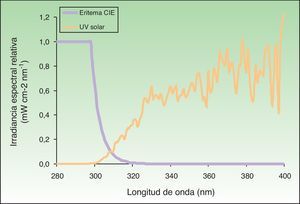
La importancia principal de conocer el espectro de acción para un determinado efecto biológico es el cálculo de la irradiancia biológica efectiva, o la ponderación de la irradiancia emitida para cada una de las longitudes de onda del espectro de una fuente de iluminación por el potencial efecto biológico que produce dicha longitud de onda. Esto permite, además, conocer la cantidad o fracción efectiva para dicho efecto, lo que al multiplicarlo por el tiempo de exposición va a resultar en la dosis biológica efectiva. En el caso del eritema, el espectro de acción fue determinado en 198728. En la figura 1 se representa, en unidades relativas, el espectro de radiación UV solar incidente en la corteza terrestre y el espectro de acción eritemático.
Espectro solar y espectro eritemático.
Sólo una peque¿na parte del espectro electromagnético solar es responsable de la aparición de eritema. Al multiplicar la energía solar incidente en cada longitud de onda por el potencial eritemático de ésta basado en el espectro de acción (en la figura se muestra como unidades relativas cuyo valor máximo es 1) se obtiene la irradiancia biológica efectiva para el eritema (casi el 100% debido a UVB).
Cuando la piel se expone a la fuente de radiación por un tiempo determinado, la cantidad de radiación recibida corregida por el efecto eritemático corresponde a la dosis de radiación eritemática. El término dosis eritemática (ó eritematosa) mínima (DEM) corresponde a la dosis de radiación emitida por una fuente de iluminación, ponderada por el efecto eritemático de cada una de las longitudes de onda capaz de producir un enrojecimiento en la piel perceptible y uniforme, con bordes claramente demarcados. A partir de los resultados, y conociendo la irradiancia de la radiación emitida por la fuente de iluminación y la irradiancia efectiva para la producción de eritema, se calcula la DEM para cada fuente de iluminación (fig. 1).
Fototipos cutáneosLa piel posee una constitución física que le confiere determinadas propiedades ópticas y por consiguiente, tanto un cambio en la estructura física (engrosamiento de capa córnea), como una mayor presencia de moléculas que absorban la radiación (cromóforos como la melanina) puede ocasionar un cambio en los valores de la DEM29. Así, además de las diferencias interindividuales de la fotosensibilidad dependientes de las características étnicas de la piel o del grado de bronceado, existen diferencias de hasta 5 veces la DEM entre las distintas partes de la piel de una misma persona30.
Para intentar estandarizar el tipo de respuesta de la piel a la luz, en 1988 se establecieron los denominados fototipos cutáneos de Fitzpatrick31 y, aunque con las limitaciones anteriormente, expuestas, se establecieron unas DEM estándar para cada fototipo (tabla 4). Sin embargo, y dadas las diferencias inter e intraindividuales de fotosensibilidad, no existe una correlación unívoca lineal entre el fototipo y la DEM, aunque en esta no parecen influir ni el sexo ni la edad32.
Características fenotípicas y correspondencia con la dosis eritematosa mínima (DEM) de los diferentes fototipos cutáneos
| Fototipo | Bronceado | Quemadura | Color de pelo | Color de ojos | DEM (mJ/cm2) |
| I | Nunca | Siempre | Pelirrojo | Azul | 15-30 |
| II | A veces | Frecuente | Rubio | Azul/Verde | 25-40 |
| III | Moderado | Moderadamente | Castaño | Gris/marrón | 30-50 |
| IV | Siempre | Raramente | Negro | Marrón/negro | 40-60 |
| V | Siempre | Raramente | Negro | Negro | 60-90 |
| VI | Siempre | Nunca | Negro | Negro | 90-150 |
Para realizar los estudios fotobiológicos es necesario un equipo específico. En primer lugar, las fuentes de luz que abarquen diferentes espectros de emisión. Segundo, para el control de emisión del equipamiento son necesarios los equipos de medida de radiación que nos permitan el calibrado de dichas fuentes y, una vez conocidos el espectro y la potencia de emisión, definir las dosis de fotoprovocación para el diagnóstico. Finalmente, para el correcto funcionamiento de una unidad de fotodiagnóstico es necesario que el personal posea un conocimiento específico sobre el manejo de la radiación electromagnética, los principios de funcionamiento y la terminología empleada en la medición y el manejo de dicha radiación.
Fuentes de luzLa naturaleza de la radiación emitida depende de la estructura física del radiador o fuente de iluminación. Atendiendo a estos criterios, se pueden clasificar las fuentes de radiación en 3 grupos.
Radiadores térmicos o lámparas incandescentesSon elementos sólidos (como el filamento de tungsteno de una bombilla) que, sometidos a un calentamiento de unos 2.800°C, generan un espectro de emisión continuo. Un ejemplo sería la lámpara de un proyector de diapositivas que emite un espectro continuo en la banda visible, utilizado en el análisis de las bandas espectrales responsables de las urticarias solares.
Lámparas de descargaCuando se hace pasar una corriente eléctrica a través de un gas sometido a una alta presión, se produce una excitación molecular del gas y el retorno al estado basal desprende energía en forma de radiación electromagnética. Dependiendo del tipo de gas (xenón, neón, etc.), el espectro de emisión será diferente, y la emisión corresponderá a picos o bandas características de cada gas. En este grupo se incluyen la mayoría de fuentes de radiación de espectro continuo UV-visible. Tipos de lámparas de descarga usadas en el fotodiagnóstico de UV-visible son las lámparas de los simuladores solares, las de los monocromadores o las de UVA de alta presión. La diferencia entre estas fuentes de iluminación radica en el espectro de emisión.
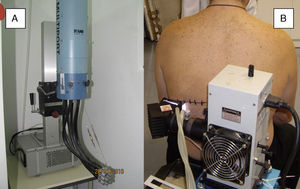
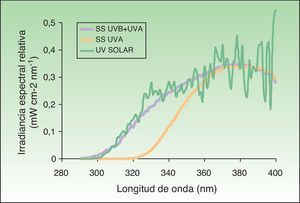
Simulador solarConsta de una fuente de luz (generalmente una lámpara de xenón), un colimador y un sistema óptico que permite seleccionar la luz emitida mediante un sistema de filtros internos (para eliminar UVC y LV) y externos (para eliminar UVB a voluntad) (fig. 2). Reproduce el espectro de la radiación solar a nivel del suelo (fig. 3). Cuando existe una combinación de varios cromóforos la selección de bandas de corte en el simulador solar nos permite una mejor selección de las bandas espectrales responsables de dicha fotodermatosis. El mayor problema es que sufren cambios en la emisión espectral con el tiempo y necesitan ser calibrados periódicamente con espectroradiómetros.
Simuladores solares.
A-Simulador solar multipuerto. Emisión de una dosis creciente de radiación solar simulada recogida por una fibra óptica en cada uno de los seis puertos para producir eritema de forma paralela (cada puerto de salida emite una intensidad diferente controlada). B-Simulador solar. El sistema de filtros y foco recoge toda la radiación emitida por la lámpara en un punto (1 cm de diámetro) y las dosis crecientes se obtienen aumentando el tiempo de exposición en cada uno de los puntos.
Es una fuente de luz continua (heterocrómica) con un sistema de dispersión (retículo o prisma) que produce una descomposición espectral de la luz en sus diferentes bandas muy estrechas del espectro, cuyo ancho puede ser seleccionado por el usuario mediante el uso de filtros de corte. Permite aislar bandas espectrales específicas para determinar cuáles son las responsables de una patología (o de la inhibición de esta). Son muy útiles para determinar el espectro de acción en las distintas fotodermatosis.
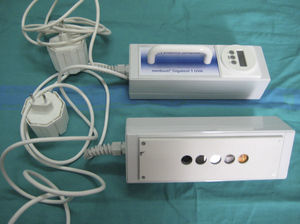
Lámparas fluorescentesDisponen de un gas metálico (generalmente vapor de mercurio) sometido a baja presión, que al paso de corriente produce radiación ultravioleta de onda corta, la cual al incidir con una capa sólida (el fósforo del casquillo del fluorescente) se excita. La vuelta al estado basal se realiza emitiendo radiación lumínica por fluorescencia de onda más larga (UVB, UVA o visible). Las lámparas de UV fluorescentes son las comúnmente utilizadas tanto para realizar la prueba del fotoparche como para la fototerapia local o corporal total. Existen equipos portátiles que son útiles para medir MED UVB y UVA y para explorar el espectro de acción y la DUM de las urticarias solares (fig. 4).
Lámpara fluorescente de mano portátil.
Lámpara de espectro continuo (PLS-special) de 9 watios con filtro integrado para el espectro de emisión, con 5 spots de 5mm que emiten el 7%-34%-63%-85%-100% del espectro en UVB o en UVA (Gigatest, Medisun, Francia) y, por tanto, determinar la dosis de exposición (en j/cm2) según el tiempo de contacto cutáneo.
Es el equipamiento necesario para la caracterización tanto del espectro de emisión de una fuente de iluminación como de la cantidad de energía emitida por unidad de tiempo.
Radiómetros de banda anchaDisponen de un sensor constituido por una ventana semitransparente a las longitudes de onda que deseamos medir (como ejemplo la ventana UVB del espectro electromagnético), y por la cual los fotones de longitud de onda comprendida en esa ventana penetran hasta el detector, constituido por una placa fotovoltaica que detecta dichos fotones y los convierte en señal eléctrica (fig. 5). A partir de unos factores determinados por el fabricante, dicha señal es convertida en la señal lumínica de irradiancia (W m-2) o flujo fotónico (moles fotones m-2 s-1). Por tanto, la medida realizada por el radiómetro de banda ancha dará un resultado integrado para el total de la banda espectral que el detector sea capaz de medir.
EspectrorradiómetrosSon los equipos de medida de radiación lumínica capaces de separar las distintas longitudes de onda y conseguir el espectro de emisión de cualquier fuente de iluminación a intervalos de nanómetros. Estos equipos disponen de monocromadores que son fuentes de luz con un sistema de dispersión (prismas) que permite separarla en intervalos muy pequeños de longitudes de onda.
Calibración y mantenimiento de los equiposCada fuente de iluminación ha de ser caracterizada espectralmente (mediante radio o espectrorradiometría) y es un requisito fundamental conocer la irradiancia por cada longitud de onda, principalmente para la caracterización posterior del potencial de efecto biológico que vayamos a medir. Normalmente, las casas comerciales suministran la distribución espectral de cada fuente de iluminación.
Es un requisito indispensable disponer de radiómetros que midan la radiación (UVB y UVA) emitida por cada fuente de iluminación para el control de emisión y la dosimetría a emplear para cada paciente. Lo ideal sería poder realizar mediciones del equipamiento justo antes de la irradiación al paciente para garantizar la dosimetría prescrita. Esto es debido a que determinadas fuentes de iluminación, tipo simulador solar o monocromador, disponen de complejos sistemas de separación espectral y es fácil la pérdida de la calibración. En el caso del uso de fuentes de iluminación más sencillas, tipo lámparas fluorescentes, la emisión de la luz es más homogénea en el tiempo y en este caso la calibración se recomienda realizarla mensualmente, ya que la vida de la lámpara afecta significativamente tanto a la potencia de emisión, como a la calidad espectral.
La ventaja de los radiómetros es su manejabilidad, la rapidez de medida y su precio. La desventaja es la necesidad de calibrarlos frente a las medidas espectrorradiométricas, para cada una de las diferentes fuentes de iluminación que utilicemos en el laboratorio (CIE, 1983), al menos con periodicidad anual.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales
Confidencialidad de datosLos autores declaran que en este artículo no aparecen datos de pacientes
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.