INTRODUCCION
El virus herpes humano tipo 8 (VHH-8) fue descubierto en 1994 y clasificado en la familia de gammaherpesvirus junto con el virus de Epstein-Barr (VEB) en virtud de su tropismo por el tejido linfoide y su potencial oncogénico. Se ha aislado universalmente en todas las variantes de sarcoma de Kaposi. Posteriormente se ha relacionado también con la enfermedad de Castleman multicéntrica y el linfoma primario de cavidades. Estas dos raras entidades son más frecuentes en la población infectada por el virus de la inmunodeficiencia humana (VIH-positiva) 1.
Se describe el caso de un paciente no infectado por el VIH (VIH-negativo) que desarrolló sucesivamente un sarcoma de Kaposi y una enfermedad de Castleman multicéntrica. Este paciente respondió satisfactoriamente al tratamiento combinado de CHOP (ciclofosfamida, hidroxidaunomicina, vincristina, prednisona) y rituximab, fármaco que se ha utilizado recientemente en la enfermedad de Castleman con respuestas muy satisfactorias. Se destaca que la coincidencia de dos enfermedades relacionadas con la infección por el VHH-8 en un paciente VIH-negativo es un hecho excepcional.
DESCRIPCION DEL CASO
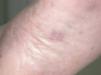
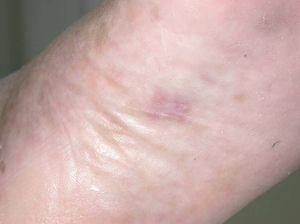
Se presenta el caso de un paciente varón de 68 años de edad VIH-negativo con antecedentes personales de hepatopatía crónica de origen enólico, hernias discales y sarcoma de Kaposi en miembros superiores e inferiores de un año de evolución en tratamiento con crioterapia (figs. 1-3). El paciente refería astenia, anorexia y pérdida de peso de dos meses de evolución detectándose a la exploración adenopatías laterocervicales, axilares e inguinales.
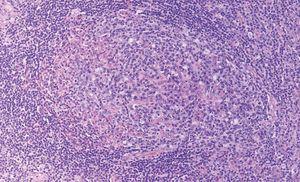
Fig. 1.--Placa eritematoviolácea situada en arco plantar que corresponde a una lesión de sarcoma de Kaposi clásico. Se aprecian máculas parduscas en los márgenes laterales del pie correspondientes a lesiones residuales de sarcoma de Kaposi. El paciente presentaba placas y nódulos similares en dorso de manos y antebrazos.
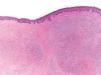
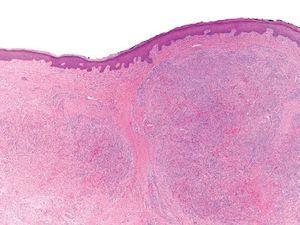
Fig. 2.--Imagen correspondiente a la biopsia de una lesión de sarcoma de Kaposi situada en dorso de mano donde se aprecia a pequeño aumento una proliferación nodular bien delimitada ocupando casi todo el espesor de la dermis.
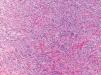
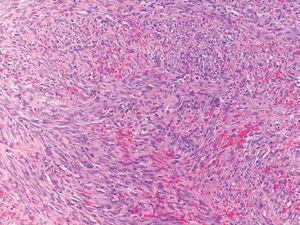
Fig. 3.--Biopsia de lesión de sarcoma de Kaposi. A mayor aumento se observan abundantes células fusiformes agrupadas en fascículos entrelazados con eritrocitos salpicados en el intersticio.
Una tomografía axial computarizada (TAC) toracoabdominopélvica confirmó la presencia de múltiples adenopatías de hasta 2 cm de diámetro en regiones axilares, mediastínicas, abdominales periaórticas, interaortocava y retrocava, ilíacas e inguinales bilaterales. Se realizó biopsia de un ganglio cervical y el estudio histopatológico mostró una arquitectura ganglionar preservada con folículos linfoides de centros germinales reactivos y manto bien desarrollado. En el espacio interfolicular se apreciaron masas de células plasmáticas de apariencia madura y estructuras vasculares de endotelio prominente que penetraban en el interior de los folículos. La pared de estas estructuras vasculares aparecía reforzada por un material hialino (figs. 4 y 5). De acuerdo con estos hallazgos histopatológicos se estableció el diagnóstico de enfermedad de Castleman subtipo de células plasmáticas. La serología para VHH-8 fue positiva (título 1/640, inmunofluorescencia indirecta). La infección por VHH-8 se confirmó mediante reacción en cadena de la polimerasa (PCR) de sangre periférica. Esta última técnica se realizó también para otros virus linfotropos (citomegalovirus, virus herpes humano 6, virus herpes humano 7, VEB) siendo negativa en todos los casos. Dada la alta frecuencia con que la enfermedad de Castleman multicéntrica y el sarcoma de Kaposi se asocian a la infección por VIH se solicitó una nueva serología (anticuerpos VIH 1/2) que resultó negativa.
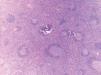
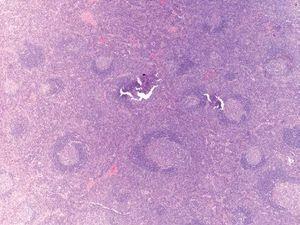
Fig. 4.--Biopsia ganglionar que muestra abundantes folículos con centros germinales de tamaño heterogéneo rodeados por un manguito de linfocitos pequeños distribuidos en capas concéntricas.
Fig. 5.--Biopsia ganglionar en la que se aprecia a mayor aumento la distribución en capas concéntricas de los linfocitos en la periferia de los folículos (folículos «en diana»), la presencia de arteriolas de pared hialinizada penetrando en el centro germinal y abundantes células plasmáticas en el espacio perifolicular, hallazgos característicos de la enfermedad de Castleman de células plasmáticas.
El análisis de sangre reveló las siguientes anomalías: velocidad de sedimentación globular de 68 mm en la primera hora; GGT: 146 UI/l; proteinograma: IgG: 3.120 mg/dl y IgA: 414 mg/dl; inmunofijación eléctrica: aumento policlonal de IgG e IgA; anticuerpos antinucleares (ANA) homogéneo al 1/160 (anti-ADNn negativo, ENA totales negativos).
Se instauró tratamiento con 8 ciclos de CHOP y rituximab, obteniéndose una remisión de las adenopatías y una resolución del síndrome general sin que haya podido observarse por el momento una extensión del sarcoma de Kaposi. Una TAC cervicotoracoabdominopélvica realizada 10 meses después de finalizado el tratamiento confirmó la ausencia de adenopatías.
DISCUSION
La enfermedad de Castleman multicéntrica es un raro trastorno linfoproliferativo secundario a la infección por VHH-8 que generalmente afecta a pacientes VIH-positivos.
Se han descrito dos formas clínicas de enfermedad de Castleman: la unicéntrica, variante de buen pronóstico que suele afectar a pacientes jóvenes y se manifiesta frecuentemente como una masa localizada en mediastino con buena respuesta al tratamiento quirúrgico; y la variante multicéntrica que se manifiesta con linfadenopatías generalizadas y afectación sistémica (fiebre, astenia, anorexia, pérdida de peso, anemia, hipergammaglobulinemia y aumento de la velocidad de sedimentación).
Se han definido tres variantes histopatológicas de enfermedad de Castleman: la variante hialinovascular, la de células plasmáticas y la mixta 2. La primera es la más frecuente y habitualmente se asocia a la forma clínica de enfermedad de Castleman unicéntrica. Se considera que las variantes de células plasmáticas o mixta son manifestación de la infección por el VHH-8 y habitualmente afectan a pacientes VIH-positivos en forma de enfermedad multicéntrica. El VHH-8 se identifica universalmente en todos los pacientes con enfermedad de Castleman multicéntrica VIH-positivos y sólo en el 40 % de los pacientes con enfermedad de Castleman multicéntrica VIH-negativos 3.
Se considera que la producción por el VHH-8 de una proteína viral similar a la interleucina-6 (vIl-6) está involucrada en la patogenia de la enfermedad de Castleman multicéntrica. La función de esta citocina consiste en promover la supervivencia y la proliferación de los linfocitos B. Se cree que la anemia hemolítica autoinmune y la gammapatía policlonal que con frecuencia se asocian a la enfermedad de Castleman multicéntrica probablemente son consecuencia de una expansión linfocítica policlonal debida a la Il-6 4.
La mayoría de los pacientes afectados por enfermedad de Castleman multicéntrica fallecen por infección fulminante, progresión de la enfermedad o neoplasias asociadas, particularmente neoplasias hematológicas. Se ha comprobado que la mayoría de los casos de enfermedad de Castleman que evolucionan a linfoma presentan linfomas no hodgkinianos de extirpe B, fundamentalmente linfomas del manto 5.
Se han utilizado diversas alternativas de tratamiento en la enfermedad de Castleman multicéntrica (esteroides, quimioterápicos vinblastina, etopósido, clorambucil, CHOP, CVAD, melfalán, antivirales ganciclovir, foscarnet, cidofovir, anticuerpos anti-Il-6) con resultados variables. El uso de rituximab, anticuerpo monoclonal quimérico anti-CD 20, solo o combinado con quimioterápicos, ha demostrado ser muy eficaz en el tratamiento de la enfermedad de Castleman multicéntrica. Marcelin et al 6 muestran la respuesta a rituximab de cinco pacientes VIH-positivos con enfermedad de Castleman multicéntrica. La remisión completa de los síntomas se logró en tres de ellos. Dos de estos pacientes presentaban lesiones de sarcoma de Kaposi que se agravaron como consecuencia del tratamiento. Se ha publicado también el caso de un paciente VIH-positivo con enfermedad de Castleman multicéntrica refractaria al tratamiento con cidofovir, anticuerpos monoclonales anti-Il-6, antirretrovirales y quimioterapia combinada, que fue tratado con una sola dosis de rituximab y alcanzó la remisión completa de los síntomas y signos de la enfermedad. Esta respuesta se mantenía 14 meses después de la infusión 7.
Casquero et al 8 publicaron el caso de un paciente VIH-positivo con antecedentes de enfermedad de Castleman multicéntrica refractaria a tratamiento con doxorrubicina y corticoides a altas dosis que fue tratado con rituximab. La respuesta clínica fue evidente a la seguda infusión y 10 meses después de finalizado el tratamiento el paciente seguía en remisión completa. Sin embargo, presentaba también lesiones de sarcoma de Kaposi que se exacerbaron a las pocas semanas de instaurar el tratamiento.
A pesar de ser enfermedades con una etiología común, la enfermedad de Castleman multicéntrica y el sarcoma de Kaposi difieren radicalmente en la respuesta al tratamiento con terapia antirretroviral y con rituximab. La terapia antirretroviral de alta eficacia logra el control de las lesiones de Kaposi en pacientes VIH-positivos pero suele desencadenar un empeoramiento de la enfermedad de Castleman. Sin embargo, el rituximab, muy eficaz en el tratamiento de la enfermedad de Castleman multicéntrica, puede agravar las lesiones de sarcoma de Kaposi 6.
Clifford et al 9 han publicado el caso de un paciente VIH-negativo con sarcoma de Kaposi clásico que se exacerbó rápidamente como consecuencia del rituximab que recibió como tratamiento de una anemia hemolítica autoinmune.
Pese al riesgo de progresión del sarcoma de Kaposi, en el paciente del presente caso, se decidió utilizar un tratamiento combinado de CHOP y rituximab, de acuerdo con el protocolo diseñado para los linfomas de alto grado, por la grave afectación sistémica que presentaba y el mal pronóstico de la enfermedad, potencialmente fatal en muchos casos. A diferencia de otros casos publicados en los que se podía apreciar un empeoramiento del sarcoma de Kaposi en relación con el uso de rituximab, en el presente caso las lesiones de sarcoma de Kaposi permanecieron estables.
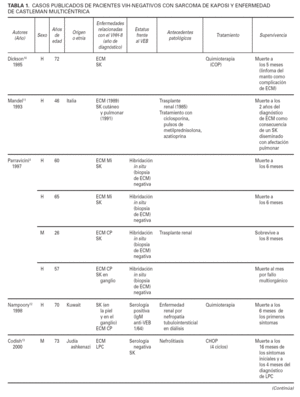
El VHH-8 se ha descrito asociado a todas las variantes de sarcoma de Kaposi (clásico, endémico, yatrógeno y epidémico), a la enfermedad de Castleman multicéntrica y al linfoma primario de cavidades. Aunque la mayoría de estos procesos se observan en el contexto del sida, se han descrito también aunque con mucha menor frecuencia en pacientes seronegativos para el VIH. La combinación de dos o tres enfermedades asociadas al VHH-8 en un paciente VIH-negativo es un hecho excepcional. La literatura recoge sólo 10 casos de pacientes VIH-negativos con sarcoma de Kaposi y enfermedad de Castleman multicéntrica. Dos de ellos presentaban también un linfoma primario de cavidades (tabla 1).
Al contrario de lo que observamos en pacientes con sida, los pacientes VIH-negativos que desarrollan sarcoma de Kaposi, enfermedad de Castleman multicéntrica o linfoma primario de cavidades habitualmente son de edad avanzada y no están coinfectados por el VEB. Es posible que en pacientes VIH-negativos exista un defecto en el sistema inmunológico que facilite la infección por el VHH-8 probablemente condicionado por la edad avanzada u otras patologías asociadas como la cirrosis, las neoplasias o el trasplante de órganos.
Declaración de conflicto de intereses
Declaramos no tener ningún conflicto de intereses.
Correspondencia:
M.A. Pastor Nieto. Valderrey 35, 6.º I. 28039 Madrid. España.
tonales@terra.es
Recibido el 2 de enero de 2006.
Aceptado el 25 de mayo de 2006.