El formaldehído es un gas incoloro de olor penetrante que se emplea como conservante en gran cantidad de productos de higiene y cosméticos, domésticos y de aplicación industrial. Tanto el formaldehído como las sustancias capaces de liberar formaldehído son una causa común de dermatitis de contacto alérgica que, a menudo, se cronifica dada la dificultad que tienen los pacientes alérgicos para evitar por completo estos alérgenos de distribución tan ubicua. El presente artículo pretende repasar las fuentes de exposición a formaldehído y liberadores de formaldehído, las manifestaciones clínicas generadas por estos alérgenos y las controversias y novedades existentes respecto a este tema en la actualidad. Además proponemos unas pautas para el diagnóstico y el tratamiento de estos pacientes.
Formaldehyde is a colorless gas with a pungent odor that is widely used as a preservative in toiletries and cosmetics and in products for household and industrial use. Both formaldehyde itself and substances that can release it are a common cause of allergic contact dermatitis. This condition often becomes chronic, given that these allergens are found nearly everywhere and it is difficult for patients to avoid them completely. This article reviews the sources of exposure to formaldehyde and formaldehyde releasers and the clinical manifestations of allergen exposure. We also review current debates and recent developments and propose guidelines for the diagnosis and treatment of patients with formaldehyde contact dermatitis.
El formaldehído presenta una potente capacidad sensibilizante y es una causa común de dermatitis de contacto alérgica. Según los datos del último estudio epidemiológico del Grupo Español para la Investigación de la Dermatitis de Contacto y Alergia Cutánea (GEIDAC), en España la prevalencia de sensibilización a formaldehído es de un 1,61%1 del total de pacientes con pruebas epicutáneas realizadas y ocupa la decimocuarta posición en la lista de alérgenos más frecuentes. A menudo los pacientes alérgicos a formaldehído sufren una dermatitis crónica de difícil manejo terapéutico, puesto que este alérgeno es muy ubicuo y, por tanto, muy difícil de evitar. Se utiliza como conservante en múltiples productos, dadas sus propiedades antifúngicas y antibacterianas, y podemos encontrarlo tanto en productos cosméticos y domésticos como en productos de uso industrial. En ocasiones estos productos pueden no contener formaldehído, pero sí agentes capaces de liberar formaldehído durante su descomposición, o sustancias sintetizadas a partir de formaldehído. Estos agentes se emplean también como conservantes tanto en productos cosméticos y domésticos como de aplicación industrial. Incluso en la industria textil se utilizan resinas que liberan formaldehído como sustancias de apresto (para evitar que los tejidos se arruguen). Todo esto complica aún más la evitación de formaldehído a los pacientes alérgicos al mismo.
Actualmente existe controversia respecto al tratamiento de estos pacientes. Mientras algunos autores defienden que los pacientes alérgicos a formaldehído deben evitar también todos los liberadores2-4, para otros autores es suficiente con que eviten aquellos liberadores que hayan resultado positivos en las pruebas epicutáneas5. Por otro lado, diferentes estudios proponen que no toda la alergia a liberadores es debida a la liberación de formaldehído6,7, ya que otros componentes de estos liberadores pueden actuar también como alérgenos e inducir sensibilización.
Los objetivos de este artículo son revisar las fuentes de exposición a formaldehído y agentes liberadores de formaldehído, proponer una metodología de estudio mediante pruebas epicutáneas de los pacientes alérgicos a formaldehído y liberadores de formaldehído y facilitar unas pautas de manejo terapéutico de estos pacientes.
Fuentes de formaldehídoA temperatura normal el formaldehído es un gas incoloro, de olor característico, que puede liberarse a partir de múltiples reacciones, como la combustión de la madera, tabaco, gas natural o keroseno. También puede aparecer de forma natural en una gran variedad de alimentos, como café, caviar, jamón ahumado o bacalao.
Su amplio espectro de acción antimicrobiana, capaz de eliminar gran cantidad de bacterias y hongos, convierte al formaldehído en un buen conservante, presente en múltiples productos. Sin embargo, su uso en cosméticos y en productos de higiene se ha reducido considerablemente debido a su toxicidad2. En su lugar se utilizan agentes capaces de liberar formaldehído lenta y progresivamente en las condiciones de uso habituales, frecuentemente asociados a otros conservantes, como metilparabeno y propilparabeno, para aumentar la actividad antifúngica.
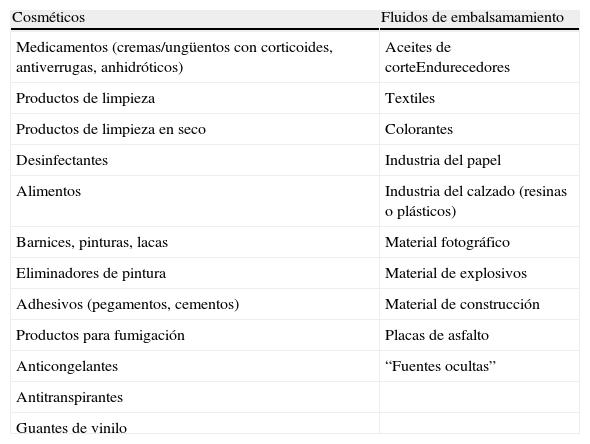
El formaldehído se emplea en productos de limpieza y en gran variedad de productos de aplicación industrial, como adhesivos, pinturas, lacas o aceites de corte (tabla 1).
Fuentes de formaldehído.
| Cosméticos | Fluidos de embalsamamiento |
| Medicamentos (cremas/ungüentos con corticoides, antiverrugas, anhidróticos) | Aceites de corteEndurecedores |
| Productos de limpieza | Textiles |
| Productos de limpieza en seco | Colorantes |
| Desinfectantes | Industria del papel |
| Alimentos | Industria del calzado (resinas o plásticos) |
| Barnices, pinturas, lacas | Material fotográfico |
| Eliminadores de pintura | Material de explosivos |
| Adhesivos (pegamentos, cementos) | Material de construcción |
| Productos para fumigación | Placas de asfalto |
| Anticongelantes | “Fuentes ocultas” |
| Antitranspirantes | |
| Guantes de vinilo |
Es necesario tener en cuenta que, además de los productos en los que específicamente el formaldehído se añade como conservante, también pueden existir “fuentes ocultas”3, donde el formaldehído se considera un contaminante. Estas fuentes ocultas son:
- 1.
El formaldehído que se emplea para la conservación de la materia prima utilizada para preparar un producto.
- 2.
El formaldehído empleado para la esterilización de los recipientes donde se prepara o almacena un producto.
- 3.
El formaldehído liberado por las resinas de formaldehído que forman parte de los tubos de los cosméticos y productos farmacéuticos. La melamina o la carbamida-formaldehído, que se utilizan como recubrimiento de los tubos de plástico, pueden, con el tiempo, liberar formaldehído8,9.
- 4.
El formaldehído formado in situ por la degradación de componentes que contiene el producto, como la autooxidación de alcoholes etoxilados10 o la oxidación de polisorbato 8011. En un estudio realizado en Suecia, 6 de los 73 medicamentos tópicos con corticoides disponibles en el mercado contenían formaldehído12. En estos casos, el formaldehído se había formado como consecuencia de la oxidación de compuestos presentes en estos medicamentos, como el polietilenglicol y sus derivados, y también por oxidación de sustancias surfactantes empleadas como emulsionantes. Para estos autores la cantidad de formaldehído encontrado en los medicamentos quizás no es suficiente para inducir sensibilización o para desencadenar una dermatitis de contacto alérgica sobre una piel intacta en pacientes previamente sensibilizados. Sin embargo, esta cantidad sí podría mantener o agravar una dermatitis preexistente en pacientes alérgicos a formaldehído.
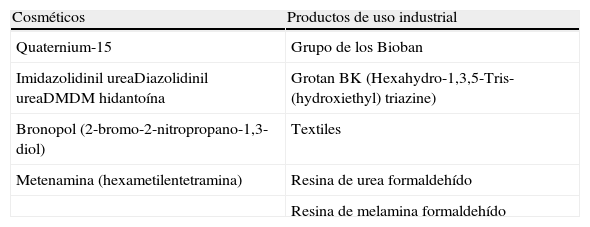
Los agentes liberadores de formaldehído se definen como sustancias que liberan formaldehído, bien durante su descomposición, bien sintetizadas a partir de formaldehído, y pueden contener residuos de formaldehído libre. Existen más de 40 sustancias descritas en la literatura como agentes liberadores de formaldehído. De estos solo unos pocos se manejan realmente en la práctica diaria de una consulta de alergia cutánea (tabla 2).
Principales agentes liberadores de formaldehído.
| Cosméticos | Productos de uso industrial |
| Quaternium-15 | Grupo de los Bioban |
| Imidazolidinil ureaDiazolidinil ureaDMDM hidantoína | Grotan BK (Hexahydro-1,3,5-Tris-(hydroxiethyl) triazine) |
| Bronopol (2-bromo-2-nitropropano-1,3-diol) | Textiles |
| Metenamina (hexametilentetramina) | Resina de urea formaldehído |
| Resina de melamina formaldehído |
Desde un punto de vista didáctico podemos dividir los liberadores de formaldehído en 2 subgrupos: el subgrupo de agentes que liberan formaldehído por descomposición y el de agentes sintetizados a partir de formaldehído.
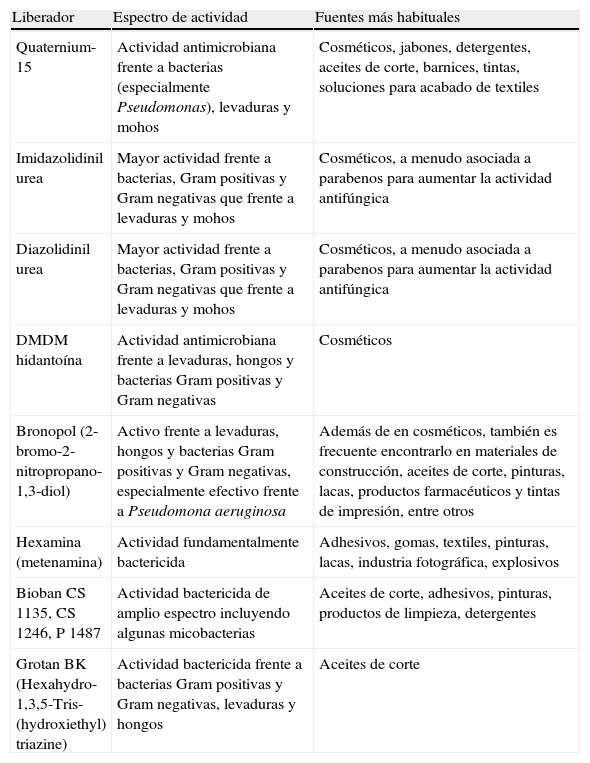
Agentes liberadores de formaldehído por descomposiciónLa mayoría de las sustancias liberadoras de formaldehído que tienen interés en alergia cutánea corresponde al grupo que libera formaldehído por descomposición. Dentro de este grupo se encuentran quaternium-15, imidazolidinil urea, diazolidinil urea, DMDM hidantoína y bronopol, que se emplean fundamentalmente en cosméticos. También pertenecen a esta categoría grotan BK y los bioban (bioban CS 1135, bioban CS 1246 y bioban P 1487), que se añaden como conservantes a productos de uso industrial (tabla 3).
Principales características de los agentes liberadores de formaldehído más habituales.
| Liberador | Espectro de actividad | Fuentes más habituales |
| Quaternium-15 | Actividad antimicrobiana frente a bacterias (especialmente Pseudomonas), levaduras y mohos | Cosméticos, jabones, detergentes, aceites de corte, barnices, tintas, soluciones para acabado de textiles |
| Imidazolidinil urea | Mayor actividad frente a bacterias, Gram positivas y Gram negativas que frente a levaduras y mohos | Cosméticos, a menudo asociada a parabenos para aumentar la actividad antifúngica |
| Diazolidinil urea | Mayor actividad frente a bacterias, Gram positivas y Gram negativas que frente a levaduras y mohos | Cosméticos, a menudo asociada a parabenos para aumentar la actividad antifúngica |
| DMDM hidantoína | Actividad antimicrobiana frente a levaduras, hongos y bacterias Gram positivas y Gram negativas | Cosméticos |
| Bronopol (2-bromo-2-nitropropano-1,3-diol) | Activo frente a levaduras, hongos y bacterias Gram positivas y Gram negativas, especialmente efectivo frente a Pseudomona aeruginosa | Además de en cosméticos, también es frecuente encontrarlo en materiales de construcción, aceites de corte, pinturas, lacas, productos farmacéuticos y tintas de impresión, entre otros |
| Hexamina (metenamina) | Actividad fundamentalmente bactericida | Adhesivos, gomas, textiles, pinturas, lacas, industria fotográfica, explosivos |
| Bioban CS 1135, CS 1246, P 1487 | Actividad bactericida de amplio espectro incluyendo algunas micobacterias | Aceites de corte, adhesivos, pinturas, productos de limpieza, detergentes |
| Grotan BK (Hexahydro-1,3,5-Tris-(hydroxiethyl) triazine) | Actividad bactericida frente a bacterias Gram positivas y Gram negativas, levaduras y hongos | Aceites de corte |
Todas estas sustancias tienen la capacidad de liberar pequeñas cantidades de formaldehído de forma lenta, mientras este se va necesitando, de manera que, cuando el formaldehído se agota, el liberador aporta más formaldehído. Así, la cantidad de formaldehído presente en el producto se mantiene baja, pero es suficiente para prevenir el crecimiento de microorganismos6. A pesar de que la capacidad biocida de los liberadores se debe en parte a la liberación de formaldehído, también muchos de estos agentes tienen capacidad antimicrobiana por sí mismos, independiente de la liberación de formaldehído13,14.
Condiciones en las que los liberadores desprenden formaldehídoEn la actualidad todavía no existen datos suficientes sobre si realmente los agentes liberadores de formaldehído suponen un riesgo para los pacientes alérgicos a formaldehído. A pesar de que no se conoce con certeza qué cantidad de formaldehído libre presente en un producto resulta segura para estos pacientes, se considera que niveles > 200 p.p.m probablemente sean capaces de suscitar una dermatitis de contacto en personas alérgicas a formaldehído15,16. La mayoría de los liberadores presentes en cosméticos, empleados a las concentraciones permitidas en Europa, son capaces de liberar > 200 p.p.m.17-21.
En el laboratorio es posible conocer la cantidad de formaldehído que libera un liberador gracias a la 13C NMR espectroscopia cuantitativa18. Se trata de un método puramente físico que evita los problemas que pueden dar otras técnicas a la hora de analizar formaldehído en presencia de liberadores. Con otras técnicas, el formaldehído es captado por un reactor de forma que, al disminuir la cantidad de formaldehído libre, el liberador aporta más formaldehído, que será de nuevo captado por el reactor. De esta manera, con la mayoría de los métodos, la cantidad de formaldehído obtenida es superior a la real. Desafortunadamente, en condiciones reales, no es posible conocer cuánto formaldehído libre existe en un producto que contiene liberadores de formaldehído. Esto se debe a que la cantidad de formaldehído liberado depende de múltiples factores, como la naturaleza del liberador y su concentración en el producto, el pH, la temperatura y el tiempo que el producto lleva almacenado o el nivel de contaminación microbiana y la presencia de otros componentes. No todos los liberadores liberan la misma cantidad de formaldehído. En un estudio17 el orden de liberación, de menor a mayor cantidad de formaldehído liberado, fue imidazolidinil urea < DMDM hidantoína< diazolidinil urean< quaternium-15. En general se considera que, de los liberadores que se emplean más frecuentemente en cosméticos, el quaternium-15 es el que más formaldehído libera, mientras que el bronopol es el que lo hace en menor cantidad. El pH influye notablemente en la liberación de formaldehído. Imidazolidinil urea, diazolidinil urea y DMDM hidantoína liberan mayor cantidad de formaldehído en pH alcalino18. A mayor temperatura, mayor es la cantidad de formaldehído presente en una solución, de la misma forma que, cuanto mayor es el tiempo que un producto lleva almacenado, mayor es la cantidad de formaldehído liberado. La presencia de otros ingredientes también va a modificar la concentración de formaldehído. Por ejemplo, en un champú libre de proteínas, quaternium-15 al 0,1% liberó 482 p.p.m. de formaldehído, mientras que en un champú con proteínas solo liberó 122 p.p.m.17, probablemente por la formación de complejos entre formaldehído y proteínas, que dio lugar a una menor cantidad de formaldehído libre.
Liberadores de formaldehído como alérgenos per seA pesar de que todas estas sustancias se engloban dentro de una misma categoría, la realidad es que se trata de compuestos con una estructura química muy diferente. Este dato puede tener interés porque actualmente se postula que probablemente no toda la alergia a liberadores de formaldehído sea debida a sensibilización a formaldehído, ya que existe un gran número de pacientes que muestran un resultado positivo a liberadores en las pruebas epicutáneas, pero sin reacción a formaldehído. Recientemente se ha publicado que únicamente el 40-60% de las reacciones a liberadores de formaldehído son debidas a reacción a formaldehído y que esta cifra es aún menor para bronopol (solo el 15% de las reacciones a bronopol se deben a sensibilización a formaldehído)22. Es decir, que probablemente existen otros componentes en los liberadores que pueden actuar también como alérgenos y provocar sensibilización, que no depende de la liberación de formaldehído. En diversos trabajos recientes se intenta encontrar los alérgenos implicados que permitan explicar esta evidencia clínica. Se ha postulado que el “compuesto HU” (4-hidroximetil-2,5-dioxoimidazolidin-4-yl)-urea), un compuesto formado a partir de la degradación de diazolidinil urea y presente también en imidazolidinil urea, podría estar implicado en la alergia a estos dos liberadores cuando esta no depende de formaldehído7,23. Esto podría explicar los numerosos casos descritos en la literatura de co-sensibilización a estos 2 liberadores sin formaldehído23-25.
Recientemente Kireche et al6 realizaron un estudio para intentar comprobar si para algunos liberadores de formaldehído existen intermediarios, diferentes a formaldehído, capaces de formar un complejo antigénico hapteno-proteínas, un paso clave en el proceso de sensibilización, y por tanto que pueda explicar que estas sustancias tengan un potencial de sensibilización per se, independiente de la liberación de formaldehído. El resultado fue que para los agentes liberadores de formaldehído escogidos, DMDM hidantoína, metenamina (hexamina) y bronopol, muchas especies reactivas, además del formaldehído, podían formar estas estructuras antigénicas.
Algunos de los liberadores, sin embargo, sí se pueden incluir dentro de un mismo grupo estructuralmente relacionado. Es el caso de DMDM hidantoína, imidazolidinil urea y diazolidinil urea, que pertenecen al grupo de hidantoínas. También se pueden incluir dentro de un mismo grupo a metenamina (hexamina) y a quaternium-15, que es un derivado cloroalil de metenamina6. Este hecho podría explicar los casos co-sensibilización a varios liberadores, químicamente relacionados, sin resultados positivos a formaldehído24,25.
Agentes sintetizados a partir de formaldehídoPor otro lado están los agentes que se sintetizan a partir de formaldehído y que pueden contener formaldehído libre como residuo. Entre estos agentes destacan las resinas de formaldehído como la melamina y la urea-formaldehído, que se empleaban habitualmente como sustancias de apresto. Estas resinas contenían gran cantidad de formaldehído libre y suponían una causa común de dermatitis de contacto alérgica por ropa en pacientes alérgicos a formaldehído. Sin embargo, las resinas que se utilizan actualmente liberan mucha menor cantidad de formaldehído y por ello este problema ha pasado a ser menos frecuente, aunque todavía existen casos de este tipo de alergia de contacto26,27.
Sustancias sin relevancia en la alergia a formaldehídoActualmente no se considera que tengan relevancia en la alergia a formaldehído las resinas de fenol-formaldehído, como fenol-3 resina de formaldehído28 y p-tert-butil fenolformaldehído resina29, ya que aunque están sintetizadas a partir de formaldehído, no liberan realmente formaldehído cuando el producto está acabado. Tampoco la resina de tosilamida-formaldehído. Esta resina, basada en toluenesulfonamida y formaldehído está presente en gran cantidad de lacas de uñas. Hoy en día se considera que la cantidad de formaldehído libre en una laca de uñas acabada y seca es casi nula. Es por esto que los pacientes no suelen sensibilizarse a formaldehído a través de las lacas de uñas y tampoco las lacas de uñas suelen dar problemas en pacientes que ya son sensibles a formaldehído16.
Tampoco consideraremos en esta revisión compuestos que pueden presentar reacciones cruzadas con formaldehído, como el glutaraldehído y el glioxal30-32.
EpidemiologíaEl formaldehído es una causa común de dermatitis de contacto alérgica. La prevalencia de sensibilización a este alérgeno es mayor en Estados Unidos, donde se encuentra en torno a un 8-9%, que en Europa, donde diferentes estudios la sitúan entre un 2-3% de los pacientes con pruebas epicutáneas realizadas. En España, según datos del último estudio epidemiológico del GEIDAC, la prevalencia de sensibilización a formaldehído es de un 1,61%1.
Las diferencias entre EE. UU. y Europa podrían explicarse por las diferencias en la legislación respecto al formaldehído entre EE. UU. y los diferentes países europeos. Mientras que en EE. UU. no existe una normativa específica, en la Unión Europea la exposición a formaldehído está regulada, de forma que el límite máximo de concentración de formaldehído libre permitido en cosméticos es del 0,2% (0,1% en productos de higiene oral). En Europa todos los productos finalizados que contengan formaldehído o liberadores de formaldehído deben ser etiquetados con la advertencia “contiene formaldehído”, siempre que la concentración exceda el 0,05%32. De Groot realizó un estudio para comprobar si en EE. UU. había disponibles a la venta una mayor cantidad de cosméticos que contenían liberadores de formaldehído comparado con Europa33. El resultado fue que el 23,8% de los cosméticos de EE. UU. (según datos de la FDA) contenía uno o varios liberadores, frente al 24,6% de los cosméticos en Europa (según datos obtenidos al analizar los cosméticos disponibles en un supermercado de una gran cadena holandesa). Por tanto, para este autor, las diferencias en la prevalencia de sensibilización entre EE. UU. y Europa no se pueden explicar por la existencia de una mayor cantidad de cosméticos con formaldehído en EE. UU., aunque queda por comprobar si existen diferencias en el patrón de consumo de cosméticos (es decir, determinar si los pacientes estadounidenses consumen mayor cantidad de cosméticos que los europeos) y también si la muestra es representativa de toda Europa, ya que únicamente se analizaron productos provenientes de un supermercado holandés.
De todas formas, a partir de 1980 existe una tendencia a la disminución de la prevalencia de sensibilización a formaldehído. Esta disminución se debe, en parte, a la sustitución del mismo por agentes liberadores de formaldehído en cosméticos y productos de higiene y al empleo de resinas con baja liberación de formaldehído para el acabado de los textiles. La disminución de la concentración de formaldehído empleado en las pruebas epicutáneas de un 3-5% al 1% en agua, recomendado actualmente, también puede haber influido en el descenso de la prevalencia de sensibilización (por un aumento en el número de falsos negativos)16.
Igual que ocurre con el formaldehído, la prevalencia de sensibilización a quaternium-15 es más elevada en EE. UU. que en Europa. En EE. UU. varía entre un 7,1 hasta un 9,6%, mientras que en Europa lo hace entre un 0,6 a un 1,9%. En el último estudio epidemiológico español la prevalencia de sensibilización a quaternium-15 es de un 1,27%1 y ocupa la decimonovena posición en la lista de los alérgenos más frecuentes. Las frecuencias de sensibilización a otros liberadores son menores, también con diferencias entre EE. UU. y Europa. Se encuentran entre un 1,3-3,3% para imidazolidinil urea (0,3-1,4% en Europa), entre 2,4-3,7% para diazolidinil urea (0,5-1,4% en Europa), entre 2,1-3,3% para bronopol (0,4-1,2%) y entre 0,5-3,4% para DMDM hidantoína (no hay datos actualizados para Europa)16.
Cuando se realizan pruebas epicutáneas con formaldehído y uno o más liberadores, es frecuente observar reacciones concomitantes. A menudo, se asume que la reacción al liberador es consecuencia de la reacción al formaldehído presente en el liberador. Varios estudios apoyan esta idea, puesto que es frecuente encontrar resultados positivos a varios liberadores, junto con formaldehído, aun cuando los liberadores no están estructuralmente relacionados22,24. Perrett y Happle34 estudiaron 13 pacientes con pruebas epicutáneas positivas a diazolidinil urea, 6 de los cuales también tenían un resultado positivo a formaldehído. A estos 13 pacientes se les realizaron pruebas epicutáneas con urea-formaldehído, urea glioxal y quaternium-15. Los 6 pacientes con pruebas positivas a diazolidinil urea y formaldehído también reaccionaron al resto de los liberadores, mientras que los pacientes que no habían reaccionado a formaldehído tampoco lo hicieron a ninguno de los liberadores. Se concluyó que, en los pacientes con reacción positiva a diazolidinil urea y formaldehído, esta era debida al formaldehído presente en la prueba epicutánea. Este y otros estudios similares corroboran que, al menos en algunos pacientes, las reacciones entre formaldehído y liberadores son debidas a sensibilización a formaldehído. Pero por otro lado, de este mismo estudio también se puede concluir que la sensibilización a liberadores puede existir sin sensibilización a formaldehído.
No todos los liberadores se asocian con la misma frecuencia de sensibilización a formaldehído. Tras revisar diversos estudios25,35,36, donde se ofrecen datos sobre la relación entre formaldehído y los liberadores, se puede concluir que, en general, en menos de un 25% de los casos (y habitualmente en muchos menos) de sensibilización a bronopol los pacientes reaccionan también a formaldehído, mientras que en más del 50% de los pacientes con pruebas epicutáneas positivas a quaternium-15 reaccionan también a formaldehído. Los datos de co-sensibilización no son tan consistentes en el caso de otros liberadores y pueden variar: entre 12-81% para diazolidinil urea, entre un 11-63% para imidazolidinil urea y entre un 37-83% para DMDM hidantoína22.
Si estudiamos el porcentaje de pacientes alérgicos a formaldehído que reaccionan también frente a liberadores observamos que menos del 10% de los pacientes alérgicos a formaldehído reaccionan a bronopol, mientras que más de un 30% de los pacientes sensibilizados a formaldehído reaccionan a quaternium-15. La presencia de quaternium-15 en la batería estándar puede explicar que esta asociación sea más frecuente, comparada con la de otros liberadores. Menos del 30% de los alérgicos a formaldehído reaccionan a diazolidinil urea, menos del 23% a imidazolidinil urea y aproximadamente uno de cada 5 pacientes sensibilizados a formaldehído reacciona a DMDM hidantoína22.
Por tanto, la asociación más fuerte es la que aparece entre formaldehído y quaternium-15, que es el liberador que mayor cantidad de formaldehído desprende. La asociación más débil, por el contrario, es la que aparece entre formaldehído y bronopol.
Conocer la frecuencia con la que los pacientes alérgicos a un liberador reaccionan frente a otro u otros liberadores puede ser también interesante25,37,38. La sensibilidad a bronopol no se suele asociar a otros liberadores. Sin embargo, es frecuente observar co-sensibilización entre imidazolidinil urea y diazolidinil urea, a menudo sin formaldehído, probablemente por la existencia de un componente común a ambas sustancias que actúa como alérgeno e induce sensibilización. Cuando imidazolidinil urea o diazolidinil urea se asocian a quaternium-15 (ocurre en aproximadamente un 50% de los pacientes) se considera entonces que el responsable de la reacción es formaldehído, ya que estos liberadores no están estructuralmente relacionados.
ClínicaEl formaldehído, además de un potente sensibilizante, es un irritante primario que puede afectar la piel, la conjuntiva y la mucosa oral, y es también considerado un potencial carcinógeno respiratorio2. Puede ser, también, responsable de urticaria de contacto39 y ha sido relacionado con migraña por ingesta de aspartamo en pacientes alérgicos a formaldehído40 (se puede formar formaldehído a partir de la digestión de este edulcorante artificial).
La dermatitis de contacto que aparece en pacientes alérgicos a formaldehído es a menudo crónica, puesto que resulta difícil para estos pacientes evitar por completo este alérgeno de distribución ubicua, tanto desde una perspectiva domiciliaria como laboral.
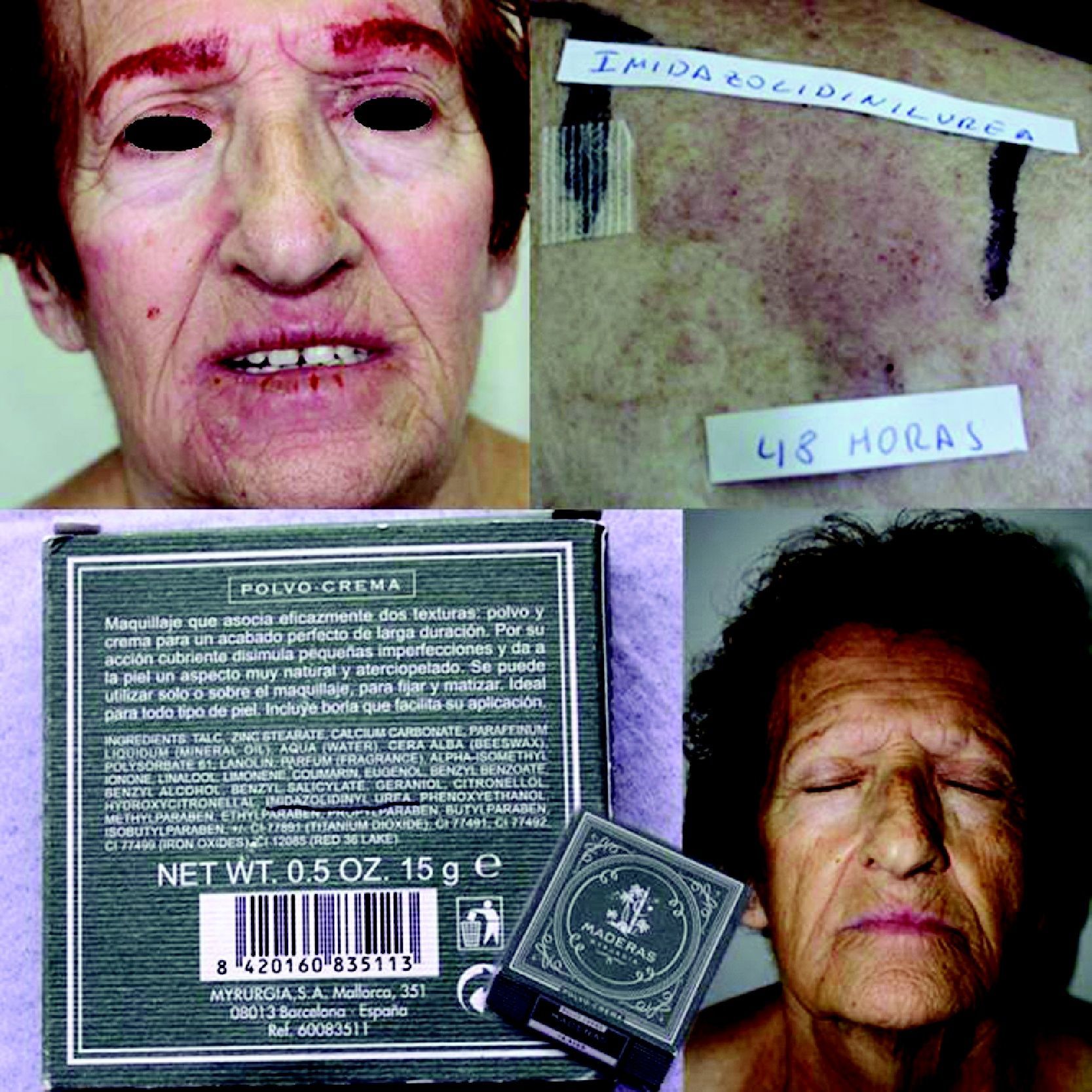
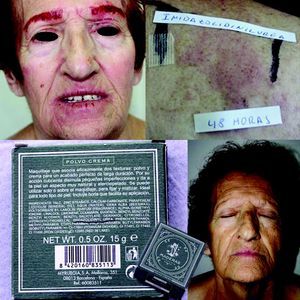
Los pacientes alérgicos a formaldehído son, a menudo, mujeres con eczema de manos con o sin afectación facial41,42. Esto se explica porque las manos están expuestas a productos de limpieza que muchas veces contienen detergentes que dañan la barrera cutánea, facilitando así la penetración de formaldehído presente en productos cosméticos, de higiene y limpieza que contienen agentes liberadores de formaldehído. La afectación facial está causada principalmente por la aplicación de cosméticos que contienen liberadores de formaldehído (fig. 1).
La dermatitis de contacto alérgica ocupacional por formaldehído aparece fundamentalmente en las manos, se considera frecuente y afecta sobre todo a trabajadores que emplean aceites de corte, y a peluqueros y profesionales sanitarios que utilizan cremas y jabones que contienen agentes liberadores35. En muchas ocasiones, la sensibilización a formaldehído no es el evento primario, sino que los pacientes presentan una dermatitis de contacto irritativa y terminan sensibilizándose al formaldehído presente en cosméticos y productos de higiene que contienen liberadores como consecuencia de su mayor penetración por la ruptura de la barrera cutánea.
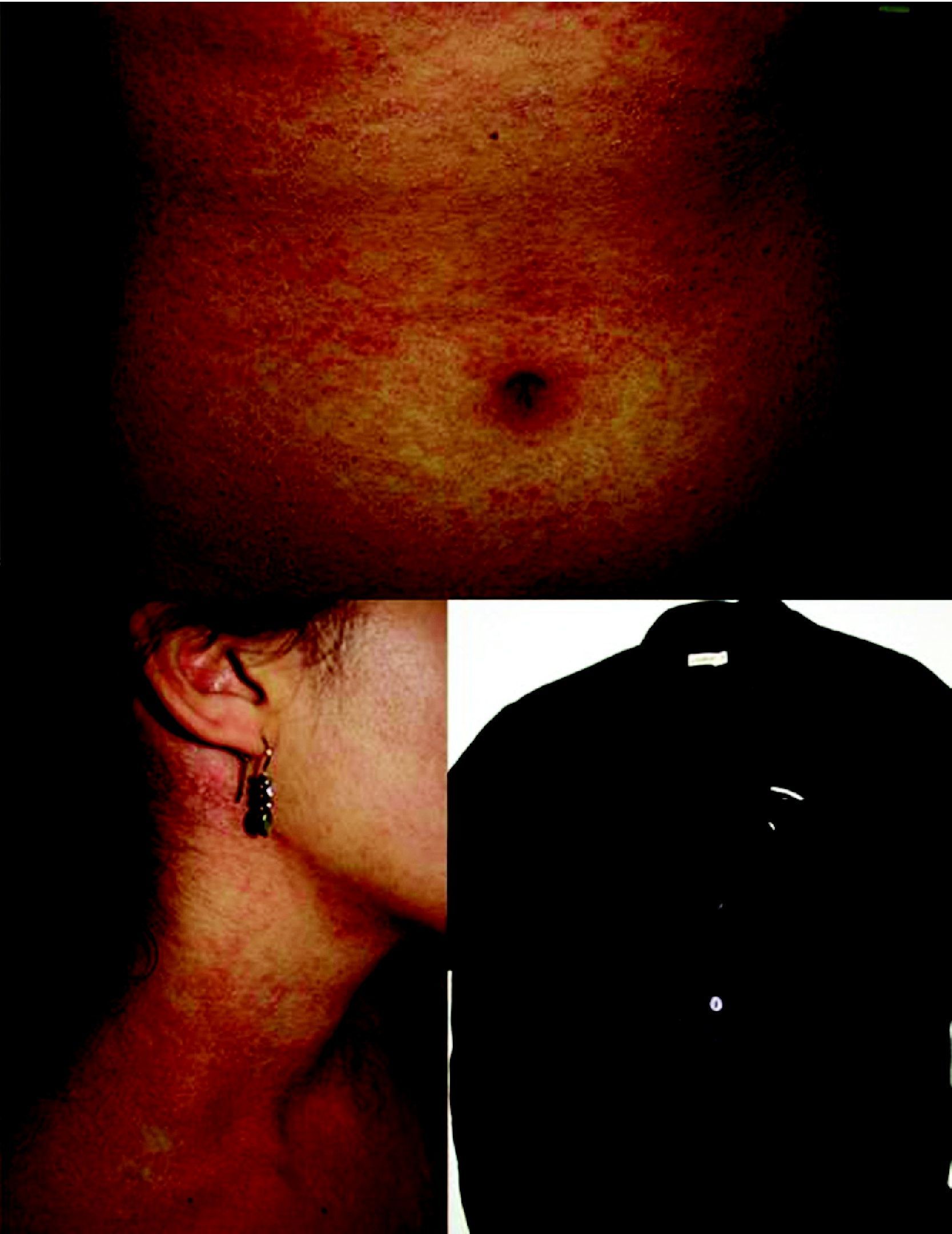
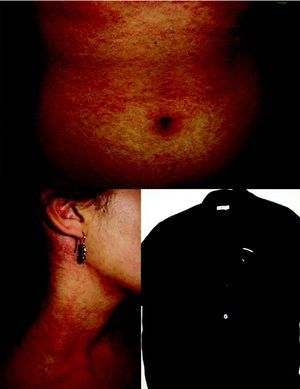
Las resinas de formaldehído presentes en textiles suelen ocasionar una dermatitis que se distribuye, fundamentalmente, en lugares de roce de la ropa con el cuerpo, como la cara interna de los muslos, el cuello y zonas donde existe mayor sudoración, como la región periaxilar, las ingles y las fosas antecubitales y poplíteas. En ocasiones, también la dermatitis de contacto alérgica por textiles se manifiesta como reacciones generalizadas que respetan la cara y las manos27,43 (fig. 2).
DiagnósticoPruebas epicutáneasEl formaldehído está incluido dentro de la batería estándar del GEIDAC. Actualmente se considera que las pruebas epicutáneas para detectar sensibilización deben realizarse con parches de formaldehído al 1% en agua. Anteriormente se empleaban parches con concentraciones mayores, entre 3 y 5%, que resultaban en gran cantidad de falsos positivos. A pesar de haber disminuido la concentración al 1%, todavía se considera que los parches de formaldehído provocan gran cantidad de falsos positivos, ya que menos de un 50% de los resultados positivos que se obtienen aparecen de nuevo cuando se retesta este alérgeno44. Por otro lado, también pueden ocurrir falsos negativos con esta concentración. Según el estudio de Trattner et al más del 40% de los pacientes alérgicos a formaldehído no se detectan cuando el formaldehído se parchea al 1% en agua en lugar de al 2% en agua45. Debemos tener en cuenta que los pacientes que reaccionan únicamente frente a formaldehído, pero no frente a liberadores, pueden tratarse de falsos positivos, mientras que los pacientes que reaccionan frente a varios liberadores, pero sin formaldehído, pueden tratarse de falsos negativos.
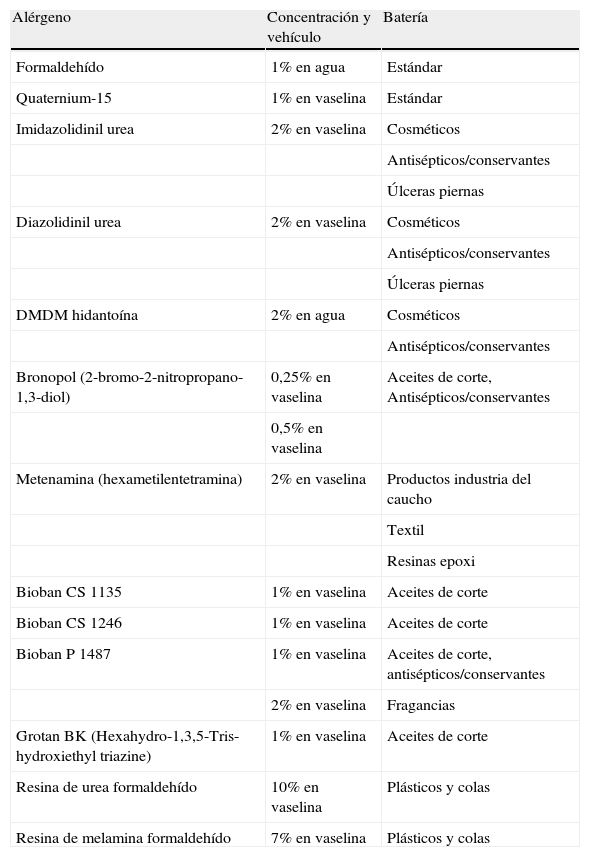
El quaternium-15 es el único liberador de formaldehído incluido en la batería estándar del GEIDAC, aunque en algunos centros también imidazolidinil urea y diazolidinil urea se testan en la batería estándar para intentar mejorar el estudio de pacientes alérgicos a formaldehído. Actualmente, los liberadores se parchean en vaselina en lugar de en agua, porque se ha visto que con vaselina se detectan más casos de sensibilización7 (tabla 4).
Formaldehído y liberadores de formaldehído más frecuentes y concentraciones y vehículos empleados para el estudio mediante pruebas epicutáneas.
| Alérgeno | Concentración y vehículo | Batería |
| Formaldehído | 1% en agua | Estándar |
| Quaternium-15 | 1% en vaselina | Estándar |
| Imidazolidinil urea | 2% en vaselina | Cosméticos |
| Antisépticos/conservantes | ||
| Úlceras piernas | ||
| Diazolidinil urea | 2% en vaselina | Cosméticos |
| Antisépticos/conservantes | ||
| Úlceras piernas | ||
| DMDM hidantoína | 2% en agua | Cosméticos |
| Antisépticos/conservantes | ||
| Bronopol (2-bromo-2-nitropropano-1,3-diol) | 0,25% en vaselina | Aceites de corte, Antisépticos/conservantes |
| 0,5% en vaselina | ||
| Metenamina (hexametilentetramina) | 2% en vaselina | Productos industria del caucho |
| Textil | ||
| Resinas epoxi | ||
| Bioban CS 1135 | 1% en vaselina | Aceites de corte |
| Bioban CS 1246 | 1% en vaselina | Aceites de corte |
| Bioban P 1487 | 1% en vaselina | Aceites de corte, antisépticos/conservantes |
| 2% en vaselina | Fragancias | |
| Grotan BK (Hexahydro-1,3,5-Tris-hydroxiethyl triazine) | 1% en vaselina | Aceites de corte |
| Resina de urea formaldehído | 10% en vaselina | Plásticos y colas |
| Resina de melamina formaldehído | 7% en vaselina | Plásticos y colas |
El estudio se puede completar con la realización de pruebas con productos propios que aporte el paciente. Dependiendo del tipo de producto se pueden aplicar como una prueba epicutánea o mediante test de aplicación abierta repetida. En caso de que un paciente alérgico a formaldehído tenga una reacción positiva a un producto propio y negativa a los componentes del producto, se puede intentar determinar la presencia de formaldehído como contaminante en ese producto.
Métodos para la detección de formaldehídoLos métodos para la detección de formaldehído quedan reflejados en la tabla 5.
Métodos para la determinación de formaldehído.
| Método de cromatografía ácida |
| Método semicuantitativo, basado en la reacción química entre un cromatógrafo ácido y formaldehído libre que da lugar a una coloración violeta. El problema es que otros aldehídos y cetonas pueden reaccionar con el cromatógrafo; esta reacción produce una decoloración amarilla que puede interferir con el test46-48 |
| Método de acetilacetona |
| Es también un método semicuantitativo. En este caso el formaldehído reacciona con acetilacetona en presencia de amonio para formar un compuesto amarillo49. La intensidad del amarillo se puede comparar con un estándar para estimar el contenido de formaldehído en la muestra |
| Cromatografía líquida de alto rendimiento |
| Es un método muy fiable, para el que se han descrito varias modificaciones21,22,47,50,51 |
| Método oficial de la Unión Europea |
| Es un método oficial para la determinación de formaldehído libre presente en cosméticos. El análisis se realiza en 3 pasos: identificación de formaldehído, determinación espectrofotométrica del contenido total de formaldehído y determinación de formaldehído libre. Esta última determinación se hace únicamente en los productos que contienen > 0,05% de formaldehído total52 |
| Test de formaldehído en tejidos |
| Es el test de la Sociedad Americana de Químicos y Coloristas Textiles (AATCC)53,54 |
| Test para determinar la presencia de formaldehído en presencia de liberadores de formaldehído |
| Se trata de la 13C NMR espectroscopia cuantitativa que tiene la ventaja de que no afecta al equilibrio alcanzado entre formaldehído libre y liberadores. Con otras técnicas el formaldehído es captado por el reactor de forma que, al disminuir la cantidad de formaldehído libre, el liberador aporta más formaldehído, que será de nuevo captado por el reactor. Así, con la mayoría de los métodos, la cantidad de formaldehído obtenida es superior a la real18 |
El abordaje terapéutico de los pacientes alérgicos a formaldehído y liberadores suele ser complicado por la dificultad de evitar estas sustancias. El formaldehído de por sí ya es difícil de evitar, dada su amplia distribución en productos de uso habitual. Además, hay que tener en cuenta el formaldehído presente en productos como contaminante y el formaldehído que se libera a partir de otras sustancias. En la actualidad todavía no existen datos suficientes que permitan conocer si los agentes liberadores de formaldehído suponen realmente un riesgo para los pacientes sensibilizados a formaldehído. Posiblemente, la cantidad de formaldehído que puede ser liberado a partir de un agente liberador no sea suficiente como para provocar una dermatitis si el producto se emplea de forma ocasional sobre una piel sana, pero sí podría agravar una dermatitis preexistente. El empleo regular de liberadores, o el empleo de varios liberadores de forma concomitante, algo relativamente frecuente, puesto que estas sustancias están presentes en múltiples productos de uso diario, sí podría desencadenar una reacción en pacientes alérgicos a formaldehído. Desafortunadamente, no existen datos para saber, a través del etiquetado de un producto, si este puede ser peligroso para un paciente sensibilizado, puesto que no es posible conocer cuál es realmente la cantidad de formaldehído libre presente en ese producto.
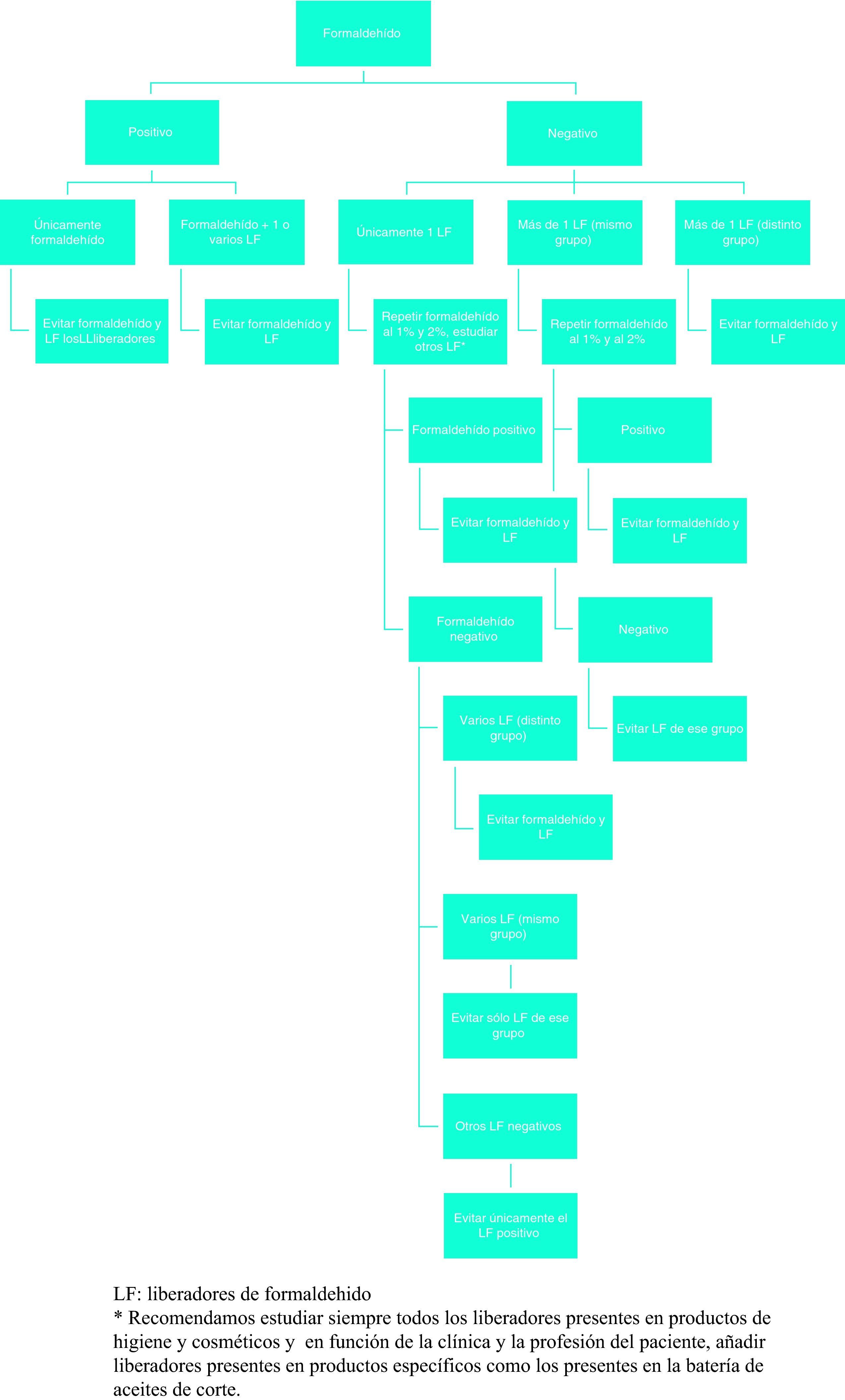
Aunque para algunos autores no es necesario evitar todos los liberadores de formaldehído5, en nuestra experiencia la dermatitis de contacto alérgica a formaldehído no se suele resolver si el paciente sigue empleando liberadores de formaldehído. Por tanto, nuestra recomendación es que los pacientes alérgicos a formaldehído eviten también todos los liberadores, sobre todo si están presentes en productos que se emplean de forma regular y sobre piel dañada. En caso de que no exista alternativa (en ocasiones es difícil encontrar productos que no contengan ni formaldehído ni liberadores), se puede intentar utilizar productos conservados en bronopol (que es el que menor cantidad de formaldehído libera), realizando previamente un test de provocación con el producto en las condiciones de uso habituales para asegurarse que resulta seguro para el paciente (fig. 3).
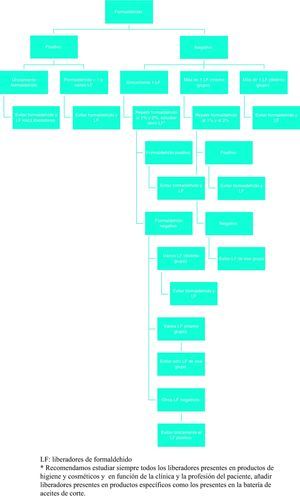
Propuesta de protocolo de manejo terapéutico.
LF: liberadores de formaldehido.
*Recomendamos estudiar siempre todos los liberadores presentes en productos de higiene y cosméticos y en función de la clínica y la profesión del paciente, añadir liberadores presentes en productos específicos como los presentes en la batería de aceites de corte.
Es necesario tener presente que, además del formaldehído y los liberadores que vienen etiquetados en el producto, pueden existir otras fuentes de formaldehído. El exceso de formaldehído empleado para sintetizar el liberador, el formaldehído empleado para esterilizar los recipientes donde se prepara el producto, el empleado como conservante en la materia prima a partir de la cual se prepara el producto o el formado a partir de otros ingredientes que pueda contener el producto, como el polietilenglicol y sus derivados, son ejemplos de estas “fuentes ocultas” de formaldehído. Si tenemos pacientes alérgicos a formaldehído que no mejoran a pesar de evitar estrictamente tanto el formaldehído como los liberadores, podemos determinar si existe formaldehído en algún producto sospechoso (por ejemplo en un textil), si las técnicas antes mencionadas están disponibles en nuestro medio.
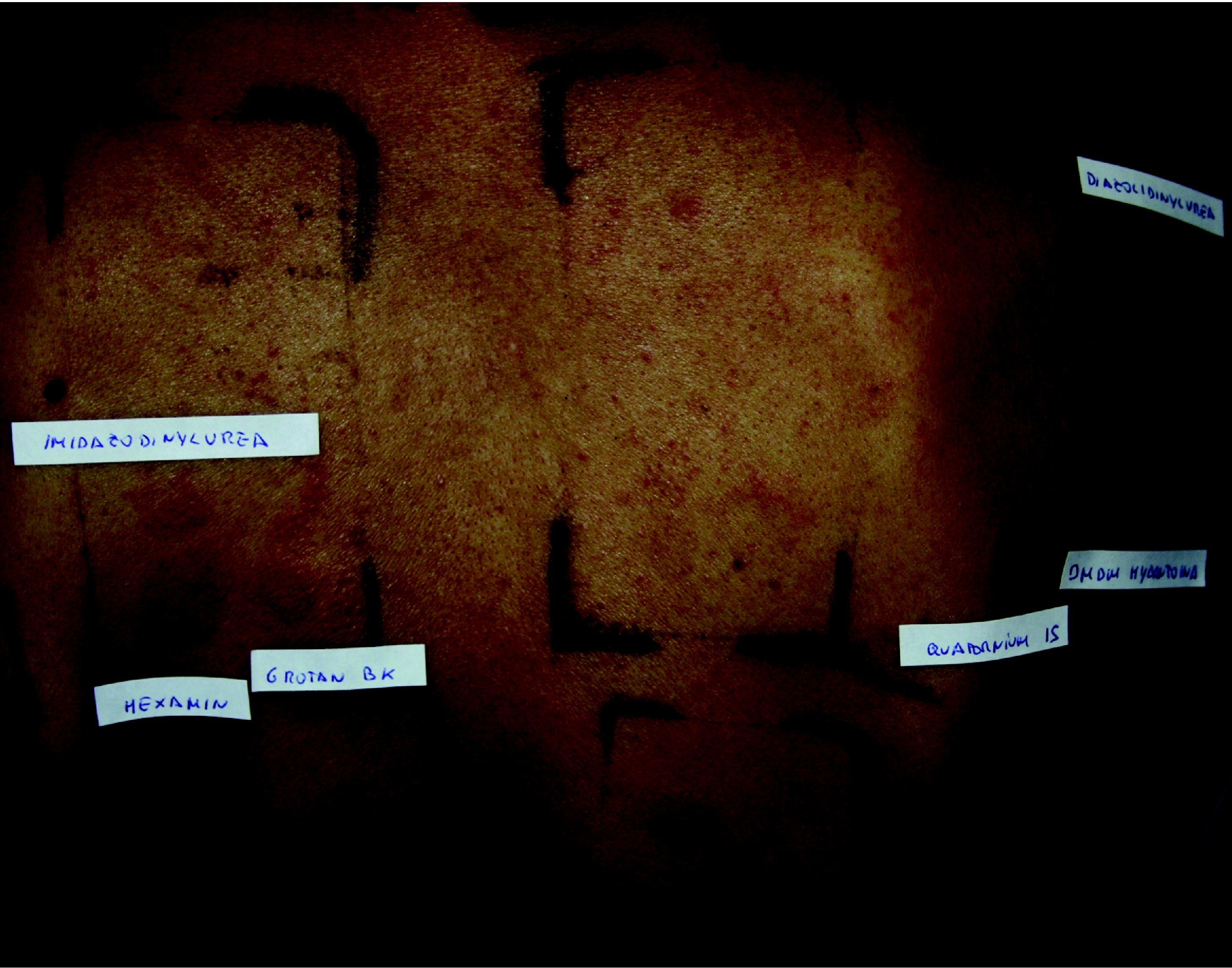
Además, parece que no toda la alergia a liberadores de formaldehído es debida a la liberación de formaldehído, sino que existen también otros componentes de estas sustancias que pueden actuar como alérgenos. Por tanto, ante un paciente con pruebas epicutáneas positivas a liberadores sin formaldehído habría que plantearse varias opciones. Una opción que podría explicar esta situación es que se trate de un falso negativo del formaldehído. Por eso, recomendamos repetir la prueba epicutánea con formaldehído (al 1 y al 2% en agua) siempre que exista positividad a liberadores sin formaldehído, para evitar los falsos negativos45. Otra opción es que realmente se trate de una sensibilización al liberador o liberadores a través de un mecanismo diferente de la liberación de formaldehído. En este último caso, la evitación únicamente del liberador o liberadores que hayan resultado positivos sería suficiente para conseguir mejorar la dermatitis del paciente. Consideramos, sin embargo, que si aparecen varios liberadores de distinto grupo químico, en este caso lo más probable es que las reacciones sean debidas a la liberación de formaldehído, y por tanto los pacientes deberían evitar tanto el formaldehído como el resto de los liberadores (fig. 4).
En la tabla 6 adjuntamos las recomendaciones que facilitamos a nuestros pacientes.
Recomendaciones para pacientes alérgicos a formaldehído y liberadores de formaldehído.
| Usted es alérgico a formaldehído. Debe evitar formaldehído y todos estos liberadores de formaldehído: quaternium-15, imidazolidinil urea, diazolidinil urea, DMDM hidantoína, bronopol (2-bromo-2-nitropropano-1,3-diol), grotan BK (Hexahydro-1,3,5-Tris-(hydroxiethyl)triazine), hexamina (metenamina). Pueden estar presentes en productos de higiene, cosméticos, productos de limpieza, farmacéuticos y jabones industriales |
| Debe evitar cambiar de productos de higiene y cosméticos si estos no le dan problemas |
| Lave todas las prendas nuevas, al menos 2 veces, antes de utilizarlas |
| Debe evitar el rayón, la pana y tejidos “resistentes a arrugas” |
| La seda, el lino, la lana, el nylon puro y la tela vaquera son tejidos no tratados y se pueden utilizar |
| El algodón mercerizado (algodón La Perla® o algodón Pearle®) y el sanforizado también se pueden utilizar |
La dermatitis de contacto alérgica a formaldehído y liberadores de formaldehído no es infrecuente. La mayoría de estos pacientes son mujeres con eczema crónico de manos, a menudo con afectación facial, o trabajadores que emplean aceites de corte y peluqueros o profesionales sanitarios que manipulan cremas o jabones. Casi todos ellos se sensibilizan a formaldehído a través de agentes liberadores de formaldehído añadidos, como conservantes a cosméticos, productos de higiene y limpieza. El manejo terapéutico de los pacientes alérgicos a formaldehído resulta complicado. Los trabajos recientes sobre este tema intentan dar respuesta a dos dudas clave: ¿son peligrosos los liberadores para los pacientes alérgicos a formaldehído? y ¿es toda la alergia a liberadores debida a formaldehído? Hasta que estas dudas se aclaren por completo, resulta prudente recomendar a los pacientes alérgicos a formaldehído que eviten también todos los liberadores, mientras que si solo uno o varios liberadores del mismo grupo son positivos, sin formaldehído, entonces se puede instruir al paciente para que evite únicamente los liberadores de ese grupo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.