Maki et al.1 publicaron anteriormente un caso de penfigoide ampolloso (PA) inducido por el inhibidor de dipeptidil peptidasa-4 (DPP4i) y dermatosis perforante adquirida reactiva (DPAR) concurrente. Recientemente observamos un caso similar en una paciente diabética.
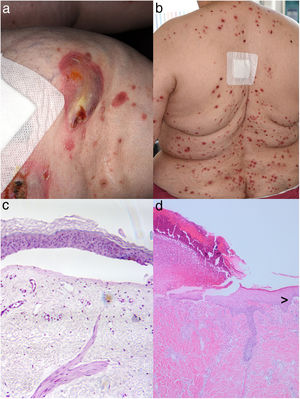
Una mujer de 69 años acudió con historia de 8 semanas de lesiones cutáneas con prurito severo. Durante el examen se observaron diversas ampollas tensas en las rodillas, así como pápulas generalizadas parcialmente umbilicadas con tapón central adherente queratócico (fig. 1a y b). No se evidenció formación de ampollas en estas últimas lesiones. También se detallan los resultados del examen histopatológico en las figuras 1c y d. La inmunofluorescencia directa reflejó depósitos lineales de IgG y C3 en la zona membranosa basal. La inmunofluorescencia indirecta (IIF) utilizando técnica de «salt-split» reflejó depósitos de IgG en forma de banda en el lado epidérmico. La prueba ELISA reveló una concentración altamente elevada de anticuerpos anti BP-180 (NC16A), de 140U/ml (< 20). Los valores de BP-230 y desmogleína 1, y 3 se situaron dentro de un rango normal. Las comorbilidades de la paciente incluyeron hipertensión, obesidad y diabetes mellitus (tipo II), que fue tratada con vildagliptina 50 mg/metformina 850mg 2veces al día durante 6 meses. Las primeras lesiones de PA se desarrollaron 4 meses después del inicio de la terapia con vildagliptina. Se diagnosticó PA inducido por DPP-4i (DPP4i-BP) con DPAR concurrente. Recomendamos sustituir vildagliptina e iniciamos tratamiento sistémico con dimentideno maleato (4mg 2veces al día) y prednisolona 150mg en régimen de dosificación reducida. La paciente mejoró con esta terapia.
Se observan ampollas explosivas costrosas en rodilla derecha (a) con múltiples pápulas y tapones oscuros centrales en la espalda (b) de una paciente diabética con terapia de DPP4i. El examen histopatológico de una muestra de biopsia cutánea tomada de la rodilla derecha reveló la presencia de bulas subepidérmicas con algunos infiltrados linfocíticos perivasculares sin eosinófilos (c). La histología obtenida de una lesión papulosa de la parte superior de la espalda reveló parcialmente la eliminación transepidérmica de haces de colágeno basofílico necrótico en una depresión epidérmica en forma de copa, mientras que la figura aquí mostrada está dominada por ulceración (d: tinción hematoxilina–eosina, amplificación 200×). De forma interesante, también se aprecia el borde de una formación de ampolla subepidérmica (>: tinción hematoxilina–eosina, amplificación 100×).
Los grandes estudios, incluyendo metaanálisis, han aportado evidencia sólida sobre que los DPP4i y, en particular, vildagliptina, desencadenan a menudo la aparición de PA, que es una enfermedad autoinmune relativamente común en las personas mayores3,4. Las observaciones detalladas han revelado que DPP4i-BP tiende a reflejar más bien un fenotipo no inflamatorio, con menos eritema que PA sin ingesta de DPP4i1-3. Además, la visión histológica refleja con frecuencia únicamente infiltrados inflamatorios dispersos (p. ej., eosinófilos)1-4. También se ha demostrado que el genotipo HLA-DQB1*03:01 está asociado a menudo a DPP4i-BP2,3. DPP4 —sinónimo de CD26— se expresa en una serie de células tales como los linfocitos T y otras células inmunes3,4. Por tanto, cabría esperar que la inhibición de DPP4 pudiera inducir alteraciones en los procesos inmunológicos, incluyendo el desarrollo de epítopes para anticuerpos de DPP4i-BP. Los anticuerpos de DPP4i-BP pueden focalizar también epítopes en BP-180, que son diferentes de los de PA no relacionados con DPP4i (NC16A) y pueden ser más precisamente detectados por los ensayos ELISA BP-180 de largo completo1-3. Como resumieron Maki et al.1, la asociación de PA no relacionado con DPP4i y DPAR se ha reportado previamente en casos esporádicos1. En los 5casos, la aparición de DPAR precedió el inicio de PA1. La patogenia de DPAR es escasamente comprendida. Las lesiones se encuentran característicamente dentro del ámbito del prurito (fig. 1b), pudiendo reproducirse experimentalmente mediante comezón cutánea5. Los investigadores han propuesto que DPAR representa una reacción cutánea al traumatismo superficial debido al prurito. DPAR se asocia con frecuencia extrema a diabetes mellitus/nefropatía, conduciendo a la idea de que el prurito puede causar microtraumatismos y necrosis de las estructuras epidérmicas/dérmicas, probablemente debidos a la microangiopatía diabética5. El prurito y el traumatismo cutáneo asociados a DPAR pueden contribuir a la realización de DPP4i-BP2-4.
En conclusión, reportamos una constelación clínica inusual en una paciente diabética tratada con DPP4i, que desarrolló simultáneamente PA y DPAR. Como el uso de DPP4i es muy frecuente a nivel mundial, es probable que surjan más casos.
Conflicto de interesesLos autores declaran la ausencia de conflicto de intereses.