Las cicatrices por quemadura suponen una elevada morbilidad en forma de contracturas, desfiguración corporal y prurito, así como un elevado impacto emocional que disminuye la calidad de vida de estos pacientes. Los dispositivos láser se han mostrado eficaces para su tratamiento, por encima de los tratamientos tópicos y complementarios a la cirugía, sin generar tanta morbilidad. Sin embargo, su uso en los departamentos de dermatología hospitalarios todavía está poco extendido. El láser más utilizado es el láser CO2 para tratar el grosor de la cicatriz, alteraciones texturales, y la posible contractura asociada, restaurando la movilidad de estos pacientes cuando se encuentra alterada. El láser de colorante pulsado es especialmente útil ante las cicatrices de quemaduras recientes con componente eritematoso y para prevenir el desarrollo de cicatrices hipertróficas posteriores. La hiperpigmentación puede mejorar con láseres de pigmento en modalidades de pulso corto (nano- y picosegundos). Revisamos la evidencia de estos dispositivos para el tratamiento de las cicatrices por quemaduras y aportamos una propuesta de algoritmo terapéutico.
Burn scars cause high morbidity in the form of contractures, body disfigurement, and itching, and they also have a high emotional impact that adversely affects patient quality of life. Laser therapy has proven effective in this setting. It is superior to topical treatments and can be used in conjunction with surgery, helping to reduce morbidity. The use of lasers in hospital dermatology departments, however, is still limited. Carbon dioxide laser resurfacing is the most widely used modality for reducing scar thickness, improving textural abnormalities, and treating contractures. Treatments improve mobility for patients with constrictions. Pulsed dye laser treatments are particularly useful for reducing erythema in recent burn scars and preventing subsequent hypertrophy. Pigment laser treatments with short pulse durations (nanoseconds or picoseconds) can improve hyperpigmentation. In this article, we review the evidence for the use of laser therapy for burn scars and propose a treatment algorithm.
Los dispositivos láser han demostrado tener una gran utilidad para el tratamiento de cicatrices en dermatología1. Su uso ha sido bien estudiado en determinados tipos de cicatrices, como las secundarias al acné, quirúrgicas, postraumáticas o queloides1,2. Sin embargo, el tratamiento con láser de las secuelas cutáneas por quemaduras es menos conocido y no está disponible en la mayoría de los centros hospitalarios.
En 2017 se estimó una prevalencia global de lesiones por quemaduras superior a 1.000 por 100.000 habitantes. La mayoría supusieron quemaduras de una extensión inferior al 20% de la superficie corporal, con afectación fundamentalmente cutánea, por lo que el papel del dermatólogo es crucial3.
Las complicaciones por estas cicatrices pueden generar una gran repercusión en la calidad de vida de estos pacientes4. Las contracturas y desfiguración generadas pueden suponer un gran impacto funcional, reducir su movilidad y generar dolor y prurito. Además, se trata de lesiones con un gran componente emocional que pueden ser estigmatizantes, especialmente las localizadas en cara y cuello, y producir ansiedad, depresión y baja autoestima5.
Tradicionalmente, se han utilizado una gran variedad de tratamientos conservadores para el manejo de las cicatrices por quemaduras, entre ellos los geles de silicona, inyecciones de corticoides, presoterapia y masajes terapéuticos6. Además, con frecuencia, es necesaria la combinación de estos tratamientos con intervenciones quirúrgicas, desde la resección de la cicatriz con aproximación de piel sana, hasta la realización de incisiones transversas, Z-plastias, colgajos o injertos cutáneos7.
Dispositivos láserEn los últimos años, los láseres han demostrado su eficacia en el manejo de estas lesiones como intervenciones mínimamente invasivas, con bajo riesgo de efectos adversos y un rápido tiempo de recuperación. Por esta razón, algunos algoritmos de tratamiento ya los incluyen entre la modesta eficacia de los tratamientos conservadores y las intervenciones quirúrgicas, que pueden ser muy efectivas pero se asocian a una elevada morbilidad8. No reemplazan necesariamente la cirugía, pero pueden reducir su extensión, y con ello, generar menos complicaciones postoperatorias9.
En función de su mecanismo de acción, los dispositivos láser se han clasificado en ablativos o no ablativos, fraccionados o no fraccionados10. Los principales dispositivos láser empleados en el tratamiento de las cicatrices por quemaduras se resumen en la tabla 1.
Principales alteraciones en las cicatrices y dispositivos láser disponibles para su tratamiento
| Alteración | Dispositivos láser |
|---|---|
| Eritema | LCP 585-595nm, LPI 500-1200nm, láser Nd:YAG 1064nm (ms), láser KTP 532nm (ms) |
| Grosor | LFALáser CO2 10600nmLáser Er:YAG 2940nmLFNALáser Er:glass 1540-1550nm |
| Flexibilidad | Láser CO2 10600nm |
| Pigmentación | LFA, LFNA, láser Alejandrita 755nm QS, láser Nd:YAG 1064nm QS, láser de rubí 694nm QS, láser KTP 532nm QS |
LCP: láser de colorante pulsado; LFA: láseres fraccionados ablativos; LFNA: láseres fraccionados no ablativos; LPI: luz pulsada intensa; ms: milisegundos (pulso largo); QS: Q-switched (nano/picosegundos, pulso corto).
En este artículo se incluyen los parámetros más habituales utilizados para el tratamiento de estas lesiones que pueden ser de utilidad de forma orientativa. Es importante remarcar que los parámetros son variables, tanto por la heterogeneidad de las mismas cicatrices como por la variedad entre dispositivos de diferentes marcas (tabla 2).
Principales láseres para el tratamiento de cicatrices por quemaduras según grado de recomendación y nivel de evidencia
| Láser | Grado de recomendación | Nivel de evidencia |
|---|---|---|
| Láser CO2 10600nm | A | I |
| Láser LCP 585-595nm | B | I |
| Láser Er:glass 1540-1550nm | B | II |
| Láser Alejandrita 755nm | C | III |
LCP: láser de colorante pulsado.
La evolución natural en las cicatrices por quemaduras resulta en una cicatrización anormal en más de un 70% de ocasiones, bien por alteraciones en el grosor, textura, eritema o pigmentación11. Esto ocurre con frecuencia en las quemaduras que afectan las capas profundas de la dermis, como las de segundo o tercer grado que son las que potencialmente van a requerir tratamiento con láser. Las quemaduras superficiales que no alcanzan la dermis reticular raramente producirán una cicatrización alterada y no suelen generar complicaciones12.
Respecto al grosor de estas cicatrices, se pueden clasificar en queloides, hipertróficas o atróficas, mientras que, en función de su pigmentación, pueden ser hipo- o hiperpigmentadas respecto a la piel no afecta del paciente. Por otro lado, es frecuente encontrar eritema, especialmente en aquellas activas y recientes11.
Para iniciar y monitorizar la estrategia terapéutica es importante evaluar la gravedad de las cicatrices. Para ello, la escala más utilizada es la Vancouver Scar Scale13 que evalúa la vascularización, grosor, flexibilidad y pigmentación de las lesiones. Sin embargo, la escala Patient and Observer Scar Assessment Scale (POSAS) es considerada la más completa, puesto que incorpora también los síntomas subjetivos del paciente, como dolor y prurito14. Una correcta evaluación de estas cicatrices permite seleccionar el láser más apropiado para su tratamiento. Además, para elegir el tipo de dispositivo láser y sus parámetros es necesario considerar tanto las características del paciente (p.ej., fototipo, comorbilidades) como la localización corporal de la cicatriz (p.ej., cabeza, cuello, extremidad).
Láser vascularEl láser de colorante pulsado (LCP) forma parte de los láseres no ablativos vasculares y emplea una longitud de onda de 585-595nm15. Se fundamenta en el principio de fototermólisis selectiva, provocando la coagulación y necrosis de los vasos sanguíneos utilizando la oxihemoglobina como molécula diana (cromóforo)16. El LCP se considera el láser de elección para tratar el componente vascular de las cicatrices por quemaduras, con un bajo riesgo de efectos secundarios.
Múltiples estudios han demostrado la efectividad del LCP para corregir el eritema de las cicatrices, que es producido por un exceso de neovascularización durante el proceso de cicatrización17. Además, también se ha visto eficaz para el tratamiento de la hipertrofia de estas cicatrices. Esto se explicaría por la destrucción de colágeno secundaria a la hipoxia tisular que genera la coagulación de sus vasos18. Allison et al.19 también demostraron una mejoría en el prurito tras corregir el componente vascular. Este último mecanismo no está del todo definido, pero se ha sugerido que responde a un cambio en las citoquinas, neuropéptidos e histamina producido por la hipoxia y calentamiento local tras el láser.
Generalmente se utilizan fluencias bajas, entre 4-8J/cm2 con un diámetro del haz del láser (spot) de 7-10mm y duraciones de pulso cortas 0,5-2ms8. El endpoint o efecto inmediato deseado es la púrpura leve, dado que un exceso de tratamiento puede conllevar alteraciones de la pigmentación. Los mejores candidatos para el tratamiento mediante LCP son los pacientes con fototipo I-III porque presentan menos melanina que compita con la hemoglobina para la absorción de energía. Habitualmente se realizan tratamientos separados entre 6-8 semanas, hasta lograr el efecto terapéutico esperado, con una media habitual de 4 sesiones15.
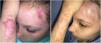
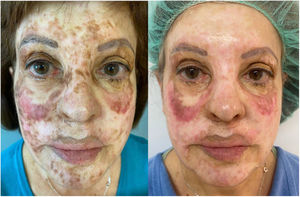
Dado que penetra aproximadamente 1,2mm en la piel, su uso en cicatrices hipertróficas gruesas es limitado. Por lo tanto, con frecuencia se utiliza asociado a los láseres fraccionados ablativos (LFA) en cicatrices gruesas con un probable efecto sinérgico de ambos15. En nuestra experiencia, los pacientes pediátricos habitualmente toleran peor el tratamiento con LFA, y el LCP en monoterapia puede ofrecer muy buenos resultados, especialmente en fases iniciales de la cicatrización (fig. 1).
Por otro lado, Al-Mohamady et al.20 demostraron en un ensayo clínico que el láser de neodymium-doped yttrium aluminium garnet (Nd:YAG) 1064nm de pulso largo y a fluencias bajas también es eficaz en el tratamiento de estas cicatrices, sin observar diferencias significativas respecto al LCP.
Finalmente, los dispositivos de luz pulsada intensa emiten un haz de luz policromática de amplio espectro entre 500-1200nm. Este puede ser delimitado mediante filtros y actuar sobre diferentes tipos de cromóforos, bajo el mecanismo de fototermólisis selectiva21. Estos dispositivos también podrían ser de utilidad para el tratamiento del componente vascular, la pigmentación e hipertrofia de las cicatrices de múltiples etiologías como las quemaduras y se podrían utilizar como una buena alternativa, aunque su evidencia en el tratamiento de cicatrices por quemadura es limitada22.
Láser fraccionado ablativoLos LFA son el pilar fundamental para el tratamiento de las cicatrices por quemaduras. Los más utilizados son el láser CO2 de 10600nm y el láser erbium-doped yttrium aluminum garnet (Er:YAG) de 2940nm que tienen como cromóforo el agua. Actúan generando columnas de daño térmico en la epidermis y en la dermis que favorecen la remodelación del colágeno, mejorando el grosor, la flexibilidad y el color de las cicatrices. La profundidad de las columnas varía de 0,2 a 4mm. Además, el tejido no dañado entre las columnas sirve como reservorio para una rápida recuperación tras el tratamiento23.
El láser CO2 tiene menos afinidad por el agua que el láser Er:YAG y genera más coagulación térmica en el tejido periférico. Este mecanismo es el que facilita la respuesta de reparación del colágeno y, por ello, el láser CO2 se considera el más efectivo y es el más empleado. Además, el láser CO2 deposita la energía a mayor profundidad, hasta 4mm, y por su actividad en la coagulación de vasos también evita parte del sangrado durante el tratamiento de la lesión8.
Existen metaanálisis recientes que demuestran que el uso de láser CO2 fraccionado mejora significativamente el grosor, la flexibilidad, la vascularización, la pigmentación, e incluso el dolor y prurito de las cicatrices por quemadura24,25.
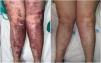
En función de las características de la cicatriz, se podrán emplear estos dispositivos superficialmente para alisar la piel, en profundidad para reducir la tensión y favorecer el remodelado del colágeno, o incluso de forma combinada26 (fig. 2).
Los parámetros utilizados de los LFA son muy variables y se ajustan a las características de la cicatriz y al fototipo del paciente. Por ejemplo, en las cicatrices más hipertróficas, se tienden a utilizar energías más altas para actuar a mayor profundidad, pero con densidades bajas para compensar el exceso de daño térmico. Los parámetros más frecuentemente empleados son potencias intermedias-altas (15-30W) y densidades bajas (5-15%). Fototipos más oscuros requieren parámetros más conservadores para evitar hiperpigmentaciones. Habitualmente se realizan una media de 3-5 sesiones de tratamiento separadas entre ellas 4-12 semanas27.
En las cicatrices hipertróficas asociadas a contracturas, más frecuentes en zonas periarticulares, se ha empleado el láser CO2 en modalidad no fraccionada continua (modo clásico) para reducir la tensión de las mismas y aumentar su movilidad. Este procedimiento consiste en la realización de incisiones perpendiculares a la zona más prominente de la contractura o en forma del logo del coche Mercedes Benz en casos extensos, dejando posteriormente la cicatrización por segunda intención28.
En las cicatrices atróficas producidas por una reducción en el colágeno dérmico, también pueden utilizarse los LFA para estimular la nueva síntesis de colágeno29.
El tratamiento mediante LFA es generalmente bien tolerado, con pocos efectos adversos asociados que, en caso de ocurrir, suelen ser leves. Han sido descritas como complicaciones, en orden de frecuencia: hipopigmentación, dolor e inflamación, eritema prolongado, vesículas, crecimiento paradójico de la cicatriz e infecciones27.
Láser fraccionado no ablativoLos láseres fraccionados no ablativos (LFNA) generan un daño térmico en la dermis en forma de columnas de coagulación sin ablación y mantienen la epidermis intacta10. Mediante este mecanismo, permiten reducir el daño superficial y calentar menos la piel, y por lo tanto tienen un tiempo de recuperación menor26. El más utilizado es el láser Er:glass de 1540-1550nm.
En comparación con los LFA, los LFNA producen un calentamiento de la piel menor, de entre 50 y 70°C, y alcanzan profundidades inferiores (1,8mm aproximadamente)8. Aunque existen escasos estudios comparativos entre LFNA y LFA para el tratamiento de cicatrices, al ejercer menos daño térmico, los LFNA muestran menos efectividad y requieren mayor número de sesiones26,30.
En un ensayo clínico, Taudorf et al.31 observaron una mejoría del grosor, flexibilidad, rugosidad de las cicatrices por quemadura, así como la normalización del colágeno a nivel histológico a los 6 meses del tratamiento, aunque con menor eficacia en las cicatrices hipertróficas.
Láser de pigmentoLos principales láseres de pigmento son el láser de rubí 694nm, el láser Alejandrita 755nm y el láser Nd:YAG 1064nm y 523nm (KTP) en modalidad Q-switched (nano- o picosegundos)32. Aunque se utilizan con frecuencia para el tratamiento de la discromía en varios tipos de cicatrices33, no hemos encontrado estudios específicos para su uso en las cicatrices por quemadura. Generalmente, el manejo de las alteraciones pigmentarias es complejo y con frecuentes recurrencias.
Los láseres ablativos que tienen como diana el agua, como el láser CO2, si bien se usan comúnmente para tratar el componente textural, también se pueden usar para eliminar de forma no selectiva la hiperpigmentación mediante la vaporización de la melanina en el tejido epidérmico. Sin embargo, los láseres cuyo cromóforo es la melanina son los más específicos puesto que destruyen selectivamente los melanosomas de los queratinocitos y melanocitos, limitando el daño térmico colateral del tejido periférico32. Por otro lado, los tratamientos tópicos despigmentantes junto a una fotoprotección estricta son el pilar fundamental de la hiperpigmentación postinflamatoria32.
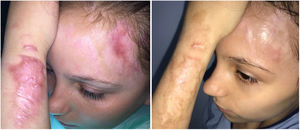
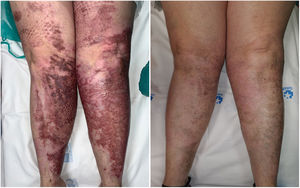
En nuestra experiencia, los láseres de pigmento como el Alejandrita 755nm de pulso corto pueden generar muy buenos resultados (fig. 3). Proponemos la utilización de fluencias bajas (1-3J/cm2), para mejorar su tolerancia, en pulsos de nano- o picosegundos y spot 3-5mm.
Finalmente, en el tratamiento de la hipopigmentación se han empleado LFA y LFNA con cierta mejoría que se podría explicar por una migración de melanocitos normales que provienen de la periferia34.
Láseres combinadosDado que las cicatrices por quemadura frecuentemente presentan alteraciones tanto en el grosor como en la textura, eritema y pigmentación, la combinación de varios dispositivos láseres permite un tratamiento más completo y específico. Existen ensayos clínicos que observan un mejor resultado con la combinación de tratamientos, especialmente LCP asociado a láser CO235,36.
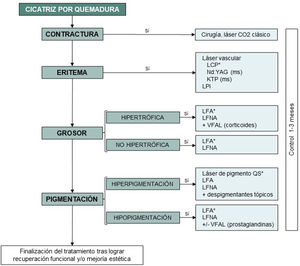
Anderson et al.8 proponen un esquema terapéutico que incluye el uso inicial de LCP para el tratamiento del eritema e inflamación y, posteriormente, la combinación con LFA para mejorar el grosor y textura de la cicatriz. En nuestra experiencia, en las cicatrices que presenten alteraciones de la pigmentación o hipertricosis también se pueden asociar láseres cuyo cromóforo es la melanina como el láser Alejandrita 755nm o Nd:YAG 1064nm. Proponemos un algoritmo terapéutico para el abordaje de las cicatrices por quemaduras basados en la revisión de la literatura y nuestra experiencia profesional (fig. 4).
Algoritmo terapéutico de las cicatrices por quemadura. *Láser de elección; ms: milisegundos; LPI: luz pulsada intensa; LCP: láser de colorante pulsado; LFA: láser fraccionado ablativo; LFNA: láser fraccionado no ablativo; QS: Q-switched (nano- o picosegundos); VFAL: vehiculización de fármacos asistida por láser.
Los tratamientos adyuvantes a los dispositivos láser pueden ofrecer un efecto sinérgico en el tratamiento de las cicatrices por quemadura. Algunos estudios indican una mejoría de las cicatrices hipertróficas al combinar LCP junto a corticoides intralesionales, principalmente la triamcinolona, y 5-fluorouracilo37.
Otra modalidad prometedora cada vez más utilizada para el tratamiento de cicatrices es la vehiculización de corticoides asistida por láser, principalmente con el láser CO2 y el Er:YAG en modalidad fraccionada. Este mecanismo se fundamenta en la introducción del fármaco a través de las columnas generadas en la epidermis aumentando su capacidad de actuación38. Esta modalidad tiene como principal beneficio la buena tolerancia del tratamiento tópico vehiculizado respecto a la corticoterapia intralesional. El fármaco utilizado habitualmente es la triamcinolona en concentraciones de 10-40mg/ml. En esta modalidad, suelen utilizarse densidades del láser bajas (<5%) y energías variables en función del grosor de la cicatriz39,40.
Recientemente, la aplicación de prostaglandinas como el latanoprost y bimatoprost tras los láseres fraccionados ha demostrado mejorías significativas de la hipopigmentación de cicatrices, fenómeno que se explicaría por el aumento de transferencia de los melanosomas de los melanocitos a los queratinocitos basales. Aunque tradicionalmente se han empleado para el tratamiento de la hiperpigmentación postinflamatoria, los retinoides tópicos en adyuvancia también se han empleado para restaurar el pigmento mediante la modulación de la actividad de la tirosinasa41.
Por otro lado, también pueden ser de utilidad la infiltración de plasma rico en plaquetas42, los injertos de grasa autóloga43 o la radiofrecuencia36.
¿Cuándo tratar?Tras la curación completa de la herida por quemadura, una intervención precoz de las cicatrices permite reducir los síntomas, la formación de contracturas y mejora el proceso de rehabilitación8. Aunque el momento idóneo para iniciar el tratamiento en las cicatrices por quemaduras no está del todo definido, en las cicatrices quirúrgicas se han empleado el LCP, LFA y LFNA el mismo día de la retirada de los puntos, observándose efectivos y seguros44,45.
Las cicatrices eritematosas e hipertróficas son frecuentes, especialmente durante el primer año de la cicatrización. Por ello, el tratamiento precoz con láseres vasculares tiene un papel importante, incluso previniendo la aparición de estas complicaciones46. En algunos pacientes, especialmente aquellos con fototipos bajos (I-II), el eritema puede volverse crónico. Se ha visto que el LCP también muestra buenos resultados al tratar estas lesiones de años de evolución47.
ConclusionesLas cicatrices por quemadura habitualmente conllevan una gran morbilidad. Los dispositivos láser, especialmente el LCP y el láser de CO2, han demostrado ser eficaces en la mejoría de su eritema, hipertrofia, pigmentación, flexibilidad y prurito, con bajo riesgo de efectos adversos y un rápido tiempo de recuperación. Consideramos de gran utilidad su implementación en el manejo de estas lesiones para mejorar la calidad de vida de estos pacientes.
FinanciaciónNo ha habido financiación para la realización de este artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.