Se ha descrito que el carcinoma basocelular avanzado (CBCa) ocupa entre 1 y 10% de los casos, mientras que el desarrollo de metástasis se estima entre 0,0028 y 0,5%1. Los pacientes con CBCa no candidatos a cirugía o radioterapia con intención curativa pueden recibir terapias dirigidas como el vismodegib con una finalidad paliativa. Sin embargo, la suspensión de este tratamiento tiene lugar en alrededor de 90% de los casos tratados, hasta 33% por progresión de la enfermedad y 25% por toxicidad2–4. En estos casos se puede ofrecer el tratamiento con radioterapia externa que asocia una tasa de efectividad de 70%, con una mediana de dosis de 55 Gy (mín. 47 Gy-máx. 85 Gy). No obstante, en tumores mayores de 30 mm el porcentaje de respuesta se reduce a 55%, lo que sugiere que a mayor volumen tumoral se consigue una efectividad menor5,6. Por tal motivo puede ser deseable una citorreducción tumoral previa a la administración de radioterapia en el CBCa, ya sea con el vismodegib, con cirugía u otros métodos destructivos (criocirugía o doble-curetaje-electrocoagulación).
En los pacientes que suspenden el vismodegib tras una respuesta completa, se ha observado una recurrencia en hasta de 37% en los primeros seis meses3,4,7. La radioterapia podría considerarse como una terapia de consolidación no solo en los pacientes con una respuesta completa, sino también tras la progresión una vez se ha obtenido una respuesta parcial inicial con el vismodegib.
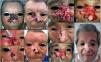
Describimos cuatro pacientes tratados en el Instituto Nacional de Cancerología de Colombia que presentaron respuestas completas, parciales o progresión durante el tratamiento con vismodegib, en quienes posterior a la citorreducción tumoral con la terapia dirigida, asociada o no a métodos destructivos locales, lograron una remisión completa sostenida en el tiempo de seguimiento luego del tratamiento de consolidación con radioterapia (tabla 1, figuras 1 y 2).
Casos de pacientes con diagnóstico de carcinoma basocelular avanzado que recibieron terapia multimodal y la respuesta clínica obtenida
| Paciente | Edad/Sexo | Localización anatómica del tumor/Diámetro mayor | Tratamiento previo al vismodegib | Núm. ciclos recibidos con vismodegib | Tipo de respuesta obtenida con el vismodebig | Efectos adversos presentados y graduación | Tratamiento(s) citorreductor(es) administrado (os) | Tipo y dosis de radioterapia | Respuesta obtenida posterior a la radioterapia/tiempo de seguimiento |
| 1(fig. 1A-D) | 69 años/masculino | CBCla centro-facial con extensión a órbita derecha 55 mm | Ninguno | 8 ciclos | Progresión por resistencia secundaria | Calambres grado 2, disgeusia grado 1 | Criocirugía doble electrocuretaje, imiquimod 5% tópico, IFN alta intralesional | Radioterapia externa 66 Gy en 33 sesiones posterior a suspender visodegib | Respuesta completa clínica y radiológica, sin recibida en 36 meses de seguimiento posradioterapia (fig. D) |
| 2(fig. 1 E-H) | 82 años/masculino | CBCla centro-facial con extensión a órbita derecha 90 mm | Ninguno | 37 ciclos | Parcial inicial posterior enfermedad estable (suspensión por toxicidad) | Calambres grado 3, disgeusia grado 1 | Criocirugía doble electrocuretaje, imiquimod 5% tópico | Radioterapia externa 55 Gy en 22 sesiones concomitante a vismodebig | Respuesta completa y clínica con compensación histológica y radiológica, sostenida 33 meses posradioterapia y 15 meses posterior a la suspensión del visodegib (fig. H) |
| 3(fig. 2A-D) | 62 años/masculino | CBCla en región temporal izquierda con extensión a canto externo y párpado inferior del ojo izquierdo 50 mm | LA 10 años antes, RL + colgajo Mustardé con reporte histológico de márgenes comprometidos 2 meses antes | 8 ciclos | Completa (suspensión por toxicidad) | Calambres grado 3 | Ninguno | Radioterapia externa 55 Gy en 20 sesiones posterior a suspender visodegib | Respuesta completa clínica y radiológica 30 meses de seguimiento posradioterapia (fig. D) |
| 4(fig. 2E-H) | 82 años/femenino | CBCla en piel de labio superior/25 mm | Ninguno | 8 ciclos | Completa (suspensión por toxicidad) | Calambres grado 3, disgeusia grado 1 | Ninguno | Radioterapia externa 55 Gy en 22 sesiones posterior a suspender visodegib | Respuesta completa clínica y radiológica, después de 34 meses de seguimiento posradioterapia (fig. H) |
Fig.: figura; Núm: número; mm: milímetros; CBCla: carcinoma basocelular localmente avanzado; LA: láser ablativo; RL: resección local; IFN: interferón; Gy: Gray.
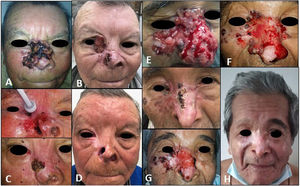
Extensión tumoral antes del inicio del vismodegib (A), respuesta parcial a nivel de dorso nasal y mejilla, con progresión en el canto interno del ojo derecho (B), citorreducción tumoral con métodos destructivos locales (C), respuesta completa sostenida luego de 36 meses de seguimiento posterior al tratamiento con radioterapia (D), compromiso tumoral antes del inicio de la terapia dirigida (E), incremento de lesiones a nivel de vertientes nasales y canto interno al completar 13 ciclos (F), saucerización y doble-electrocuretaje en áreas de mayor volumen tumoral y criocirugía en vertientes nasales (G), remisión completa sostenida 15 meses posterior a la suspensión del vismodegib y 33 meses posterior al tratamiento con radioterapia (H).
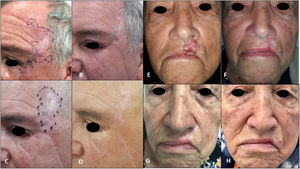
Compromiso tumoral antes de la intervención quirúrgica por parte de oftalmología oncológica para resección local a nivel de canto y párpado (A), tumor residual confirmado por biopsia a nivel temporal y ciliar izquierdo asociado a márgenes quirúrgicos comprometidos previo al inicio de vismodegib (B), respuesta clínica completa al finalizar ocho ciclos de vismodegib e inicio de radioterapia externa (C), remisión completa sostenida luego de 30 meses de seguimiento (D), extensión del tumor antes de iniciar terapia con vismodegib (E), respuesta completa luego de tres ciclos de tratamiento (F), respuesta completa luego de ocho ciclos de vismodegib previo a radioterapia (G), remisión completa luego de 34 meses de seguimiento posterior a la radioterapia (H).
El paciente 1 presentó una resistencia secundaria al vismodegib, por lo que recibió una terapia combinada con métodos destructivos locales con criocirugía y doble-curetaje y electrocoagulación previa al tratamiento de consolidación con radioterapia con una dosis total de 66 Gy, que obtuvo una respuesta clínica y radiológica completa, sin signos de recaída tumoral tras 36 meses de seguimiento. El segundo paciente obtuvo una estabilización del tamaño tumoral con el uso de vismodegib, que le produjo calambres grado 3 ocasionales. Durante la terapia dirigida recibió tratamiento combinado con doble-curetaje y electrocoagulación más criocirugía para citorreducción tumoral, seguido de radioterapia concomitante al vismodegib con una dosis total de 55 Gy. Se constató una respuesta clínica y radiológica completa libre de recaída 33 meses después de haber finalizado la radioterapia y 15 meses tras la suspensión del vismodegib.
En los pacientes 3 y 4 la terapia de inducción con vismodegib logró una respuesta completa, pero se requirió suspender el medicamento por la presencia de calambres grado 3. Se administró una terapia secuencial de consolidación con radioterapia con una dosis total de 55 Gy. Los pacientes obtuvieron una remisión completa libre de recaída tras 30 y 34 meses de seguimiento, respectivamente.
El uso de la radioterapia en combinación con el vismodegib que logra una respuesta completa en el tratamiento del CBCa ha sido ilustrado en algunas series en diferentes escenarios con seguimientos de hasta de 15 meses. En un primer escenario se describe la terapia con vismodegib y radioterapia concomitante que se continúa con vismodegib oral sin evidencia de toxicidad agravada por la combinación. Otro esquema corresponde a la terapia combinada trimodal que consiste en la inducción con vismodegib seguida de radioterapia y una resección quirúrgica local. También se ha descrito la inducción con vismodegib seguida de radioterapia8–10.
Yom Sue et al., en mayo del 2013 iniciaron un ensayo clínico fase 2 (NCT01835626), para demostrar la eficacia de la terapia combinada utilizando una inducción con vismodegib durante 12 semanas seguido de un esquema de radioterapia de cinco fracciones por semana durante siete semanas, sin embargo, los resultados están pendientes de publicación.
Con los casos descritos, ilustramos la utilidad de una terapia combinada basada en un tratamiento de inducción con vismodegib asociada o no a métodos destructivos locales, seguida de una terapia de consolidación con radioterapia, que podría considerarse como una excelente alternativa terapéutica para pacientes con CBCa logrando incluso remisiones completas duraderas. No obstante, se requiere la realización de estudios analíticos de mayor validez metodológica que permitan aclarar estos resultados y concluir sobre esta indicación y su uso expansivo.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.